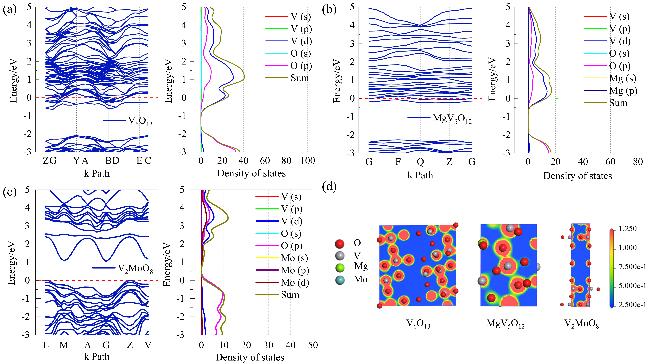
图5为三种材料在费米能级附近能带结构、态密度图(图S3为整体图). V
6O
13 [
图5(a)]的能带与费米能级相交, 显示出固有的金属性质
[54]. 其态密度图在费米能级附近形成明显峰值, 表明该材料具有较高的电子态密度, 有利于提高导电性, 其中V(d)轨道对电子态密度的贡献尤为显著. MgV
5O
12 [
图5(b)]同样显示了金属特性, 费米能级附近的电子态密度主要由V(s, p, d)轨道贡献, 特别是d轨道, 而O(s, p)和Mg(s, p)轨道也有一定贡献但相对较小. 相比之下, V
2MoO
8 [
图5(c)]的费米能级位于价带顶和导带底之间, 表现出半金属特性
[55], O(p)轨道对其电子态密度贡献最大. 总体上, 这三种材料均展现了良好的导电能力, 但V
6O
13在费米能级附近的电子态密度最高, 显示出更优的导电性能
[56].
图5(d)展示了三种材料的电子密度分布情况, 右侧的颜色条表示相对电子密度, 红色代表较高密度, 蓝色表示较低密度. 对于V
6O
13, 电子密度主要集中在氧上, 由于锂离子通常是通过与阴离子(在这里主要是氧原子)之间的库仑力进行吸附的, 因此高电子密度区域能够增强锂离子的吸附强度
[57]. 此外, 电子云的密集分布可能有助于形成稳定的锂插入位点, 这对于实现高效的充放电循环至关重 要
[58]. 针对MgV
5O
12, 除了氧原子外, 还可以观察到电子密度聚集在镁原子周围, 表明镁的存在会改变局部电子环境, 影响锂离子的吸附位置或方式
[59]. 有研究表明, 如果某些电子密度高的区域靠近镁原子, 则可能成为锂离子优先选择的吸附位点
[60]. 至于V
2MoO
8, 虽然电子密度依然主要集中在氧原子上, 但钼原子周围的电子密度不容忽视, 作为过渡金属, 未填满的d轨道能够参与成键并影响电子云的形状, 这可能导致特定的电子密度模式, 使得锂离子更容易找到合适的吸附位点
[61].