1 引言
2 动态中空结构的实现策略
2.1 动态基元
2.1.1 两亲性聚合物
2.1.2 无机纳米颗粒
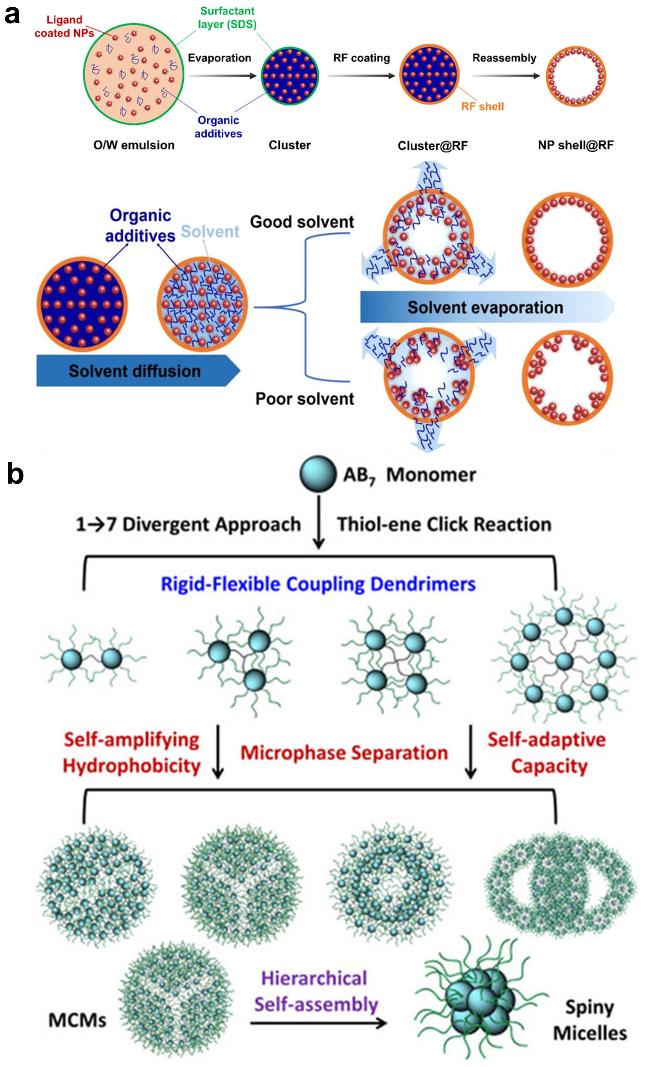
图3 动态中空结构自下而上的合成策略. (a)在聚合物纳米胶囊内将胶体纳米颗粒组装成中空结构的过程示意图. 经参考文献[21]许可转载, 版权2021 Wiley-VCH. (b)不同形貌的POSS基组装体合成示意图. 经参考文献[26]许可转载, 版权2021 Chinese Chemical SocietyFigure 3 Bottom-up strategy to synthesize dynamic hollow structure. (a) Schematic diagram of the process of assembling colloidal nanoparticles into hollow structures inside polymer nanocapsules. Reprinted with permission from ref. [21]. Copyright © 2021 Wiley-VCH. (b) Synthesis diagram of POSS-based assemblies with different morphologies. Reprinted with permission from ref. [26]. Copyright © 2021 Chinese Chemical Society |
2.1.3 生物分子
2.2 驱动力
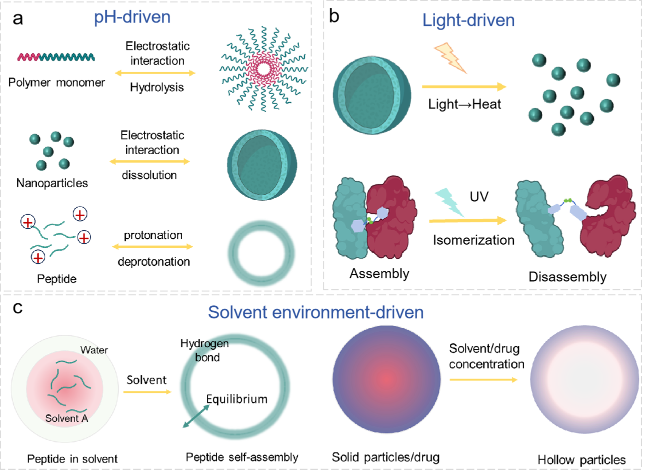
2.2.1 pH驱动
2.2.2 光驱动
2.2.3 溶剂环境驱动
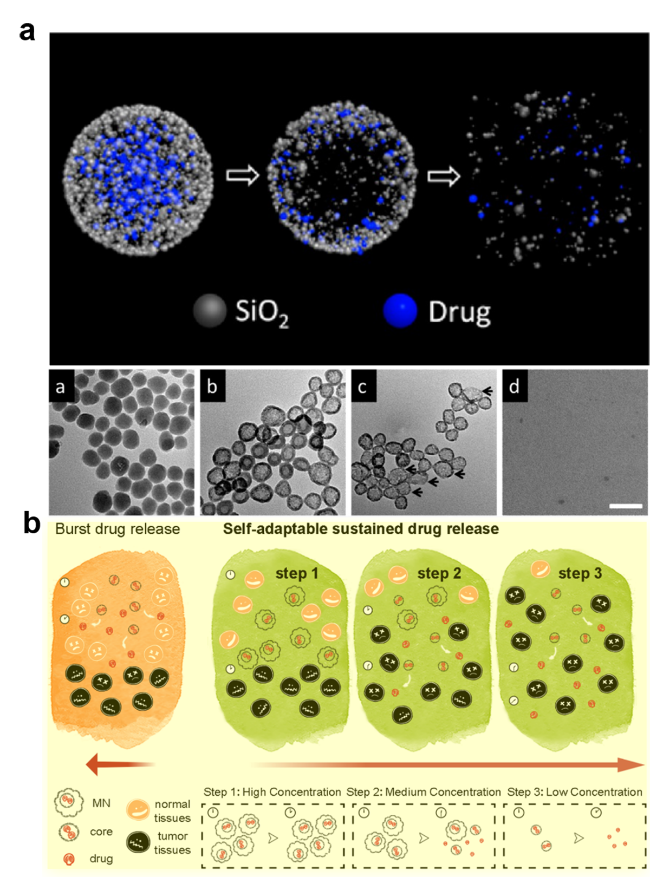
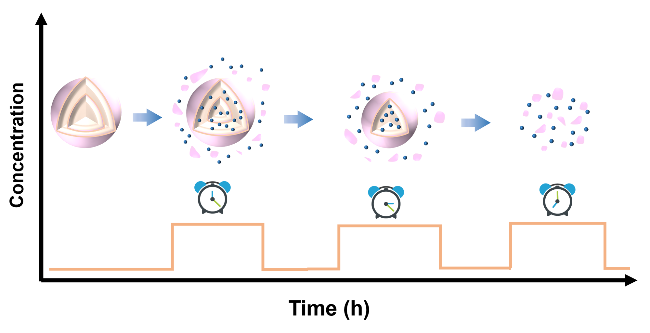
图4 动态中空二氧化硅的设计及药物递送. (a)可降解的SiO2药物载体作用示意图. 经参考文献[31]许可转载. 版权2013 American Chemical Society. (b)可降解的中空多壳层SiO2用于自适应药物递送示意图. 经参考文献[32]许可转载. 版权2022 American Chemical SocietyFigure 4 Design and drug delivery of dynamic hollow silica. (a) Schematic diagram of biodegradable SiO2 drug carrier. Reprinted with permission from ref. [31]. Copyright © 2013 American Chemical Society. (b) Schematic diagram of biodegradable hollow multi-shell SiO2 for adaptive drug delivery. Reprinted with permission from ref. [32]. Copyright © 2022 American Chemical Society |
3 动态中空结构在生物医药中的应用
3.1 药物递送
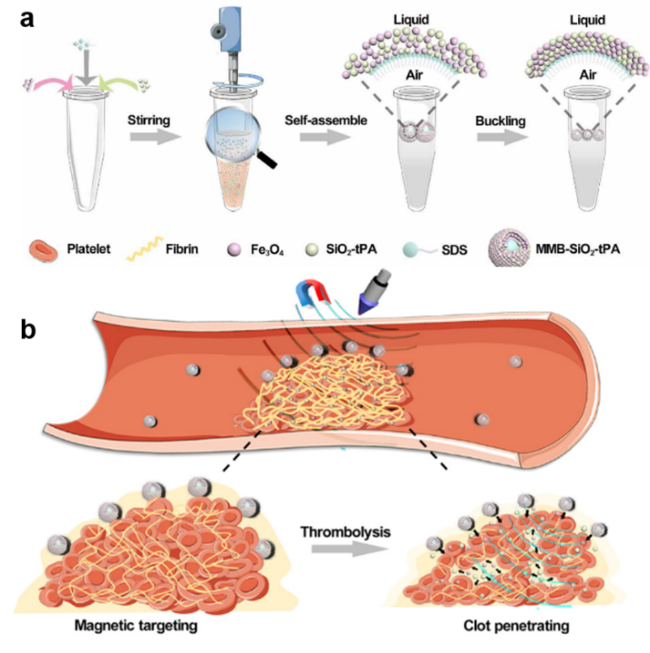
图5 动态中空结构用于药物递送. (a)以纳米药物为壳层的微气泡组装体合成示意图. (b)微气泡的靶向抗血栓递送应用示意图. 经参考文献[34]许可转载. 版权2020 AAASFigure 5 Dynamic hollow structure for drug delivery. (a) Schematic diagram of synthesis of microbubble assembly with nanomedicine as shells. (b) Schematic diagram of targeted delivery of microbubble for thrombolysis. Reprinted with permission from ref. [34]. Copyright © 2020 AAAS |
3.2 疾病检测
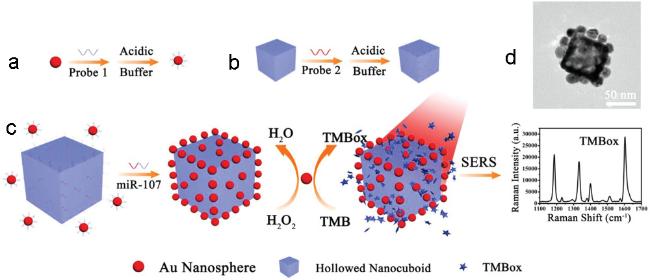
图6 动态中空结构用于疾病检测. (a) Au纳米球的表面修饰; (b)金/银合金立方体的表面修饰; (c) miRNA触发的自组装及检测; (d)组装体的透射电子显微镜照片. 经参考文献[38]许可转载. 版权2019 Wiley-VCHFigure 6 Dynamic hollow structure for disease detection. (a) Surface modification of Au nanospheres; (b) Surface modification of gold/silver alloy cubes; (c) miRNA-triggered self-assembly and detection; (d) TEM images of the assembly. Reprinted with permission from ref. [38]. Copyright © 2019 Wiley-VCH |
3.3 肿瘤治疗
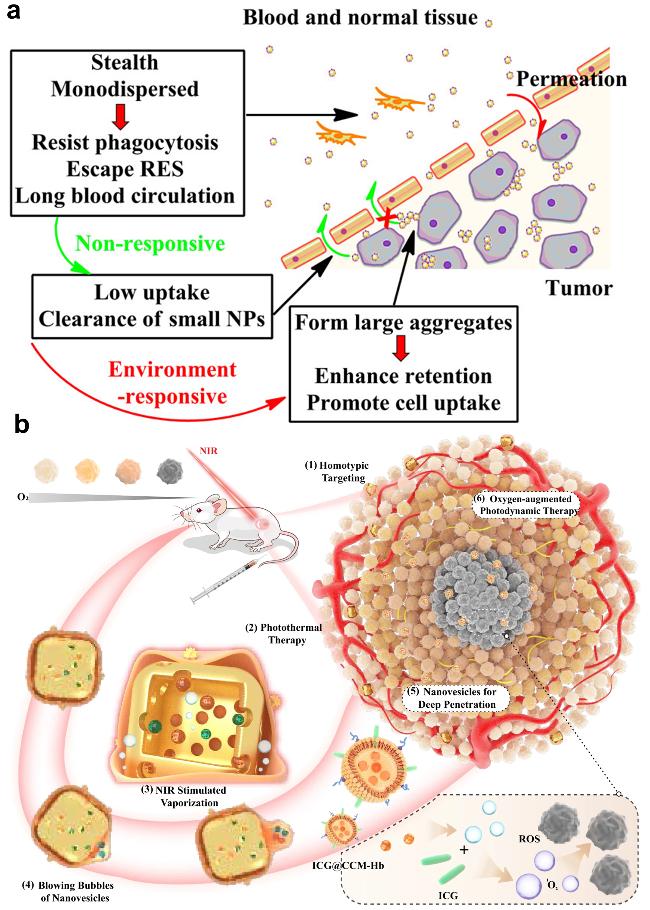
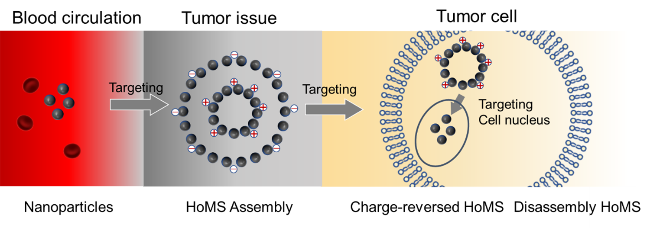
图7 动态中空材料在肿瘤治疗中的应用. (a)肿瘤环境诱导的颗粒聚集增强保留和细胞摄取策略. 经参考文献[45]许可转载. 版权2013 ACS Publications. (b)诱导肿瘤环境中的小尺寸囊泡生成促进肿瘤深层渗透策略. 经参考文献[49]许可转载. 版权2023 Springer NatureFigure 7 Application of dynamic hollow materials in tumor therapy. (a) Tumor environment-induced particle aggregation enhances retention and cell uptake strategy. Reprinted with permission from ref. [45], Copyright © 2013 ACS Publications. (b) Strategies to induce small-size vesicles in the tumor environment to promote deep tumor penetration. Reprinted with permission from ref. [49], Copyright © 2023 Springer Nature |