1 引言
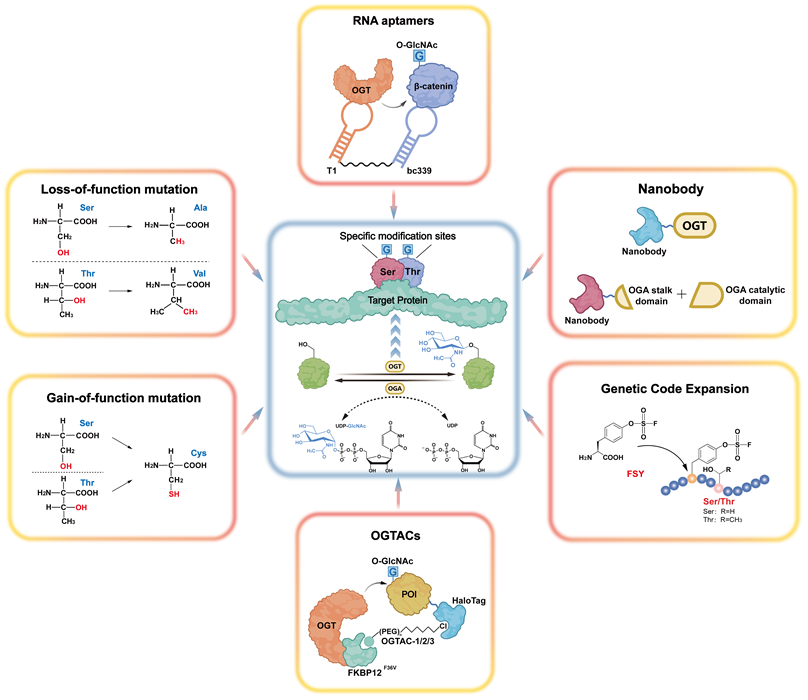
2 靶向特定蛋白质的O-GlcNAc糖基化精准调控工具
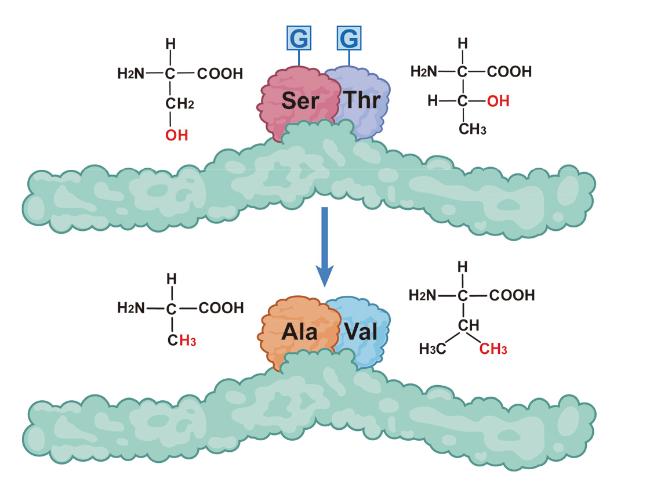
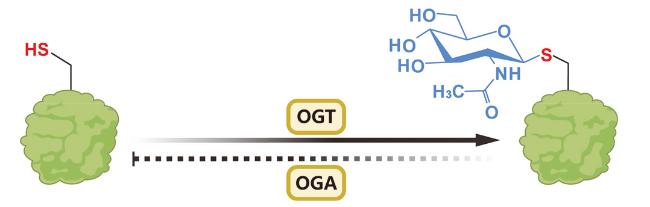
2.1 功能丧失性O-GlcNAc修饰位点突变
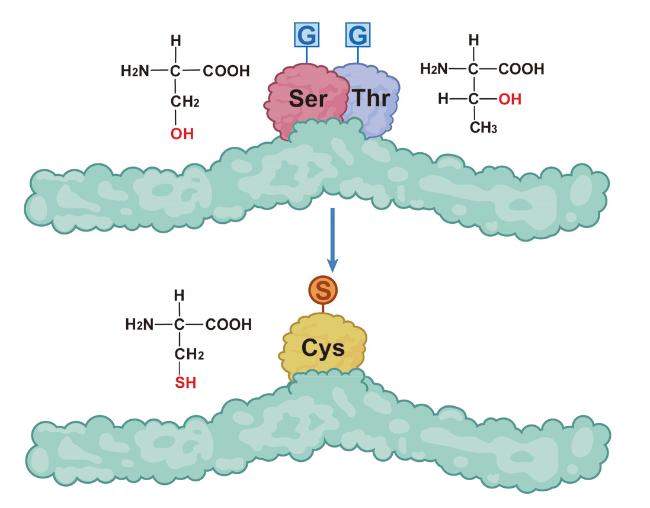
2.2 功能获得性O-GlcNAc修饰位点突变
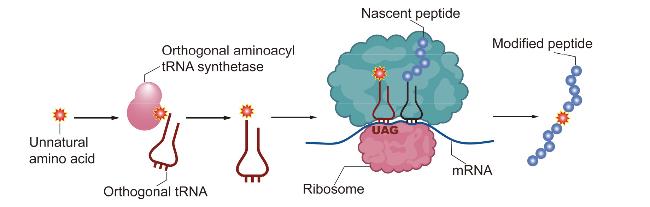
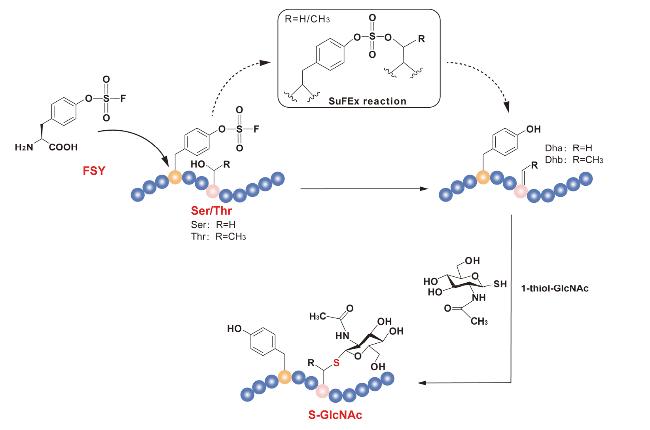
2.3 遗传密码扩展引入位点特异性O-GlcNAc修饰
2.4 基于纳米抗体的O-GlcNAc修饰靶向调控
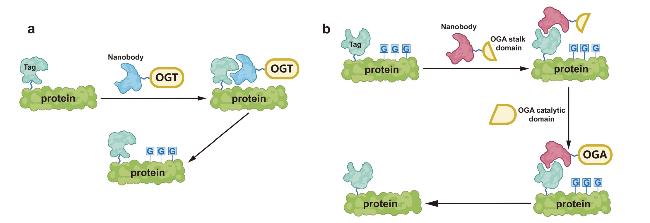
图8 基于纳米抗体的O-GlcNAc修饰靶向调控: (a) OGT通过标签纳米抗体空间接近靶蛋白, 使融合表达标签的靶蛋白O-GlcNAc修饰增加. (b) OGA通过标签纳米抗体去除靶蛋白O-GlcNAc修饰. OGA茎和催化结构域的分裂可抑制脱靶活性Figure 8 Nanobody-based targeted regulation of O-GlcNAcylation. (a) OGT is recruited into proximity of the target protein via a tag-specific nanobody, leading to increased O-GlcNAcylation on the tagged target protein. (b) OGA removes O-GlcNAc from the target protein via the tag-specific nanobody. Splitting the OGA stalk and catalytic domains can suppress off-target activity |
2.5 靶向特定蛋白O-GlcNAc修饰的嵌合体分子
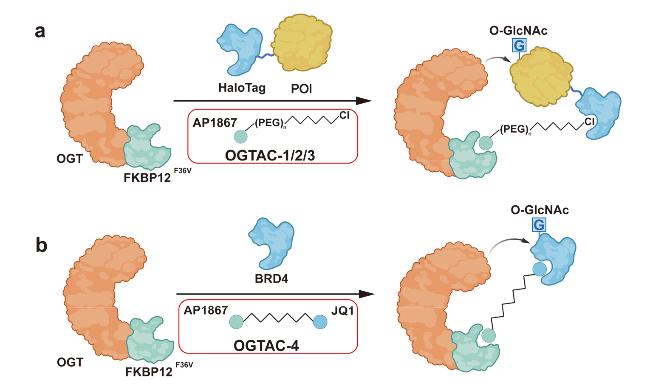
图9 靶向特定蛋白O-GlcNAc修饰的嵌合体分子. (a) FKBP12F36V融合表达的OGT通过OGTAC-1/2/3与融合表达HaloTag的靶蛋白结合, 催化靶蛋白发生O-GlcNAc修饰. (b) FKBP12F36V融合表达的OGT通过OGTAC-4与内源蛋白BRD4直接结合, 催化BRD4发生O-GlcNAc修饰Figure 9 Chimeric molecules for targeting O-GlcNAcylation to specific proteins. (a) OGT fused to FKBP12F36V is recruited to HaloTag-fused target proteins via OGTAC-1/2/3, resulting in O-GlcNAcylation of the target proteins. (b) OGT fused to FKBP12F36V directly binds the endogenous protein BRD4 through OGTAC-4, leading to O-GlcNAcylation of BRD4 |