1 结果与讨论
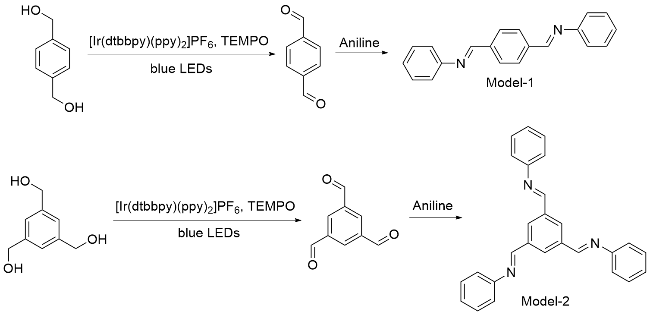
1.1 模型反应
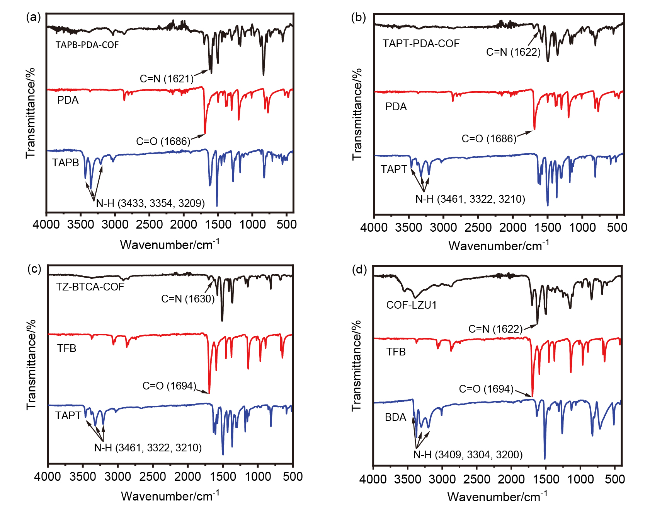
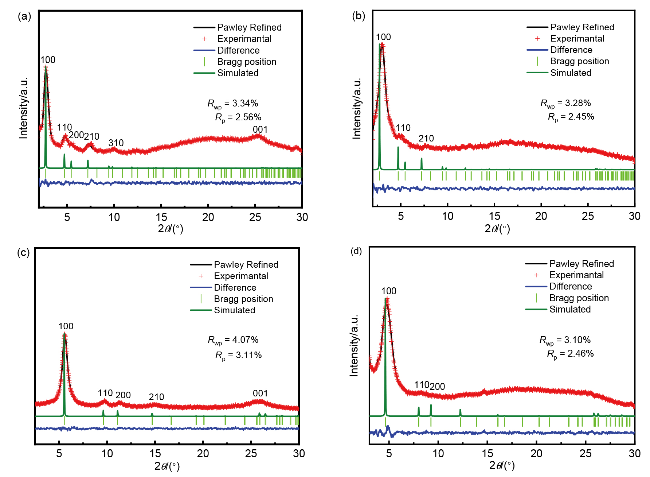
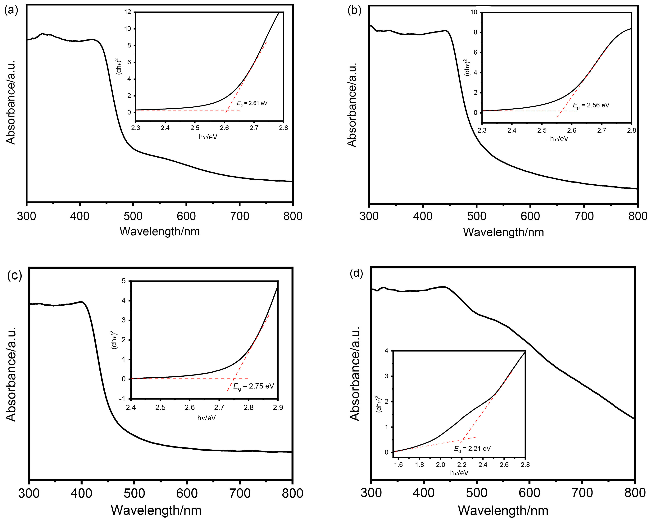
1.2 COFs的合成及表征
1.3 光催化硫醚氧化反应
表1 反应条件优化aTable 1 Optimization of the reaction conditions |
| Entry | TZ-BTCA-COF/mg | Oxidant | Solvent | Yield b/% |
|---|---|---|---|---|
| 1 | 6 | O2 | EtOH | 83 |
| 2 | 6 | O2 | MeOH | 99 |
| 3 | 6 | O2 | CH3CN | 68 |
| 4 | 6 | O2 | THF | 66 |
| 5 | 6 | O2 | CH2Cl2 | 42 |
| 6 | 6 | O2 | CHCl3 | 60 |
| 7 | 6 | O2 | Acetone | 43 |
| 8 | 4 | O2 | MeOH | 96 |
| 9 | 8 | O2 | MeOH | 98 |
| 10c | 6 | O2 | MeOH | 20 |
| 11d | 6 | O2 | MeOH | 32 |
| 12e | 6 | O2 | MeOH | N.R. |
| 13 | 6 | Air | MeOH | 59 |
| 14 | 6 | N2 | MeOH | N.R. |
| 15 | — | O2 | MeOH | N.R. |
a Reaction conditions: 0.2 mmol 1a, and corresponding TZ-BTCA-COF were added in 2 mL solvent, and the solution was irradiated under blue LEDs (λ= 440 nm) in oxygen for 12 h at room temperature. b Isolated yields. c Irradiated under green LEDs (λ=520 nm). d Irradiated under white LEDs (λ=420~650 nm). e In dark. |
表2 光氧化反应的底物范围aTable 2 Scope of the photooxidation reaction |
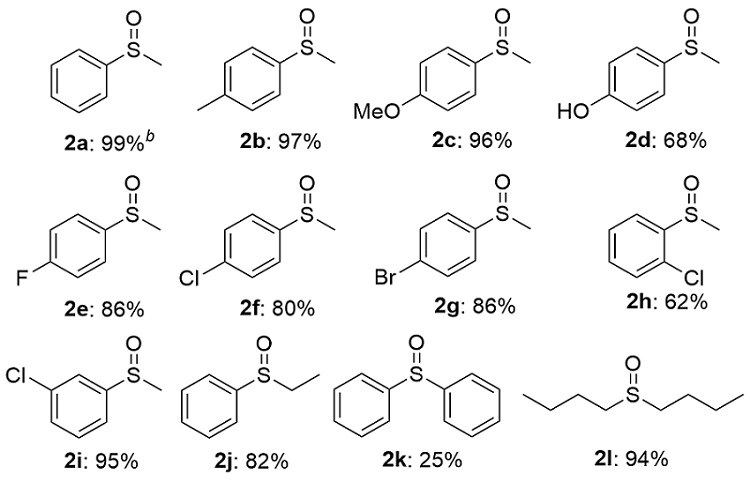 |
a Reaction conditions: 0.2 mmol 1, 6 mg TZ-BTCA-COF were added in 2 mL CH3OH, and the solution was irradiated under blue LEDs (λ=440 nm) in oxygen for 12 h at room temperature. b Isolated yields. |