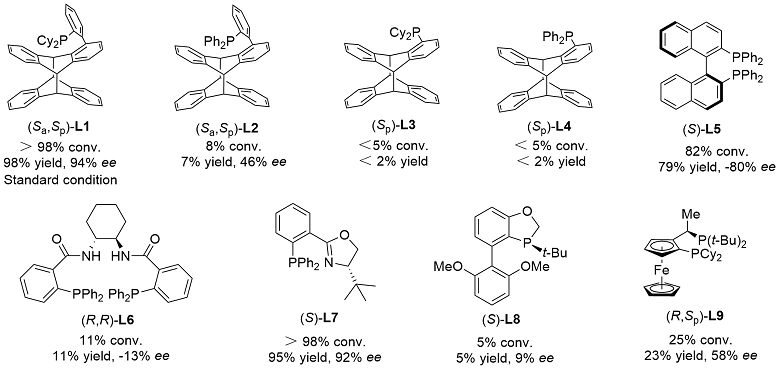
在手套箱中, 向8 mL反应瓶中加入[Pd(η3-C3H5)-Cl]2 (3.4 mg, 0.0092 mmol)和(Sa,Sp)-L1 (13.9 mg, 0.022 mmol), 并将混合物溶解在干燥的乙二醇二甲醚(2.3 mL)中. 将溶液在25 ℃下搅拌15 min, 从而得到8.0 mM的Pd-(Sa,Sp)-L1催化剂储备液.
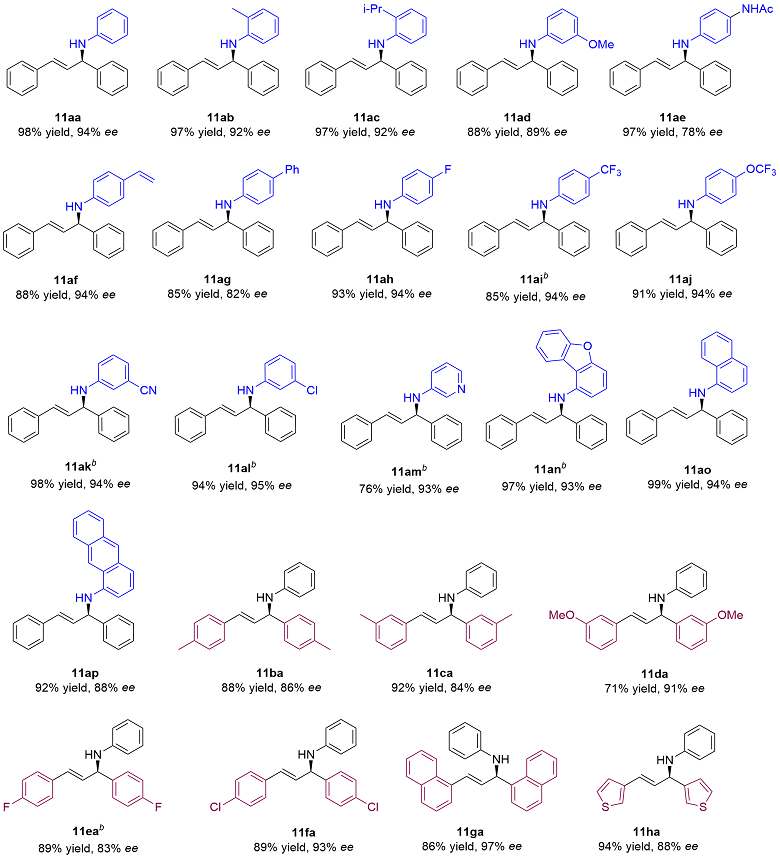
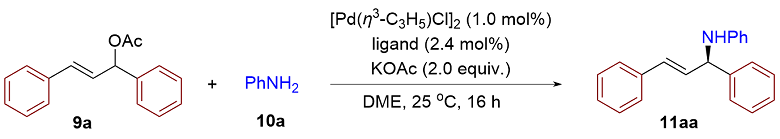
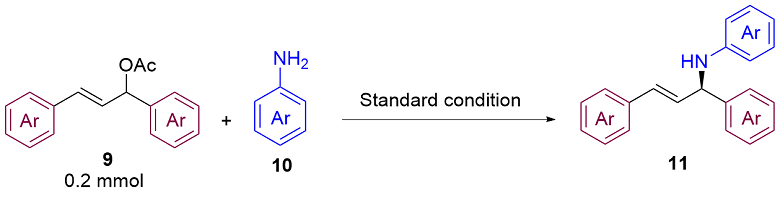
在手套箱中, 向另一个8 mL反应瓶中入[Pd(C3H5)-Cl]2-(Sa,Sp)-L1的储备液(8.0 mmol/L, 0.50 mL, 0.020 equiv.). 随后依次加入9 (0.20 mmol, 1.0 equiv., 溶于0.50 mL乙二醇二甲醚中)、10 (0.40 mmol, 2.0 equiv.)和KOAc (39 mg, 0.40 mmol, 2.0 equiv.). 将反应瓶盖紧密封, 从手套箱中取出, 在25 ℃下搅拌16 h. 随后浓缩反应混合物并通过硅胶柱色谱法(PE/EA(乙酸乙酯)/2% Et3N)纯化, 得到产物11(所有外消旋产物均使用rac-L1按照相同条件制备).
(
R,
E)-
N-(1,3-二苯基烯丙基)苯胺(
11aa): 黄色油状物, 55.9 mg, 产率98%, 94%
ee. [
α]-81.2 (
c 0.58, CH
2Cl
2);
1H NMR (400 MHz, CDCl
3)
δ: 7.36~7.31 (m, 2H), 7.30~7.24 (m, 4H), 7.22~7.16 (m, 3H), 7.15~7.12 (m, 1H), 7.08~7.00 (m, 2H), 6.65~6.58 (m, 1H), 6.58~6.49 (m, 3H), 6.30 (dd,
J=15.8, 6.2 Hz, 1H), 4.99 (d,
J=6.2 Hz, 1H), 4.00 (s, 1H). HPLC [Chiralpak AD-H,
V(
n-hexane)/
V(
i-PrOH)=95/5, 流速=1.0 mL/min,
λ=254 nm]:
tR=9.25 min (major), 11.44 min (minor). 表征数据与文献相同
[14h].
(R,E)-N-(1,3-二苯基烯丙基)-2-甲基苯胺(11ab): 淡黄色油状物, 58.1 mg, 产率97%, 92% ee. [α]-65.5 (c 1.2, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.38~7.35 (m, 2H), 7.32~7.26 (m, 4H), 7.24~7.19 (m, 3H), 7.17~7.12 (m, 1H), 7.01~6.98 (m, 1H), 6.95 (td, J=7.7, 1.6 Hz, 1H), 6.58 (td, J=7.4, 1.2 Hz, 1H), 6.56~6.47 (m, 2H), 6.35 (dd, J=15.8, 6.3 Hz, 1H), 5.06 (d, J=6.3 Hz, 1H), 3.87 (s, 1H), 2.13 (s, 3H); 13C NMR (101 MHz, CDCl3) δ: 145.1, 142.2, 136.6, 131.1, 130.9, 130.0, 128.8, 128.5, 127.7, 127.5, 127.1, 127.0, 126.5, 122.1, 117.3, 111.3, 60.5, 17.7. HRMS calcd for C22H21NNa [M+Na]+ 322.1566, found 322.1567. HPLC [Chiralpak OD-H, V(n-hexane)/V(i-PrOH)=99/1, 流速=1.0 mL/min, λ=254 nm]: tR=18.17 min (minor), 24.36 min (major).
(R,E)-N-(1,3-二苯基烯丙基)-2-异丙基苯胺(11ac): 淡黄色油状物, 63.5 mg, 产率97%, 92% ee. [α] -53.4 (c 1.1, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.39~7.33 (m, 2H), 7.31~7.24 (m, 4H), 7.24~7.18 (m, 3H), 7.17~7.11 (m, 1H), 7.08 (dd, J=7.6, 1.6 Hz, 1H), 6.93 (td, J=7.7, 1.6 Hz, 1H), 6.66 (td, J=7.5, 1.2 Hz, 1H), 6.57~6.48 (m, 2H), 6.35 (dd, J=15.8, 6.2 Hz, 1H), 5.05 (d, J=6.2 Hz, 1H), 4.05 (s, 1H), 2.85 (h, J=6.8 Hz, 1H), 1.21 (dd, J=10.7, 6.8 Hz, 6H); 13C NMR (101 MHz, CDCl3) δ: 143.8, 142.3, 136.7, 132.2, 131.2, 131.0, 128.8, 128.5, 127.7, 127.4, 127.1, 126.6, 126.5, 124.8, 117.7, 112.0, 60.7, 27.4, 22.4, 22.3. HRMS calcd for C24H25NNa [M+Na]+ 350.1879, found 350.1880. HPLC [Chiralpak OD-H, V(n-hexane)/V(i-PrOH)=99/1, 流速=1.0 mL/min, λ=254 nm]: tR=7.13 min (major), 7.81 min (minor).
(R,E)-N-(1,3-二苯基烯丙基)-3-甲氧基苯胺(11ad): 淡黄色油状物, 55.6 mg, 产率88%, 89% ee. [α] -47.0 (c 1.5, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.38~7.32 (m, 2H), 7.31~7.25 (m, 4H), 7.25~7.18 (m, 3H), 7.18~7.12 (m, 1H), 6.97 (t, J=8.1 Hz, 1H), 6.54 (dd, J=15.9, 1.4 Hz, 1H), 6.31 (dd, J=15.8, 6.2 Hz, 1H), 6.23~6.15 (m, 2H), 6.14~6.10 (m, 1H), 5.00 (d, J=6.2 Hz, 1H), 4.06 (s, 1H), 3.64 (s, 3H); 13C NMR (101 MHz, CDCl3) δ: 160.7, 148.6, 142.0, 136.6, 131.1, 130.7, 129.9, 128.8, 128.5, 127.7, 127.5, 127.2, 126.5, 106.7, 102.9, 99.7, 60.7, 55.0. HRMS calcd for C22H21ONNa [M+Na]+ 338.1515, found 338.1518. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=18.26 min (minor), 20.56 min (major).
(R,E)-N-(4-((1,3-二苯基烯丙基)氨基)苯基)乙酰胺(11ae): 淡黄色油状物, 66.7 mg, 产率97%, 78% ee. [α] -24.0 (c 2.3, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.37~7.32 (m, 2H), 7.31~7.25 (m, 4H), 7.24~7.19 (m, 3H), 7.17~7.10 (m, 3H), 7.03 (s, 1H), 6.57~6.47 (m, 3H), 6.30 (dd, J=15.8, 6.1 Hz, 1H), 4.97 (d, J=6.2 Hz, 1H), 4.01 (s, 1H), 2.02 (s, 3H); 13C NMR (151 MHz, CDCl3) δ: 168.1, 144.4, 141.9, 136.6, 131.1, 130.6, 128.8, 128.5, 128.4, 127.7, 127.5, 127.2, 126.5, 122.2, 113.8, 60.8, 24.2. HRMS calcd for C23H22ON2Na [M+Na]+ 365.1624, found 365.1625. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=80/20, 流速=1.0 mL/min, λ=254 nm]: tR=24.25 min (major), 29.61 min (minor).
(R,E)-N-(1,3-二苯基烯丙基)-4-乙烯基苯胺(11af): 黄色油状物, 55.1 mg, 产率88%, 94% ee. [α] -82.4 (c 1.1, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.37~7.10 (m, 12H), 6.57~6.46 (m, 4H), 6.31 (dd, J=15.8, 6.1 Hz, 1H), 5.43 (dd, J=17.6, 1.1 Hz, 1H), 5.02 (dd, J=6.2, 1.3 Hz, 1H), 4.92 (dd, J=10.9, 1.1 Hz, 1H), 4.11 (s, 1H); 13C NMR (101 MHz, CDCl3) δ: 146.9, 141.8, 136.6, 136.5, 131.2, 130.4, 128.8, 128.6, 127.7, 127.6, 127.5, 127.22, 127.19, 126.5, 113.5, 109.6, 60.5. HRMS calcd for C23H21NNa [M+Na]+ 334.1566, found 334.1564. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=13.22 min (major), 16.97 min (minor).
(R,E)-N-(1,3-二苯基烯丙基)-[1'-联苯]-4-胺(11ag): 无色油状物, 61.7 mg, 产率85%, 82% ee. [α] -71.1 (c 1.5, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.46~7.40 (m, 2H), 7.39~7.36 (m, 2H), 7.35~7.25 (m, 8H), 7.25~7.19 (m, 3H), 7.18~7.12 (m, 2H), 6.65~6.61 (m, 2H), 6.57 (dd, J=15.9, 1.3 Hz, 1H), 6.33 (dd, J=15.9, 6.2 Hz, 1H), 5.05 (t, J=5.3 Hz, 1H), 4.13 (d, J=4.8 Hz, 1H); 13C NMR (101 MHz, CDCl3) δ: 146.6, 141.9, 141.2, 136.6, 131.2, 130.6, 130.5, 128.9, 128.60, 128.56, 127.8, 127.7, 127.6, 127.2, 126.5, 126.3, 126.1, 113.8, 60.7. HRMS calcd for C27H23NNa [M+Na]+ 384.1723, found 384.1721. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=19.21 min (major), 24.82 min (minor).
(
R,
E)-
N-(1,3-二苯基烯丙基)-4-氟苯胺(
11ah): 无色油状物, 56.7 mg, 产率93%, 94%
ee. [
α] -46.4 (
c 0.73, CH
2Cl
2);
1H NMR (600 MHz, CDCl
3)
δ: 7.37~7.30 (m, 2H), 7.30~7.24 (m, 4H), 7.23~7.17 (m, 3H), 7.16~7.12 (m, 1H), 6.75 (t,
J=8.6 Hz, 2H), 6.52 (d,
J=15.8 Hz, 1H), 6.47 (dd,
J=8.8, 4.4 Hz, 2H), 6.29 (dd,
J=15.8, 6.3 Hz, 1H), 4.92 (d,
J=6.3 Hz, 1H), 3.92 (s, 1H). HPLC [Chiralpak AD-H,
V(
n-hexane)/
V(
i-PrOH)=90/10, 流速=1.0 mL/min,
λ=254 nm]:
tR=8.63 min (major), 10.25 min (minor). 表征数据与文献相同
[21].
(
R,
E)-
N-(1,3-二苯基烯丙基)-4-(三氟甲基)苯胺(
11ai): 淡黄色油状物, 60.3 mg, 产率85%, 94%
ee. [
α] -47.4 (
c 1.3, CH
2Cl
2);
1H NMR (400 MHz, CDCl
3)
δ: 7.39~7.27 (m, 8H), 7.26~7.20 (m, 3H), 7.19~7.14 (m, 1H), 6.60~6.48 (m, 3H), 6.30 (dd,
J=15.8, 6.1 Hz, 1H), 5.05 (t,
J=5.6 Hz, 1H), 4.36 (d,
J=5.1 Hz, 1H). HPLC [Chiralpak AD-H,
V(
n-hexane)/
V(
i-PrOH)=95/5, 流速=1.0 mL/min,
λ=254 nm]:
tR=11.34 min (major), 13.97 min (minor). 表征数据与文献相同
[22].
(R,E)-N-(1,3-二苯基烯丙基)-4-(三氟甲氧基)苯胺(11aj): 淡黄色油状物, 67.4 mg, 产率91%, 94% ee. [α] -34.4 (c 1.5, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.37~7.26 (m, 6H), 7.26~7.19 (m, 3H), 7.18~7.13 (m, 1H), 6.96~6.86 (m, 2H), 6.60~6.45 (m, 3H), 6.29 (dd, J=15.9, 6.2 Hz, 1H), 4.96 (dd, J=6.2, 1.3 Hz, 1H), 4.10 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 145.9, 141.6, 140.7, 140.6, 136.4, 131.4, 130.2, 128.9, 128.6, 127.8, 127.7, 127.2, 126.5, 123.2, 122.3, 121.5, 119.8, 118.1, 113.8, 60.9; 19F NMR (377 MHz, CDCl3) δ: -58.4. HRMS calcd for C22H18ONF3Na [M+Na]+ 392.1233, found 392.1225. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=9.30 min (major), 12.52 min (minor).
(R,E)-3-((1,3-二苯基烯丙基)氨基)苯甲腈(11ak): 黄色油状物, 61.1 mg, 产率98%, 94% ee. [α] -45.5 (c 1.1, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.43~7.33 (m, 6H), 7.33~7.27 (m, 3H), 7.26~7.21 (m, 1H), 7.20~7.15 (m, 1H), 6.95 (d, J=7.5 Hz, 1H), 6.85~6.77 (m, 2H), 6.60 (dd, J=15.9, 1.3 Hz, 1H), 6.35 (dd, J=15.9, 6.1 Hz, 1H), 5.10~5.02 (m, 1H), 4.35 (d, J=5.0 Hz, 1H); 13C NMR (101 MHz, CDCl3) δ: 147.3, 140.9, 136.2, 131.7, 129.8, 129.4, 129.0, 128.6, 127.9, 127.1, 126.5, 121.1, 119.4, 117.8, 115.9, 112.8, 60.3. HRMS calcd for C22H18N2Na [M+Na]+ 333.1362, found 333.1353. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=85/15, 流速=1.0 mL/min, λ=254 nm]: tR=14.63 min (major), 20.61 min (minor).
(
R,
E)-3-氯-
N-(1,3-二苯基烯丙基)苯胺(
11al): 淡黄色油状物, 60.2 mg, 产率94%, 95%
ee. [
α] -64.1 (
c 0.78, CH
2Cl
2);
1H NMR (600 MHz, CDCl
3)
δ: 7.35~7.31 (m, 2H), 7.30~7.25 (m, 4H), 7.25~7.18 (m, 3H), 7.17~7.13 (m, 1H), 6.95 (t,
J=8.0 Hz, 1H), 6.58 (ddd,
J=7.9, 2.0, 0.9 Hz, 1H), 6.56~6.50 (m, 2H), 6.41 (ddd,
J=8.2, 2.3, 0.9 Hz, 1H), 6.28 (dd,
J=15.8, 6.1 Hz, 1H), 4.98 (d,
J=6.1 Hz, 1H), 4.10 (s, 1H). HPLC [Chiralpak OD-H,
V(
n-hexane)/
V(
i-PrOH)=90/10, 流速=1.0 mL/min,
λ=254 nm]:
tR=13.79 min (minor), 23.04 min (major). 表征数据与文献相同
[14h].
(R,E)-N-(1,3-二苯基烯丙基)吡啶-3-胺(11am): 黄色油状物, 43.3 mg, 产率76%, 93% ee. [α] -48.1 (c 0.81, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 8.01 (d, J=2.9 Hz, 1H), 7.88 (dd, J=4.7, 1.4 Hz, 1H), 7.37~7.33 (m, 2H), 7.32~7.25 (m, 4H), 7.25~7.19 (m, 3H), 7.19~7.14 (m, 1H), 6.95 (dd, J=8.3, 4.7 Hz, 1H), 6.79 (ddd, J=8.3, 2.9, 1.4 Hz, 1H), 6.54 (dd, J=15.8, 1.3 Hz, 1H), 6.30 (dd, J=15.9, 6.2 Hz, 1H), 5.02~4.98 (m, 1H), 4.13 (d, J=4.9 Hz, 1H); 13C NMR (101 MHz, CDCl3) δ: 143.1, 141.2, 139.1, 136.9, 136.3, 131.5, 129.8, 129.0, 128.6, 127.9, 127.8, 127.1, 126.5, 123.6, 119.3, 60.3. HRMS calcd for C20H18N2Na [M+Na]+ 309.1362, found 309.1362. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=90/10, 流速=1.0 mL/min, λ=254 nm]: tR=20.80 min (minor), 26.11 min (major).
(R,E)-N-(1,3-二苯基烯丙基)二苯并[b,d]呋喃-1-胺(11an): 淡黄色油状物, 73.0 mg, 产率97%, 93% ee. [α] -6.9 (c 1.4, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.78 (dd, J=7.6, 1.3 Hz, 1H), 7.59~7.49 (m, 3H), 7.44~7.36 (m, 5H), 7.34~7.27 (m, 4H), 7.25~7.19 (m, 2H), 6.98 (d, J=8.1 Hz, 1H), 6.71 (dd, J=15.8, 1.3 Hz, 1H), 6.55~6.47 (m, 2H), 5.34 (d, J=6.2 Hz, 1H), 4.81 (s, 1H); 13C NMR (101 MHz, CDCl3) δ: 157.1, 155.3, 143.4, 141.7, 136.5, 131.6, 130.4, 129.0, 128.6, 128.4, 127.8, 127.7, 127.1, 126.6, 125.5, 123.9, 122.5, 120.3, 111.4, 110.7, 105.7, 101.4, 60.6. HRMS calcd for C27H21ONNa [M+Na]+: 398.1515, found 398.1509. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=97/3, 流速=1.0 mL/min, λ=254 nm]: tR=7.37 min (minor), 8.39 min (major).
(R,E)-N-(1,3-二苯基烯丙基)萘-1-胺(11ao): 黄色油状物, 66.5 mg, 产率99%, 94% ee. [α] -48.7 (c 2.2, CH2Cl2); 1H NMR (400 MHz, CDCl3) δ: 7.86~7.79 (m, 1H), 7.76~7.69 (m, 1H), 7.46~7.40 (m, 2H), 7.40~7.34 (m, 2H), 7.34~7.27 (m, 4H), 7.26~7.19 (m, 3H), 7.18~7.12 (m, 3H), 6.61 (dd, J=15.9, 1.2 Hz, 1H), 6.51 (dd, J=6.1, 2.5 Hz, 1H), 6.43 (dd, J=15.8, 6.2 Hz, 1H), 5.19 (d, J=6.2 Hz, 1H), 4.72 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 142.1, 141.9, 136.6, 134.2, 131.4, 130.6, 128.9, 128.7, 128.6, 127.7, 127.6, 127.2, 126.6, 126.5, 125.7, 124.8, 123.5, 119.9, 117.7, 106.3, 60.8. HRMS calcd for C25H21NNa [M+Na]+ 358.1566, found 358.1566. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=8.05 min (major), 9.75 min (minor).
(R,E)-N-(1,3-二苯基烯丙基)蒽-1-胺(11ap): 黄绿色油状物, 70.6 mg, 产率92%, 88% ee. [α] -26.9 (c 1.2, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 8.43 (s, 1H), 8.35 (s, 1H), 8.06~7.91 (m, 2H), 7.56~7.52 (m, 2H), 7.46~7.35 (m, 7H), 7.33~7.27 (m, 3H), 7.26~7.20 (m, 2H), 6.70 (d, J=15.6 Hz, 1H), 6.59~6.46 (m, 2H), 5.33 (d, J=6.3 Hz, 1H), 4.99 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 141.8, 141.7, 136.6, 132.5, 131.53, 131.52, 130.9, 130.5, 128.9, 128.6, 128.4, 127.8, 127.7, 127.3, 126.7, 126.6, 126.1, 125.5, 125.1, 123.7, 118.5, 117.9, 104.3, 60.9. HRMS calcd for C29H23NNa [M+Na]+ 408.1723, found 408.1733. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm): tR=11.91 min (minor), 16.26 min (major).
(R,E)-N-(1,3-二对甲苯基烯丙基)苯胺(11ba): 淡黄色油状物, 55.4 mg, 产率88%, 86% ee. [α] -27.2 (c 0.94, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.33~7.29 (m, 2H), 7.26~7.23 (m, 2H), 7.17~7.08 (m, 6H), 6.70~6.66 (m, 1H), 6.63~6.60 (m, 2H), 6.57 (dd, J=15.8, 1.3 Hz, 1H), 6.32 (dd, J=15.8, 6.2 Hz, 1H), 5.02 (dd, J=6.2, 1.3 Hz, 1H), 4.07 (s, 1H), 2.33 (s, 3H), 2.31 (s, 3H); 13C NMR (151 MHz, CDCl3) δ: 147.3, 139.2, 137.4, 137.1, 133.9, 130.7, 129.9, 129.4, 129.2, 129.1, 127.1, 126.4, 117.5, 113.6, 60.4, 21.2, 21.1. HRMS calcd for C23H22N [M-H]+ 312.1747, found 312.1746. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=11.11 min (major), 13.75 min (minor).
(R,E)-N-(1,3-二间甲苯基烯丙基)苯胺(11ca): 淡黄色油状物, 57.4 mg, 产率92%, 84% ee. [α] -29.5 (c 1.3, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.26~7.21 (m, 3H), 7.20~7.16 (m, 3H), 7.15~7.12 (m, 2H), 7.09 (d, J=7.1 Hz, 1H), 7.04 (d, J=7.1 Hz, 1H), 6.70 (dd, J=7.4, 7.4 Hz, 1H), 6.66~6.54 (m, 3H), 6.37 (dd, J=15.8, 6.2 Hz, 1H), 5.02 (dd, J=6.1, 1.4 Hz, 1H), 4.09 (s, 1H), 2.35 (s, 3H), 2.31 (s, 3H); 13C NMR (151 MHz, CDCl3) δ: 147.4, 142.1, 138.5, 138.1, 136.6, 130.9, 130.6, 129.1, 128.7, 128.43, 128.39, 128.3, 127.9, 127.2, 124.3, 123.7, 117.6, 113.6, 60.7, 21.5, 21.3. HRMS calcd for C23H22N [M-H]+ 312.1747, found 312.1746. HPLC [Chiralpak OD-H, V(n-hexane)/V(i-PrOH)=90/10, 流速=1.0 mL/min, λ=254 nm]: tR=9.55 min (minor), 11.49 min (major).
(R,E)-N-(1,3-双(3-甲氧基苯基)烯丙基)苯胺(11da): 无色油状物, 48.9 mg, 产率71%, 91% ee. [α] -36.4 (c 0.75, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.27 (dd, J=7.9, 7.9 Hz, 1H), 7.20 (dd, J=7.9, 7.9 Hz, 1H), 7.16-7.12 (m, 2H), 7.02 (d, J=7.6 Hz, 1H), 6.99~6.97 (m, 1H), 6.95 (d, J=7.6 Hz, 1H), 6.90~6.88 (m, 1H), 6.82 (dd, J=8.2, 2.6 Hz, 1H), 6.78 (dd, J=8.2, 2.6 Hz, 1H), 6.70 (t, J=7.3 Hz, 1H), 6.65~6.61 (m, 2H), 6.59 (dd, J=15.9, 1.3 Hz, 1H), 6.37 (dd, J=15.8, 6.2 Hz, 1H), 5.04 (d, J=6.2 Hz, 1H), 4.11 (s, 1H), 3.79 (d, J=3.0 Hz, 6H); 13C NMR (151 MHz, CDCl3) δ: 160.0, 159.8, 147.2, 143.8, 138.1, 131.0, 130.9, 129.8, 129.5, 129.1, 119.5, 119.2, 117.7, 113.6, 113.5, 112.9, 112.8, 111.7, 60.7, 55.21, 55.20. HRMS calcd for C23H22NO2 [M-H]+ 344.1645, found 344.1646. HPLC [Chiralpak IC-H, V(n-hexane)/V(i-PrOH)=99/1, 流速=1.0 mL/min, λ=254 nm]: tR=18.73 min (major), 22.26 min (minor).
(R,E)-N-(1,3-双(4-氟苯基)烯丙基)苯胺(11ea): 无色油状物, 57.2 mg, 产率89%, 83% ee. [α] -34.7 (c 1.8, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.38 (dd, J=8.4, 5.4 Hz, 2H), 7.31 (dd, J=8.5, 5.4 Hz, 2H), 7.14 (dd, J=7.7, 7.7 Hz, 2H), 7.07~7.01 (m, 2H), 6.98 (t, J=8.4 Hz, 2H), 6.71 (dd, J=7.3, 7.3 Hz, 1H), 6.60 (d, J=8.0 Hz, 2H), 6.54 (d, J=15.8 Hz, 1H), 6.27 (dd, J=15.8, 6.2 Hz, 1H), 5.05 (d, J=6.2 Hz, 1H), 4.06 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 163.2, 162.9, 161.6, 161.3, 146.9, 137.7, 137.6, 132.62, 132.60, 130.2, 130.21, 130.19, 130.16, 129.18, 128.8, 128.7, 128.1, 128.0, 117.9, 115.7, 115.59, 115.55, 115.4, 113.6, 59.9; 19F NMR (565 MHz, CDCl3) δ: -114.0, -115.0. HRMS calcd for C21H16F2N [M-H]+ 320.1245, found 320.1244. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=13.31 min (major), 19.30 min (minor).
(R,E)-N-(1,3-双(4-氯苯基)烯丙基)苯胺(11fa): 无色油状物, 62.8 mg, 产率89%, 93% ee. [α] -41.6 (c 1.2, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.37~7.31 (m, 4H), 7.29~7.22 (m, 4H), 7.16~7.12 (m, 2H), 6.72 (dd, J=7.3, 7.3 Hz, 1H), 6.61-6.56 (m, 2H), 6.53 (dd, J=15.8, 1.4 Hz, 1H), 6.32 (dd, J=15.8, 6.3 Hz, 1H), 5.06~5.02 (m, 1H), 4.07 (br, 1H); 13C NMR (151 MHz, CDCl3) δ: 146.8, 140.3, 134.9, 133.5, 133.3, 130.8, 130.4, 129.2, 129.0, 128.7, 128.5, 127.7, 118.1, 113.6, 60.0. HRMS calcd for C21H16Cl2N [M-H]+ 352.0654, found 352.0652. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=16.29 min (major), 23.86 min (minor).
(R,E)-N-(1,3-二(萘-1-基)烯丙基)苯胺(11ga): 无色油状物, 66.4 mg, 产率86%, 97% ee. [α] -25.2 (c 2.5, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 8.21~8.17 (m, 1H), 7.93~7.90 (m, 1H), 7.87 (d, J=8.3 Hz, 1H), 7.85~7.79 (m, 2H), 7.76~7.72 (m, 2H), 7.60 (d, J=7.2 Hz, 1H), 7.55~7.49 (m, 2H), 7.49~7.45 (m, 2H), 7.45~7.42 (m, 2H), 7.42~7.39 (m, 1H), 7.20~7.16 (m, 2H), 6.79~6.69 (m, 3H), 6.57 (dd, J=15.7, 5.2 Hz, 1H), 5.93 (d, J=5.2 Hz, 1H), 4.28 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 147.3, 137.0, 134.7, 134.2, 133.5, 132.9, 131.25, 131.17, 129.5, 129.3, 129.0, 128.5, 128.4, 128.0, 126.5, 126.0, 125.77, 125.75, 125.6, 125.5, 125.0, 123.9, 123.8, 123.5, 117.7, 113.4, 56.7. HRMS calcd for C29H22N [M-H]+ 384.1747, found 384.1743. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=8.30 min (major), 11.96 min (minor).
(R,E)-N-(1,3-二(噻吩-3-基)烯丙基)苯胺(11ha): 淡黄色油状物, 55.7 mg, 产率94%, 88% ee. [α] -26.8 (c 1.3, CH2Cl2); 1H NMR (600 MHz, CDCl3) δ: 7.31 (dd, J=5.0, 3.0 Hz, 1H), 7.27~7.22 (m, 2H), 7.20 (dd, J=5.1, 1.3 Hz, 1H), 7.18~7.14 (m, 2H), 7.13~7.12 (m, 1H), 7.10 (dd, J=5.0, 1.3 Hz, 1H), 6.71 (dd, J=7.4, 7.4 Hz, 1H), 6.67~6.59 (m, 3H), 6.25 (dd, J=15.8, 6.1 Hz, 1H), 5.15 (d, J=6.1 Hz, 1H), 4.04 (s, 1H); 13C NMR (151 MHz, CDCl3) δ: 147.1, 143.3, 139.2, 130.0, 129.2, 126.8, 126.3, 126.1, 125.3, 125.0, 122.4, 121.8, 117.8, 113.5, 56.1. HRMS calcd for C17H14NS2 [M-H]+ 296.0562, found 296.0562. HPLC [Chiralpak AD-H, V(n-hexane)/V(i-PrOH)=95/5, 流速=1.0 mL/min, λ=254 nm]: tR=17.02 min (major), 21.82 min (minor).
辅助材料(Supporting Information) 化合物
3~
5、
L3、
11aa~
11ha的NMR谱图, 以及化合物
4、
L1~
L4的氧化物,
11aa~
11ha的HPLC谱图. 这些材料可以免费从本刊网站(
http://sioc-journal.cn/)上下载.