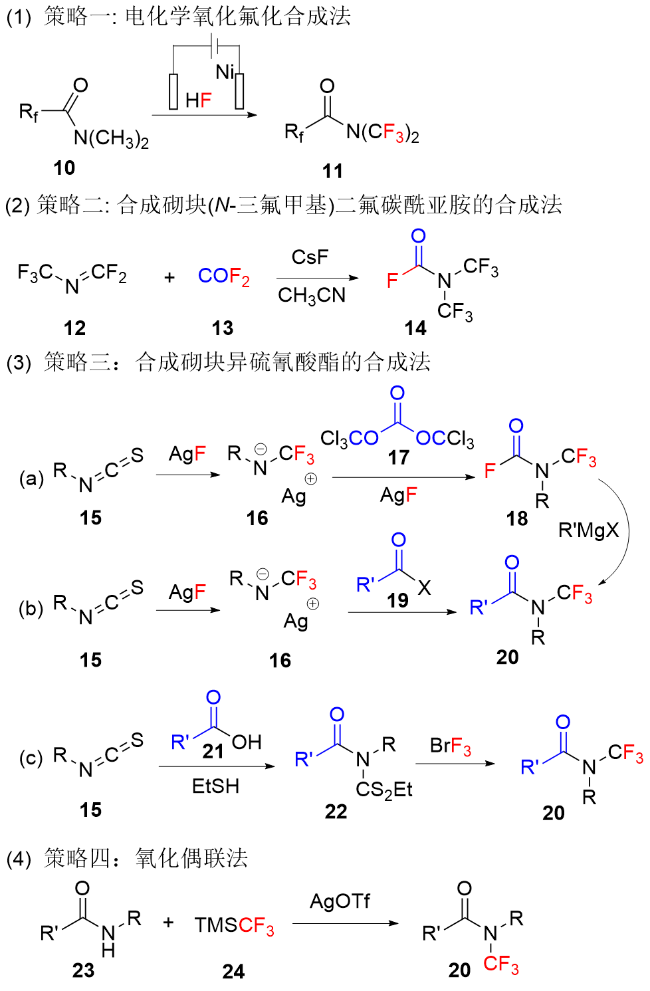
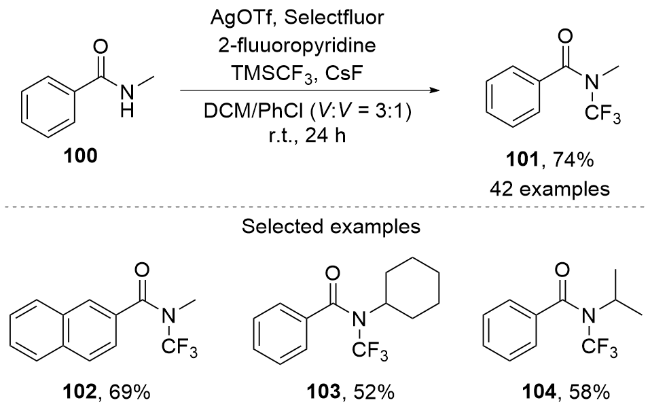
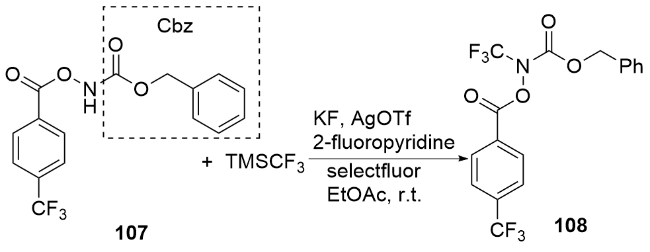
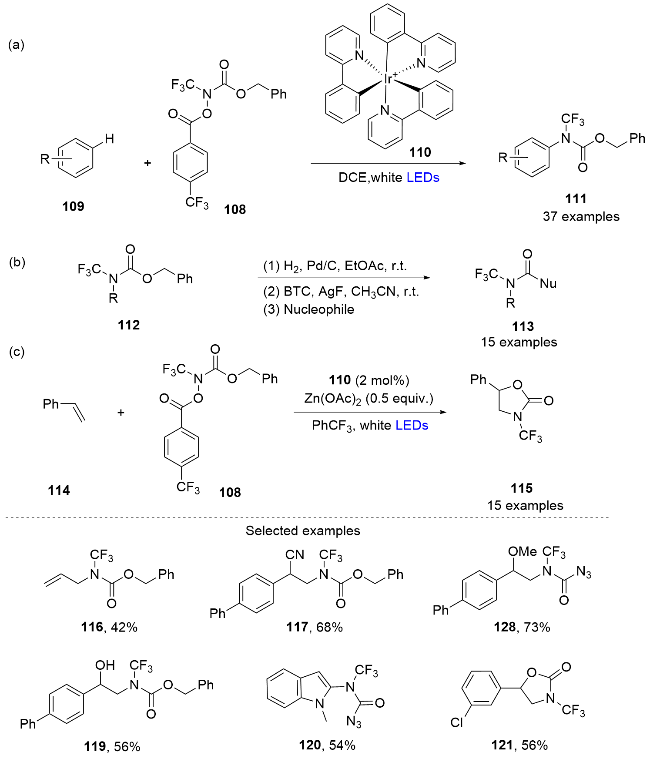
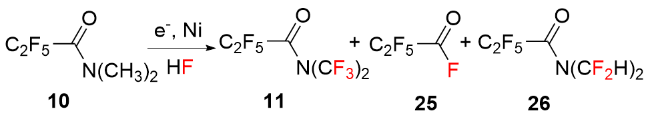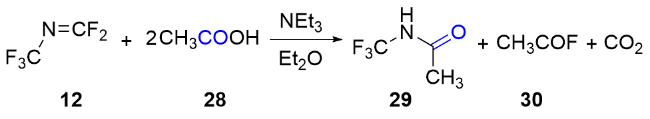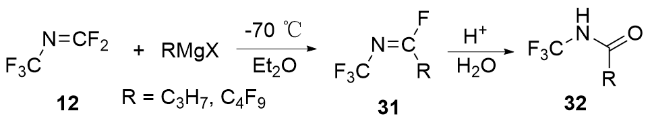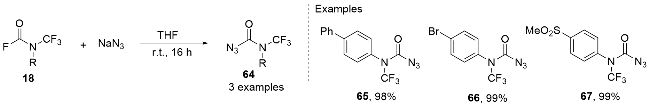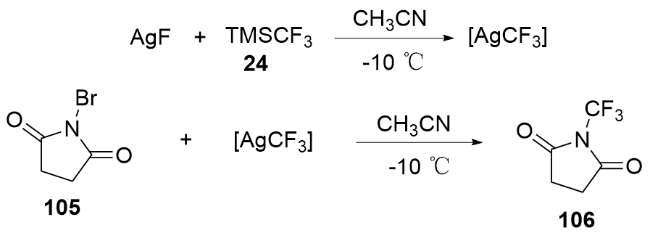1 对C—H键电化学氧化氟化合成法
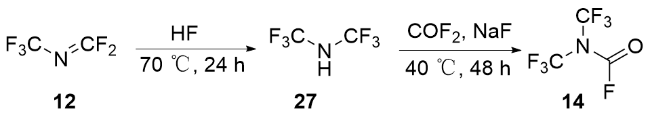
2 采用合成砌块(N-三氟甲基)二氟碳酰亚胺的合成法
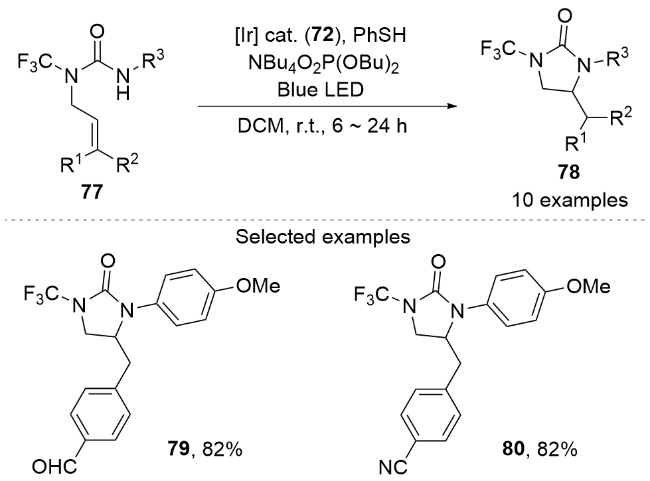
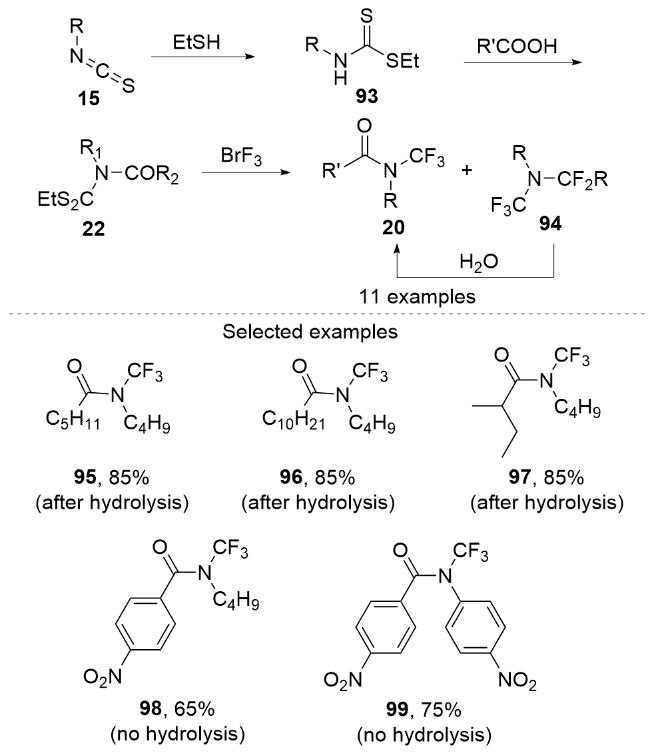
3 采用异硫氰酸酯作为原料合成N-三氟甲基酰胺及其衍生物
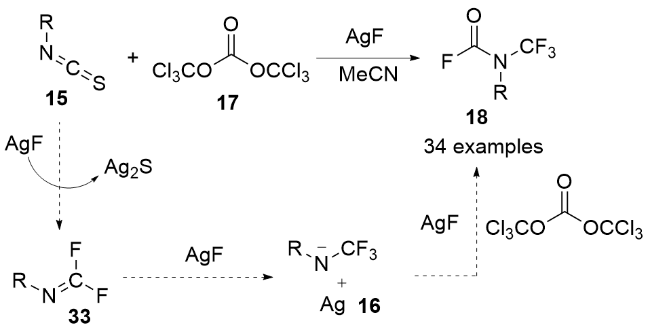
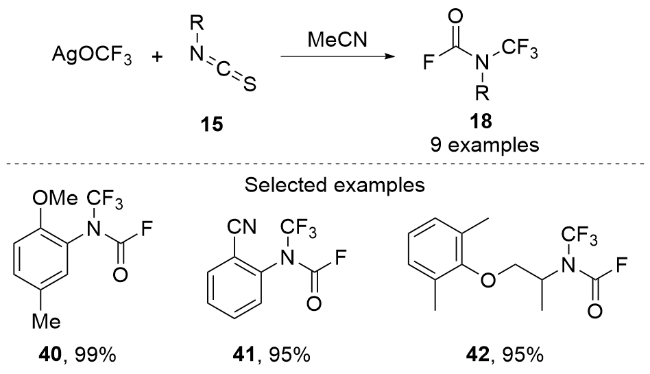
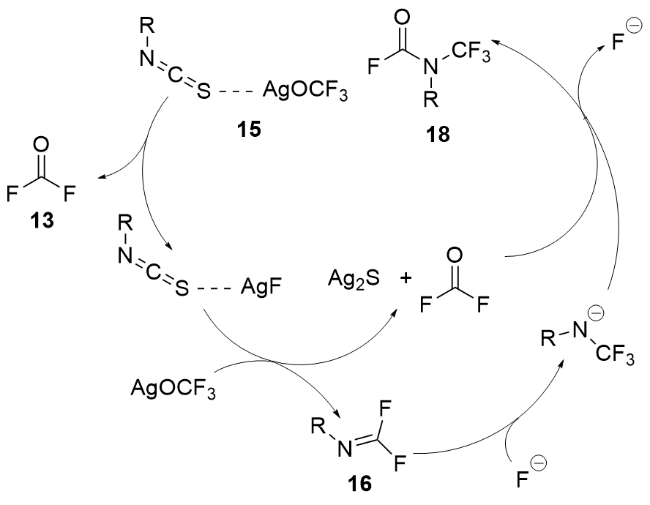
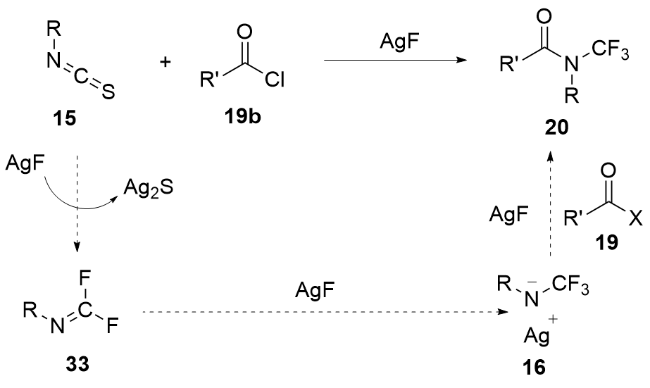
3.1 经历关键中间体N-三氟甲基氨基甲酰氟的合成法
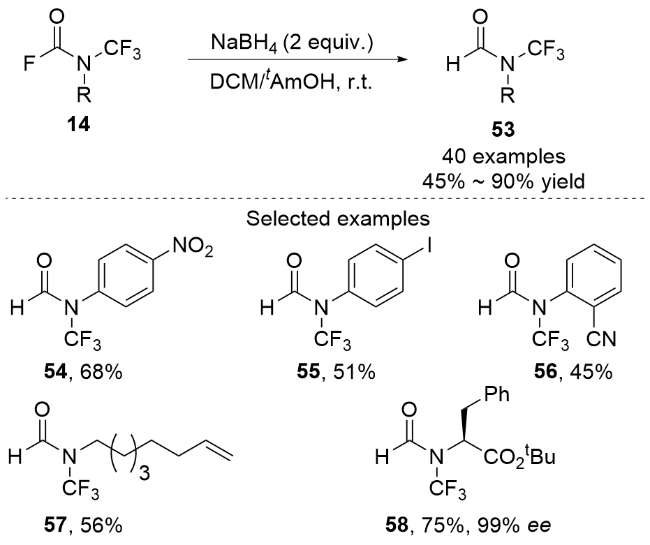
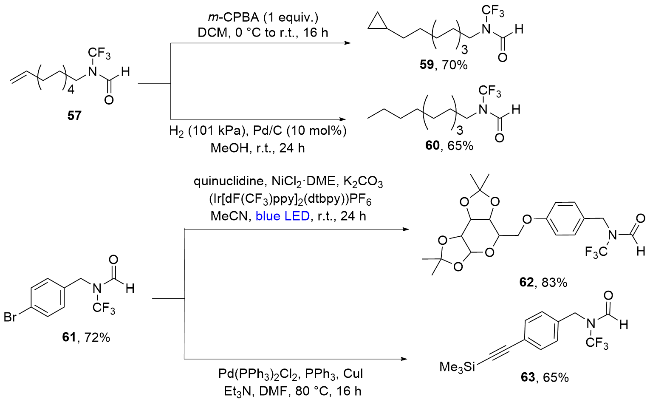
图式10 通过中间体AgOCF3制备N-三氟甲基甲酰氟的合成法Scheme 10 Synthetic method of N-trifluoromethyl formyl fluorides from intermediate AgOCF3 |
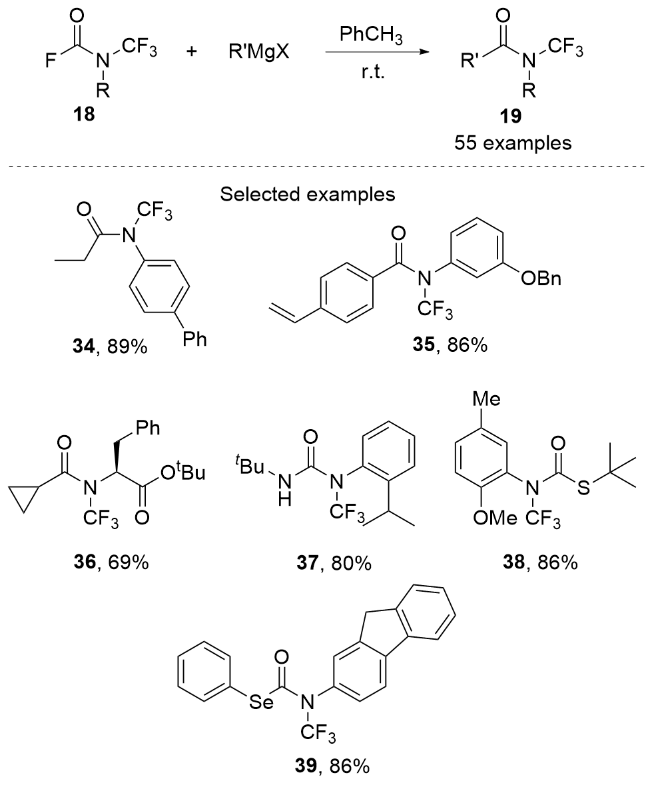
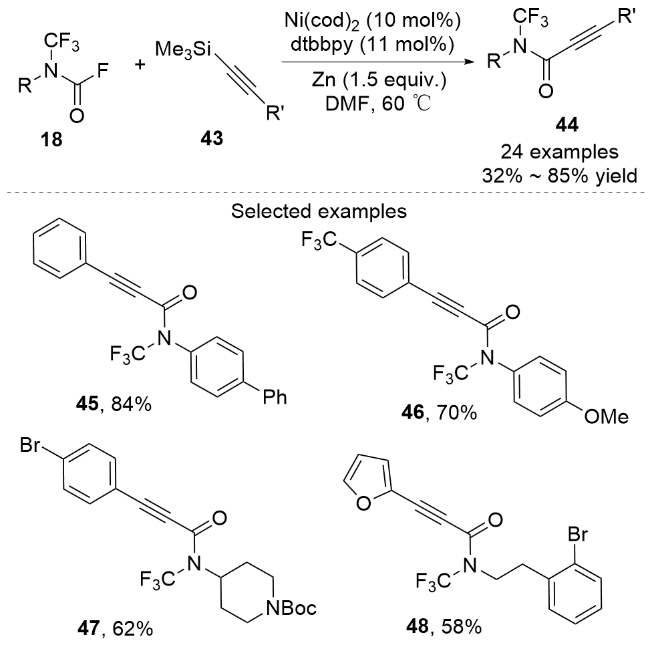
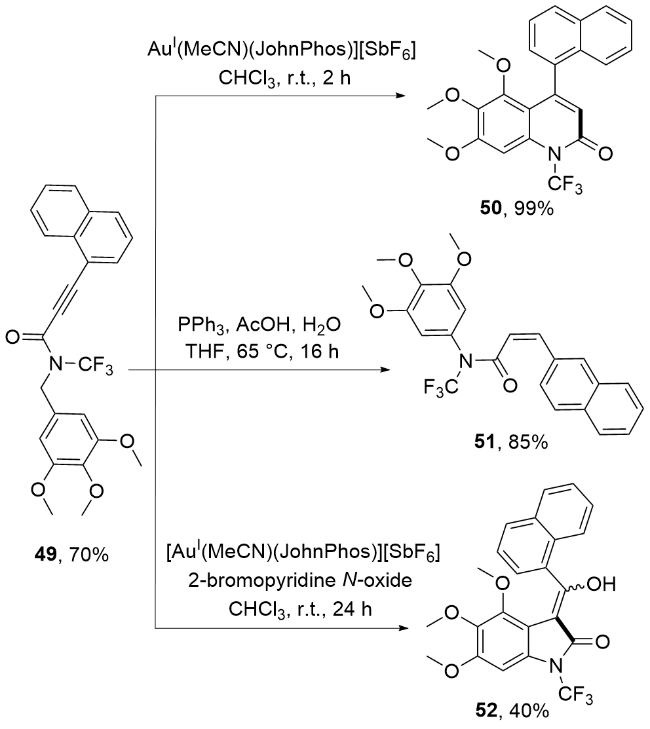
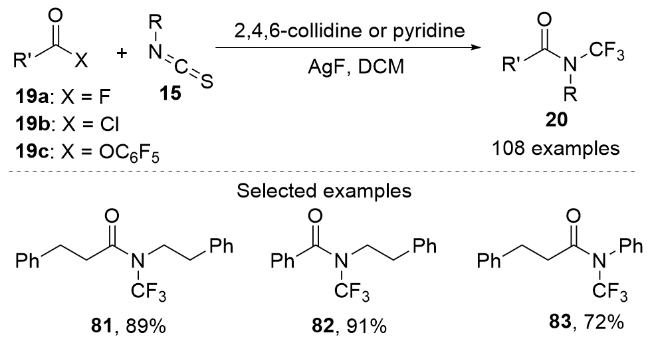
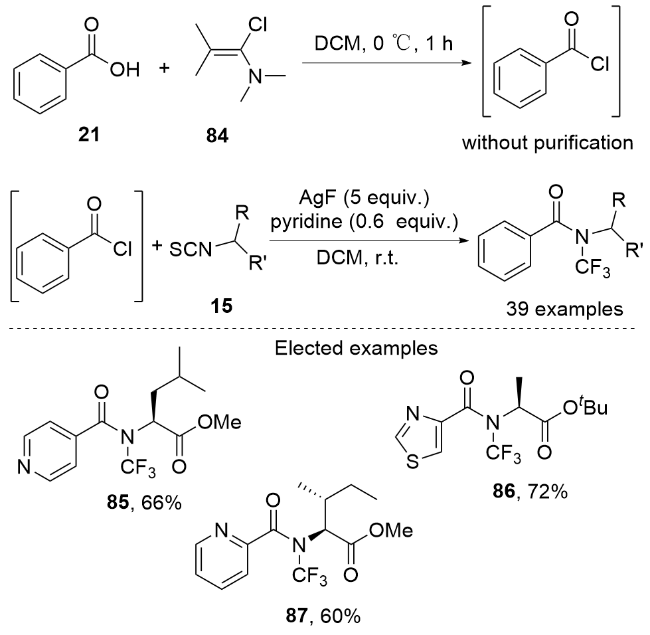
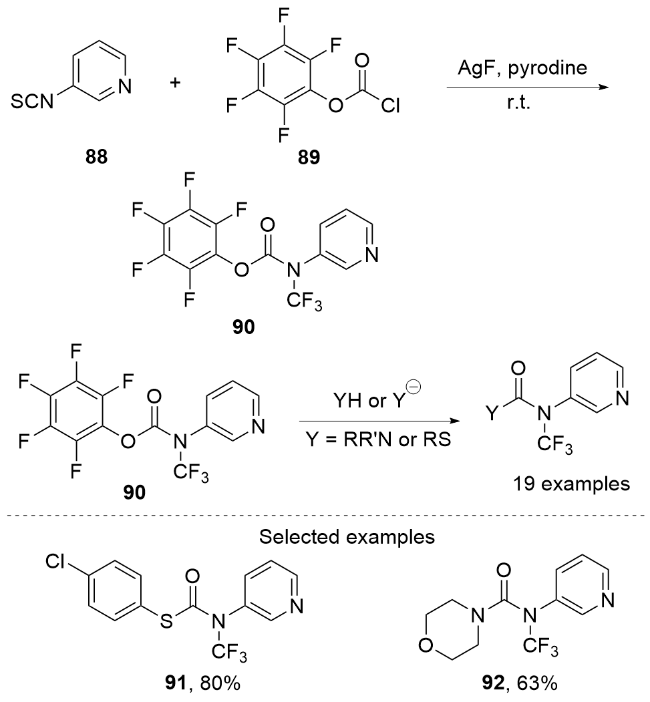
3.2 经历关键中间体N-三氟甲基胺基银与酰氯衍生物反应的合成法
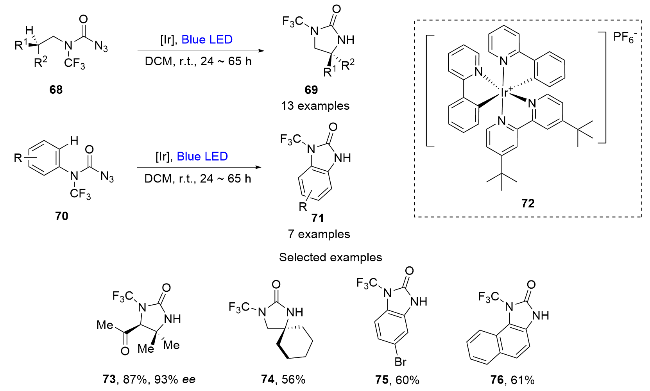
图式19 通过中间体N-三氟甲基胺基银与酰卤反应合成N-三氟甲基酰胺Scheme 19 Synthesizing N-trifluoromethylamides by the reactions between the intermediate N-trifluoromethylamine silvers and the acyl halide derivatives |