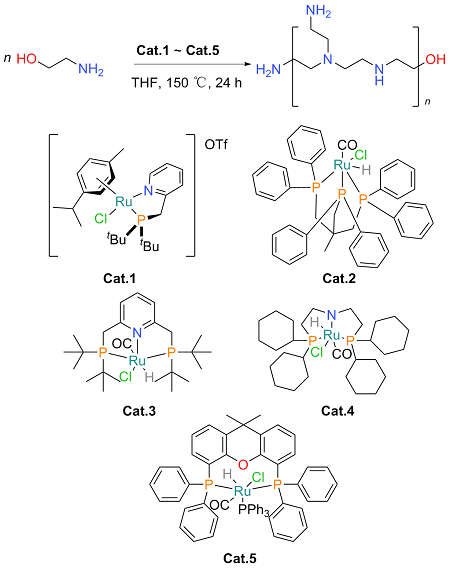
催化剂
Cat.1根据文献[
38]方法制备. 在手套箱中, 将2-(二叔丁基膦基甲基)吡啶(237.00 mg, 1.00 mmol) 溶解在5 mL二氯甲烷中备用. 在另一个装有磁子的50 mL三口瓶中, 将二氯(对甲基异丙基苯基)钌(II)二聚体(310.00 mg, 0.50 mmol)和三氟甲磺酸钠(330.00 mg, 1.90 mmol)悬浮于10 mL二氯甲烷中. 剧烈搅拌悬浮液, 然后将上述含2-(二叔丁基膦基甲基)吡啶的二氯甲烷溶液缓慢滴加至反应瓶中, 搅拌1 h. 过滤溶液以除去氯化钠和过量的三氟甲磺酸钠, 滤饼用10 mL乙醚洗涤. 真空干燥得到[(
η6-cymene)RuCl(PyCH
2P
tBu
2)]OTf (
Cat.1), 橙黄色固体, 480 mg, 收率73%.
1H NMR (500 MHz, Chloroform-
d)
δ: 8.98 (dd,
J=5.9, 1.6 Hz, 1H), 7.89 (td,
J=7.7, 1.7 Hz, 1H), 7.75 (d,
J=7.7 Hz, 1H), 7.40 (s, 1H), 6.14 (dd,
J=5.9, 1.2 Hz, 1H), 6.05~6.00 (m, 1H), 5.78 (dd,
J=6.0, 1.2 Hz, 1H), 4.83 (dd,
J=5.9, 1.1 Hz, 1H), 4.50 (t,
J=17.0 Hz, 1H), 3.95 (dd,
J=16.4, 1.9 Hz, 1H), 3.08 (hept,
J=6.9 Hz, 1H), 1.72 (s, 3H), 1.54 (d,
J=14.6 Hz, 9H), 1.45 (d,
J=6.9 Hz, 3H), 1.39 (d,
J=6.9 Hz, 3H), 0.80 (d,
J=14.9 Hz, 9H);
13C NMR (126 MHz, CDCl
3)
δ: 157.19, 139.86, 128.74, 124.20, 119.49, 100.32, 98.90, 79.13, 73.79, 36.35, 36.66, 33.48, 31.14, 26.84, 23.62, 21.47, 17.60;
31P NMR (202 MHz, CDCl
3)
δ: 76.31;
19F NMR (471 MHz, CDCl
3)
δ: -78.12.