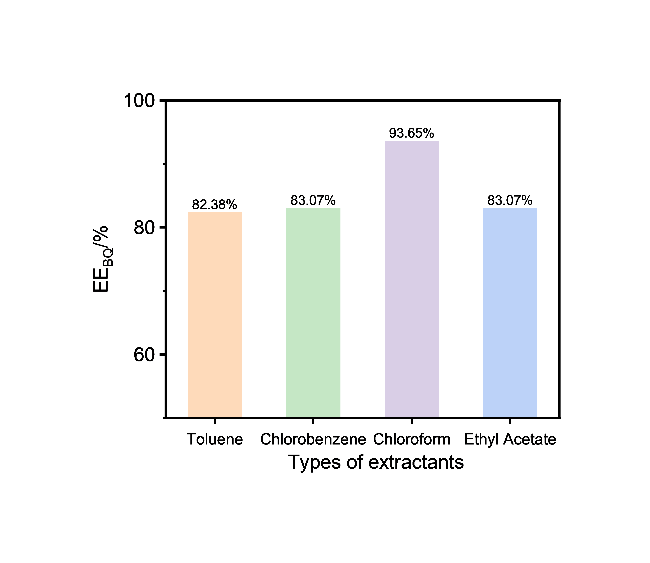对苯二酚(Hydroquinone)作为重要的芳香族二元酚化合物, 在染料、医药、化妆品及高分子合成等领域具有广泛的应用
[1-4]. 据统计, 全球对苯二酚市场规模在2023年约为12亿至15亿美元, 受益于橡胶防老剂、显影剂、医药中间体等传统需求以及新能源电池等新兴领域的推动, 预计到2030年, 市场规模将以年均5%的速度增长至16亿至20亿美元. 当前对苯二酚工业化生产以苯酚羟基化法
[5-7]为主, 占总产能约50%. 然而该工艺存在对苯二酚选择性低
[8-13], 催化剂循环稳定性差, 以及高浓度过氧化氢存在分解风险
[14-21]等问题. 虽然对二异丙苯法
[22]在工艺路线上具有一定替代潜力, 但其经济性受到丙酮市场波动和石油基原料供应的制约, 且面临较大的环境压力. 苯胺氧化法
[23]因原料成本低、产品质量高曾被广泛采用, 但其在生产过程中产生大量含重金属的废液, 环境污染严重, 目前正在逐步被淘汰. 因此, 开发一种绿色环保、高效节能的对苯二酚生产工艺具有重要的意义.
有机电合成以电子直接驱动反应为核心机制, 具备原子经济性高, 无需有毒氧化剂和还原剂, 反应条件温和等显著优势, 根本上契合绿色合成理念. 此外, 有机电合成模块化设计与可再生能源如风电、光伏的结合, 为化工行业实现低碳化、低能耗、近零排放提供了革新路径. 因此, 利用电子作为清洁氧化还原剂, 为对苯二酚的绿色合成开辟了新的技术路线
[24-26].
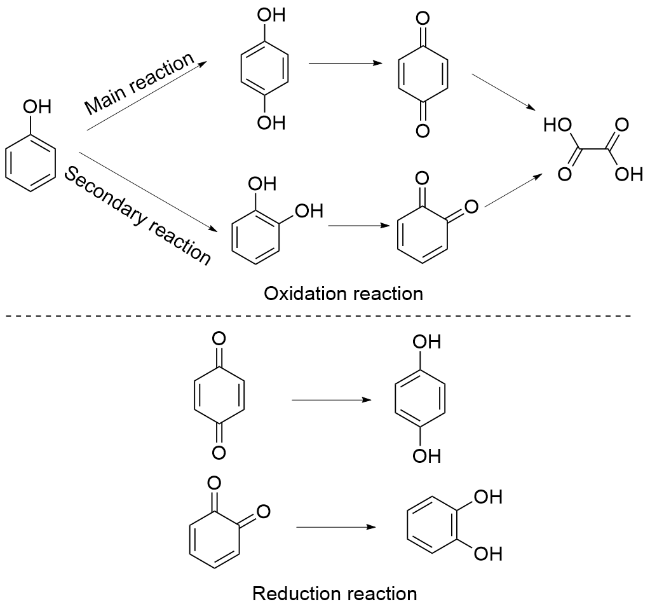
近年来, 成对电合成技术通过在同一电解池中耦合苯酚的阳极氧化与对苯醌的阴极还原反应, 显著提升了原子经济性与能量效率, 展现出突出的工业化应用潜 力
[27-31]. 本课题组
[30]报道了一种苯酚成对电解和刷新铅电极制备对苯二酚的方法, 在双室电解槽中制得对苯二酚的产率为77.4%, 对苯二酚浓度约为8 g/L. 该方法使用甲基异丁基酮(MIBK)分离对苯二酚, 电解液循环使用4次后, 对苯二酚产率降低至71%. Zhang等
[32]报道了在单室电解槽中苯酚成对电解制备对苯二酚的工作, 得到苯酚的转化率为94.5%和对苯二酚选择性为72.1%的实验结果, 对苯二酚浓度约为1.8 g/L. 尽管取得了这些进展, 但诸如此类电化学法合成对苯二酚的工业化应用仍受限于两大瓶颈问题
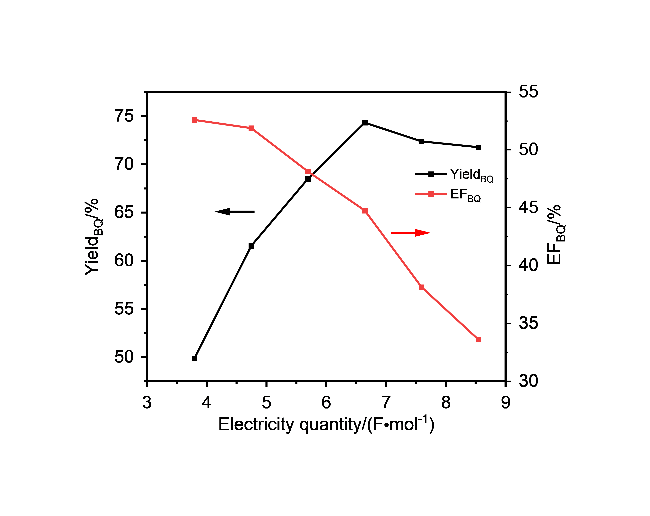
[31-35]: 一方面是电解液中对苯二酚浓度较低, 这归因于提高苯酚浓度会加剧电极钝化和对苯醌的过度氧化反应, 进而降低对苯二酚产率
[36-41]. 另一方面使用传统的酮类萃取剂(如甲基异丁基酮)分离对苯二酚, 电解液循环使用过程中会积累萃取剂, 进而导致对苯二酚的产率逐渐降低
[30]. 因此电解液需进一步处理以去除积累的萃取剂, 这增加了工艺复杂性和生产成本, 从而限制了该方法的工业化应用.
为解决上述问题, 本研究提出了一种循环萃取耦合电解的新型策略(
Scheme 1), 实现了电解液的可循环使用和对苯二酚的高效富集. 与传统成对电合成法合成对苯二酚
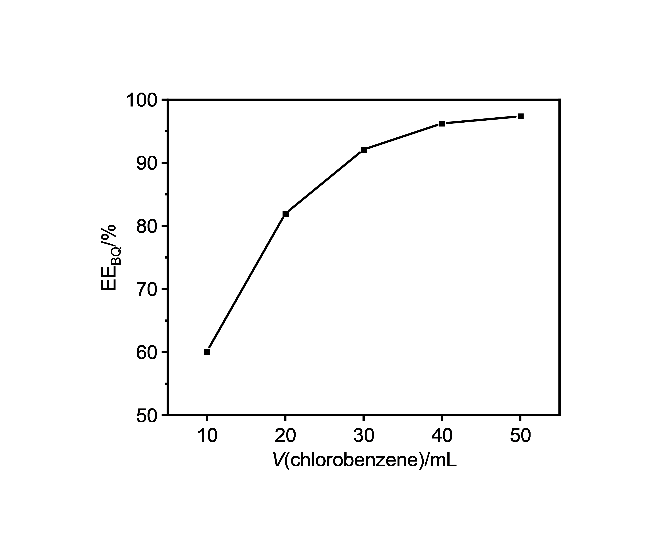
[30]相比, 一方面, 该策略采用了氯苯萃取分离阳极液中的对苯醌, 基于氯苯的低水溶性, 水相中残留的微量氯苯对苯酚电氧化反应的影响较小, 这一特性使得阳极液能够高效循环使用. 另一方面, 该策略创新性地构建了阳极液与阴极液独立循环体系, 循环使用阴极液可实现产物对苯二酚的高效富集. 此外, 通过简易的冷却结晶工艺可直接分离电解液中的对苯二酚, 从而提升整体的经济性与环境友好性. 综上所述, 该循环萃取耦合电解策略在电解液的可循环性、产品浓度提升及产品纯度方面均优于传统电化学方法, 为实现对苯二酚的绿色、高效生产提供了新的技术路径和理论支撑.