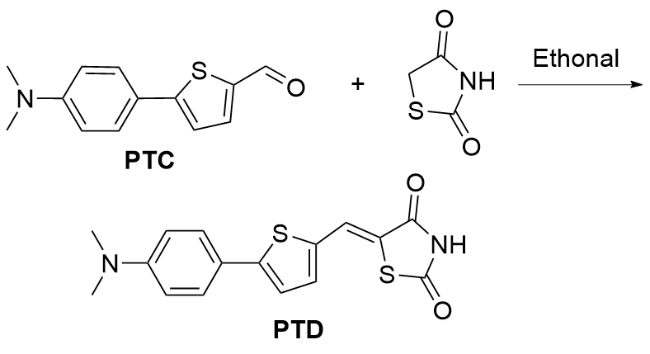
1 结果与讨论
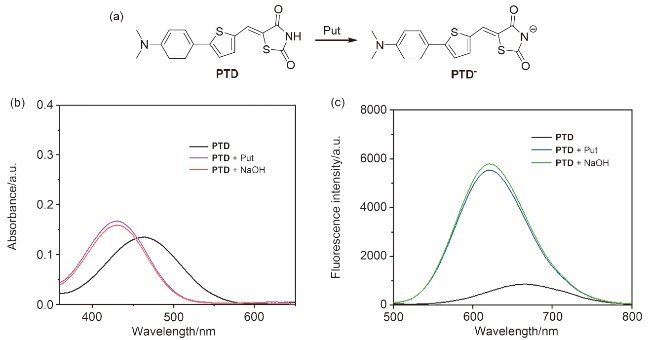
1.1 PTD对胺的紫外响应
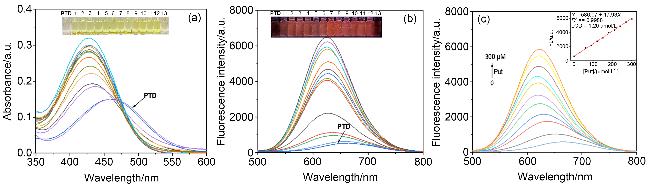
图1 (a) PTD溶液中加入不同胺的紫外-可见吸收光谱[内插图为日光颜色变化, 1: 色胺, 2: 氨水, 3: 二甲胺, 4: 三乙胺, 5: 乙胺, 6: 精胺, 7: 尸胺, 8: 酪胺, 9: 2-苯乙胺, 10: 二乙胺, 11: 三甲胺, 12: 腐胺(Put), 13: 苯胺)]; (b) PTD溶液中加入不同胺的荧光光谱(内插图为荧光变化); (c) PTD溶液中加入不同浓度腐胺后的荧光光谱[内插图为625 nm 波长下腐胺浓度(0~300 μmol/L)与荧光强度的线性关系图]Figure 1 (a) Ultraviolet-visible absorption spectra of different amines added to PTD solution (Inset: color changes of sunlight, 1: tryptamine, 2: ammonia water, 3: dimethylamine, 4: triethylamine, 5: ethylamine, 6: spermatine, 7: cothiamine, 8: tyramine, 9: 2-phenyl- ethylamine, 10: diethylamine, 11: trimethylamine, 12: putrescine (Put), 13: aniline); (b) fluorescence spectra of different amines added to PTD solution (Inset: fluorescence changes); (c) fluorescence spectra of PTD solution after adding different concentrations of putsamine (Inset: linear relationship graph between the concentration of putsamine (0~300 μmol/L) and fluorescence intensity at a wavelength of 625 nm) |
1.2 PTD对胺的荧光响应
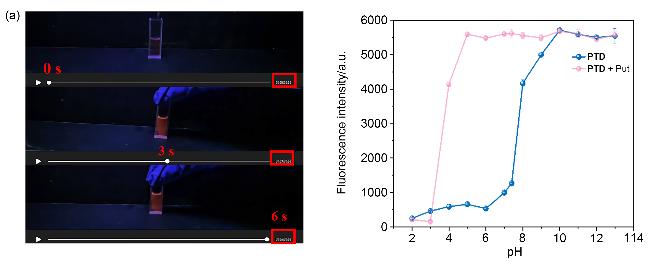
1.3 响应时间和pH对PTD性能的影响
1.4 PTD对生物胺的响应机理
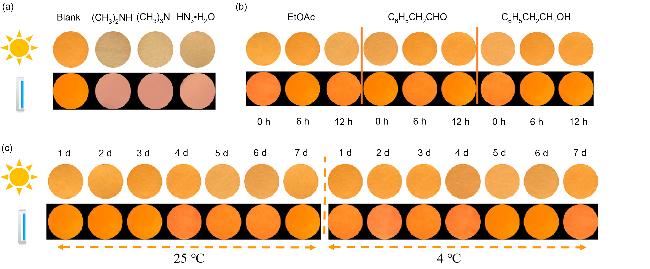
1.5 负载PTD的指示标签对胺的响应
1.6 风味物质、温度和时间对负载PTD的指示标签的影响
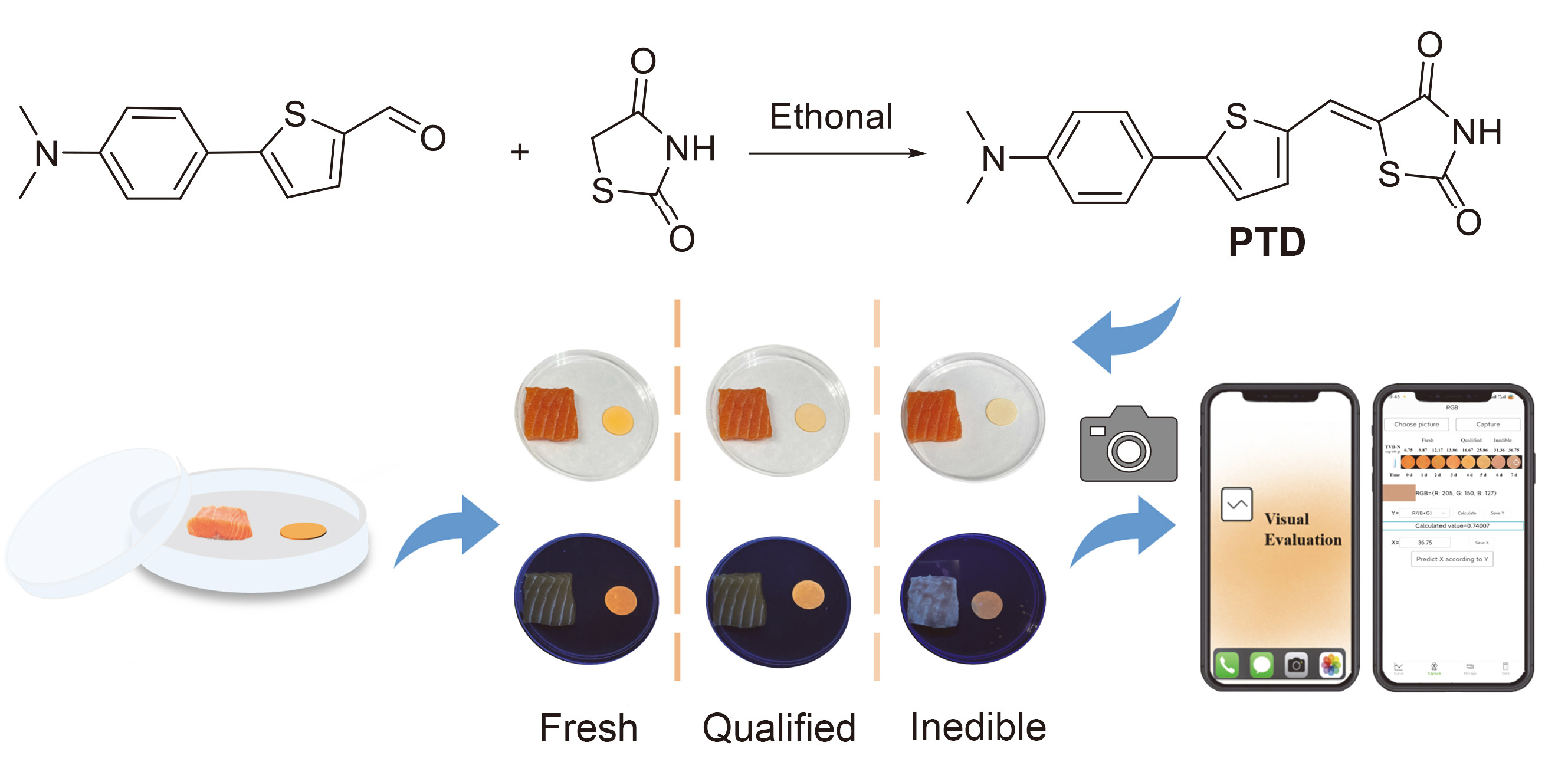
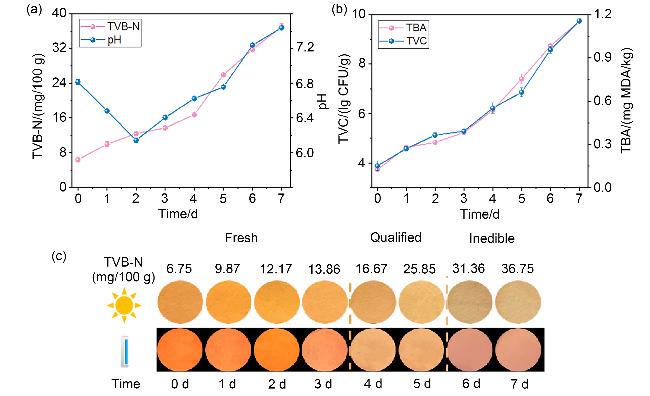
1.7 负载PTD的指示标签对三文鱼肉新鲜度的监测
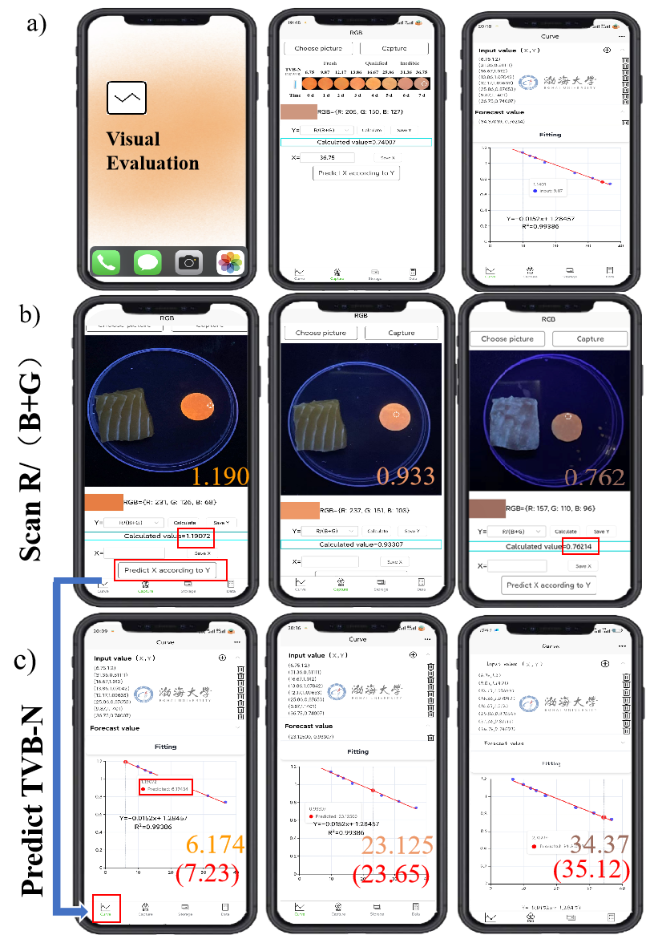
1.8 智能一体化平台对三文鱼肉新鲜度的监测与验证
图6 (a)智能手机VE软件示意图、智能手机的RGB提取功能及PTD指示标签的R/(B+G)值与三文鱼肉TVB-N含量的线性关系; (b)在25 ℃条件下智能手机软件提取三个时间节点的R/(B+G)值; (c)由图b得到的R/(B+G)值自动输出相应的TVB-N值, 并与国标法测出的TVB-N值(括号内的数值)进行对比验证Figure 6 (a) Schematic diagram of the VE software of the smart phone, RGB extraction function of the smart phone, and the linear relationship between the R/(B+G) value of the PTD indication label and the TVB-N content of salmon meat; (b) Under the condition of 25 ℃, the R/(B+G) values of the three time nodes extracted by the smart phone software; (c) TVB‑N values automatically output from the R/(B+G) values obtained from Figure B and compared and verified with those determined by the national standard method (the values in parentheses) |