

Baeyer-Villiger单加氧酶的蛋白质改造及其催化氧化反应研究新进展
收稿日期: 2018-10-19
修回日期: 2018-12-13
网络出版日期: 2018-12-28
基金资助
国家自然科学基金(Nos.21472169,21574113)资助项目.
Recent Developments in Protein Engineering and Catalytic Oxidations of Baeyer-Villiger Monooxygenase
Received date: 2018-10-19
Revised date: 2018-12-13
Online published: 2018-12-28
Supported by
Project supported by the National Natural Science Foundation of China (Nos.21472169,21574113).
Baeyer-Villiger单加氧酶(BVMO)作为一种重要的生物催化剂,可以催化各种有机酮/醛化合物的Baeyer-Villiger氧化反应,以及一些含硫、硒、硼等杂原子底物的氧化反应.Baeyer-Villiger单加氧酶催化的氧化反应具有选择性高、反应条件温和、高效等优点,已成为不可或缺的有机合成工具,被广泛应用于各种手性化合物的合成中.近年来利用生物信息学分析和基因挖掘技术,从众多微生物中找到了多种新型的BVMO·另外利用蛋白质工程技术对已知的野生型BVMO进行改造,从而扩大底物范围,提高热稳定性和反应活性,改善酶的立体、区域和化学选择性.这些都进一步扩大了Baeyer-Villiger单加氧酶催化氧化反应的应用范围.以不同底物结构的Baeyer Villiger氧化反应为主线,综述了近5年来国内外对野生型以及蛋白质工程改造的BVMO催化氧化反应研究的新进展.
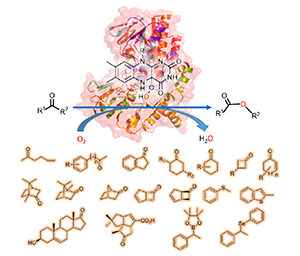
关键词: Baeyer-Villiger单加氧酶; Baeyer-Villiger氧化反应; 生物催化; 手性合成; 蛋白质改造
郑禾 , 周玉珂 , 林贤福 , 吴起 . Baeyer-Villiger单加氧酶的蛋白质改造及其催化氧化反应研究新进展[J]. 有机化学, 2019 , 39(4) : 903 -915 . DOI: 10.6023/cjoc201810023
Baeyer-Villiger monooxygenase (BVMO) is an important biocatalyst for Baeyer-Villiger oxidation of various organic ketone/aldehyde compounds, and sulfur, selenium, or boron-containing heteroatoms compounds. As an indispensable tool, BVMO-catalyzed oxidation displays some advantages, such as high selectivity, mild reaction conditions and high efficiency, leading to wide applications into the synthesis of chiral compounds. In recent years, bioinformatics analysis and genome mining have been used to find more novel BVMOs from microorganisms. Besides natural substrates, these BVMOs can accept various organic compounds showing wide substrate scope. Meanwhile, protein engineering has been widely used to improve the catalytic performance of BVMOs, such as the expanded substrate scope, high thermostability and activity, high stereo-, regio-and chemo-selectivities. Based on the Baeyer-Villiger oxidation reaction with different substrate structures, the recent advancements in the research on the catalytic oxidation of wild type and protein-engineered BVMOs in the past five years are summarized.

[1] Balke, K.; Kadow, M.; Mallin, H.; Sass, S.; Bornscheuer, U. T. Org. Biomol. Chem. 2012, 10, 6249.
[2] Leisch, H.; Morley, K.; Lau, P. C. Chem. Rev. (Washington, DC, U. S.) 2011, 111, 4165.
[3] (a) Dong, J.; Fernandez-Fueyo, E.; Hollmann, F.; Paul, C. E.; Pesic, M.; Schmidt, S.; Wang, Y.; Younes, S.; Zhang, W. Angew. Chem., Int. Ed. 2018, 57, 9238.
(b) Balke, K.; Beier, A.; Bornscheuer, U. T. Biotechnol. Adv. 2018, 36, 247.
(c) Liang, Y.; Wei, J.; Qiu, X.; Jiao, N. Chem. Rev. 2018, 118, 4912.
[4] Ceccoli, R. D.; Bianchi, D. A.; Fink, M. J.; Mihovilovic, M. D.; Rial, D. V. AMB Express 2017, 7, 87.
[5] Beneventi, E.; Niero, M.; Motterle, R.; Fraaije, M.; Bergantino, E. J. Mol. Catal. B:Enzym. 2013, 98, 145.
[6] Fiorentini, F.; Romero, E.; Fraaije, M. W.; Faber, K.; Hall, M.; Mattevi, A. ACS Chem Biol. 2017, 12, 2379.
[7] Fink, M. J.; Mihovilovic, M. D. Chem. Commun. (Cambridge, U. K.) 2015, 51, 2874.
[8] van Beek, H. L.; Romero, E.; Fraaije, M. W. ACS Chem Biol. 2017, 12, 291.
[9] Pereira, J. P. C.; van der Wielen, L. A. M.; Straathof, A. J. J. Bioresour. Technol. 2018, 256, 187.
[10] Carvalho, A. T. P.; Dourado, D.; Skvortsov, T.; de Abreu, M.; Ferguson, L. J.; Quinn, D. J.; Moody, T. S.; Huang, M. Phys. Chem. Chem. Phys. 2018, 20, 2558.
[11] Song, J. W.; Jeon, E. Y.; Song, D. H.; Jang, H. Y.; Bornscheuer, U. T.; Oh, D. K.; Park, J. B. Angew. Chem., Int. Ed. 2013, 52, 2534.
[12] Jeon, E.-Y.; Seo, J.-H.; Kang, W.-R.; Kim, M.-J.; Lee, J.-H.; Oh, D.-K.; Park, J.-B. ACS Catal. 2016, 6, 7547.
[13] Seo, E. J.; Yeon, Y. J.; Seo, J. H.; Lee, J. H.; Bongol, J. P.; Oh, Y.; Park, J. M.; Lim, S. M.; Lee, C. G.; Park, J. B. Bioresour. Technol. 2018, 251, 288.
[14] (a) Rehdorf, J.; Zimmer, C. L.; Bornscheuer, U. T. Appl. Environ. Microbiol. 2009, 75, 3106.
(b) Geitner, K.; Rehdorf, J.; Snajdrova, R.; Bornscheuer, U. T. Appl. Microbiol. Biotechnol. 2010, 88, 1087.
[15] Riebel, A.; Dudek, H. M.; de Gonzalo, G.; Stepniak, P.; Rychlewski, L.; Fraaije, M. W. Appl. Microbiol. Biotechnol. 2012, 95, 1479.
[16] Ferroni, F. M.; Smit, M. S.; Opperman, D. J. J. Mol. Catal. B:Enzym. 2014, 107, 47.
[17] (a) Fraaije, M. W.; Wu, J.; Heuts, D. P.; van Hellemond, E. W.; Spelberg, J. H.; Janssen, D. B. Appl. Microbiol. Biotechnol. 2005, 66, 393.
(b) de Gonzalo, G.; Mihovilovic, M. D.; Fraaije, M. W. ChemBioChem 2010, 11, 2208.
[18] Pazmino, D. E. T.; Snajdrova, R.; Rial, D. V.; Mihovilovic, M. D.; Fraaije, M. W. Adv. Synth. Catal. 2007, 349, 1361.
[19] Dudek, H. M.; de Gonzalo, G.; Pazmino, D. E.; Stepniak, P.; Wyrwicz, L. S.; Rychlewski, L.; Fraaije, M. W. Appl. Environ. Microbiol. 2011, 77, 5730.
[20] Dudek, H. M.; Fink, M. J.; Shivange, A. V.; Dennig, A.; Mihovilovic, M. D.; Schwaneberg, U.; Fraaije, M. W. Appl. Microbiol. Biotechnol. 2014, 98, 4009.
[21] Franceschini, S.; van Beek, H. L.; Pennetta, A.; Martinoli, C.; Fraaije, M. W.; Mattevi, A. J. Biol. Chem. 2012, 287, 22626.
[22] Bisagni, S.; Summers, B.; Kara, S.; Hatti-Kaul, R.; Grogan, G.; Mamo, G.; Hollmann, F. Top. Catal. 2013, 57, 366.
[23] Messiha, H. L.; Ahmed, S. T.; Karuppiah, V.; Suardiaz, R.; Ascue Avalos, G. A.; Fey, N.; Yeates, S.; Toogood, H. S.; Mulholland, A. J.; Scrutton, N. S. Biochemistry 2018, 57, 1997.
[24] Alexander, A. K.; Biedermann, D.; Fink, M. J.; Mihovilovic, M. D.; Mattes, T. E. J. Mol. Catal. B:Enzym. 2012, 78, 105.
[25] Fink, M. J.; Fischer, T. C.; Rudroff, F.; Dudek, H.; Fraaije, M. W.; Mihovilovic, M. D. J. Mol. Catal. B:Enzym. 2011, 73, 9.
[26] Rudroff, F.; Fink, M. J.; Pydi, R.; Bornscheuer, U. T.; Mihovilovic, M. D. Monatsh. Chem. 2017, 148, 157.
[27] Balke, K.; Schmidt, S.; Genz, M.; Bornscheuer, U. T. ACS Chem Biol. 2016, 11, 38.
[28] Zhang, Z. G.; Parra, L. P.; Reetz, M. T. Chem.-Eur. J. 2012, 18, 10160.
[29] Rodríguez-Mata, M.; Lavandera, I.; Gotor-Fernández, V.; Gotor, V.; García-Cerrada, S.; Mendiola, J.; de Frutos, Ó.; Collado, I. Tetrahedron 2016, 72, 7268.
[30] Reetz, M. T.; Brunner, B.; Schneider, T.; Schulz, F.; Clouthier, C. M.; Kayser, M. M. Angew. Chem., Int. Ed. 2004, 43, 4075.
[31] Clouthier, C. M.; Kayser, M. M.; Reetz, M. T. J. Org. Chem. 2006, 71, 8431.
[32] Polyak, I.; Reetz, M. T.; Thiel, W. J. Phys. Chem. B 2013, 117, 4993.
[33] Zhang, Z.-G.; Roiban, G.-D.; Acevedo, J. P.; Polyak, I.; Reetz, M. T. Adv. Synth. Catal. 2013, 355, 99.
[34] Parra, L. P.; Agudo, R.; Reetz, M. T. ChemBioChem 2013, 14, 2301.
[35] Wu, S.; Acevedo, J. P.; Reetz, M. T. Proc. Natl. Acad. Sci. U. S. A. 2010, 107, 2775.
[36] Yachnin, B. J.; McEvoy, M. B.; MacCuish, R. J.; Morley, K. L.; Lau, P. C.; Berghuis, A. M. ACS Chem Biol. 2014, 9, 2843.
[37] Iwaki, H.; Grosse, S.; Bergeron, H.; Leisch, H.; Morley, K.; Hasegawa, Y.; Lau, P. C. Appl. Environ. Microbiol. 2013, 79, 3282.
[38] Schmidt, S.; Genz, M.; Balke, K.; Bornscheuer, U. T. J. Biotechnol. 2015, 214, 199.
[39] Mallin, H.; Wulf, H.; Bornscheuer, U. T. Enzyme Microb. Technol. 2013, 53, 283.
[40] Staudt, S.; Bornscheuer, U. T.; Menyes, U.; Hummel, W.; Groger, H. Enzyme Microb. Technol. 2013, 53, 288.
[41] Oberleitner, N.; Peters, C.; Rudroff, F.; Bornscheuer, U. T.; Mihovilovic, M. D. J. Biotechnol. 2014, 192, 393.
[42] Schmidt, S.; Scherkus, C.; Muschiol, J.; Menyes, U.; Winkler, T.; Hummel, W.; Groger, H.; Liese, A.; Herz, H. G.; Bornscheuer, U. T. Angew. Chem., Int. Ed. 2015, 54, 2784.
[43] Milker, S.; Fink, M. J.; Oberleitner, N.; Ressmann, A. K.; Bornscheuer, U. T.; Mihovilovic, M. D.; Rudroff, F. ChemCatChem 2017, 9, 3420.
[44] Kohl, A.; Srinivasamurthy, V.; Bottcher, D.; Kabisch, J.; Bornscheuer, U. T. Enzyme Microb. Technol. 2018, 108, 53.
[45] Reignier, T.; de Berardinis, V.; Petit, J. L.; Mariage, A.; Hamze, K.; Duquesne, K.; Alphand, V. Chem. Commun. (Cambridge, U. K.) 2014, 50, 7793.
[46] Morrill, C.; Jensen, C.; Just-Baringo, X.; Grogan, G.; Turner, N. J.; Procter, D. J. Angew. Chem., Int. Ed. 2018, 57, 3692.
[47] Kadow, M.; Loschinski, K.; Sass, S.; Schmidt, M.; Bornscheuer, U. T. Appl. Microbiol. Biotechnol. 2012, 96, 419.
[48] Fink, M. J.; Rial, D. V.; Kapitanova, P.; Lengar, A.; Rehdorf, J.; Cheng, Q.; Rudroff, F.; Mihovilovic, M. D. Adv. Synth. Catal. 2012, 354, 3491.
[49] Leipold, F.; Wardenga, R.; Bornscheuer, U. T. Appl. Microbiol. Biotechnol. 2012, 94, 705.
[50] Kadow, M.; Balke, K.; Willetts, A.; Bornscheuer, U. T.; Backvall, J. E. Appl. Microbiol. Biotechnol. 2014, 98, 3975.
[51] Furst, M. J.; Savino, S.; Dudek, H. M.; Gomez Castellanos, J. R.; Gutierrez de Souza, C.; Rovida, S.; Fraaije, M. W.; Mattevi, A. J. Am. Chem. Soc. 2017, 139, 627.
[52] Balke, K.; Baumgen, M.; Bornscheuer, U. T. ChemBioChem 2017, 18, 1627.
[53] Butinar, L.; Mohorcic, M.; Deyris, V.; Duquesne, K.; Iacazio, G.; Claeys-Bruno, M.; Friedrich, J.; Alphand, V. Phytochemistry 2015, 117, 144.
[54] Romero, E.; Castellanos, J. R.; Mattevi, A.; Fraaije, M. W. Angew. Chem., Int. Ed. 2016, 55, 15852.
[55] van Beek, H. L.; de Gonzalo, G.; Fraaije, M. W. Chem. Commun. (Cambridge, U. K.) 2012, 48, 3288.
[56] Mascotti, M. L.; Palazzolo, M. A.; Bisogno, F. R.; Kurina-Sanz, M. Steroids 2016, 109, 44.
[57] Bosserman, M. A.; Downey, T.; Noinaj, N.; Buchanan, S. K.; Rohr, J. ACS Chem Biol. 2013, 8, 2466.
[58] Chen, K.; Wu, S.; Zhu, L.; Zhang, C.; Xiang, W.; Deng, Z.; Ikeda, H.; Cane, D. E.; Zhu, D. Biochemistry 2016, 55, 6696.
[59] Minerdi, D.; Zgrablic, I.; Castrignano, S.; Catucci, G.; Medana, C.; Terlizzi, M. E.; Gribaudo, G.; Gilardi, G.; Sadeghi, S. J. Antimicrob. Agents Chemother. 2016, 60, 64.
[60] Qiao, K.; Chooi, Y. H.; Tang, Y. Metab. Eng. 2011, 13, 723.
[61] Hu, Y.; Dietrich, D.; Xu, W.; Patel, A.; Thuss, J. A.; Wang, J.; Yin, W. B.; Qiao, K.; Houk, K. N.; Vederas, J. C.; Tang, Y. Nat. Chem. Biol. 2014, 10, 552.
[62] de Gonzalo, G.; Torres Pazmiño, D. E.; Ottolina, G.; Fraaije, M. W.; Carrea, G. Tetrahedron:Asymmetry 2006, 17, 130.
[63] (a) Branchaud, B. P.; Walsh, C. T. J. Am. Chem. Soc. 1985, 107, 2153.
(b) Walsh, C. T.; Chen, Y. C. J. Angew. Chem., Int. Ed. Engl. 1988, 27, 333.
[64] Gonzalo, G. D.; Pazmiño, D. E. T.; Ottolina, G.; Fraaije, M. W.; Carrea, G. Tetrahedron:Asymmetry 2005, 16, 3077.
[65] Ceccoli, R. D.; Bianchi, D. A.; Rial, D. V. Front. Microbiol. 2014, 5, 25.
[66] Brondani, P. B.; de Gonzalo, G.; Fraaije, M. W.; Andrade, L. H. Adv. Synth. Catal. 2011, 353, 2169.
[67] Das, B. C.; Thapa, P.; Karki, R.; Schinke, C.; Das, S.; Kambhampati, S.; Banerjee, S. K.; Van Veldhuizen, P.; Verma, A.; Weiss, L. M.; Evans, T. Future Med. Chem. 2013, 5, 653.
[68] Alphand, V.; Wohlgemuth, R. Curr. Org. Chem. 2010, 14, 1928.
[69] Bordewick, S.; Beier, A.; Balke, K.; Bornscheuer, U. T. Enzyme Microb. Technol. 2018, 109, 31.
[70] de Gonzalo, G.; Franconetti, A. Enzyme Microb. Technol. 2018, 113, 24.
[71] Mascotti, M. L.; Juri Ayub, M.; Dudek, H.; Sanz, M. K.; Fraaije, M. W. AMB Express 2013, 3, 33.
[72] Zhai, X. H.; Ma, Y. H.; Lai, D. Y.; Zhou, S.; Chen, Z. M. J. Ind. Microbiol. Biotechnol. 2013, 40, 797.
[73] Zhang, Z. G.; Lonsdale, R.; Sanchis, J.; Reetz, M. T. J. Am. Chem. Soc. 2014, 136, 17262.
[74] Dudek, H. M.; Popken, P.; van Bloois, E.; Duetz, W. A.; Fraaije, M. W. J. Biomol. Screening. 2013, 18, 678.
[75] Nikodinovic-Runic, J.; Coulombel, L.; Francuski, D.; Sharma, N. D.; Boyd, D. R.; Ferrall, R. M.; O'Connor, K. E. Appl. Microbiol. Biotechnol. 2013, 97, 4849.
[76] Zhang, Y.; Liu, F.; Xu, N.; Wu, Y. Q.; Zheng, Y. C.; Zhao, Q.; Lin, G.; Yu, H. L.; Xu, J. H. Appl. Environ. Microbiol. 2018, 84.
[77] Andrade, L. H.; Pedrozo, E. C.; Leite, H. G.; Brondani, P. B. J. Mol. Catal. B:Enzym. 2011, 73, 63.
[78] Brondani, P. B.; Guilmoto, N. M. A. F.; Dudek, H. M.; Fraaije, M. W.; Andrade, L. H. Tetrahedron 2012, 68, 10431.
/
| 〈 |
|
〉 |