表1 与TICs相比的优缺点Table 1 Advantages and disadvantages compared with TICs |
| Feature | MNPs | TICs |
|---|---|---|
| Catalytic activity | High | Lower |
| Recoverability | Magnetic recovery | Difficult to recycle |
| Stability | Less stable | Stable |
| Manufacturing cost | Higher | Lower |
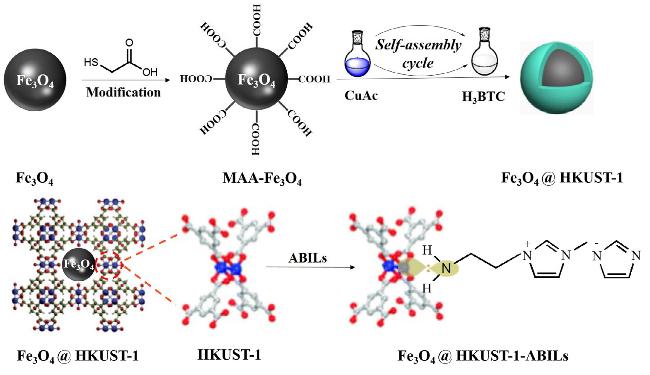
1 超顺磁性纳米颗粒负载酸性催化剂
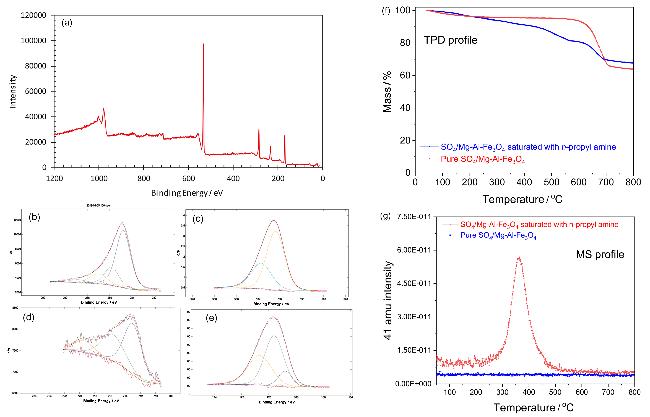
图2 AC-Fe(10)-SO3Cl催化剂的(a)全扫描谱、(b) C1s谱、(c) O1s谱、(d) Fe 2p谱、(e) S 2p谱; 纯正丙胺饱和SO4/Mg-Al-Fe3O4催化剂的(f)程序升温脱附(TPD)谱图和(g)质谱图[21,23]Figure 2 (a) Survey scan, (b) C 1s spectrum, (c) O 1s spectrum, (d) Fe 2p spectrum, (e) S 2p of AC-Fe(10)-SO3Cl catalyst; (f) TPD profiles and (g) mass spectra for SO4/Mg-Al-Fe3O4 catalyst of pure and saturated with n-propylamine[21,23] |
表2 磁性酸催化剂Table 2 Magnetic acid catalyst |
| Catalyst | Feedstocks | Rection condition | Yielda/% | Reuse time | Ref. |
|---|---|---|---|---|---|
| S2O82−/ZrO2‑TiO2‑Fe3O4 | Styrax confusus Hemsl oil | 1.5 h, 100 ℃, ω=5%, 8∶1 | 90.02 | 4 | [33] |
| Magnetic solid acid catalyst | Waste frying cooking oil | 9 h, 70 ℃, 50 mg, 15∶1 | 98.90 | 6 | [34] |
| Ni0.5-xZnxFe2O4 (0≤x≤0.4) | Soybean oil | 1 h, 180 ℃, ω=4%, 20∶1 | 85.00 | 4 | [35] |
| Fe3O4@Al2O3 | Waste cooking oil | 2.95 h, 99.8 ℃, ω=5%, 32.1∶1 | 99.10 | 4 | [36] |
| Zn1-xMnxFe2O4 (0≤x≤0.5) | Used cooking oil | 50 min, 65 ℃, ω=4%, 21∶1 | 98.30 | 10 | [37] |
| SiO2-SO3H/CoFe2O4 | Nephelium lappaceum oil | 10 h, 65 ℃, ω=5%, 20∶1 | 95.00 | 5 | [38] |
| AC-600-SO3H@Fe/C | High acid value oil | 10 h, 200 ℃, ω=10%, 24∶1 | 90.50 | 3 | [39] |
| C-SO3H@Fe/JHC | Jatropha oil | 2 h, 90 ℃, ω=10%, 12∶1 | 96.70 | 3 | [40] |
| FCHC-SO3H | Oleic acid | 3 h, 80 ℃, ω=4%, 15∶1 | 96.70 | 5 | [41] |
| nM-CP-SO3H | Sillettia pinnata seed oil | 45 min, 65 ℃, 3 g, 11∶1 | 98.70 | 5 | [42] |
| ZrFe-SA-SO3H | Oleic acid | 4 h, 90 ℃, ω=9%, 12∶1 | 96.60 | 5 | [43] |
| Fe3O4-PDA-SO3H | Levulinic acid | 5 h, 90 ℃, ω=20%, 11∶1 | 95.87 | 6 | [44] |
| Fe3O4@GO@PBIL | Thlaspi arvense L. Seed oil | 4 h, 60 ℃, ω=25%, 10∶1 | 92.38 | 6 | [45] |
| CoFe2O4-SL(n) | Oleic acid | 6 h, 100 ℃, ω=9%, 10∶1 | 80.00 | 5 | [46] |
| MCMSA | Wet microalgae | 6 h, 800 ℃, ω=5%, 10∶1 | 98.51 | 5 | [47] |
| MTCRH(0.1)@SO3Hii | Oleic acid | 4.8 h, 74.8 ℃, ω=9.9%, 16∶1 | 98.11 | 6 | [48] |
| Zn0.4Ni0.6Fe2O4@SO3H | Salicornia seeds oil | 4 h, 60 ℃, ω=5%, 5∶1 | 96.00 | 5 | [40] |
| MSNC | Oleic acid | 5 h, 80 ℃, ω=075%, 2∶1 | 96.00 | 5 | [50] |
a Yields under their optimal experimental conditions. |
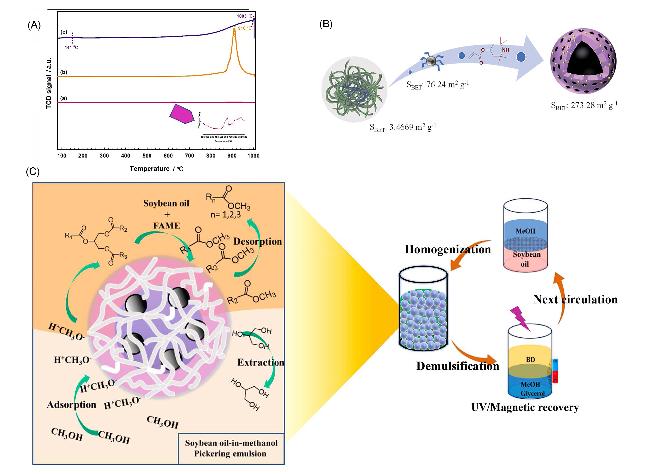
2 超顺磁性纳米颗粒负载碱性催化剂
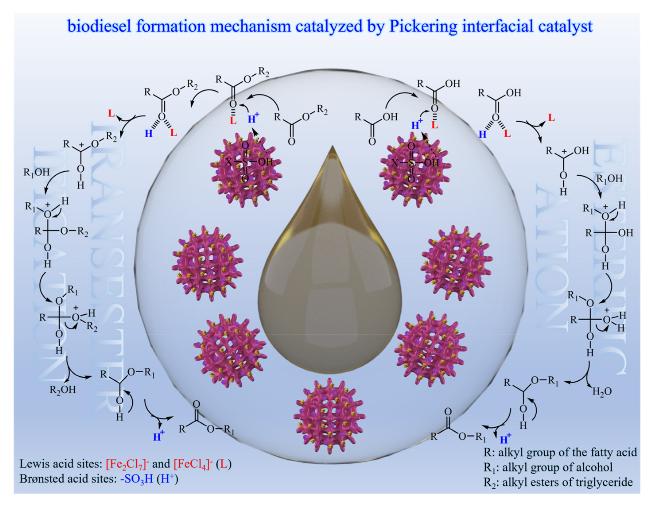
图7 (A) MGF (a), K2CO3 (b)和30KC/MGF (c)的CO2-TPD图; (B)末端烯烃改性Fe3O4@SiO2和单体TEMPA对p(xTEMPA- yFDABCO-zDVB)@Fe3O4比表面积的影响; (C) P[3SPA-2DABCO]@SiO2@Fe3O4颗粒催化大豆油与甲醇酯交换反应的机理[57,59-60]Figure 7 (A) CO2-TPD plot of MGF (a), K2CO3 (b) and 30KC/MGF (c); (B) effect of terminal alkene modified Fe3O4@SiO2 and monomer TEMPA on the specific surface area of p(xTEMPA-yFDABCO-zDVB)@Fe3O4; (C) mechanism of P[3SPA-2DABCO]@- SiO2@Fe3O4 particles catalyzed the transesterification of soybean oil and methanol[57,59-60] |
表3 磁性碱催化剂Table 3 Magnetic base catalyst |
| Catalyst | Feedstocks | Rection condition | Yielda/% | Reuse time | Ref. | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| MgFe2O4@CaO | Soybean oil | 3 h, 70 ℃, ω=1%, 12∶1 | 98.30 | 5 | [61] | |||||
| CaO@(Sr2Fe2O5-Fe2O3) | Soybean oil | 2 h, 70 ℃, ω=0.5%, 12∶1 | 94.90 | 5 | [62] | |||||
| Ca/Fe3O4@SiO2 | Waste sunflower oil | 5 h, 65 ℃, ω=8%, 15∶1 | 97.00 | 6 | [63] | |||||
| CaO@γ-Fe2O3 | Soybean oil | 3 h, 70 ℃, ω=2.0%, 15∶1 | 98.00 | 4 | [64] | |||||
| SrO/CoFe2O4 | Babassu oil | 3 h, 60 ℃, ω=4%, 15∶1 | 96.00 | 4 | [65] | |||||
| Fe3O4@SiO2@CPTMS@amine | Soybean oil | 3 h, 160 ℃, ω=6%, 36∶1 | 98.00 | 2 | [66] | |||||
| K/BC-Fe2O3 | soybean oil | 1 h, 60 ℃, ω=2.5%, 8∶1 | 98.00 | 4 | [67] | |||||
| ZnO/BiFeO3 | Canola oil | 6 h, 65 ℃, ω=4%, 15∶1 | 95.43 | 5 | [68] | |||||
| (CaO-Y2O3)@LiFe5O8 | Palm oil | 4.36 h, 64.96 ℃, ω=3.73%, 13∶1 | 96.21 | 4 | [69] | |||||
| K/Fe2O3-Al2O3 | Microalgae | 4 h, 65 ℃, ω=4%, 6∶1 | 95.60 | 6 | [70] | |||||
| Ca80Fe20 | Palm oil | 2 h, 65 ℃, ω=11%, 12∶1 | 96.12 | 5 | [71] | |||||
| Fe3O4/Cs2O | Tannery waste | 5 h, 65 ℃, ω=7%, 21∶1 | 97.10 | 9 | [72] | |||||
| CS2 | Waste frying oil | 0.5 h, 60 ℃, ω=3%, 18∶1 | 90.24 | 5 | [73] | |||||
| PEG/MgO/ZSM-5@Fe3O4 | Spirulina platensis | 40 min, 70 ℃, ω=2%, 8∶1 | 95.80 | 6 | [74] | |||||
| Fe3O4@PS-PTMG | Soybean oil | 6 h, 60 ℃, ω=3%, 15∶1 | 98.60 | 5 | [75] | |||||
| ISnO | Pongamia pinnata oil | 2 h, 60 ℃, 1 g, 10∶1 | 99.00 | 5 | [76] | |||||
| Fe3O4/SiO2@ZnO | Waste cooking oil | 30.13 min, 50 ℃, ω=2.67%, 9.90∶1 | 97.23 | 7 | [77] | |||||
| CaO/Fe2O3/Feldspar | Waste oils | 6 h, 40 ℃, ω=1.0%, 5∶1 | 99.90 | 4 | [78] | |||||
| Fe3O4•Cs2O | Madhuca indica oil | 5 h, 65 ℃, ω=7%, 18∶1 | 97.40 | 12 | [79] | |||||
| Na2SiO3@Fe3O4/C | Soybean oil | 20 min, 65 ℃, ω=5%, 7∶1 | 97.90 | 5 | [80] | |||||
| Na2SiO3@Ni/JRC | Jatropha-hull | 2 h, 90 ℃, ω=10%, 12∶1 | 96.70 | 3 | [40] | |||||
| KOH/Fe3O4@Al2O3 | Canola oil | 6 h, 65 ℃, ω=6%, 12∶1 | 98.80 | 6 | [81] | |||||
| KOH/ZSM-5-Fe3O4 | Canola oil | 3.26 h, 65 ℃, ω=9.03%, 12.3∶1 | 93.65 | 5 | [82] | |||||
| KOH/Fe3O4@γ-Al2O3 | Canola oil | 5.43 h, 65 ℃, ω=6.45%, 16.14∶1 | 97.40 | 3 | [83] | |||||
| Na2SiO3/Fe3O4-SBC600 | Soybean oil | 3 h, 65 ℃, ω=8%, 13∶1 | 96.50 | 8 | [84] | |||||
| KF/KOH-Fe3O4 | Microalgae | 2 h, 25 ℃, ω=1.5%, 6∶1 | 96.80 | 5 | [85] | |||||
a Yields under their optimal experimental conditions. |
3 超顺磁性纳米颗粒负载酸碱双功能催化剂
表4 磁性酸碱双功能催化剂Table 4 Magnetic acid-base bifunctional catalyst |
| Catalyst | Feedstocks | Rection condition | Yielda/% | Reuse time | Ref. |
|---|---|---|---|---|---|
| CaSO4/Fe2O3-SiO2 | Jatropha curcus | 4 h, 120 ℃, ω=12%, 9∶1 | 94.00 | 9 | [93] |
| ZnO-Ni0.5Zn0.5Fe2O4-Fe2O3 | Residual oil | 1 h, 200 ℃, ω=5%, 15∶1 | 96.16 | 3 | [94] |
| SO42−/Fe3O4-Al2O3 | Microalgae | 4 h, 120 ℃, ω=8%, 9∶1 | 87.60 | 5 | [95] |
| SrO/MgFe2O4 | Waste cooking oil | 3 h, 45 ℃, ω=2%, 12∶1 | 96.80 | 3 | [96] |
a Yields under their optimal experimental conditions. |
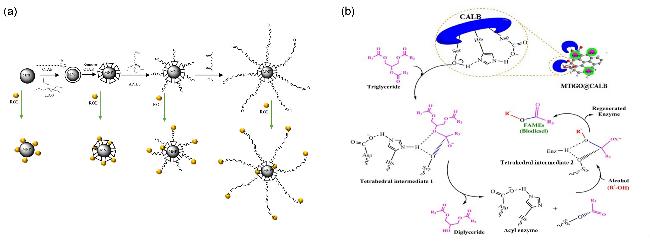
4 超顺磁性纳米颗粒负载酶催化剂
表5 磁性负载酶催化剂Table 5 Magnetic enzyme catalyst |
| Catalyst | Feedstocks | Rection condition | Yielda/% | Reuse time | Ref. |
|---|---|---|---|---|---|
| His-TLL-MNPs | Waste grease | 24 h, 50 ℃, ω=5% | 94.00 | 7 | [101] |
| ECCNs-TLL | Soybean oil | 3 h, 40 ℃, 4∶1 | 96.00 | — | [102] |
| m-MWCNTs-PAMAM-RML | Waste vegetable oil | 30 h, 50 ℃, ω=6%, 4∶1 | 94.00 | 10 | [103] |
| Fe3O4-AP-EN-LIP | Palm oil | 24 h, 50 ℃, ω=23.2%, 4.7∶1 | 97.20 | 5 | [104] |
| mMWCNTs-PAMAM-BCL | Soybean oil | 24 h, 35 ℃, ω=10%, 4∶1 | 96.00 | 10 | [105] |
| mMWCNTs-PAMAM-RML | Soybean oil | 36 h, 50 ℃, ω=10%, 5∶1 | 96.00 | 10 | [105] |
| mMWCNTs-PAMAM-CRL | Soybean oil | 40 h, 40 ℃, ω=10%, 4∶1 | 85.00 | 10 | [105] |
| Fe3O4@SiO2-CALB | Waste cooking oil | 50 ℃, 100 mg, 3∶1 | 100.0 | 6 | [106] |
| Fe3O4/Au@CA_L | Waste tomato | 24 h, 45 ℃, ω=30%, 6∶1 | 98.50 | 3 | [107] |
| MGO-CRL | Soybean oil | 60 h, 40 ℃, ω=25%, 4∶1 | 92.80 | 5 | [108] |
| Fe3O4@MIL-100(Fe) | Soybean oil | 60 h, 40 ℃, ω=25%, 4∶1 | 92.30 | 5 | [109] |
| Magnetic nanoparticle | Olive oil | 4 h, 45 ℃, 300 mg, 4∶1 | 84.00 | 5 | [110] |
| MRL | Soybean oil | 28 h, 41 ℃, ω=9%, 4∶1 | 82.20 | 10 | [111] |
| Fe3O4@PS-NH-lipase | Soybean oil | 30 h, 30 ℃, 1.38 g, 15∶1 | 89.30 | 5 | [112] |
| mCLEAs | Palm oil | 24 h, 37 ℃, ω=30%, 3∶1 | 95.00 | 5 | [113] |
a Yields under their optimal experimental conditions. |