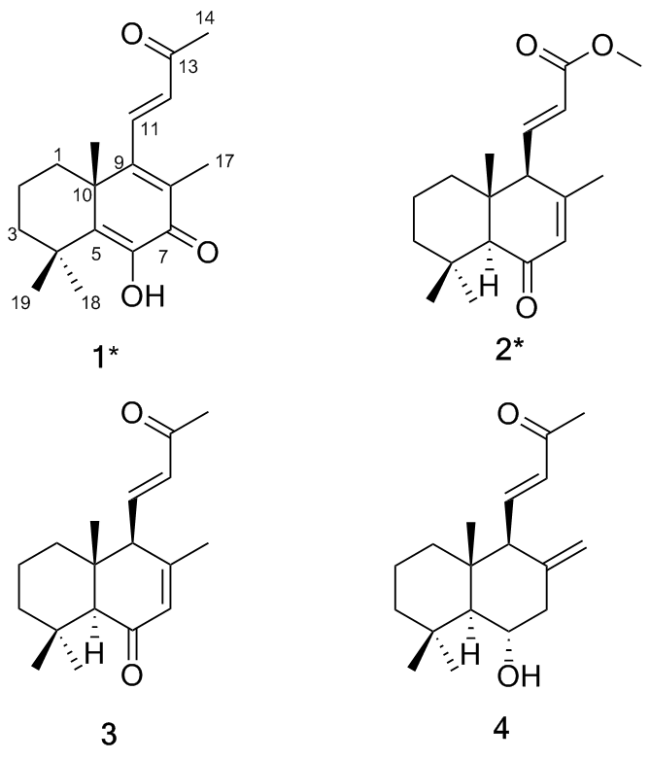
(11
E)-6
α-羟基-15,16-二降-半日花烷-8(17),11-二烯-13-酮(
4), 浅黄色油状物.
1H NMR (600 MHz, CDCl
3)
δ: 6.91 (dd,
J=15.8/10.3 Hz, 1H, H-11), 6.09 (d,
J=15.9 Hz, 1H, H-12), 4.96 (d,
J=1.6 Hz, 1H, H-17), 4.68 (d,
J=1.6 Hz, 1H, H-17), 4.44~4.40 (m, 1H, H-6), 2.52 (d,
J=10.3 Hz, 1H, H-9), 2.45~2.35 (m, 2H, H-7), 2.28 (s, 3H, H-14), 1.64~1.53 (m, 1H, H-2b), 1.48~1.39 (m, 1H, H-3b), 1.41~1.34 (m, 2H, H-1b/2a), 1.23 (s, 3H, H-19), 1.20 (s, 3H, H-20), 1.20~1.17 (m, 1H, H-3a), 1.11 (d,
J=2.0 Hz, 1H, H-5), 1.10~1.04 (m, 1H, H-1a), 1.02 (s, 3H, H-18);
13C NMR (150 MHz, CDCl
3)
δ: 44.0 (CH
2, C-1), 19.3 (CH
2, C-2), 44.1 (CH
2, C-3), 34.7 (C, C-4), 56.7 (CH, C-5), 68.9 (CH, C-6), 46.6 (CH
2, C-7), 144.8 (C, C-8), 61.4 (CH, C-9), 40.5 (C, C-10), 145.8 (CH, C-11), 134.0 (CH, C-12), 198.2 (C, C-13), 27.4 (CH
3, C-14), 112.1 (C, C-17), 33.7 (CH
3, C-18), 24.0 (CH
3, C-19), 18.3 (CH
3, C-20); HR-ESI-MS calcd for C
18H
29O
2 [M+H]
+ 277.2162, found 277.2155. 数据与文献报道基本一致
[25].