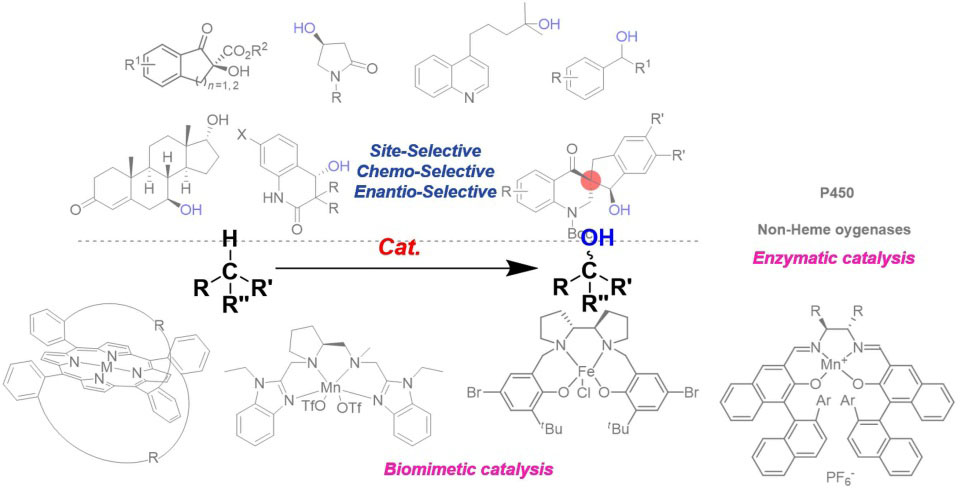
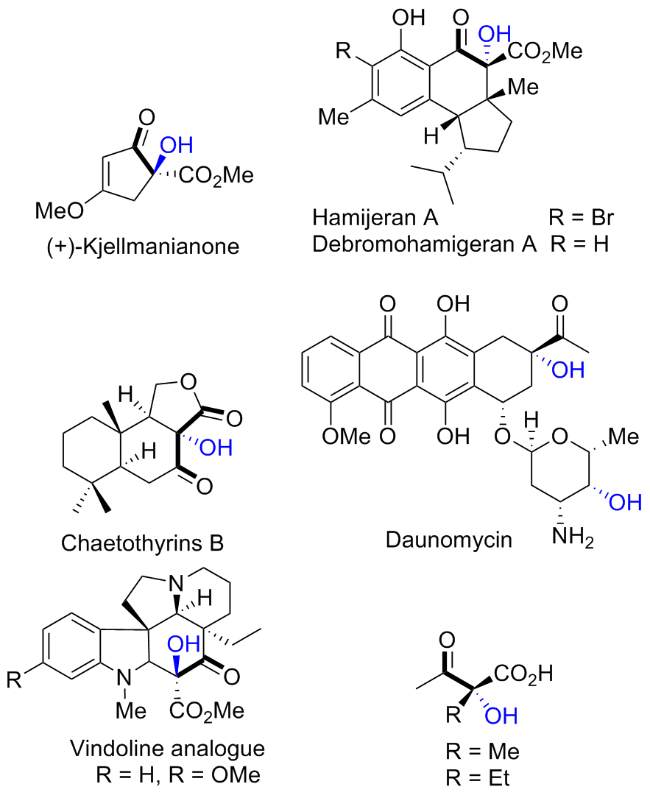
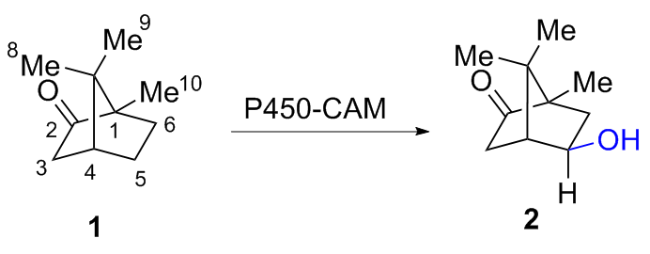
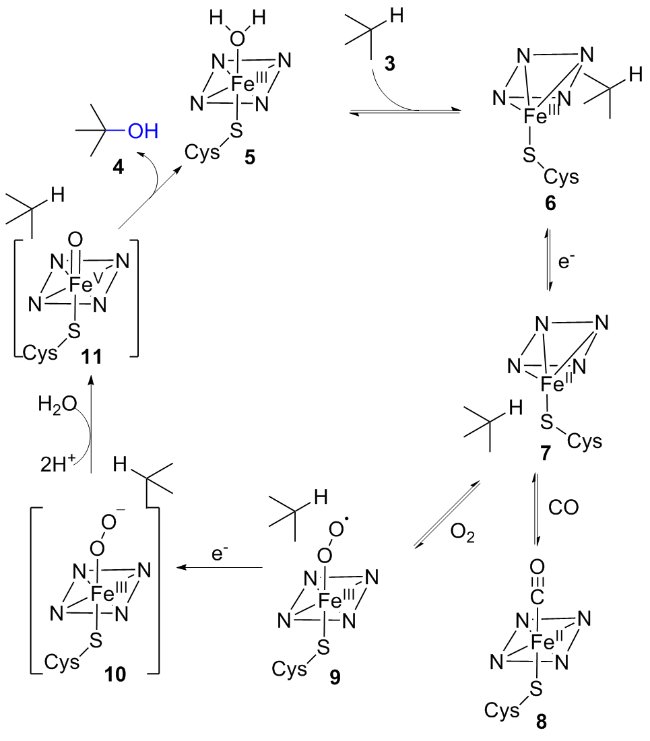
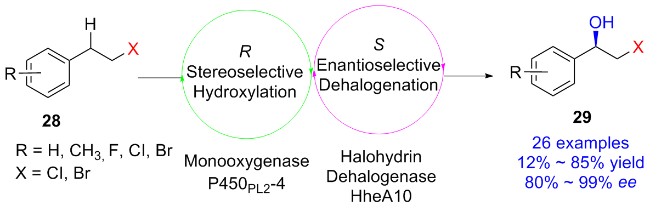1 生物催化C—H键不对称羟基化反应
1.1 P450酶催化不对称羟基化反应
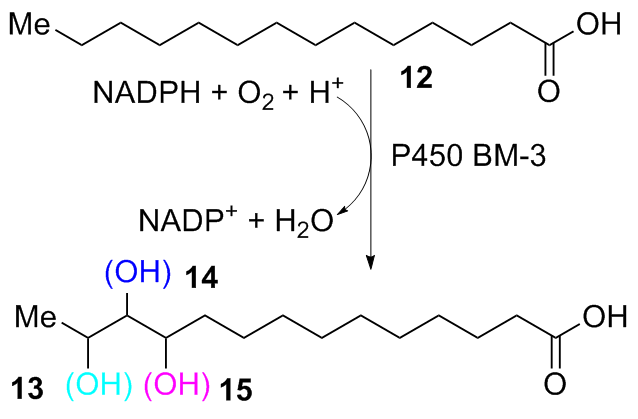
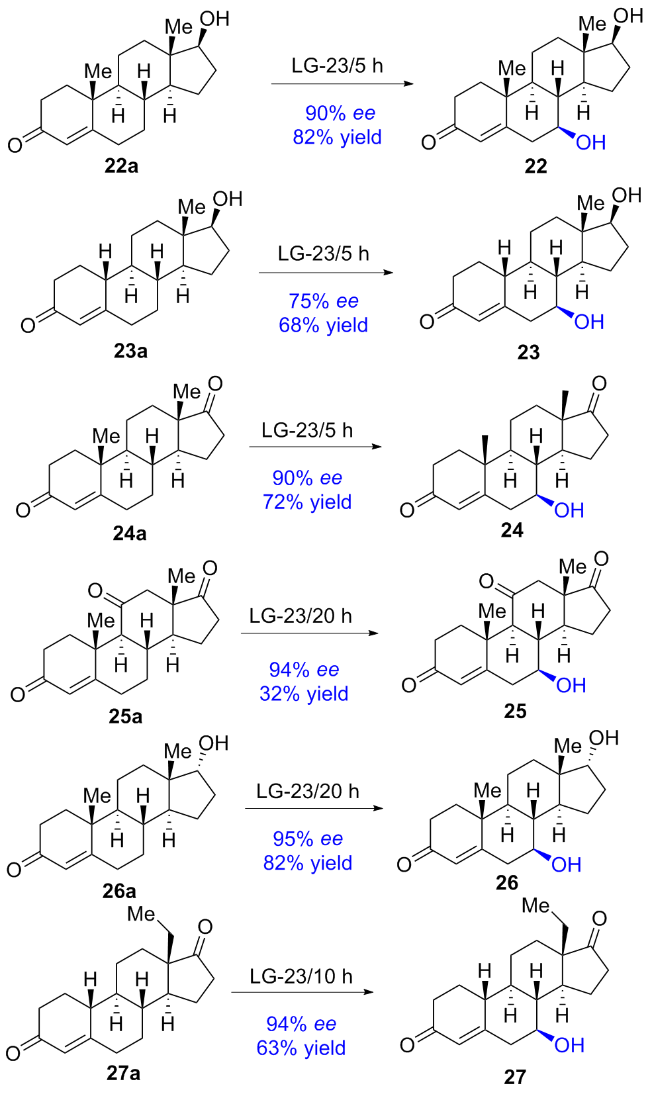
1.1.1 P450酶催化脂肪族C—H键不对称羟基化反应
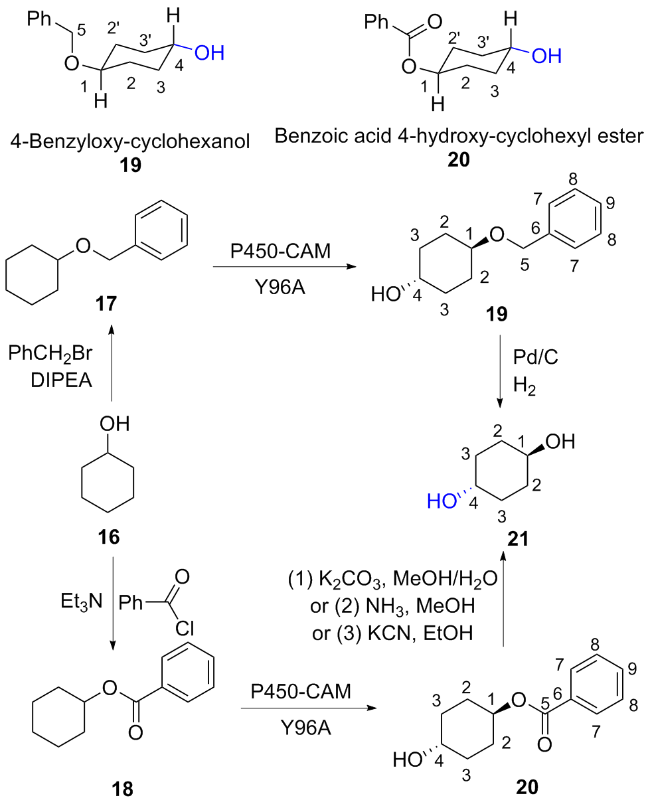
1.1.2 P450酶催化苄位C—H键不对称羟基化反应
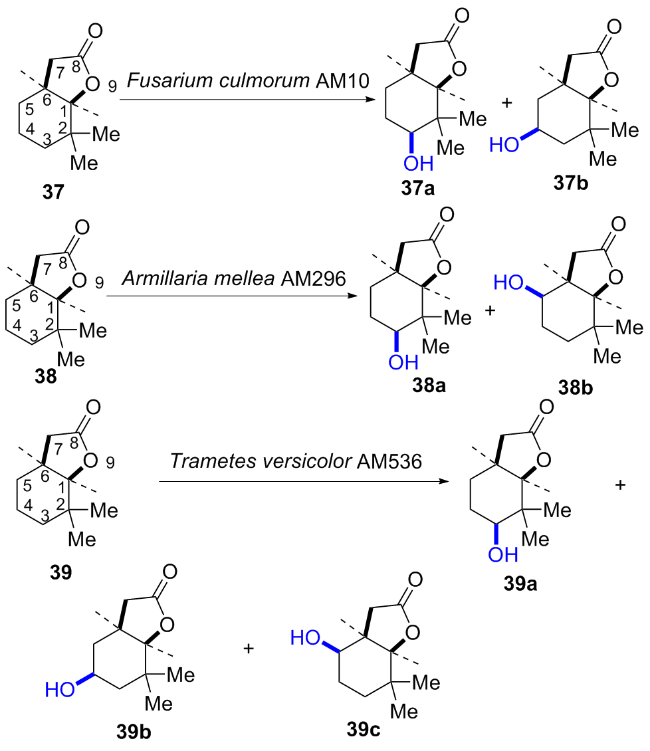
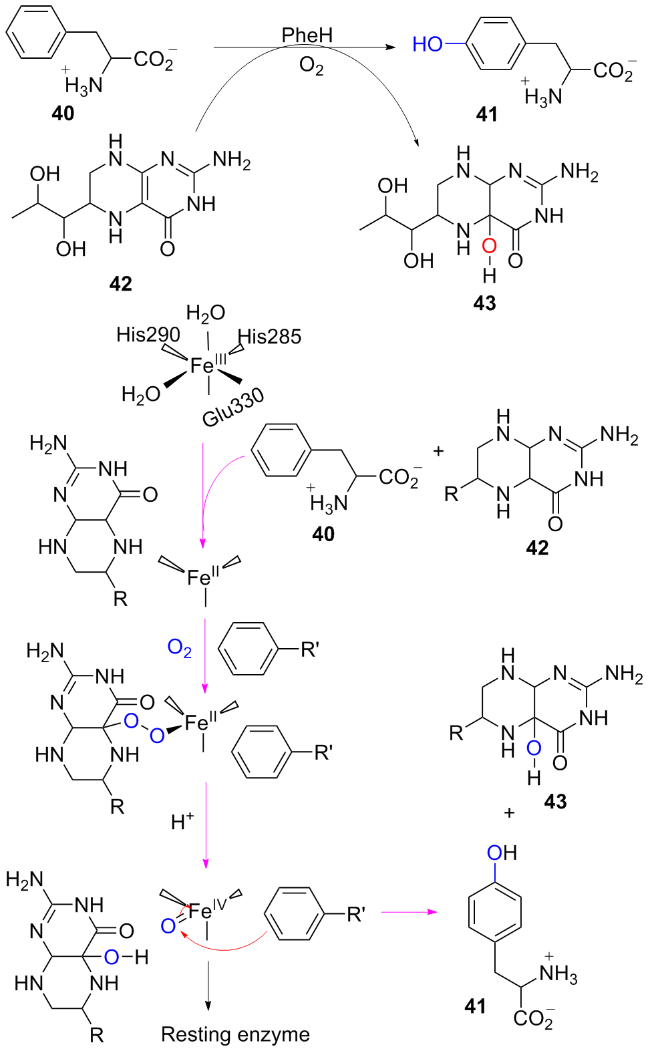
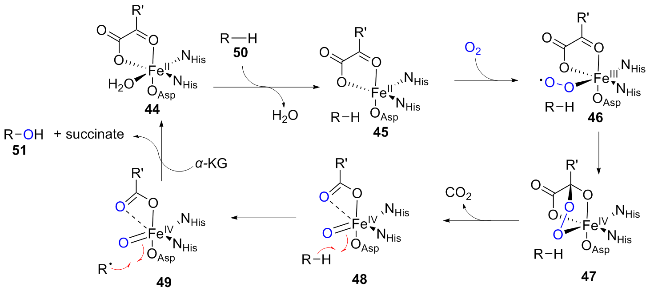
1.2 非血红素加氧酶催化的不对称羟基化反应
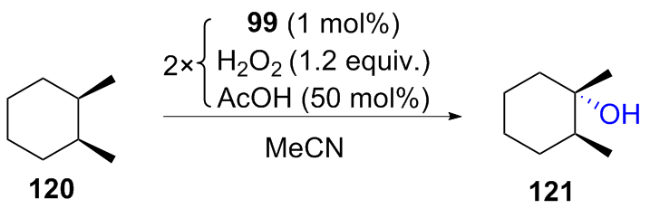
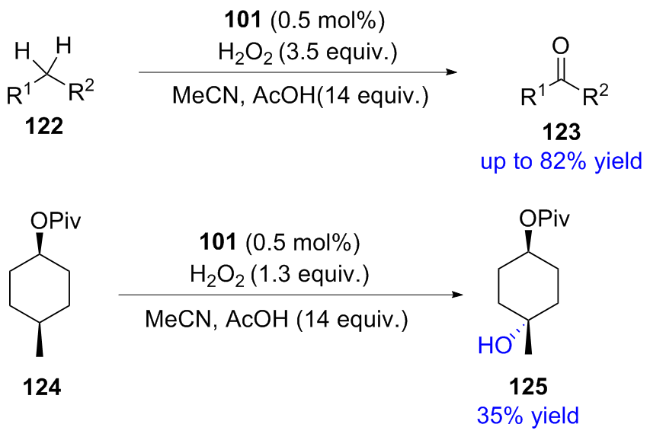
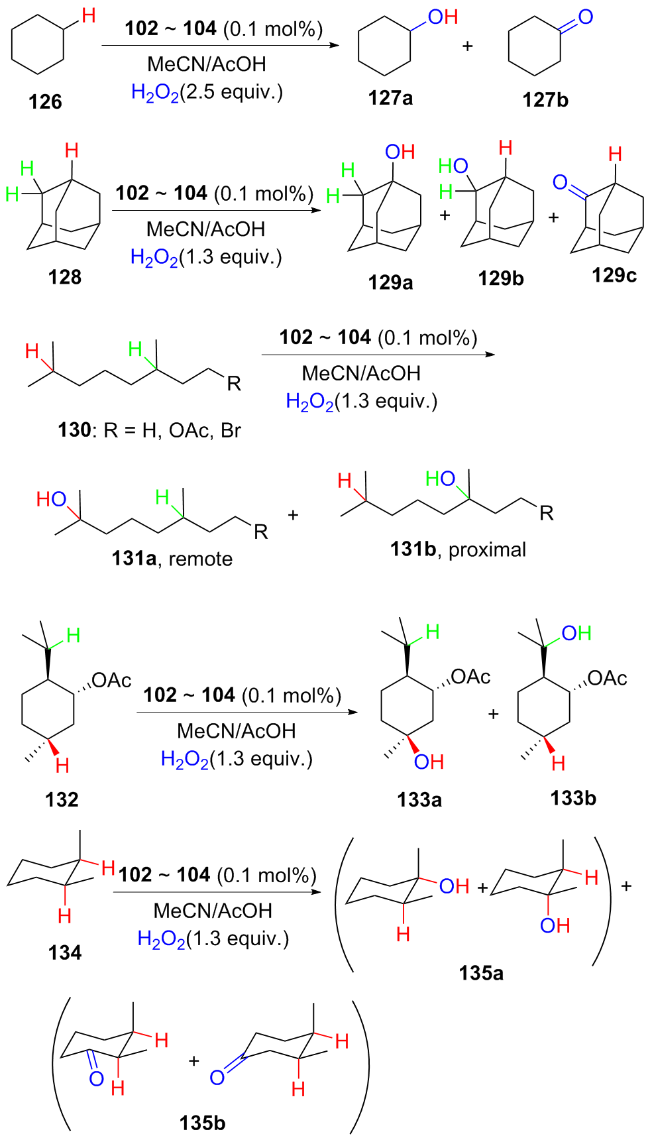
2 仿生催化不对称羟基化反应
2.1 基于金属-porphyrin体系催化的不对称羟基化反应
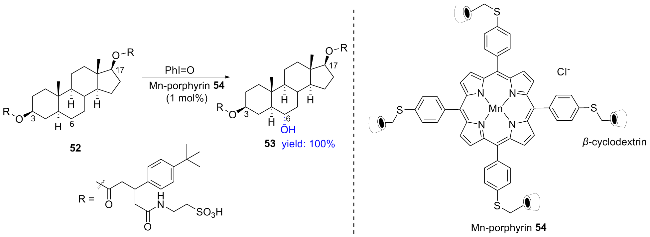
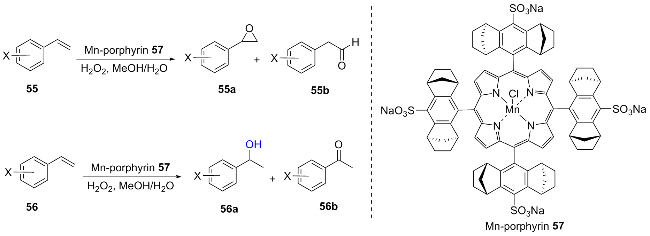
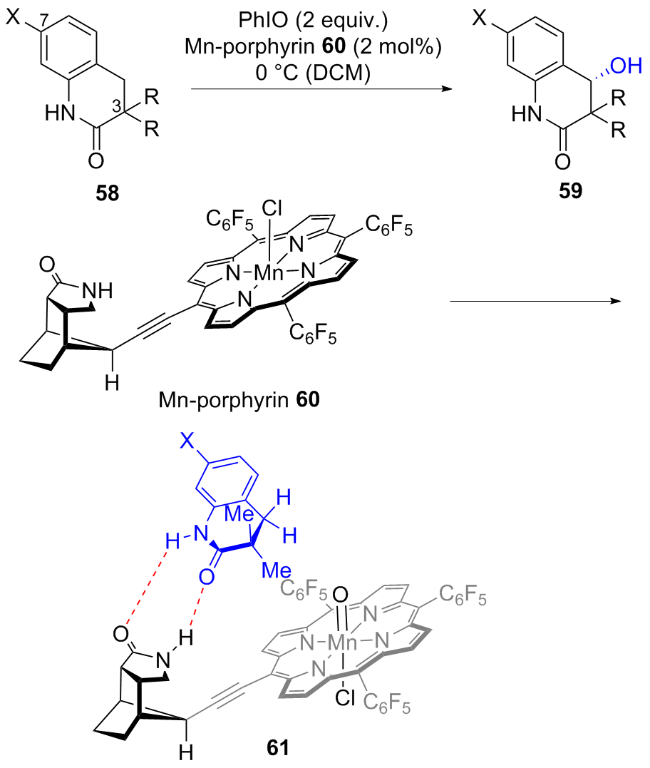
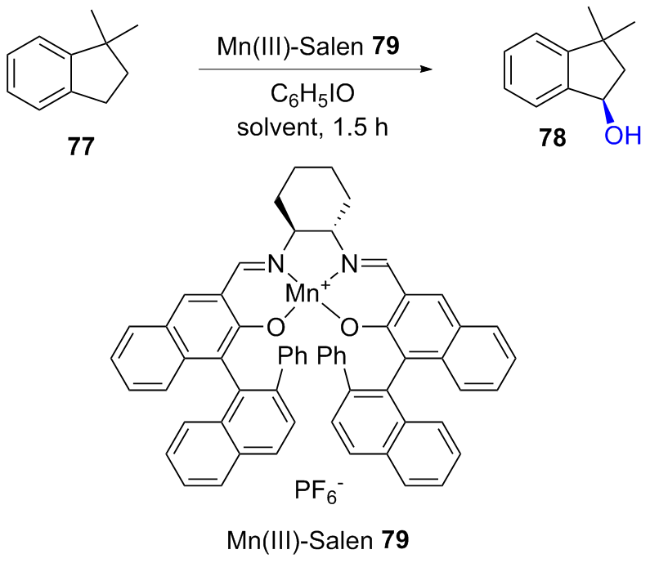
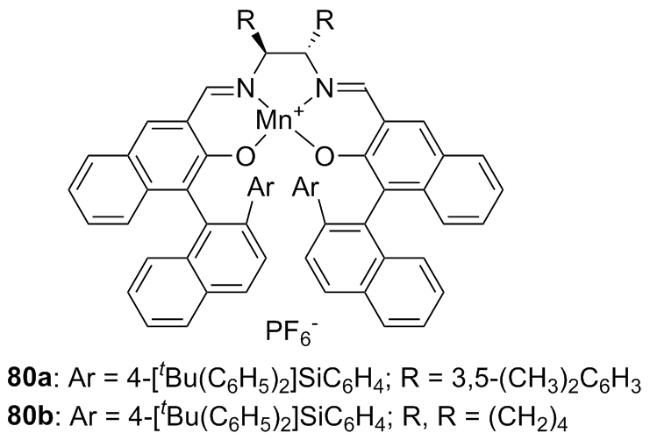
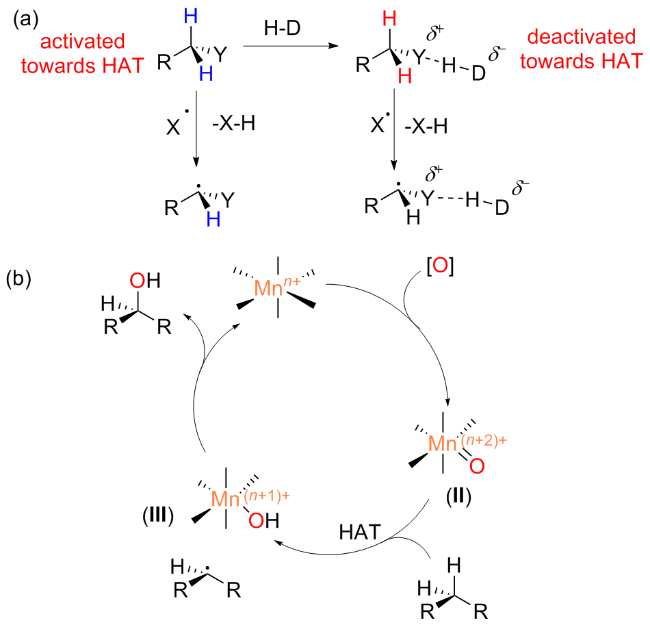
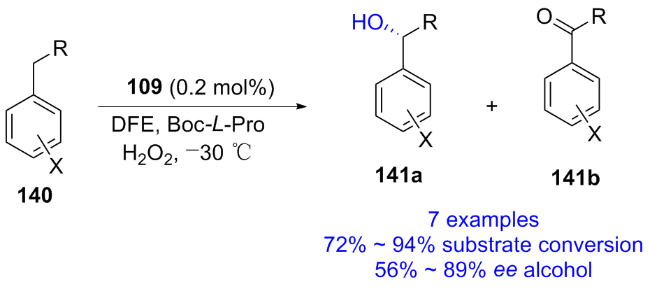
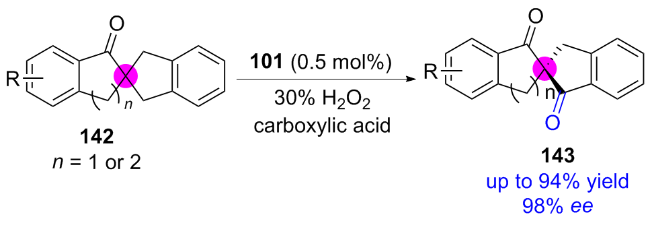
2.1.1 Mn-porphyrin催化的不对称羟基化反应
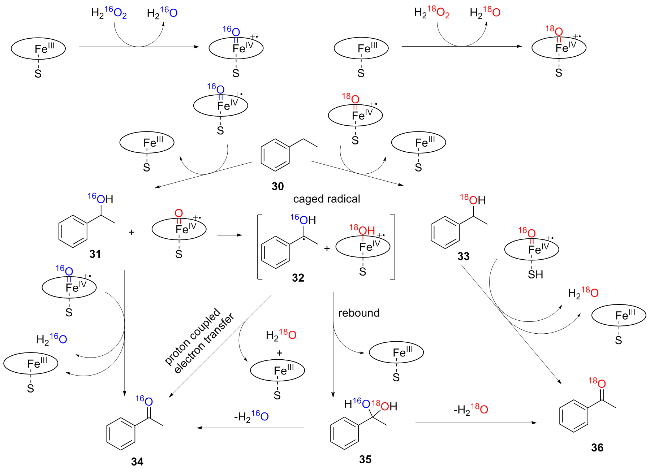
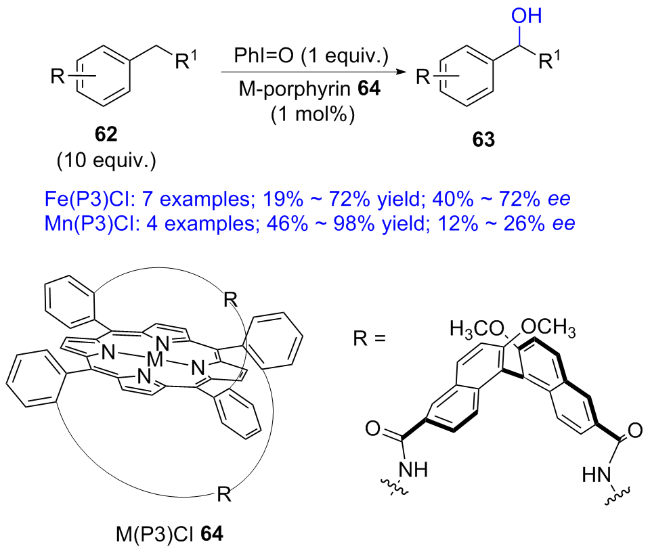
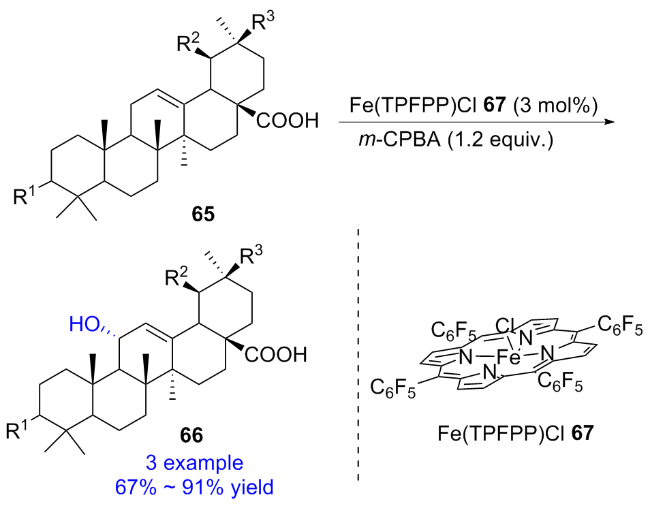
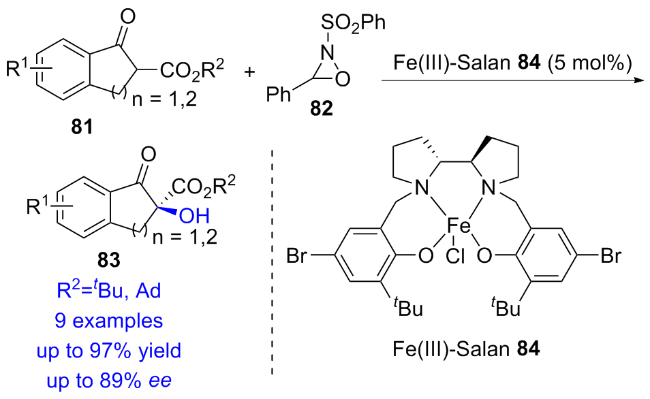
2.1.2 Fe-porphyrin催化的不对称羟基化反应
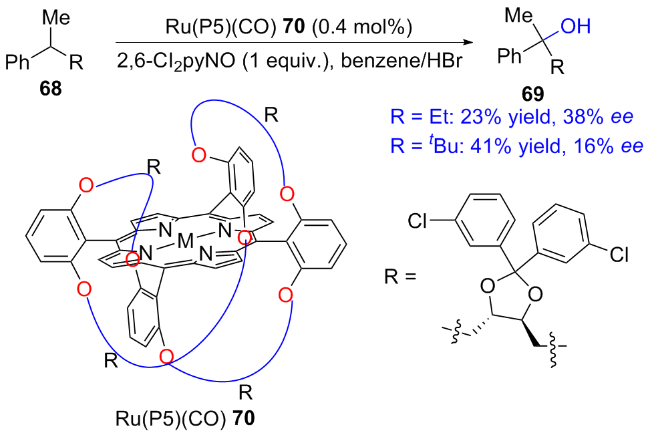
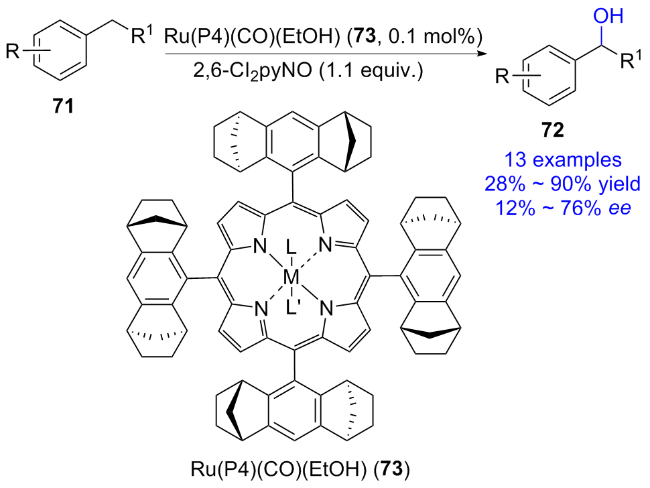
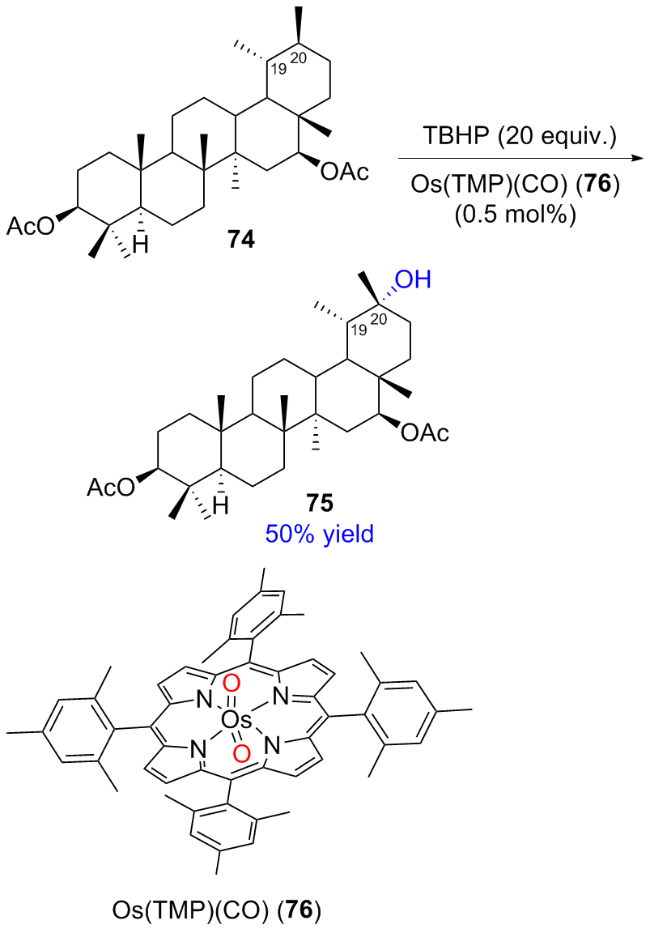
2.1.3 Ru/Os-porphyrin催化的不对称羟基化反应
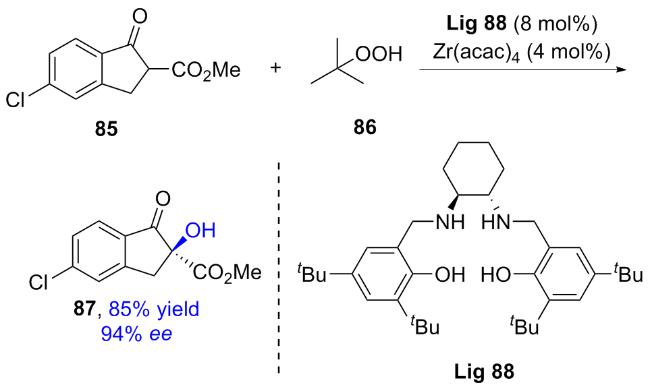
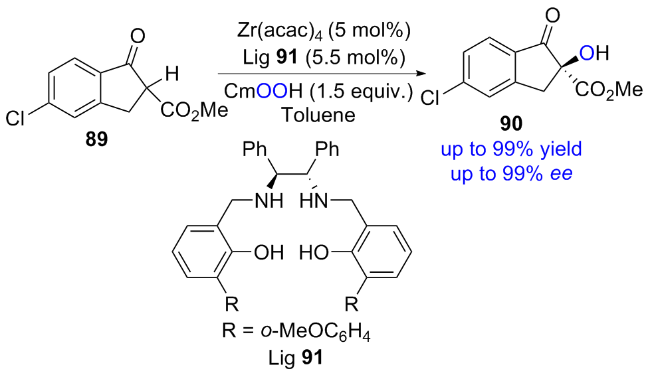
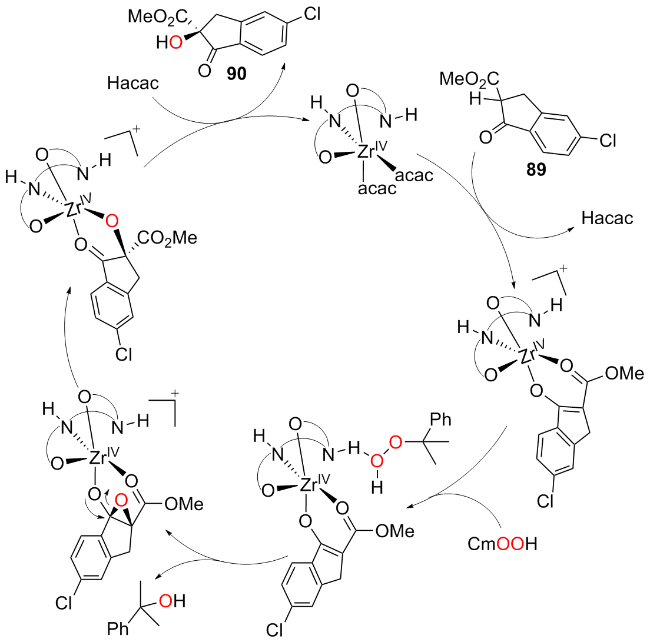
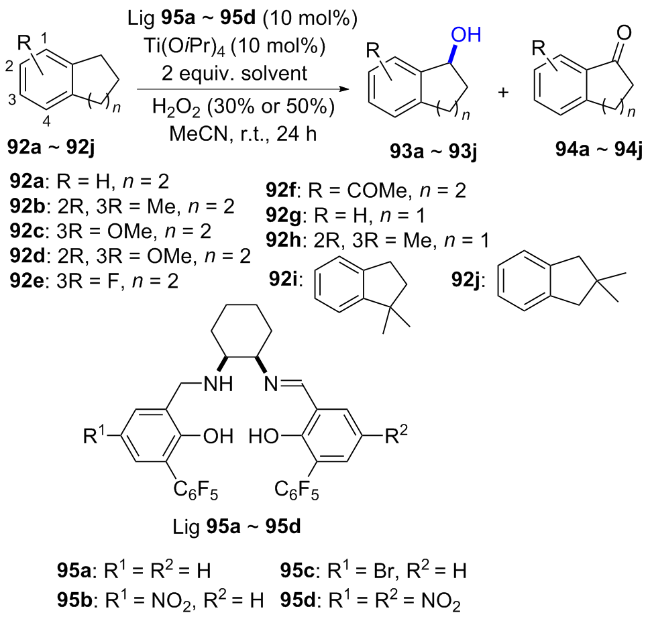
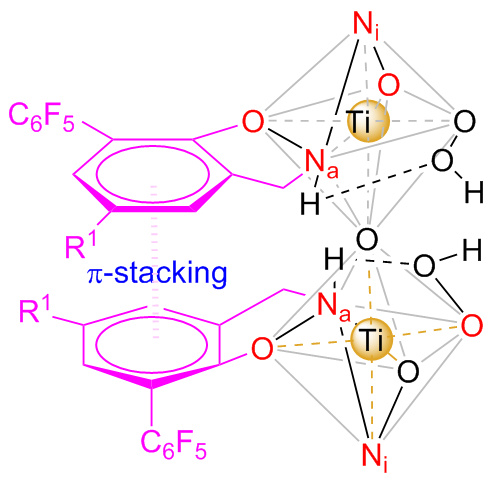
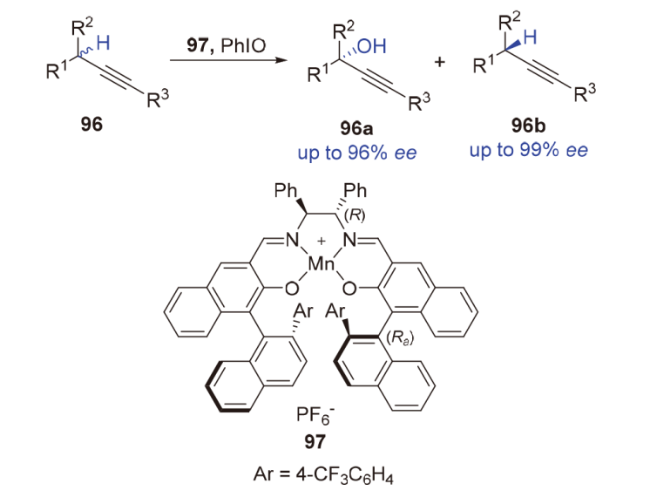
2.2 基于金属-Salen体系催化不对称羟基化反应
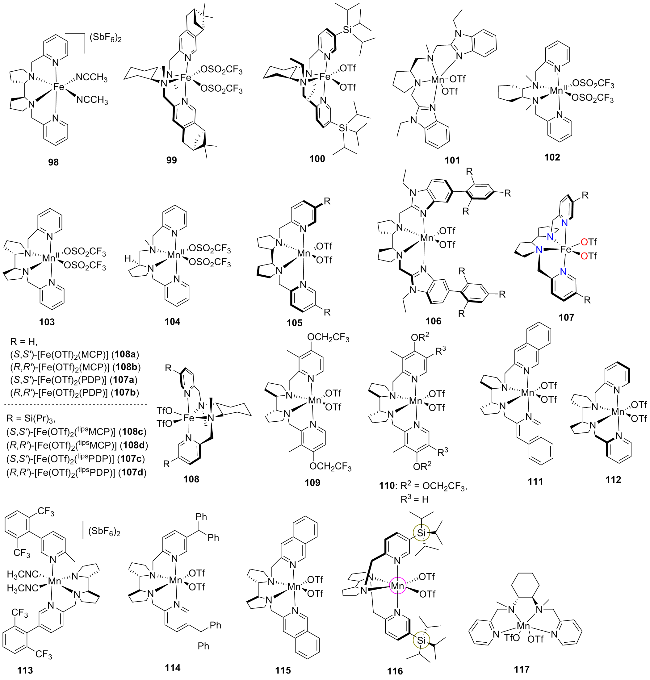
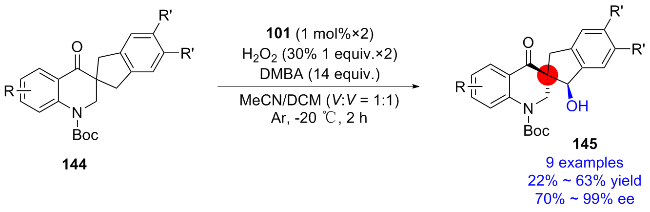
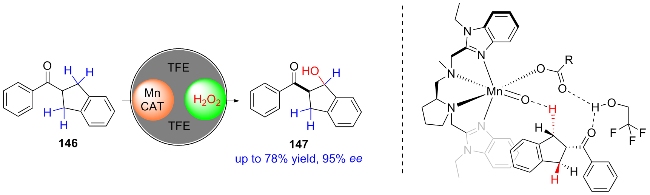
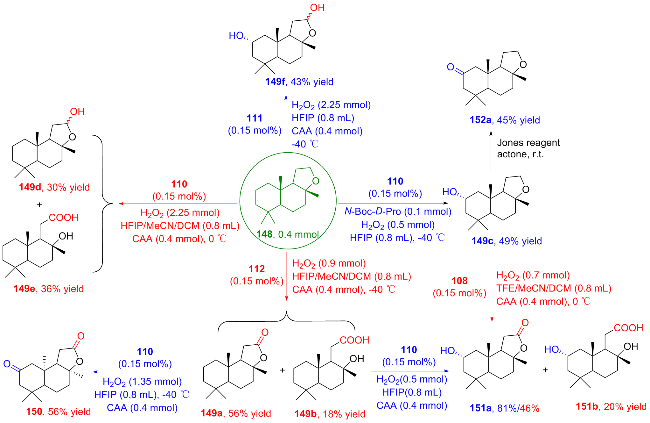
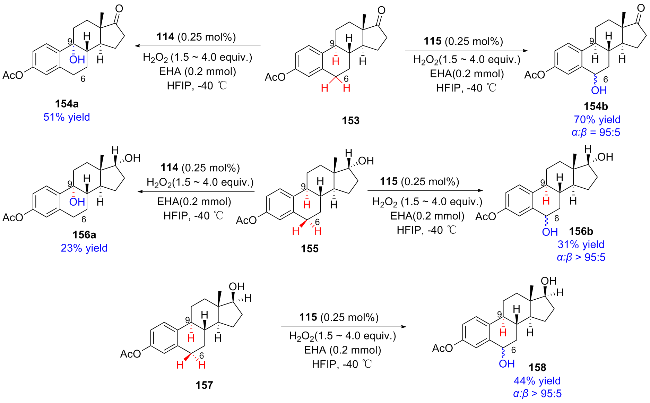
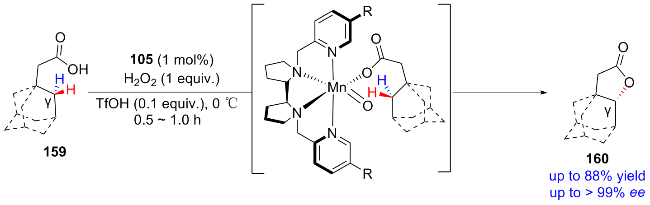
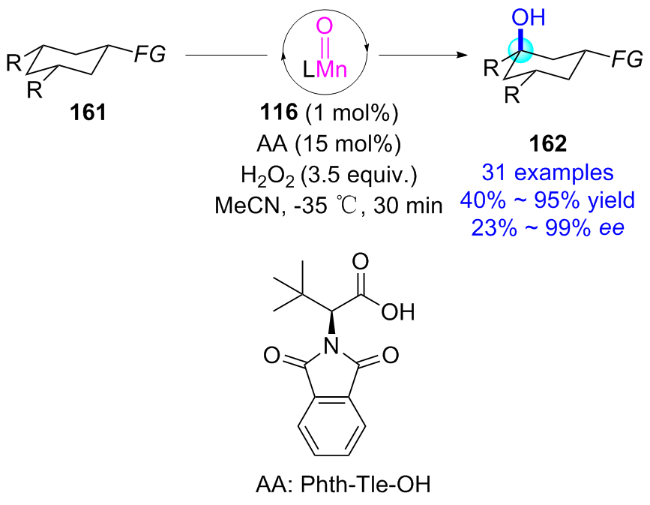
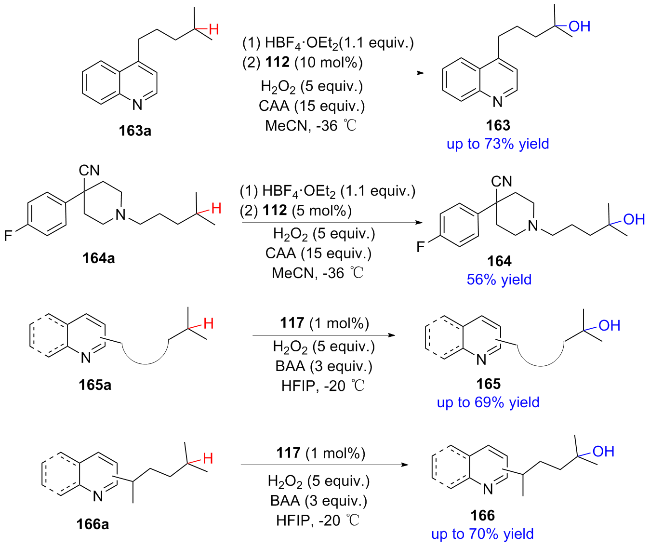
2.3 金属-氨基吡啶体系催化的不对称羟基化反应
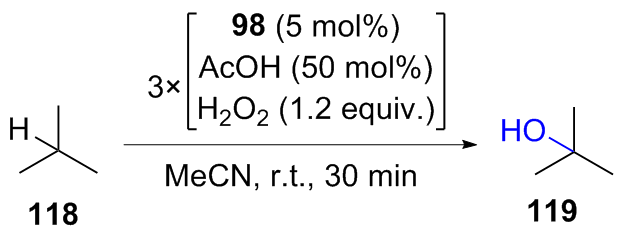
表1 催化剂98对不同类型底物的适用范围Table 1 Range of 98 for different types of substrates |
| Entry | Product | Isolated yield/% (rsma) |
|---|---|---|
| 1 |  | 46 (26) |
| 2 | 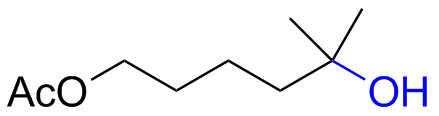 | 53 (43) |
| 3 | 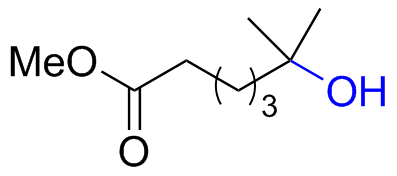 | 60 (18) |
| 4 | 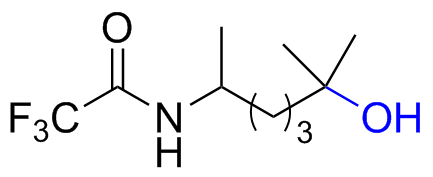 | 43 (33) |
| 5 | 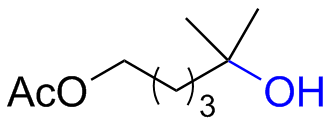 | 52 (21) |
| 6 | 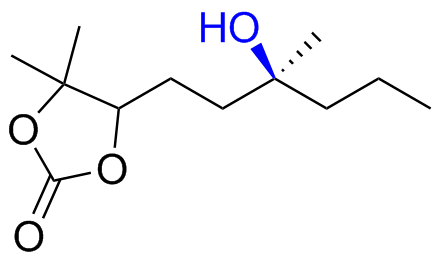 | 57 (27) |
| 7 | 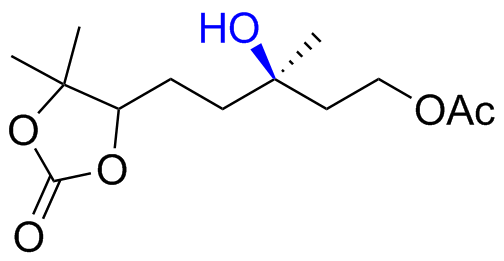 | 43 (42) |
| 8 | 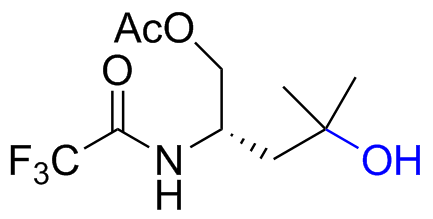 | 33 (67) 90*,b (8) |
| 9 | 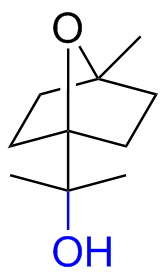 | 52 (20) |
| 10 | 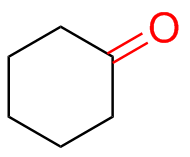 | 92* |
a Recovered starting material. b GC yield. |
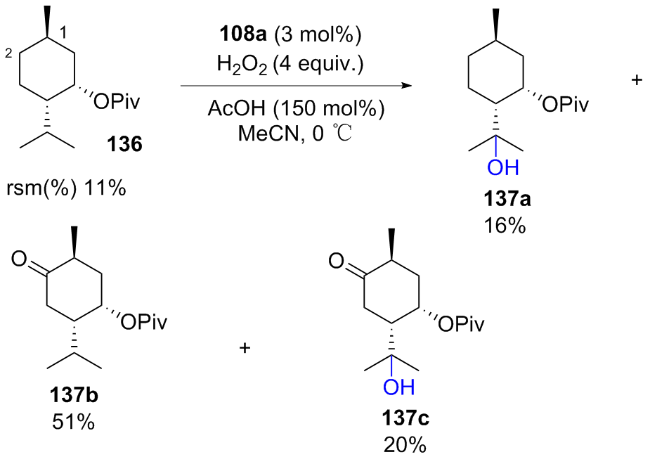
图式33 (+)-新薄荷脑新戊酸酯136选择性氧化反应Scheme 33 Selective oxidation of (+)-neomenthol neopentanoate 136 |
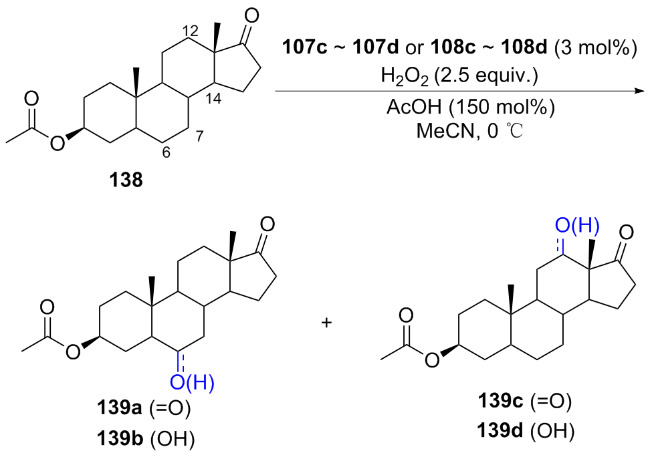
图式34 反式雄酮醋酸酯138的催化氧化Scheme 34 Selective oxidation of (+)-neomenthol neopentanoate 138 |
表2 反式雄酮醋酸酯的氧化Table 2 Oxidation of trans-androsterone acetate |
| Entry | Cat. | Conv/% | Total yield (isolated yield)/% | C6/C7/C12/C14 |
|---|---|---|---|---|
| 1 | 107c | 85 | 70 (50) | 75/5/23/— |
| 2 | 107d | 86 | 80 (71) | 11/1/88/— |
| 3 | 108c | 83 | 60 (49) | 82/12/3/3 |
| 4 | 108d | 50 | 48 (33) | 22/6/69/3 |