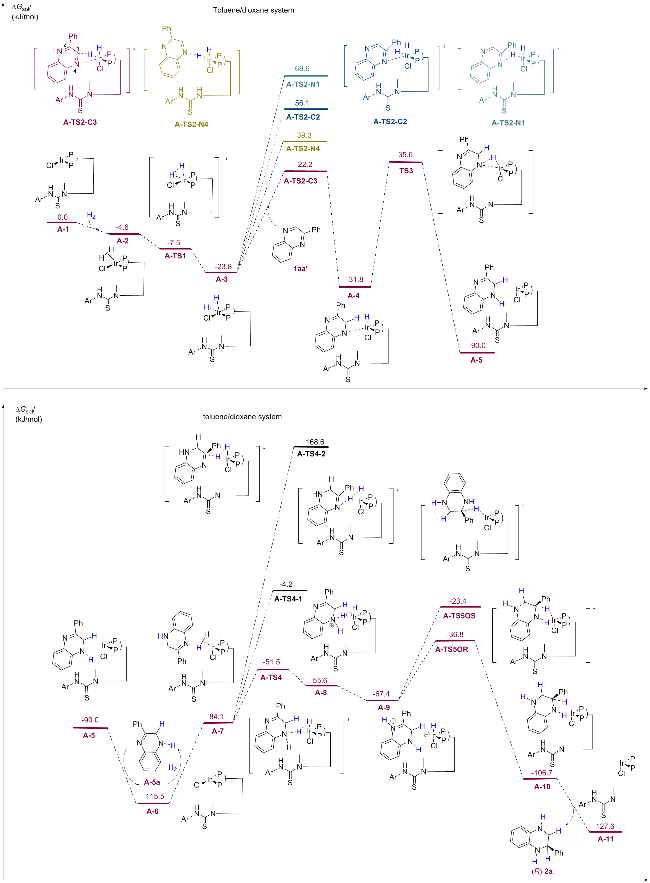
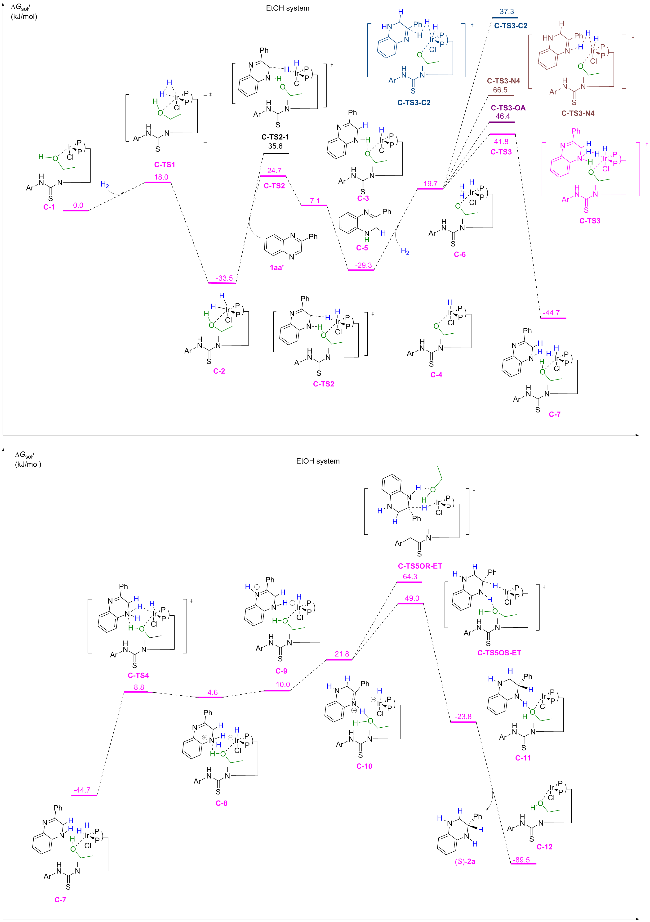
2-苯基喹喔啉在乙醇反应体系中势能面计算结果如
图4. 首先, 催化剂
C-1经过18.0 kJ/mol过渡态
C-TS1与氢气发生氧化加成, 生成稳定的Ir(III)中间体
C-3(-33.5 kJ/mol). 在第一次氢转移过程中, 通过两个C=N双键不同的反应活性结合对照实验(辅助材料, Scheme S3)确定第一次氢转移发生的两个活性位点N1、C2, 金属Ir配位的负氢与乙醇分子羟基中的活泼氢同时参与反应, 通过协同转移的方式经历六元环过渡态(
C-TS2, 能量为24.7 kJ/mol)分别转移到底物分子的N1和C2位点上, 生成中间体
C-4. 然后, 为保证催化剂Ir的六配位结构另一分子氢气再通过
σ电子与Ir空轨道配位形成中间体
C-6(能量为19.7 kJ/mol). 催化剂上活化的氢原子首先从Ir转移至底物分子的N1位点, 并促进N1上已有的一个氢原子向乙醇氧发生转移. 这一过程通过六元环过渡态
C-TS3(能量为41.8 kJ/mol)实现, 并释放大量自由能生成稳定的中间体
C-7(能量为-47.7 kJ/mol). 随后, Ir中心上的另一个氢原子继续转移至N1位点, 伴随着乙醇分子中OH基团的氢与N1形成氢键, 最终生成产物中间体
C-8(能量为4.6 kJ/mol). 此后, 底物中N1位上的氢通过质子转移过程转移至 N
4 位点, 进一步形成产物
C-9(能量为10.0 kJ/mol). 最后, Ir配位中心的最后一个氢原子转移到底物的C3位点, 完成最终的产物生成. 氢化物通过
C-TS5OR-ET或
C- TS5OS-ET从底物的
Re或
Si面向C2位转移, 该过程为对映选择性决定步. 计算结果表明,
C-TS5OS-ET过渡态的能垒为93.7 kJ/mol, 明显低于
C-TS5OR-ET过渡态, 该计算结果与实验结果一致, 氢化产物为
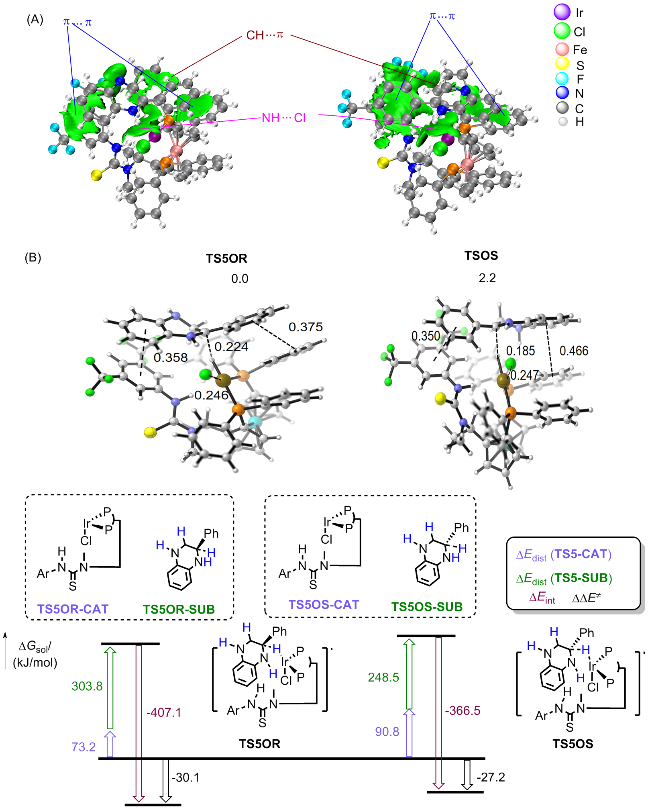
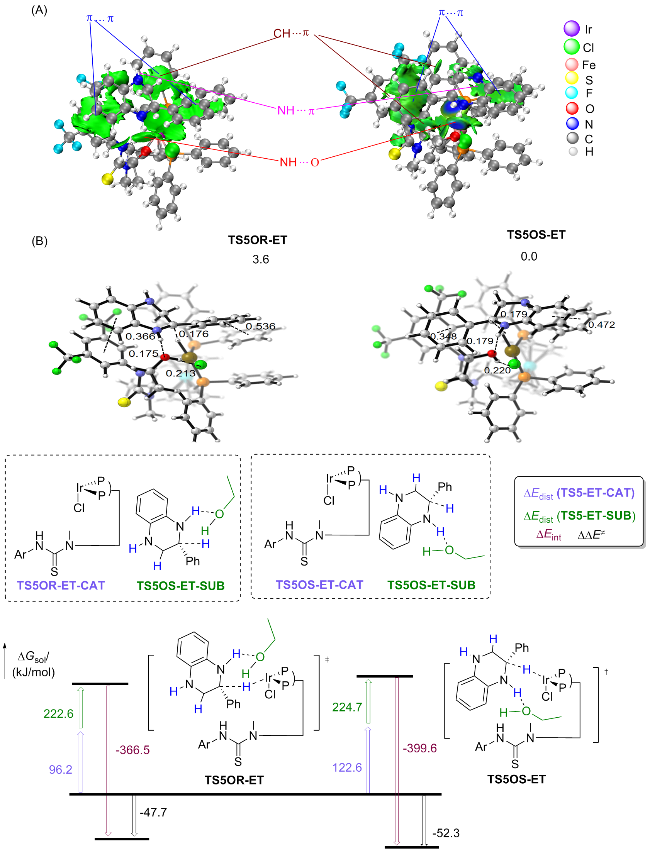
S-构型. 我们同样对过渡态
C-TS5OR-ET、
C-TS5OS-ET进行了IGMH分析和distortion-interaction分析(
图5). 图中复合物分为2-苯基喹喔啉和催化剂片段. 分析表明,
C-TS5OR-ET中四氢喹喔啉底物和催化剂的相互作用能为52.3 kJ/mol, 高于
A-TS5OS, 这很大一部分归因于
C-TS5OR-ET内底物和配体之间较强的π-π相互作用(
A-TS5OR和
A-TS5OS中两个苯环之间的距离分别为0.366和0.348 nm). 两个过渡态自由能差异便是乙醇系统中对映选择性的来源. 整个反应过程体现了Ir催化剂的高效活化作用、底物和催化剂的相互作用, 以及乙醇溶剂通过氢键对过渡态的稳定作用, 最终实现对映选择性的不对称氢化. 手性Ir催化剂在氢气分子活化与选择性氢转移过程中起到了核心作用, 并通过多步协同反应实现底物的高效转化.