C—O键的定向构建在新药开发及材料科学等应用领域有着重要意义, 通过该方式可以合成各种天然产物和具有重要生物学意义的支架
[1-3], 这些化合物可用于合成治疗不同疾病的药物
[4]. Kim等
[5]使用分子内醚化的方式构建C—O键, 合成了汉城链霉素的关键中间体, 并且该中间体具有汉城链霉素的所有必需功能. 二芳基醚是广泛存在于合成或天然药物、农药、聚合物、配体和生命科学等行业的一类重要中间体
[6], 其中, 间苯氧基苯甲醛是合成高效、广谱、安全且低毒的拟除虫菊酯类农药的关键中间体. 因此, 通过C—O偶联开发实用且可扩展的新合成路线或改进现有的二芳基醚制备路线具有重要的工业应用价值
[7]. 目前, 在国内工业生产中普遍采用的是以间苯氧基甲苯为原料, 先经氯化得到一氯苄和二氯苄, 再使用混酸或者稀硝酸水解得到间苯氧基苯甲醛的方法
[8]. 由卤代芳烃与苯酚偶联是制备间苯氧基苯甲醛的另一个简单高效路线
[9-10]. 使用贵金属催化剂如Pd催化卤代芳烃与苯酚C—O偶联制备二芳基醚是一种效率较高的生产方式
[11-13]. 但是, 钯的催化体系价格高昂, 限制了其规模应用
[14-15]. 非贵金属Cu催化剂价格低廉, 且在合成二芳基醚的研究中取得了重大进展
[16-18]. Ruta等
[19]将铜原子吸附在吡咯配体上, 开发了一种新型的单原子铜催化剂, 该催化剂在芳基溴和苯酚的C—O偶联反应中表现出较好的催化反应性能. 值得注意的是, 马大为团队
[20-22]进行了一系列草酰胺配体的研究, 并且实现了氯代芳烃与苯酚的C—O偶联反应, 可以使二芳香醚键的构建朝着低催化剂用量和低反应温度的方向发展. 我们也对催化卤代芳烃与苯酚的 C—O偶联反应有着极大的兴趣
[23], 设计并制备了一种离子聚合物负载的CuO纳米催化剂, 并证明了该催化剂对芳基卤化物与酚的交叉偶联有着较高的反应活性
[24].
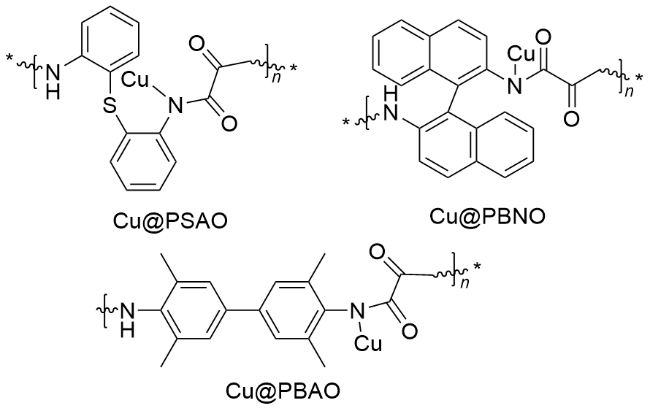
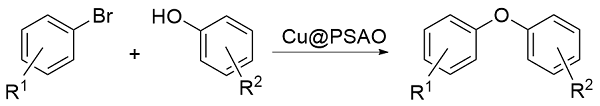
本工作在前人研究的基础上, 探索并制备了一系列草酰二胺聚合物. 将金属Cu化合物和不同的草酰二胺聚合物复合, 通过Cu(I)和草酰二胺聚合物进行配位, 得到催化剂Cu@PSAO, Cu@PBNO和Cu@PBAO(
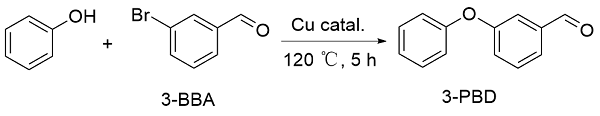
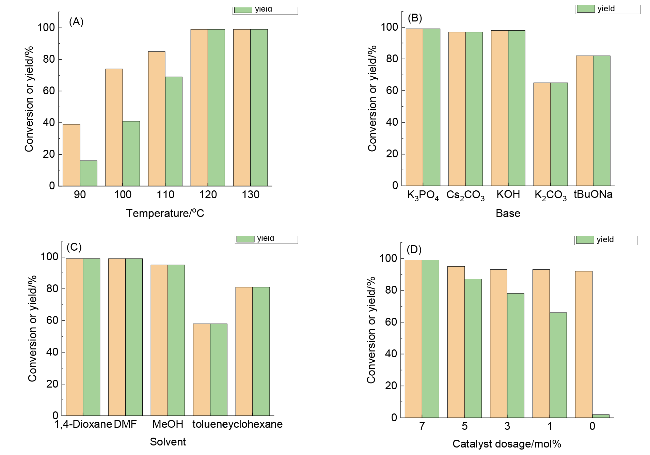
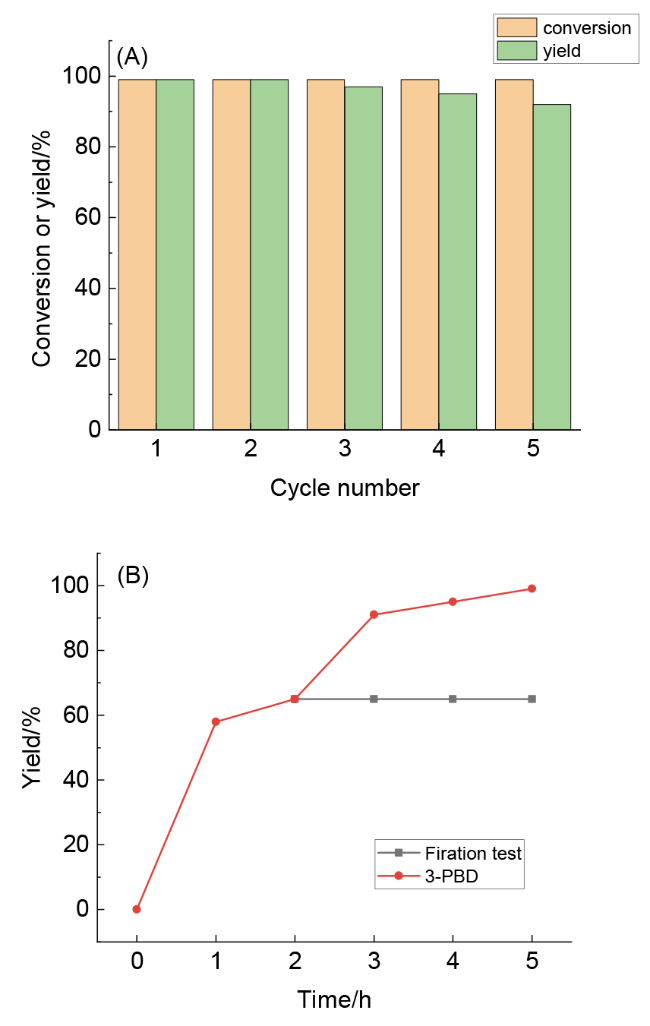
图1). 用这些催化剂研究了间溴苯甲醛和苯酚C—O偶联制备间苯氧基苯甲醛的反应性能. 其中Cu@PSAO催化剂表现出优异的反应选择性和很高的反应活性, 在优化反应条件后间苯氧基苯甲醛的收率可达99%以上. 与之前报道的基于Cu(I)、Cu(II)或Pd的催化体系相比, 催化剂Cu@PSAO价格低廉且稳定, 可以回收和重复使用至少五次, 且其催化活性不会显著降低. 催化剂Cu@PSAO对苯酚和间溴苯甲醛C—O偶联反应选择性高, 很好地避免了溴苯甲醛在碱性条件下的歧化副反应, 具有较好的应用前景.