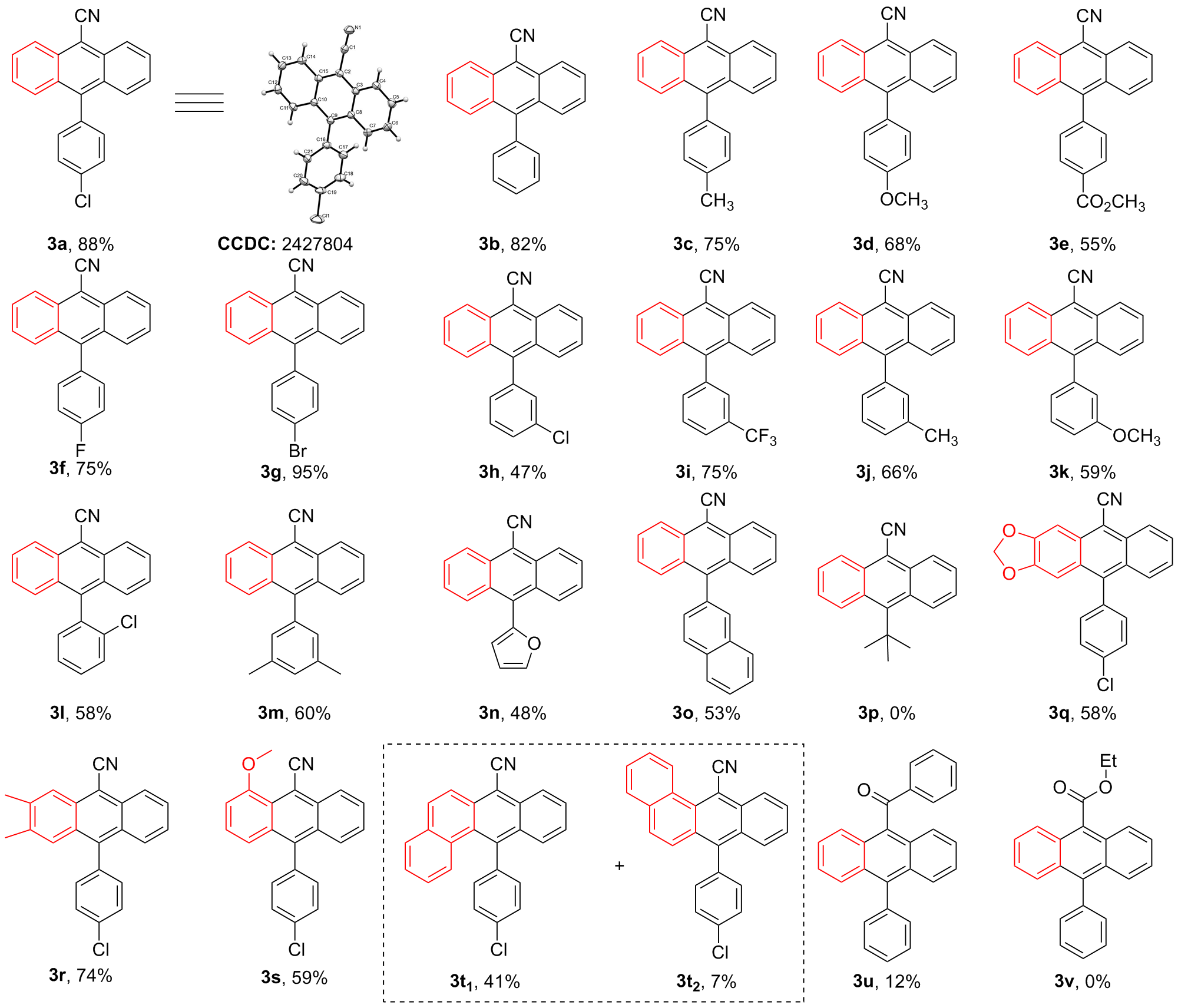
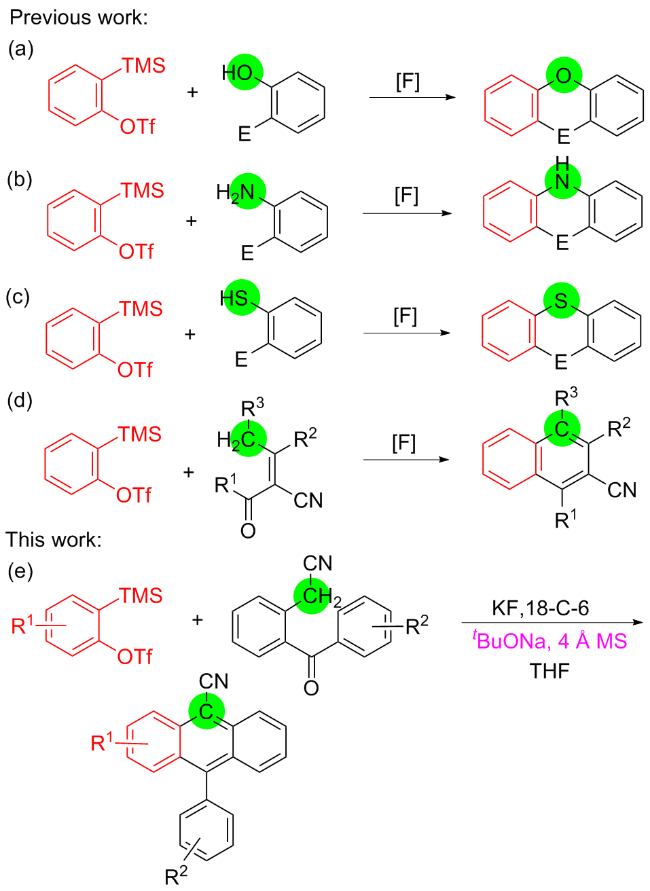
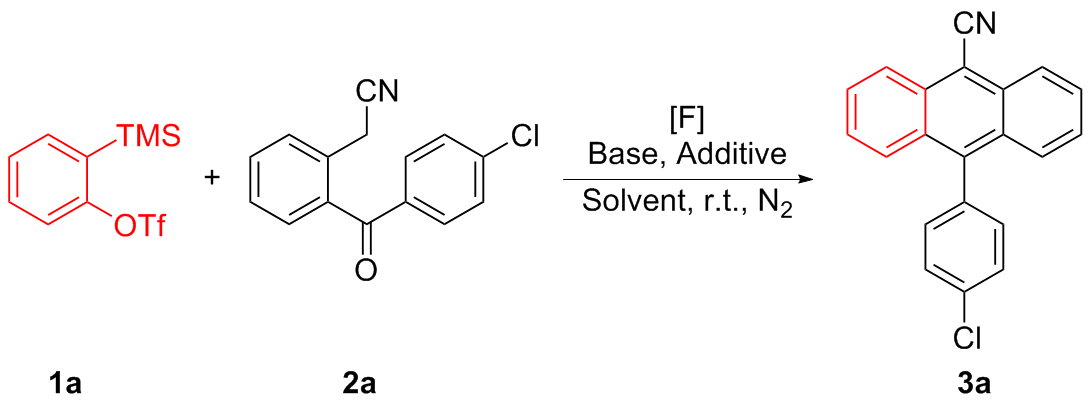
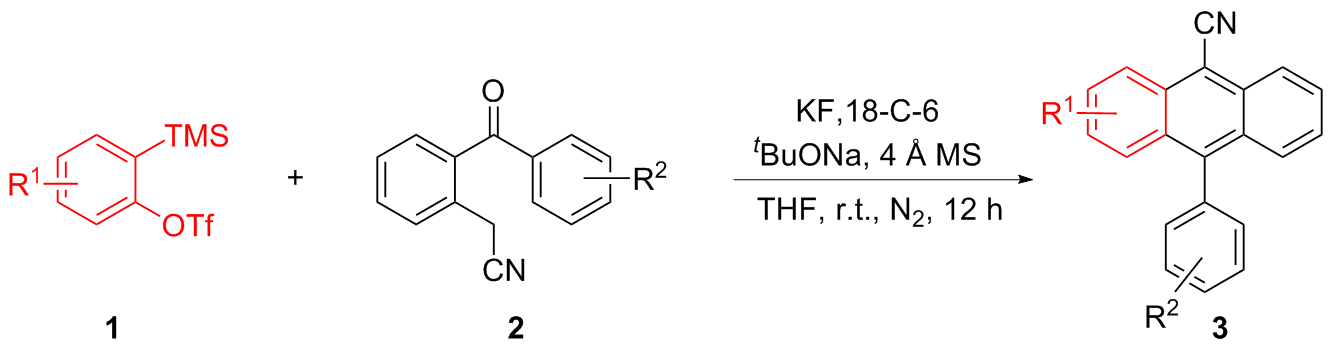
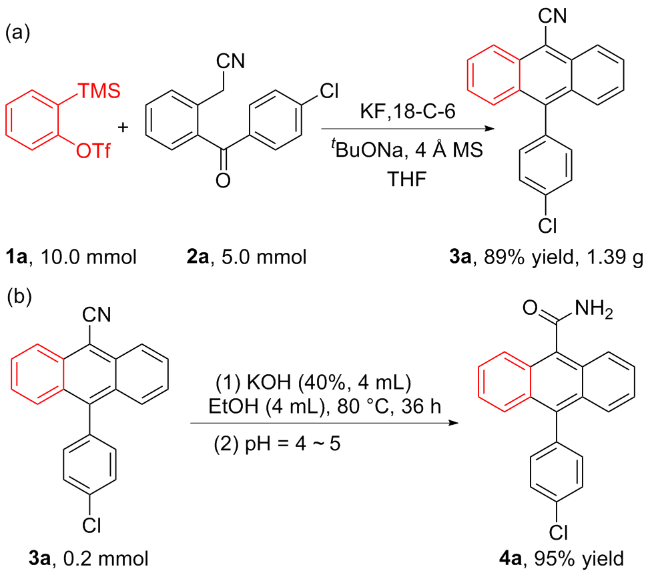
向装有磁子的10 mL反应管中依次加入苯甲酰苯乙腈2 (0. 20 mmol)、4 Å MS(200 mg)、tBuONa (0.6 mmol)、KF (0.8 mmol)和18-C-6 (0.8 mmol), 抽真空换氮气(N2)三次后加入溶剂THF (2.0 mL), 然后缓慢滴加苯炔前体1 (0. 40 mmol), 室温搅拌12 h后(通过TLC监测)用二氯甲烷稀释反应液, 用水(20 mL×3)萃取, 合并有机相, 使用无水硫酸钠干燥, 过滤, 减压浓缩得到粗产品, 经硅胶柱层析(石油醚/二氯甲烷, V∶V=5∶1)纯化, 得到目标产物3.
10-(4-氯苯基)蒽-9-甲酮(
3a)
[12]: 黄色固体, 55.1 mg, 产率88%. m.p. 263.7~263.9 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.49 (d,
J=8.8 Hz, 2H), 7.74~7.67 (m, 4H), 7.63~7.57 (m, 2H), 7.50~7.45 (m, 2H), 7.36~7.30 (m, 2H);
13C NMR (100 MHz, Chloroform-
d)
δ: 142.3, 135.8, 134.6, 133.1, 132.1, 129.7, 129.0, 128.8, 127.5, 126.6, 125.7, 117.5, 106.2.
10-苯基蒽-9-甲酮(
3b)
[11]: 黄色固体, 45.9 mg, 产率82%. m.p. 198.4~198.6 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.48 (d,
J=8.4 Hz, 2H), 7.73~7.67 (m, 4H), 7.63~7.56 (m, 3H), 7.47~7.42 (m, 2H), 7.41~7.36 (m, 2H);
13C NMR (100 MHz, Chloroform-
d)
δ: 143.9, 137.4, 133.2, 130.7, 129.7, 128.7, 128.7, 128.4, 128.0, 126.3, 125.6, 117.6, 105.7.
10-(对甲苯基)蒽-9-甲酮(
3c)
[12]: 黄色固体, 44.1 mg, 产率75%. m.p. 239.8~240.1 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.49 (d,
J=8.8 Hz, 2H), 7.76 (d,
J=8.8 Hz, 2H), 7.72~7.67 (m, 2H), 7.47~7.40 (m, 4H), 7.31~7.26 (m, 2H), 2.54 (s, 3H);
13C NMR (100 MHz, Chloroform-
d)
δ: 144.2, 138.2, 134.3, 133.2, 130.7, 129.9, 129.4, 128.7, 128.1, 126.2, 125.5, 117.7, 105.5, 21.5.
10-(4-甲氧基苯基)蒽-9-甲酮(
3d)
[11]: 黄色固体, 41.6 mg, 产率68%. m.p. 227.4~227.7 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.48 (d,
J=8.4 Hz, 2H), 7.78 (d,
J=8.8 Hz, 2H), 7.73~7.66 (m, 2H), 7.49~7.42 (m, 2H), 7.33~7.28 (m, 2H), 7.16~7.11 (m, 2H), 3.96 (s, 3H);
13C NMR (100 MHz, Chloroform-
d)
δ: 159.7, 143.9, 133.3, 132.0, 130.1, 129.3, 128.7, 128.1, 126.2, 125.6, 117.7, 114.1, 105.5, 55.6.
4-(10-氰基蒽-9-基)苯甲酸甲酯(3e): 黄色固体, 37.2 mg, 产率55%. m.p. 260.2~260.5 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.50 (d, J=8.8 Hz, 2H), 8.32~8.27 (m, 2H), 7.75~7.69 (m, 2H), 7.64 (d, J=8.8 Hz, 2H), 7.52~7.44 (m, 4H), 4.02 (s, 3H); 13C NMR (100 MHz, Chloroform-d) δ: 166.9, 142.4, 142.4, 133.1, 131.0, 130.4, 130.0, 129.4, 128.9, 127.5, 126.7, 125.7, 117.4, 106.3, 52.5.
10-(4-氟苯基)蒽-9-甲酮(
3f)
[12]: 黄色固体, 44.8 mg, 产率75%. m.p. 214.3~214.6 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.49 (d,
J=8.6 Hz, 2H), 7.74~7.67 (m, 4H), 7.50~7.44 (m, 2H), 7.39~7.28 (m, 4H);
13C NMR (100 MHz, Chloroform-
d)
δ: 162.9, (d,
J=264.4 Hz), 142.6, 133.2, (d,
J=5.6 Hz) 132.5, (d,
J=8.0 Hz), 129.9, 128.8, 127.7, 126.6, 125.7, 117.5, 116.0, 115.8, 106.1;
19F NMR (376 MHz, Chloroform-
d)
δ: 113.38.
10-(4-溴苯基)蒽-9-甲酮(
3g)
[12]: 黄色固体, 68.6 mg, 产率96%. m.p. 283.5~283.7 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.50 (d,
J=8.8 Hz, 2H), 7.77~7.67 (m, 6H), 7.51~7.45 (m, 2H), 7.30~7.26 (m, 2H);
13C NMR (100 MHz, Chloroform-
d)
δ: 142.3, 136.3, 133.2, 132.5, 132.0, 129.6, 128.9, 127.6, 126.7, 125.7, 122.8, 117.5, 106.2.
10-(3-氯苯基)蒽-9-甲酮(3h): 黄色固体, 29.7 mg, 产率47%. m.p. 161.7~161.9 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.50 (d, J=8.8 Hz, 2H), 7.75~7.67 (m, 4H), 7.59~7.47 (m, 4H), 7.44~7.37 (m, 1H), 7.32~7.27 (m, 1H); 13C NMR (100 MHz, Chloroform-d) δ: 141.9, 139.3, 134.8, 133.1, 130.8, 130.1, 129.6, 129.0, 128.8, 128.7, 127.5, 126.7, 125.7, 117.4, 106.3.
10-(3-(三氟甲基)苯基)蒽-9-甲酮(3i): 黄色固体, 52.2 mg, 产率75%. m.p. 180.0~180.3 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.52 (dt, J=8.8, 1.2 Hz, 2H), 7.90~7.85 (m, 1H), 7.79~7.69 (m, 4H), 7.63~7.59 (m, 3H), 7.53~7.47 (m, 2H); 13C NMR (100 MHz, Chloroform-d) δ: 141.6, 138.3, 134.2, 133.1, 131.4, (q, J=32.3 Hz), 129.6, 129.4, 128.9, 127.5, (q, J=3.8 Hz), 127.3, 126.9, 125.7, 125.4, (q, J=4.0 Hz), 122.7, 117.3, 106.6. 19F NMR (376 MHz, Chloroform-d) δ: 62.49.
10-(间甲苯基)蒽-9-甲酮(
3j)
[12]: 黄色固体, 38.5 mg, 产率66%. m.p. 154.1~154.3 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.48 (d,
J=8.8 Hz, 2H), 7.76~7.66 (m, 4H), 7.50~7.37 (m, 4H), 7.21~7.16 (m, 2H), 2.47 (s, 3H);
13C NMR (100 MHz, Chloroform-
d)
δ: 144.2, 138.4, 137.3, 133.2, 131.3, 129.7, 129.1, 128.7, 128.5, 128.1, 127.8, 126.2, 125.5, 117.7, 105.5, 21.6.
10-(3-甲氧基苯基)蒽-9-甲酮(
3k)
[12]: 黄色固体, 36.2 mg, 产率59%. m.p. 184.1~184.4 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.48 (d,
J=8.8 Hz, 2H), 7.78~7.67 (m, 4H), 7.54~7.43 (m, 3H), 7.14~7.09 (m, 1H), 7.00~6.92 (m, 2H), 3.86 (s, 3H);
13C NMR (100 MHz, Chloroform-
d)
δ: 159.8, 143.7, 138.8, 133.2, 129.8, 129.7, 128.8, 128.0, 126.4, 125.6, 123.2, 117.6, 116.3, 114.0, 105.7, 55.5.
10-(2-氯苯基)蒽-9-甲酮(3l): 黄色固体, 36.0 mg, 产率58%. m.p. 212.4~212.6 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.52 (d, J=8.8 Hz, 2H), 7.75~7.66 (m, 3H), 7.59~7.46 (m, 6H), 7.34 (dd, J=7.2, 1.6 Hz, 1H); 13C NMR (100 MHz, Chloroform-d) δ: 140.6, 136.2, 134.7, 133.2, 132.4, 130.2, 130.1, 129.5, 128.9, 127.2, 127.2, 126.9, 125.8, 117.5, 106.5.
10-(3,5-二甲基苯基)蒽-9-甲酮(3m)[12:] 黄色固体, 36.7 mg, 产率60%. m.p. 197.5~197.8 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.48 (d, J=8.8 Hz, 2H), 7.76 (dt, J=8.8, 1.0 Hz, 2H), 7.72~7.66 (m, 2H), 7.47~7.42 (m, 2H), 7.22~7.18 (m, 1H), 7.03~6.92 (m, 2H), 2.43 (s, 6H); 13C NMR (100 MHz, Chloroform-d) δ: 144.5, 138.2, 137.3, 133.2, 129.9, 129.8, 128.7, 128.5, 128.2, 126.2, 125.5, 117.8, 105.4, 21.5.
10-(呋喃-2-基)蒽-9-甲酮(3n): 黄色固体, 25.7 mg, 产率48%. m.p. 190.4~190.7 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.35 (d, J=8.8 Hz, 2H), 7.89 (d, J=8.8 Hz, 2H), 7.68 (t, J=1.6 Hz, 1H), 7.63~7.56 (m, 2H), 7.46~7.40 (m, 2H), 6.65 (d, J=1.2 Hz, 2H); 13C NMR (100 MHz, Chloroform-d) δ: 148.9, 143.9, 133.1, 132.1, 130.7, 128.9, 127.4, 127.1, 125.6, 117.4, 113.7, 111.4, 107.4.
10-(萘-2-基)蒽-9-甲酮(
3o)
[12]: 黄色固体, 35.1 mg, 产率53%. m.p. 226.1~226.3 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 8.53 (d,
J=8.8 Hz, 2H), 8.08 (d,
J=8.4 Hz, 1H), 8.05~8.01 (m, 1H), 7.93~7.89 (m, 2H), 7.77~7.74 (m, 2H), 7.73~7.69 (m, 2H), 7.66~7.60 (m, 2H), 7.51 (dd,
J=8.3, 1.7 Hz, 1H), 7.46~7.40 (m, 2H);
13C NMR (100 MHz, Chloroform-
d)
δ: 143.8, 134.8, 133.3, 133.2, 133.1, 130.0, 129.9, 128.8, 128.6, 128.4, 128.2, 128.1, 128.0, 127.0, 126.9, 126.4, 125.6, 117.7, 105.8.
10-(4-氯苯基)蒽[3-d][1,3]二氧代-5-酮(3q): 黄色固体, 41.6 mg, 产率58%. m.p. 211.4~211.6 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.39 (dt, J=8.4, 1.2 Hz, 1H), 7.73 (s, 1H), 7.67~7.61 (m, 1H), 7.60~7.53 (m, 3H), 7.43~7.39 (m, 1H), 7.31~7.28 (m, 2H), 6.84 (s, 1H), 6.11 (s, 2H); 13C NMR (100 MHz, Chloroform-d) δ: 150.9, 148.9, 140.5, 136.3, 134.6, 132.6, 132.0, 132.0, 129.2, 129.0, 128.1, 127.1, 126.1, 125.2, 117.9, 104.8, 102.1, 102.1, 100.7.
10-(4-氯苯基)-2,3-二甲基蒽-9-甲酮(3r): 黄色固体, 50.5 mg, 产率74%. m.p. 177.2~177.6 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.44 (dt, J=8.8, 1.2 Hz, 1H), 8.23 (s, 1H), 7.69~7.58 (m, 4H), 7.45~7.40 (m, 1H), 7.38 (s, 1H), 7.34~7.30 (m, 2H), 2.54 (s, 3H), 2.37 (s, 3H); 13C NMR (100 MHz, Chloroform-d) δ: 140.92, 140.02, 137.28, 136.17, 134.43, 132.70, 132.17, 129.30, 129.03, 128.96, 128.25, 127.44, 126.20, 126.09, 125.58, 124.66, 117.89, 104.57, 20.71, 20.68.
10-(4-氯苯基)-2-甲氧基蒽-9-甲酮(3s): 黄色固体, 40.0 mg, 产率59%. m.p. 211.2~211.5 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.45 (d, J=8.8, 1.2 Hz, 1H), 8.10 (dd, J=8.8, 1.2 Hz, 1H), 7.72~7.66 (m, 1H), 7.64~7.58 (m, 1H), 7.56~7.52 (m, 1H), 7.48~7.39 (m, 3H), 7.24~7.16 (m, 2H), 6.74 (d, J=7.2, 1H), 3.49 (s, 3H); 13C NMR (100 MHz, Chloroform-d) δ: 157.5, 141.3, 140.4, 135.0, 133.0, 132.7, 132.1, 130.6, 130.4, 129.3, 129.0, 129.0, 128.1, 127.6, 126.3, 125.3, 122.6, 118.3, 117.8, 106.2, 104.9, 55.6.
12-(4-氯苯基)四烯-7-甲酮(3t1): 黄色固体, 29.0 mg, 产率41%. m.p. 265.1~265.4 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 8.51 (d, J=8.6 Hz, 1H), 8.31 (d, J=9.2 Hz, 1H), 7.86~7.81 (m, 2H), 7.78~7.73 (m, 1H), 7.67~7.61 (m, 3H), 7.55~7.48 (m, 3H), 7.34~7.30 (m, 2H), 7.23~7.17 (m, 1H); 13C NMR (100 MHz, Chloroform-d) δ: 141.6, 139.7, 134.7, 134.6, 133.4, 132.0, 131.9, 131.7, 131.5, 130.5, 130.2, 129.3, 128.8, 128.8, 127.7, 127.5, 127.1, 126.7, 125.4, 124.2, 117.7, 107.5.
7-(4-氯苯基)四烯-12-甲酮(3t2): 黄色固体, 6.2 mg, 产率7%. m.p. 216.4~216.6 ℃; 1H NMR (400 MHz, Chloroform-d) δ: 9.99 (d, J=8.4 Hz, 1H), 8.74 (d, J=8.8 Hz, 1H), 7.89~7.84 (m, 1H), 7.83~7.74 (m, 3H), 7.63~7.53 (m, 1H), 7.63~7.54 (m, 4H), 7.41 (d, J=9.4 Hz, 1H), 7.36~7.32 (m, 2H); 13C NMR (100 MHz, Chloroform-d) δ: 142.2, 136.5, 134.6, 133.7, 133.2, 132.2, 132.0, 130.3, 129.3, 129.1, 129.0, 128.9, 128.7, 128.5, 127.5, 127.4, 127.1, 126.7, 126.1, 125.0, 120.4, 104.0.
苯基(10-苯基蒽-9-基)甲酮(
3u)
[22]: 黄色固体, 8.6 mg, 产率12%. m.p. 199.5~199.7 ℃;
1H NMR (400 MHz, Chloroform-
d)
δ: 7.96~7.85 (m, 2H), 7.80~7.73 (m, 2H), 7.73~7.66 (m, 2H), 7.64~7.54 (m, 4H), 7.53~7.42 (m, 4H), 7.40~7.32 (m, 4H);
10-(4-氯苯基)蒽-9-甲酰胺(4a): 白色固体, 62.9 mg, 产率95%. m.p. 341.6~341.8 ℃; 1H NMR (400 MHz, DMSO-d6) δ: 8.37 (s, 1H), 8.19~8.10 (m, 3H), 7.75~7.70 (m, 2H), 7.63-7.57 (m, 2H), 7.54 (dt, J=8.8, 1.2 Hz, 2H), 7.50~7.35 (m, 4H); 13C NMR (100 MHz, DMSO-d6) δ: 170.3, 136.7, 135.5, 134.5, 132.8, 132.5, 129.0, 128.8, 126.4, 126.1, 126.1, 126.0, 125.8. HRMS (ESI) calcd for C21H16ClNO [M+H]+ 332.0837, found 332.0837.
辅助材料(Supporting Information) 化合物
3a~
3t和
4a的
1H NMR和
13C NMR谱图,
3f和
3i的
19F NMR谱图以及化合物
3a的单晶表征数据. 这些材料可以免费从本刊网站(
http://sioc-journal.cn/)上下载.