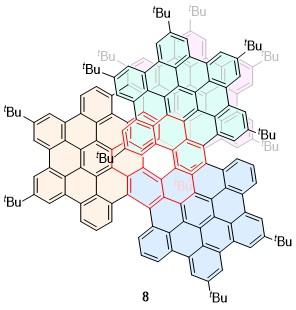
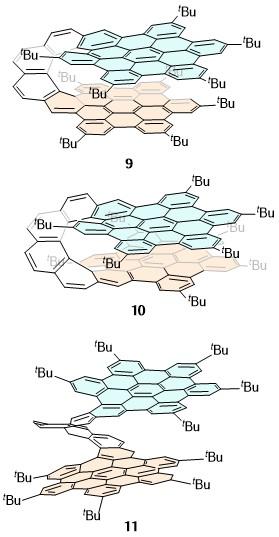
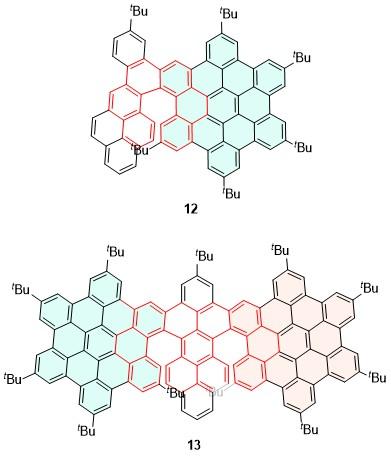
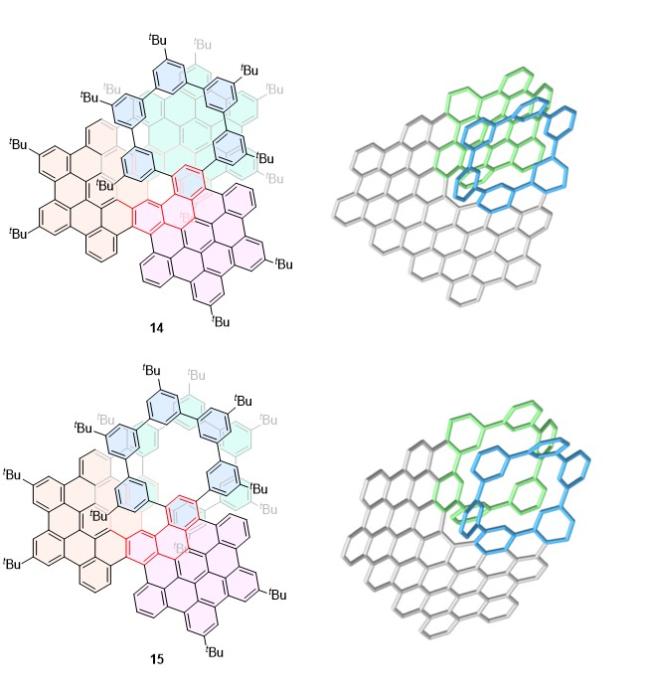
表1 螺烯衍生物1~84的光物理、手性光学性质Table 1 Photophysical and chiral optical properties of helicene derivatives 1~84 |
| Compd. | λPL/nm | ΦF/% | |glum|/10-3 | |gabs|/10-3 | BCPL/(L• mol-1•cm-1) | Ref. | Compd. | λPL/nm | ΦF/% | |glum|/10-3 | |gabs|/10-3 | BCPL/(L• mol-1•cm-1) | Ref. |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
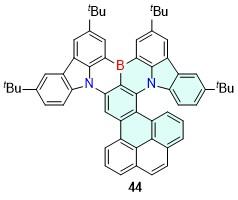
| 1 | 977 | 4.6 | — | — | — | [25] | 44 | 527 | 90 | 0.52 | — | — | [49] |
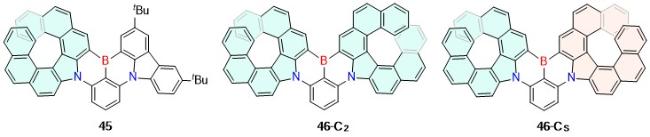
| 2-1 | 625 | 10.9 | 1.5 | — | — | [26] | 45 | 520 | 85 | 1.1 | 1.3 | 36 | [50] |
| 2-2 | 625 | 8.2 | 1.5 | — | — | [26] | 46-C2 | 543 | 72 | 1.5 | 1.7 | 65 | [50] |
| 3 | 652 | 93 | 0.8 | 7.0 | 32 | [27] | 46-CS | 546 | 78 | — | — | — | [50] |
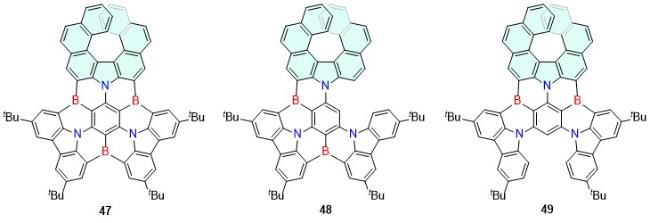
| 4 | 654 | 31.9 | 4.5 | 3.0 | — | [28] | 47 | 484 | 59 | 2.3 | 4.1 | — | [51] |
| 5 | 812 | 15.0 | 1.3 | 8.5 | — | [28] | 48 | 500 | 85 | 1.9 | 2.7 | — | [51] |
| 6 | 817 | 13.7 | 1.4 | 3.0 | — | [28] | 49 | 508 | 81 | 0.75 | 1.0 | — | [51] |
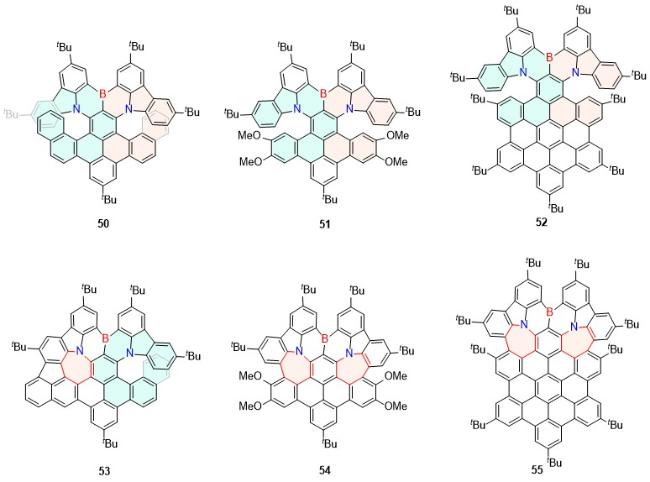
| 7 | 1010 | 6.5 | — | 1.2 | — | [28] | 50 | 595 | 68.3 | 2.7 | 7.4 | 41.5 | [52] |
| 8 | 684 | 10 | 45.2 | 27.6 | 304 | [29] | 51 | 585 | 65.7 | 2.5 | 8.6 | 45.8 | [52] |
| 9 | 575 | 22 | 36 | 36 | 81 | [30] | 52 | 598 | 74.3 | 2.7 | 3.1 | 58.7 | [52] |
| 10 | 543 | 10 | 10 | 16 | 21 | [30] | 53 | 622 | 10.8 | 2.9 | 4.7 | 2.0 | [52] |
| 11 | 528 | 11 | 9 | 10 | 28 | [30] | 54 | 563 | 27.3 | — | — | — | [52] |
| 12 | 519 | 29 | 3 | — | 41 | [31] | 55 | 595 | 1.7 | 5.0 | 6.6 | 4.0 | [52] |
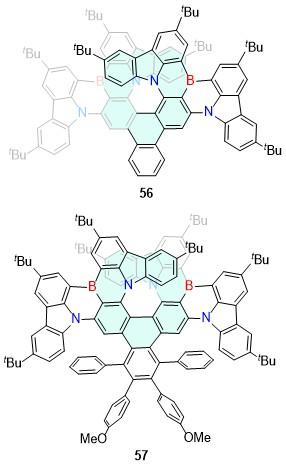
| 13 | 572 | 52 | 5 | — | 305 | [31] | 56 | 578 | 98 | 5.8 | 5.6 | 220 | [53] |
| 14 | 626 | 18.3 | 14.1 | 10.8 | 254 | [32] | 57 | 584 | 51 | — | — | — | [54] |
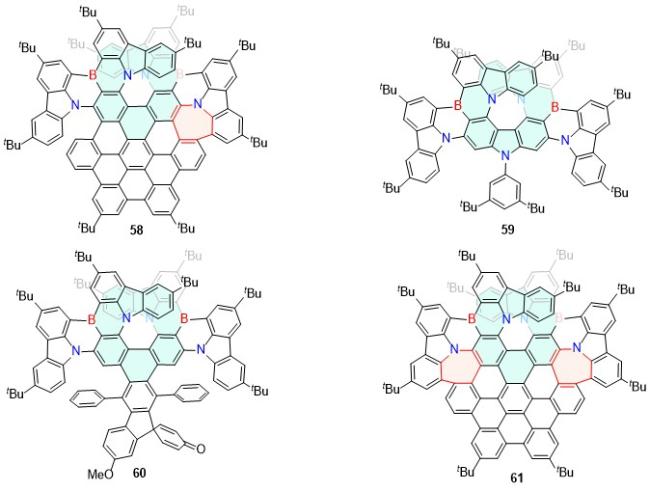
| 15 | 589 | 15.6 | 2.6 | 3.7 | 6.35 | [32] | 58 | 648 | 68 | — | — | — | [54] |
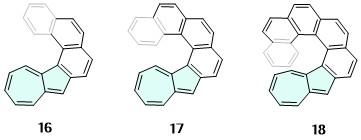
| 16 | 481 | <10 | — | — | — | [33] | 59 | 520 | 88 | — | — | — | [54] |
| 17 | 499 | <10 | — | 22 | — | [33] | 60 | 600 | 48 | — | — | — | [54] |
| 18 | 463 | <10 | — | 21 | — | [33] | 61 | 660 | 22 | — | — | — | [54] |
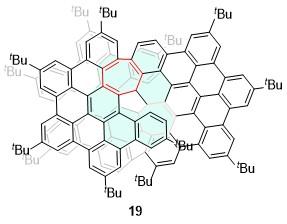
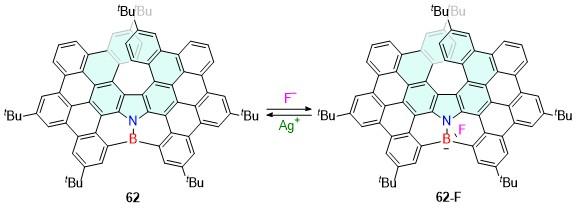
| 19 | 602 | 32 | 1.3 | 6.6 | — | [34] | 62 | 493 | — | 0.47 | 1.6 | — | [55] |
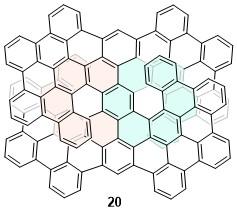
| 20 | 635 | 18 | — | 19 | — | [35] | 62-F | 502 | — | 1.7 | 3.0 | — | [55] |
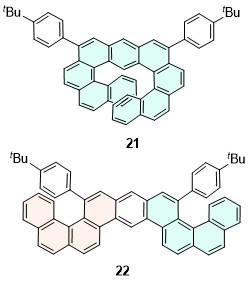
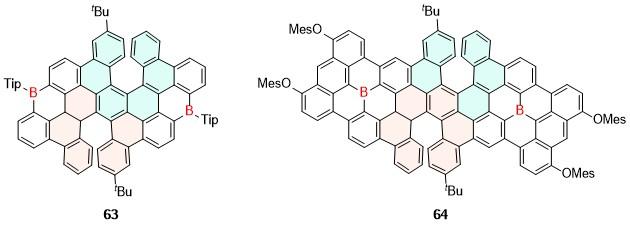
| 21 | — | — | — | — | — | [36] | 63 | 618 | 22 | — | — | — | [56] |
| 22 | — | — | — | — | — | [36] | 64 | — | — | — | — | — | [56] |
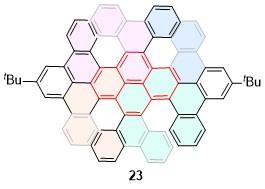
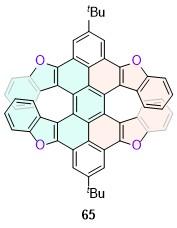
| 23 | 612 | 58 | 0.78 | 6.9 | — | [37] | 65 | 511 | 71 | 0.75 | — | — | [57] |
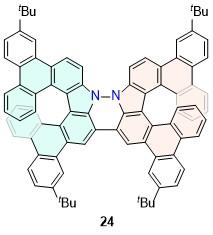
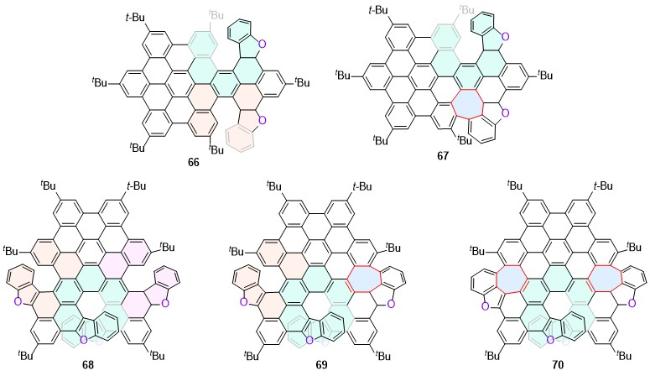
| 24 | 583 | 86 | 0.22 | 0.48 | 13.2 | [38] | 66 | 535 | 48.5 | 0.6 | 5.2 | 10.8 | [58] |
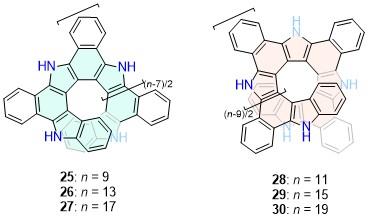
| 25 | 423 | 21 | 4.5 | 5.6 | — | [39] | 67 | 542 | 3.4 | 1.5 | 3.3 | 1.7 | [58] |
| 26 | 459 | 11 | 1.7 | 4.2 | — | [39] | 68 | 575 | 53.9 | 0.5 | 4.6 | 13.9 | [58] |
| 27 | 483 | 18 | — | — | — | [39] | 69 | 590 | 26.2 | 1.6 | 4.0 | 14.7 | [58] |
| 28 | 452 | 17 | 4.2 | 4.2 | — | [39] | 70 | 594 | 10.2 | 2.1 | 3.6 | 7.1 | [58] |
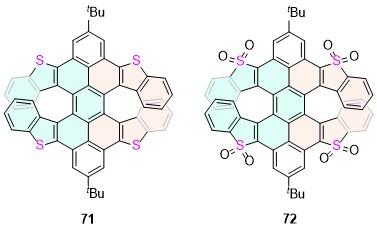
| 29 | 466 | 9 | 5.7 | 1.7 | — | [39] | 71 | 558 | 43 | 1.1 | 14 | — | [59] |
| 30 | 508 | 8 | — | — | — | [39] | 72 | 614 | 31 | 1.2 | 7.2 | — | [59] |
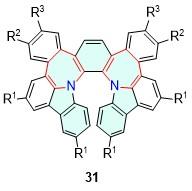
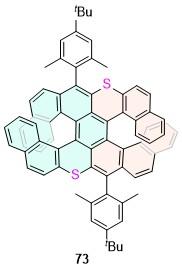
| 31 | 625 | — | 17 | — | — | [40] | 73 | 666 | 48 | 0.59 | 7.5 | 5.71 | [60] |
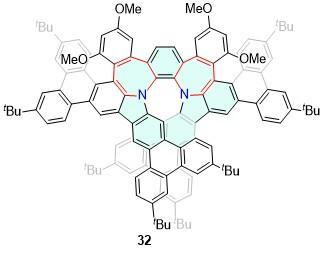
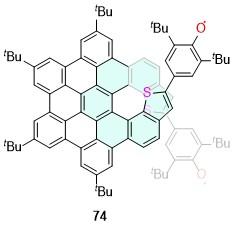
| 32 | 517 | — | 2 | — | — | [40] | 74 | — | — | — | — | — | [61] |
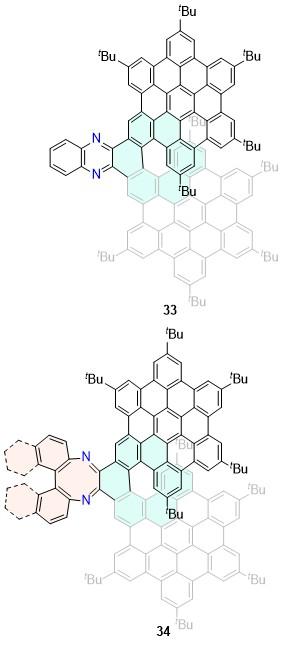
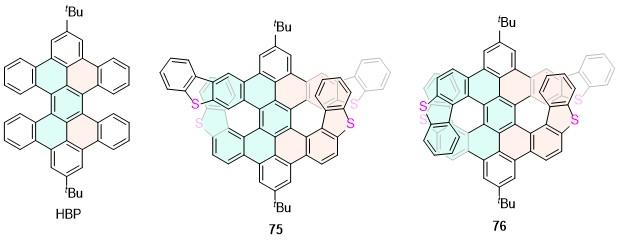
| 33 | 646 | 44 | 0.73 | 1.24 | 14.13 | [41] | 75 | 569 | 83 | 2.2 | 4.0 | 84.9 | [62] |
| 34 | 576 | 79 | 5.5 | 2.99 | 145.99 | [41] | 76 | 583 | 91 | 2.3 | 5.3 | 65 | [62] |
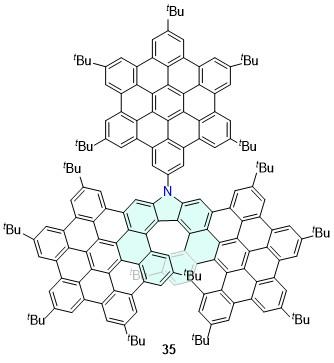
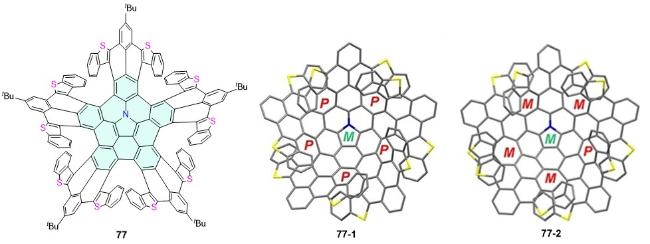
| 35 | 628 | 40 | 0.43 | 2.98 | 32.5 | [42] | 77-1 | 778 | 14 | — | — | — | [63] |
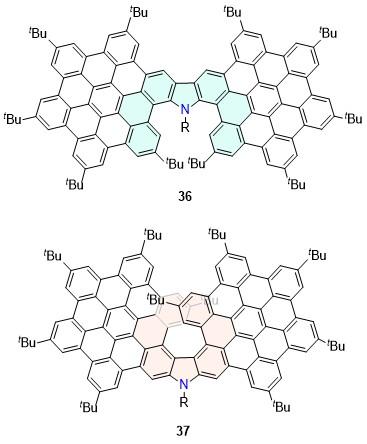
| 36 | 497 | 68 | — | — | — | [43] | 77-2 | 769 | 11 | — | — | — | [63] |
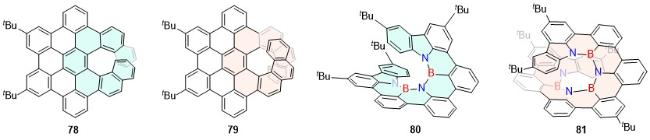
| 37 | 542 | 75 | 1.12 | 3.91 | 45.77 | [43] | 78 | 495 | 25 | 0.77 | 1.24 | 1.1 | [64] |
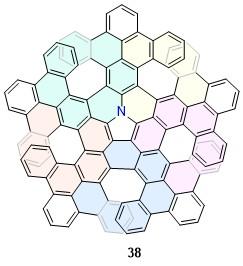
| 38 | 770 | 28 | — | — | — | [44] | 79 | 528 | 41 | 7.44 | 10.58 | 12.6 | [64] |
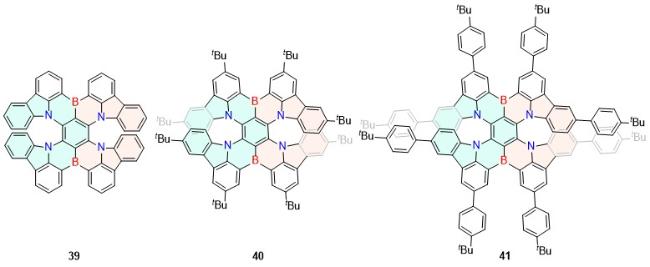
| 39 | 660 | 100 | 2 | 33 | 28.5 | [46] | 80 | 409 | 31 | 24 | 36 | 294 | [65] |
| 40 | 684 | 99 | 2 | 31 | 37.1 | [46] | 81 | 430 | 24 | 48 | 61 | 292 | [65] |
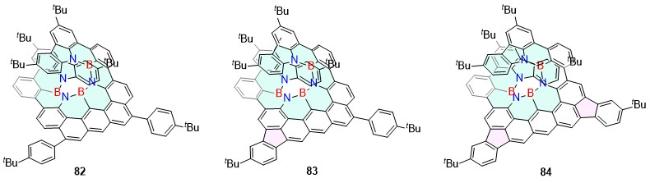
| 41 | 696 | 90 | 2 | 26 | 40 | [46] | 82 | 515 | 82 | 17 | 24 | 583 | [66] |
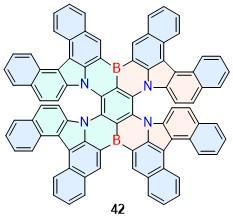
| 42 | 737 | 60 | — | — | — | [47] | 83 | 529 | 67 | 11 | 11 | 374 | [66] |
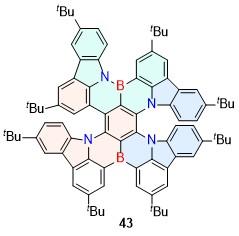
| 43 | 617 | 96 | 1.4 | 2 | 20.8 | [48] | 84 | 535 | 72 | 8 | 12 | 349 | [66] |