细菌感染已经成为全球主要的公共卫生问题
[1-2]. 尽管抗生素的发现和使用对治疗细菌感染性疾病具有显著意义
[3-4], 但由于近年来抗生素的滥用, 细菌耐药已成为一个全球性日益的严重问题, 严重威胁着人类健康
[5-6]. 大多数的抗生素都是针对细菌的内过程, 而细菌的生物膜是天然的屏障, 能够有效阻止和延缓许多抗生素渗入细菌内部, 因此, 可用于临床治疗的药物较少, 且导致细菌易产生耐药性
[7-8]. 因此, 研究新型的抗菌疗法以解决细菌耐药性问题至关重要.
荧光成像介导的光动力疗法(Photodynamic therapy, PDT)作为一种非侵入性、时空选择性强及光敏药物荧光可视化的诊疗技术, 近年来在抗感染领域展现出重要应用潜力
[9-12]. 其核心机制依赖于光敏剂(Photosensitizer, PS)在特定波长光激发下产生活性氧(Reactive oxygen species, ROS), 通过氧化应激破坏细菌细胞膜、蛋白质及核酸, 最终实现病原体灭活. 然而, 传统商用化光敏剂在抗菌应用中面临诸多挑战
[13], 例如聚集导致的荧光猝灭和低效的ROS产生, 以及依赖高浓度光敏剂药物或强辐照剂量带来的潜在毒性和副作用等问题. 因此, 优化光敏剂的荧光量子效率和ROS效率对于提高光动力诊疗效果至关重要. 传统提高ROS效率的方法主要包含两种: 其一为在光敏剂分子中引入重原子(如碘、溴)以增强单线态和三线态之间的自旋轨道耦合效应(Spin-orbit coupling, SOC)
[14]; 其二为构筑强电子给体-受体(Donor-Acceptor, D-A)结构以促进分子内电荷转移(Intramolecular charge transfer, ICT), 降低单线态和三线态之间能垒. 以上两种策略均通过促进单线态和三线态之间的系间窜越(Intersystem crossing, ISC)过程, 从而提高光敏剂产生ROS的效率
[15]. 然而, 重原子效应虽能促进ISC过程, 但可能引发材料的荧光聚集淬灭(Aggregation caused quenching, ACQ). D-A结构导致分子构象扭曲, 不利于提高光敏剂的摩尔吸光系数. 这些问题在耐药菌治疗中尤为突出, 因为细菌生物膜的存在可能进一步削弱光穿透性和药物渗透, 迫使临床需采用高浓度光敏剂或长时间高辐照剂量, 增加了治疗副作用风险.
具有聚集诱导发光(Aggregation-induced emission, AIE)特性的光敏剂因其在聚集状态下分子运动受限(Restriction of intramolecular motions, RIM), 导致非辐射跃迁通道受阻, 致使更多的单线态能量可以通过辐射跃迁实现良好的荧光量子效率; 或者通过ISC过程产生更多的三线态能量, 进而大大提高ROS效率
[16-17]. 因此, AIE型光敏剂具有越聚越亮和越聚ROS越高的独特优势, 在癌细胞和细菌的荧光可视化和可控光动力治疗方面应用广泛
[18-21]. 因此, 如何提高AIE光敏剂的聚集态荧光量子效率和ROS效率是决定光诊疗效率的关键所在. Zhu等
[22]以三苯胺为电子给体、噻吩为π桥、吡啶盐为电子受体, 制备了一款高效AIE自由基光敏剂(Pys-QM-TT). 该分子具有显著的分子内电荷转移效应, 降低了单线态与三线态之间的能级差, 促进了分子内ISC, 最终提升了自由基型ROS效率
[22]. 我们团队前期以强电子给体5,10-二氢还原吩嗪为核心, 进而引入不同类型的电子受体制备AIE自由基光敏剂. 实验结果发现, 随着电子受体的吸电子能力增强, 光敏剂产生的自由基型ROS效率越高
[23]. Zhang等
[24]联合I型光敏剂和H
2S气体疗法, 实现了良好的肿瘤协同治疗效果. 尽管通过强化分子内ICT效应可以有效提高AIE光敏剂的ROS效率, 但其荧光量子效率大大降低. 因此, 同时提高AIE光敏剂的荧光量子效率和ROS效率面临较大挑战.
离子型光敏剂具有良好的细胞线粒体靶向性, 强的自由基型ROS产生效率等优点, 在肿瘤治疗和促伤口愈合等领域具有广泛的应用前景
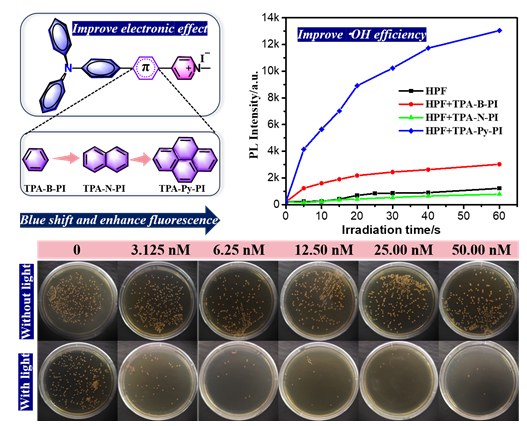
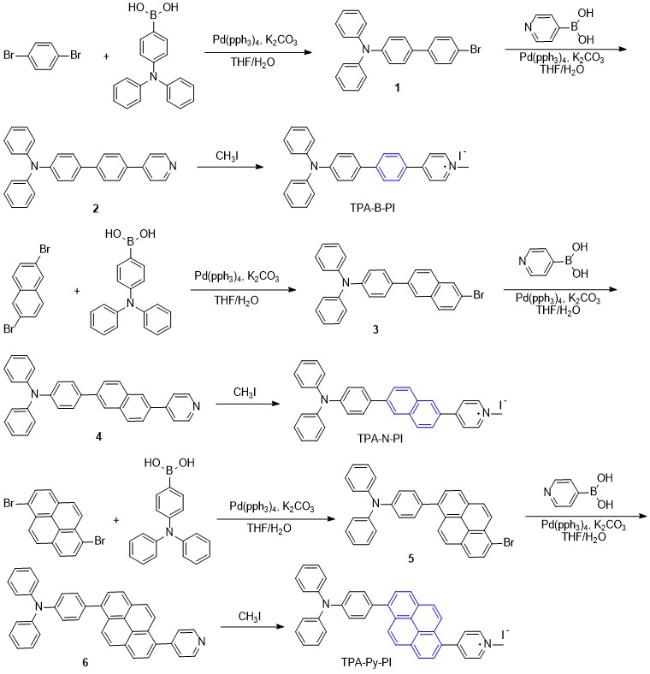
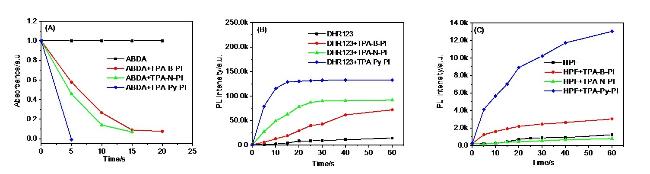
[25-27]. 因此, 为解决上述问题, 本研究以离子型AIE分子设计为指导, 系统调控分子内电荷转移激发态, 成功制备三种离子型AIE光敏剂, 分别命名为TPA-B-PI, TPA-N-PI和TPA-Py-PI. 光敏剂的分子结构及合成路线如
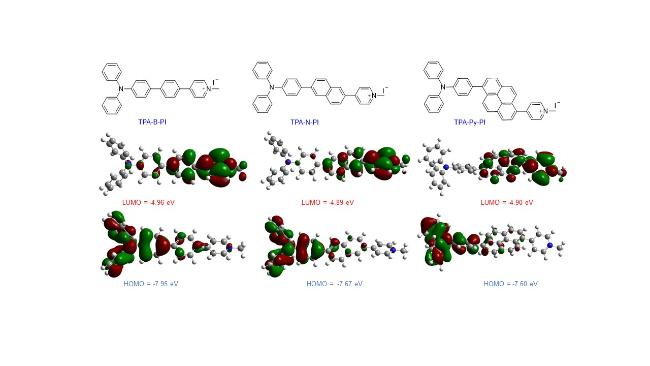
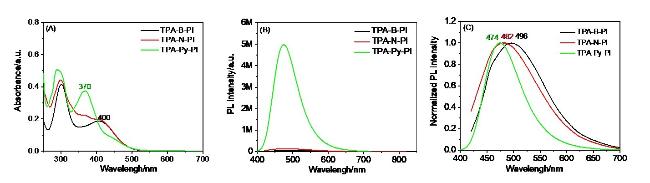
Scheme 1所示, 选用三苯胺(TPA)为电子给体, 赋予分子AIE特性, 从而抑制分子在聚集态的非辐射跃迁速率, 降低单线态能量的无效损耗; 以电荷型吡啶杂环为电子受体, 一方面构筑分子内ICT效应, 促进单线态与三线态之间的ISC过程, 提高光敏剂产生ROS效率, 另一方面, 强化光敏剂与革兰氏阳性菌的作用力, 促进光敏剂进入细菌菌体内部而充分发挥光动力灭菌功效. 通过在D-A单元间引入不同电子共轭程度的苯、萘和芘基元, 从而调控分子内局域激发和电荷转移激发态. 实验结果显示, 由于芘基元具有较大的共轭结构, 导致TPA-Py-PI分子的摩尔吸光系数显著优于TPA-B-PI和TPA-N-PI, 从而显著优化了TPA-Py-PI产生ROS的效率. 不仅如此, 芘基元的引入也弱化了分子内ICT效应, 强化了分子辐射跃迁效率, 显著提高了TPA-Py-PI的荧光量子效率. 选用TPA-Py-PI对革兰氏阳性菌(金黄色葡萄球菌和耐甲氧西林金黄色葡萄球菌)和阴性菌(大肠杆菌)进行光动力灭菌效果评估, 结果显示, TPA-Py-PI可以对革兰氏阳性和阴性菌均具有良好的光动力疗效. 更为重要的是, 在低白光辐照剂量(20 mW/cm
2)和低光敏剂浓度(25 nmol/L)条件下, 实现了对
MRSA超过99.99%的灭菌效果. 该工作为高效率光敏剂的设计提供重要参考依据.