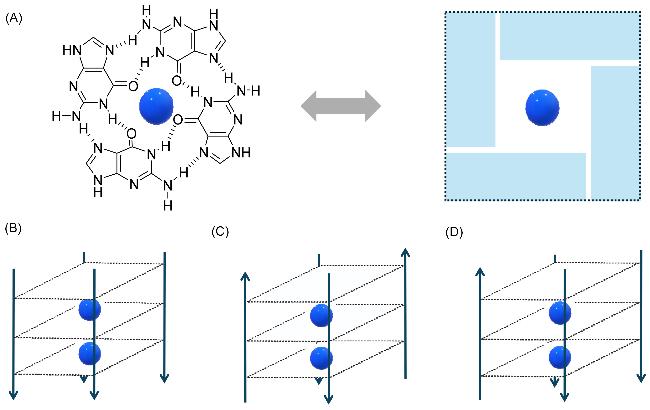
1 G4结构
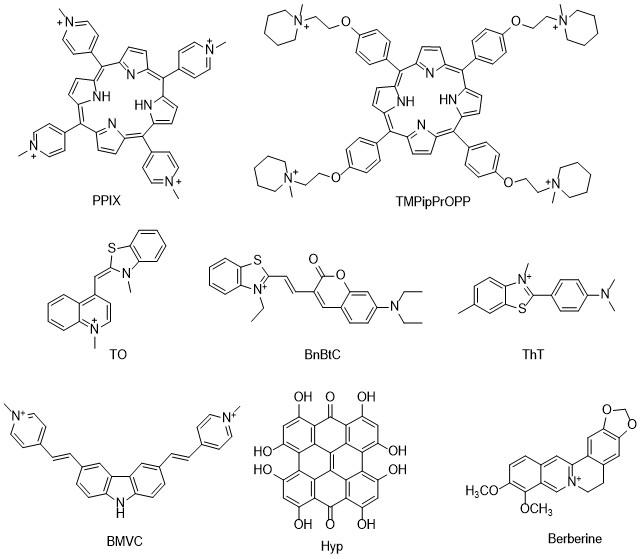
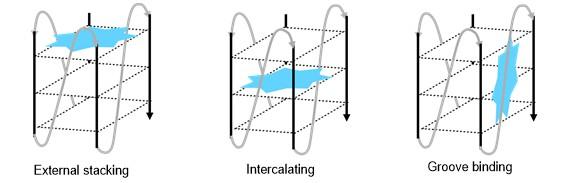
2 G4与配体的相互作用
3 G4生物传感应用
3.1 金属离子检测
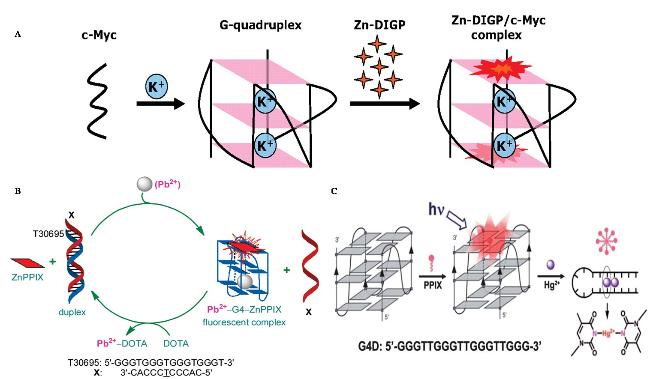
图4 基于G4进行金属离子检测应用实例: (A)基于G4与Zn-DIGP的特异性结合进行钾离子(K+)的检测[31]; (B)基于T30695和ZnPPIX的特异性结合和铅离子(Pb2+)诱导的G4组装完成铅离子(Pb2+)的检测[34]; (C)利用T-Hg-T与G4结构稳定性差异实现汞离子(Hg2+)的灵敏分析[36]Figure 4 Examples of metal ion detection applications based on G4: (A) Detection of potassium ions (K+) based on the specific binding of G4 to Zn-DIGP;[31] (B) Detection of lead ions (Pb2+) based on the specific binding of T30695 and ZnPPIX and lead ion-induced G4 assembly;[34] (C) Sensitive analysis of mercury ions (Hg2+) by using the difference in structural stability between T-Hg-T and G4[36] (A) Copyright (2010) American Chemical Society; (B) Copyright (2010) American Chemical Society; (C) Copyright (2014) The Royal Society of Chemistry |
3.2 蛋白检测
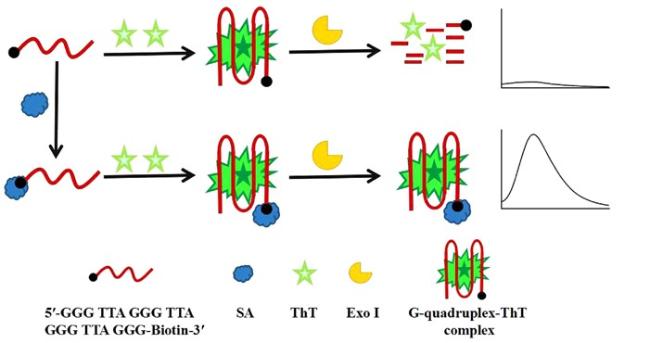
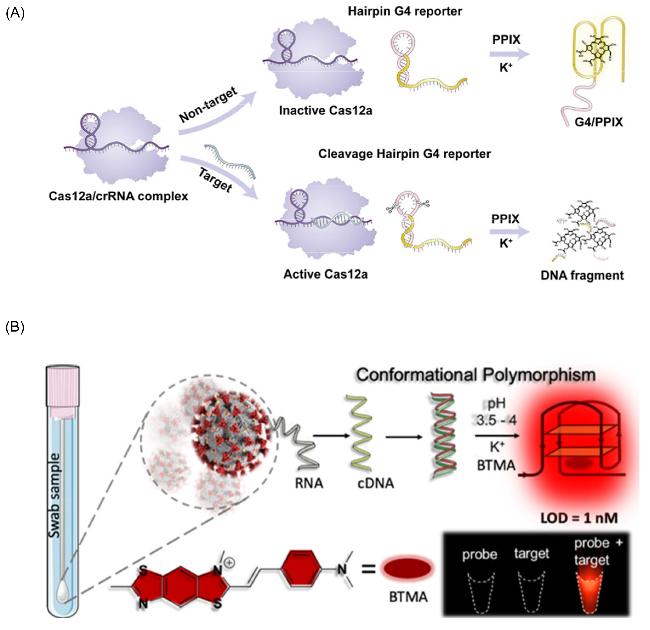
3.3 核酸分析
图6 基于G4进行核酸分析检测平台构建实例: (A) CRISPER/Cas12a与G4结合进行多种核酸目标链检测[57]; (B)基于pH调控cDNA的构型特异性地与BTMA结合进行SARS-CoV-2的定量分析[58]Figure 6 Examples of nucleic acid analysis and detection platform construction based on G4: (A) CRISPER/Cas12a combined with G4 for multiple nucleic acid target strand detection;[57] (B) Quantitative analysis of SARS-CoV-2 based on the configuration of pH-regulated cDNA that binds specifically to BTMA[58] (A) Copyright (2024) American Chemical Society; (B) Copyright (2022) American Chemical Society |
4 成像及治疗
4.1 生物成像
表1 部分G4探针的光物理性质Table 1 Photophysical properties of some G4 probes |
| Fluorescent ligand | G4 name | G4 topology | Ex/Em/nm | Kd/(µmol•L-1) | References |
|---|---|---|---|---|---|
| NIRG-2 | Pu22 | Parallel | 850/940 | 1.71±1.13 | [19] |
| 5a | Pu22 | Parallel | 575/650 | 1.549±0.080 | [81] |
| 5b | Pu22 | Parallel | 550/630 | 1.783±0.210 | [81] |
| AI7 | 21CTA | Hybrid | 389/500 | 1.3 | [82] |
| IZIN-1 | mt6363 | Parallel | 538/660 | — | [89] |
| ISAP | c-Myc | Parallel | 640/702 | 1.09 | [92] |
| SF3 | mt6363 | Parallel | 550/650 | 3.5 | [93] |
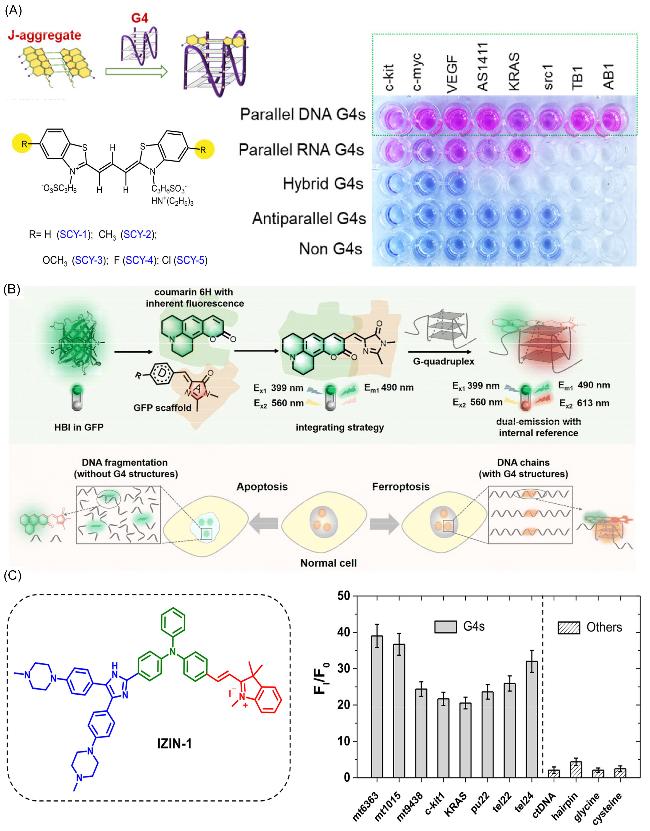
图7 基于G4进行细胞成像平台构建的实例: (A) SCY-5与不同G4和核酸链结合后荧光响应效果[78]; (B) NHCouI的合成路线及其与G4结合机制[79]; (C) IZIN-1分子结构及不同G4和核酸链结合后的荧光响应效果[89]Figure 7 Examples of cell imaging platform construction based on G4: (A) Fluorescence response effect of SCY-5 after binding to different G4 and nucleic acid chains;[78] (B) Synthesis route of NHCouI and its binding mechanism with G4;[79] (C) IZIN-1 molecular structure and fluorescence response effects of different G4 and nucleic acid chains binding[89] (A) Copyright (2024) American Chemical Society; (B) Copyright (2023) The Royal Society of Chemistry; (C) Copyright (2021) Elsevier B.V. |
表2 已报道的G4序列信息Table 2 Reported G4 sequence information |
| Name | Sequence (5'-3') |
|---|---|
| Pu27 | TTATGGGGAGGGTGGGGAGGGTGGGGAAGG |
| Myc-2345 | TGAGGGTGGGGAGGGTGGGGAA |
| Myc-1245 | TGGGGAGGGTTTTTAGGGTGGGGA |
| Myc-22 | TGAGGGTGGGTAGGGTGGGTAA |
| Pu241 | TGAGGGTGGIGAGGGTGGGGAA GG |
| ckit1 | CAGAGGGAGGGCGCTGGGAGGAGGGGCTG |
| ckit2 | CCCCGGGCGGGCGCGAGGGGAGGGGAGGC |
| bcl-2 | GTCGGGGCGAGGGCGGGGGAAGGAGGGCGCGGGCGGGGA |
| K-ras | GGGAGGGAGGGAAGGAGGGAGGGAGGGA |
| VEGF | CCCGGGGCGGGCCGGGGGCGGGGTCCCGGCGGGGCGGAG |
| HIF-1α | GCGAGGGCGGGGGAGAGGGGAGGGGCGCG |
4.2 疾病诊疗方法的开发
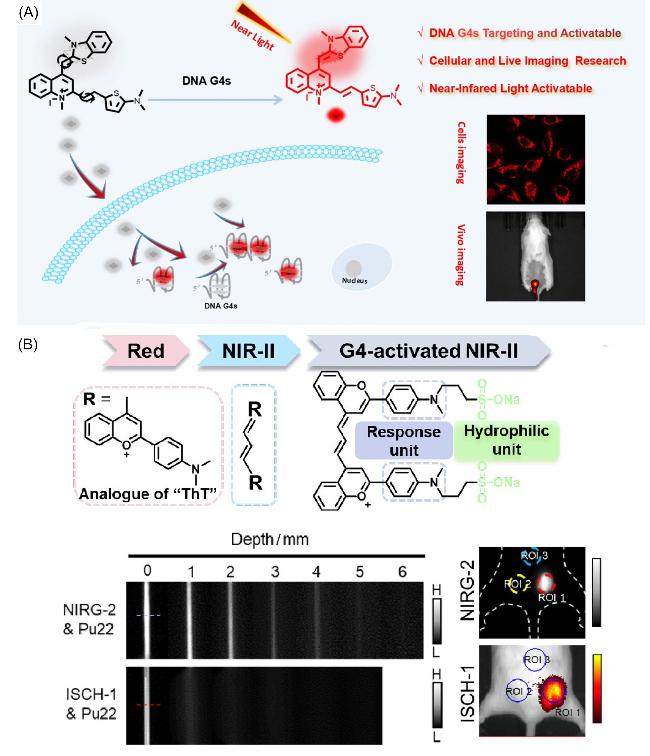
图8 基于G4进行癌症治疗方法实例. (A) TOH与G4结合进行的体内成像原理及成像图[91]. (B) NIRG-II荧光探针分子设计及用于肿瘤淋巴转移可视化监测[19]Figure 8 Example cancer treatment methods based on G4. (A) (A) In vivo imaging principle and imaging diagram of TOH combined with G4.[91] Copyright (2024) Elsevier B.V. (B) Molecular design of NIRG-II fluorescent probe and its application in visualization of tumor lymphatic metastasis.[19] Copyright (2024) American Chemical Society |