化学学报 ›› 2025, Vol. 83 ›› Issue (7): 667-673.DOI: 10.6023/A25050172 上一篇 下一篇
研究论文
张杰豪a, 徐明金a, 古满珍a,b, 马浩文b, 蔡倩b,*( )
)
投稿日期:2025-05-15
发布日期:2025-07-28
基金资助:
Jiehao Zhanga, Mingjin Xua, Manzhen Gua,b, Haowen Mab, Qian Caib,*( )
)
Received:2025-05-15
Published:2025-07-28
Contact:
*E-mail: caiqian@zjnu.edu.cn
Supported by:文章分享
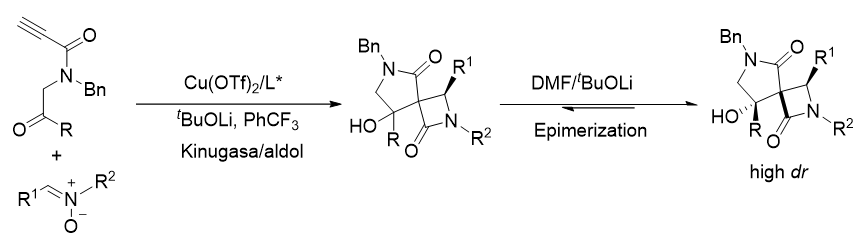
β-内酰胺和螺β-内酰胺是多种天然产物和生物活性化合物中的关键骨架结构, 因其重要的生物学意义而备受关注. Kinugasa反应, 即铜催化末端炔烃与硝酮的环加成反应, 是构建β-内酰胺最直接高效的方法之一. 通过将Kinugasa反应与其他反应结合, 已发展出多种串联或一锅法策略, 用于合成多取代的手性β-内酰胺或螺β-内酰胺. 在前期工作中, 发展了铜催化N-(2-酰基芳基)丙炔酰胺与硝酮的不对称Kinugasa/Aldol串联反应, 成功构建了手性螺环β-内酰胺-二氢喹啉酮. 该反应中, 碱促进的retro-aldol/aldol差向异构化过程发挥了关键作用, 这一过程将次要非对映异构体转化为主要产物, 实现了非对映体富集, 显著提升了产物的非对映选择性. 在本研究中, 为进一步拓展反应适用范围, 探索了线性烷基酮连接的丙炔酰胺与硝酮的反应. 该类反应在PhCF3中进行, 但由于反应条件下烷基醇产物的retro-aldol/aldol过程难以进行, 导致级联反应的非对映选择性较低. 为提高非对映选择性, 在反应完成后引入极性溶剂N,N-二甲基甲酰胺(DMF), 成功促进了retro-aldol/aldol差向异构化过程, 从而以中等收率合成了一系列具有高非对映选择性的手性螺环β-内酰胺产物.
张杰豪, 徐明金, 古满珍, 马浩文, 蔡倩. 铜催化不对称Kinugasa/Aldol反应构建手性螺环β-内酰胺[J]. 化学学报, 2025, 83(7): 667-673.
Jiehao Zhang, Mingjin Xu, Manzhen Gu, Haowen Ma, Qian Cai. Copper(I)-Catalyzed Asymmetric Kinugasa/Aldol Reactions for the Construction of Chiral Spiro β-Lactams[J]. Acta Chimica Sinica, 2025, 83(7): 667-673.
| Entry | L* | Solvent | Base | Yieldb/% | drc (3aa/3aa') | erd (3aa) |
|---|---|---|---|---|---|---|
| 1 | L1 | PhCF3 | tBuOLi | 41 | 4∶1 | 62∶38 |
| 2 | L2 | PhCF3 | tBuOLi | 39 | 10∶1 | 53∶47 |
| 3 | L3 | PhCF3 | tBuOLi | 58 | 8∶1 | 55∶45 |
| 4 | L4 | PhCF3 | tBuOLi | 66 | 3∶1 | 90∶10 |
| 5 | L5 | PhCF3 | tBuOLi | 58 | 7∶1 | 55∶45 |
| 6 | L4 | MeCN | tBuOLi | 51 | 1∶1 | 53∶47 |
| 7 | L4 | DCE | tBuOLi | 36 | 6∶1 | 64∶36 |
| 8 | L4 | 1,4-dioxane | tBuOLi | 47 | 2∶1 | 86∶14 |
| 9 | L4 | THF | tBuOLi | 41 | 3∶1 | 88∶12 |
| 10 | L4 | DMF | tBuOLi | n.d. | — | — |
| 11 | L4 | PhCF3 | K2CO3 | 46 | 3∶1 | 80∶20 |
| 12 | L4 | PhCF3 | Cs2CO3 | 44 | 2∶1 | 85∶15 |
| 13 | L4 | PhCF3 | NaH | 35 | 3∶1 | 75∶25 |
| Entry | L* | Solvent | Base | Yieldb/% | drc (3aa/3aa') | erd (3aa) |
|---|---|---|---|---|---|---|
| 1 | L1 | PhCF3 | tBuOLi | 41 | 4∶1 | 62∶38 |
| 2 | L2 | PhCF3 | tBuOLi | 39 | 10∶1 | 53∶47 |
| 3 | L3 | PhCF3 | tBuOLi | 58 | 8∶1 | 55∶45 |
| 4 | L4 | PhCF3 | tBuOLi | 66 | 3∶1 | 90∶10 |
| 5 | L5 | PhCF3 | tBuOLi | 58 | 7∶1 | 55∶45 |
| 6 | L4 | MeCN | tBuOLi | 51 | 1∶1 | 53∶47 |
| 7 | L4 | DCE | tBuOLi | 36 | 6∶1 | 64∶36 |
| 8 | L4 | 1,4-dioxane | tBuOLi | 47 | 2∶1 | 86∶14 |
| 9 | L4 | THF | tBuOLi | 41 | 3∶1 | 88∶12 |
| 10 | L4 | DMF | tBuOLi | n.d. | — | — |
| 11 | L4 | PhCF3 | K2CO3 | 46 | 3∶1 | 80∶20 |
| 12 | L4 | PhCF3 | Cs2CO3 | 44 | 2∶1 | 85∶15 |
| 13 | L4 | PhCF3 | NaH | 35 | 3∶1 | 75∶25 |
| Entry | Solvent 2 | Yieldb/% | drc (3aa/3aa') |
|---|---|---|---|
| 1 | PhCF3 | 46 | 3∶1 |
| 2 | DCE | 36 | 4∶1 |
| 3 | THF | 38 | 3∶1 |
| 4 | MeCN | 41 | 6∶1 |
| 5 | 1,4-dioxane | 46 | 3∶1 |
| 6 | DMF | 51 | 9∶1 |
| Entry | Solvent 2 | Yieldb/% | drc (3aa/3aa') |
|---|---|---|---|
| 1 | PhCF3 | 46 | 3∶1 |
| 2 | DCE | 36 | 4∶1 |
| 3 | THF | 38 | 3∶1 |
| 4 | MeCN | 41 | 6∶1 |
| 5 | 1,4-dioxane | 46 | 3∶1 |
| 6 | DMF | 51 | 9∶1 |
| [1] |
(a)
pmid: 21861821 |
|
(b)
pmid: 21861821 |
|
|
(c)
pmid: 21861821 |
|
|
(d)
pmid: 21861821 |
|
|
(e)
pmid: 21861821 |
|
|
(f)
pmid: 21861821 |
|
| [2] |
For reviews and examples about synthesis of β-lactams and spiro β-lactams, see: (a)
pmid: 25003801 |
|
(b)
doi: 10.1021/cr500127b pmid: 25003801 |
|
|
(c)
pmid: 25003801 |
|
|
(d)
pmid: 25003801 |
|
|
(e)
pmid: 25003801 |
|
|
(f)
pmid: 25003801 |
|
|
(g)
pmid: 25003801 |
|
|
(h)
pmid: 25003801 |
|
| [3] |
For reviews about Staudinger cycloaddition, see: (a)
doi: 10.1021/cr0307300 pmid: 17649981 |
|
(b)
pmid: 17649981 |
|
|
(c)
pmid: 17649981 |
|
|
(d)
pmid: 17649981 |
|
| [4] |
For a book and selected examples, see: (a)
|
|
(b)
|
|
|
(c)
|
|
|
(d)
|
|
| [5] |
For reviews about the Kinugasa reaction, see: (a)
|
|
(b)
|
|
|
(c)
|
|
|
(邱孔茜, 李杰, 马浩文, 周伟, 蔡倩, 化学学报, 2023, 81, 42.)
doi: 10.6023/A22100419 |
|
|
(d)
|
|
| [6] |
|
| [7] |
|
| [8] |
For selected examples of racemic Kinugasa reactions, see: (a)
|
|
(b)
|
|
|
(c)
|
|
|
(d)
|
|
|
(e)
|
|
| [9] |
For selected examples of asymmetric Kinugasa reactions, see: (a)
pmid: 21744801 |
|
(b)
pmid: 21744801 |
|
|
(c)
pmid: 21744801 |
|
|
(d)
pmid: 21744801 |
|
|
(e)
doi: 10.1002/chem.201702070 pmid: 21744801 |
|
|
(f)
doi: 10.1021/jo2010846 pmid: 21744801 |
|
|
(g)
pmid: 21744801 |
|
|
(h)
pmid: 21744801 |
|
|
(i)
pmid: 21744801 |
|
|
(王琳璇, 徐政虎, 有机化学, 2022, 42, 3912.)
doi: 10.6023/cjoc202200067 pmid: 21744801 |
|
| [10] |
(a)
|
|
(b)
|
|
|
(c)
|
|
|
(d)
|
|
| [11] |
|
| [12] |
|
| [13] |
(a)
|
|
(b)
|
|
| [14] |
|
| [15] |
(a)
|
|
(b)
|
|
|
(c)
|
|
|
(d)
|
|
| [16] |
For the crystal structures of 3aa and 3aa′, see CCDC (2426984, 2458837) and Supporting Information.
|
| [1] | 李晖, 殷亮. 一价铜催化的酮或酮亚胺的不对称烯丙基化反应研究进展[J]. 化学学报, 2024, 82(12): 1274-1288. |
| [2] | 鱼章龙, 李忠良, 杨昌江, 顾强帅, 刘心元. 铜催化的二醇类化合物对映选择性去对称化反应研究进展★[J]. 化学学报, 2023, 81(8): 955-966. |
| [3] | 孟庆端, 韩佳宏, 潘一骁, 郝伟, 范青华. C1-对称手性氮杂环卡宾(NHC)配体的不对称合成及其催化性能研究★[J]. 化学学报, 2023, 81(10): 1271-1279. |
| [4] | 王晓晨, 季泽尧, 刘健, 王炳福, 金辉, 张立新. 硫酯参与的有机催化不对称反应研究进展[J]. 化学学报, 2023, 81(1): 64-83. |
| [5] | 邱孔茜, 李杰, 马浩文, 周伟, 蔡倩. 捕捉环加成反应中的有机亚铜中间体构筑氮杂环化合物研究进展[J]. 化学学报, 2023, 81(1): 42-63. |
| [6] | 徐清浩, 魏立谱, 张震, 肖斌. 铜促进的锗亲电试剂与烷基溴合成四烷基锗※[J]. 化学学报, 2022, 80(4): 428-431. |
| [7] | 满清敏, 付尊蕴, 刘甜甜, 郑明月, 蒋华良. Cu催化偶联反应合成烷基芳基醚的DFT机理研究[J]. 化学学报, 2021, 79(7): 948-952. |
| [8] | 邓卓基, 欧阳溢凡, 敖运林, 蔡倩. 铜催化不对称去对称化分子内烯基C—N偶联反应[J]. 化学学报, 2021, 79(5): 649-652. |
| [9] | 张荣华, 许冰, 张展鸣, 张俊良. Ming-Phos/铜催化的亚甲胺叶立德与硝基烯烃的不对称[3+2]环加成反应[J]. 化学学报, 2020, 78(3): 245-249. |
| [10] | 黄浩, 林华鑫, 王敏, 廖建. 1,2-苯基异噁唑为氮源的铜催化苯乙烯不对称硼胺化[J]. 化学学报, 2020, 78(11): 1229-1234. |
| [11] | 梁欢, 苟阿龙, 高珠鹏, 雷林生, 王博文, 余兰, 徐学涛, 王少华. 铜催化的α-氨基丙二腈的脱氰氧代反应:一种合成叔酰胺的新方法[J]. 化学学报, 2020, 78(10): 1064-1068. |
| [12] | 成忠明, 陈品红, 刘国生. 光/铜共催化远程C—H键的不对称氰基化反应[J]. 化学学报, 2019, 77(9): 856-860. |
| [13] | 张衡, 牟学清, 陈弓, 何刚. 铜催化苯甲酰亚胺高烯丙酯的分子内胺化全氟烷基化反应[J]. 化学学报, 2019, 77(9): 884-888. |
| [14] | 林凤闺蓉, 梁宇杰, 郦鑫耀, 宋颂, 焦宁. 氧气氧化铜催化的苯胺邻位叠氮化反应[J]. 化学学报, 2019, 77(9): 906-910. |
| [15] | 蔡倩, 马浩文. 手性高价碘试剂的发展及展望[J]. 化学学报, 2019, 77(3): 213-230. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||