

通过邻羟基苯基膦和醛的缩合反应合成苯并氧杂磷杂环戊烯
收稿日期: 2022-02-10
修回日期: 2022-03-16
网络出版日期: 2022-03-30
基金资助
国家自然科学基金(22171245); 国家自然科学基金(21672193)
Synthesis of Dihydrobenzooxaphospholes via Cyclocondensation of 2-Phosphinylphenol and Aldehydes
Received date: 2022-02-10
Revised date: 2022-03-16
Online published: 2022-03-30
Supported by
National Natural Science Foundation of China(22171245); National Natural Science Foundation of China(21672193)
朱雪莉 , 杨绍丽 , 郏彩霞 , 李静 , 段征 . 通过邻羟基苯基膦和醛的缩合反应合成苯并氧杂磷杂环戊烯[J]. 有机化学, 2022 , 42(7) : 2201 -2213 . DOI: 10.6023/cjoc202202012
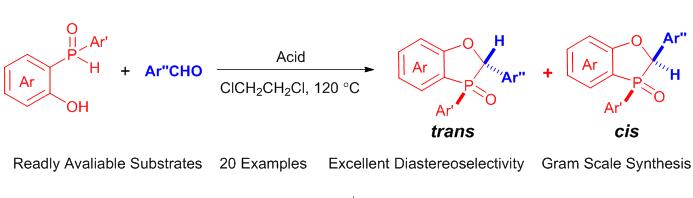
A facile method to synthesize dihydrobenzooxaphospholes was developed from a p-toluenesulfonic acid (p-TSA)- promoted intermolecular cyclocondensation of the readily available 2-phosphinylphenol and aromatic aldehydes. The desired products were obtained as a mixture of stereoisomers. Interestingly, the diastereoisomers could be separated easily by flash column chromatography. The gram-scale and diastereoselective syntheses were also successfully performed.
| [1] | Tang, W.; Qu, B.; Capacci, A. G.; Rodriguez, S.; Wei, X.; Haddad, N.; Narayanan, B.; Ma, S.; Grinberg, N.; Yee, N. K.; Krishnamurthy, D.; Senanayake, C. H. Org. Lett. 2010, 12, 176. |
| [2] | (a) Qu, B.; Samankumara, L. P.; Ma, S.; Fandrick, K. R.; Desrosiers, J.-N.; Rodriguez, S.; Li, Z.; Haddad, N.; Han, Z. S.; McKellop, K.; Pennino, S.; Grinberg, N.; Gonnella, N. C.; Song, J. J.; Senanayake, C. H. Angew. Chem., Int. Ed. 2014, 53, 14428. |
| [2] | (b) Rodriguez, S.; Qu, B.; Fandrick, K. R.; Buono, F.; Haddad, N.; Xu, Y.; Herbage, M. A.; Zeng, X.; Ma, S.; Grinberg, N.; Lee, H.; Han, Z. S.; Yee, N. K.; Senanayake, C. H. Adv. Synth. Catal. 2014, 356, 301. |
| [2] | (c) Qu, B.; Mangunuru, H. P. R.; Wei, X.; Fandrick, K. R.; Desrosiers, J.-N.; Sieber, J. D.; Kurouski, D.; Haddad, N.; Samankumara, L. P.; Lee, H.; Savoie, J.; Ma, S.; Grinberg, N.; Sarvestani, M.; Yee, N. K.; Song, J. J.; Senanayake, C. H. Org. Lett. 2016, 18, 4920. |
| [2] | (d) Handa, S.; Andersson, M. P.; Gallou, F.; Reilly, J.; Lipshutz, B. Angew. Chem., Int. Ed. 2016, 55, 4914. |
| [2] | (e) Qu, B.; Haddad, N.; Rodriguez, S.; Sieber, J. D.; Desrosiers, J.-N.; Patel, N. D.; Zhang, Y.; Grinberg, N.; Lee, H.; Ma, S.; Ries, U. J.; Yee, N. K.; Senanayake, C. H. J. Org. Chem. 2016, 81, 745. |
| [2] | (f) Wei, X.; Qu, B.; Zeng, X.; Savoie, J.; Fandrick, K. R.; Desrosiers, J.-N.; Tcyrulnikov, S.; Marsini, M. A.; Buono, F.; Li, Z.; Yang, B.-S.; Tang, W.; Haddad, N.; Gutierrez, O.; Wang, J.; Lee, H.; Ma, S.; Campbell, S.; Lorenz, J. C.; Eckhardt, M.; Himmelsbach, F.; Peters, S.; Patel, N. D.; Tan, Z.; Yee, N. K.; Song, J. J.; Roschangar, F.; Kozlowski, M. C.; Senanayake, C. H. J. Am. Chem. Soc. 2016, 138, 15473. |
| [2] | (g) Haddad, N.; Mangunuru, H. P. R.; Fandrick, K. R.; Qu, B.; Sieber, J. D.; Rodriguez, S.; Desrosiers, J.-N.; Patel, N. D.; Lee, H.; Kurouski, D.; Grinberg, N.; Yee, N. K.; Song, J. J.; Senanayake, C. H. Adv. Synth. Catal. 2016, 358, 3522. |
| [2] | (h) Li, G.; Wang, X.-J.; Zhang, Y.; Tan, Z.; Decroos, P.; Lorenz, J. C.; Wei, X.; Grinberg, N.; Yee, N. K.; Senanayake, C. H. J. Org. Chem. 2017, 82, 5456. |
| [2] | (i) Patel, N. D.; Sieber, J. D.; Tcyrulnikov, S.; Simmons, B. J.; Rivalti, D.; Duvvuri, K.; Zhang, Y.; Gao, D. A.; Fandrick, K. R.; Haddad, N.; Lao, K. S.; Mangunuru, H. P. R.; Biswas, S.; Qu, B.; Grinberg, N.; Pennino, S.; Lee, H.; Song, J. J.; Gupton, B. F.; Garg, N. K.; Kozlowski, M. C.; Senanayake, C. H. ACS Catal. 2018, 8, 10190. |
| [2] | (j) Zatolochnaya, O. V.; Rodriguez, S.; Zhang, Y.; Lao, K. S.; Tcyrulnikov, S.; Li, G.; Wang, X.-J.; Qu, B.; Biswas, S.; Mangunuru, H. P. R.; Rivalti, D.; Sieber, J. D.; Desrosiers, J.-N.; Leung, J. C.; Grinberg, N.; Lee, H.; Haddad, N.; Yee, N. K.; Song, J. J.; Kozlowski, M. C.; Senanayake, C. H. Chem. Sci. 2018, 9, 4505. |
| [2] | (k) Lu, Z.; Jasinski, J. B.; Handa, S.; Hammond, G. B. Org. Biomol. Chem. 2018, 16, 2748. |
| [2] | (l) Li, G.; Zatolochnaya, O. V.; Wang, X.-J.; Rodriguez, S.; Qu, B.; Desrosiers, J.-N.; Mangunuru, H. P. R.; Biswas, S.; Rivalti, D.; Karyakarte, S. D.; Sieber, J. D.; Grinberg, N.; Wu, L.; Lee, H.; Haddad, N.; Fandrick, D. R.; Yee, N. K.; Song, J. J.; Senanayake, C. H. Org. Lett. 2018, 20, 1725. |
| [2] | (m) Xu, G.; Senanayake, C. H.; Tang, W. Acc. Chem. Res. 2019, 52, 1101. |
| [3] | Zhu, J.; Huang, L.; Dong, W.; Li, N.; Yu, X.; Deng, W.-P.; Tang, W. Angew. Chem., Int. Ed. 2019, 58, 16119. |
| [4] | Li, C.; Wan, F.; Chen, Y.; Peng, H.; Tang, W.; Yu, S.; McWilliams, J. C.; Mustakis, J.; Samp, L.; Maguire, R. J. Angew. Chem., Int. Ed. 2019, 58, 13573. |
| [5] | Dong, W.; Xu, X.; Ma, H.; Lei, Y.; Lin, Z.; Zhao, W. J. Am. Chem. Soc. 2021, 143, 10902. |
| [6] | Qian, C.; Tang, W. Org. Lett. 2020, 22, 4483. |
| [7] | Xiong, W.; Xu, G.; Yu, X.; Tang, W. Organometallics 2019, 38, 4003. |
| [8] | (a) Takale, B. S.; Thakore, R. R.; Handa, S.; Gallou, F.; Reilly, J.; Lipshutz, B. H. Chem. Sci. 2019, 10, 8825. |
| [8] | (b) Sieber, J. D.; Buono, F.; Brusoe, A.; Desrosiers, J. N.; Haddad, N.; Lorenz, J. C.; Xu, Y.; Wu, H.; Zhang, L.; Han, Z. S. Roschangar, F.; Song, J. J.; Yee, N. K.; Senanayake, C. H. J. Org. Chem. 2019, 84, 4926. |
| [9] | Yang, H.; Sun, J.; Gu, W.; Tang, W. J. Am. Chem. Soc. 2020, 142, 8036. |
| [10] | Li, B.; Li, T.; Aliyu, M.; Li, Z. H.; Tang, W. Angew. Chem., Int. Ed. 2019, 58, 11355. |
| [11] | Wu, T.; Kang, X.; Bai, H.; Xiong, W.; Xu, G.; Tang, W. Org. Lett. 2020, 22, 4602. |
| [12] | Heinicke, J.; Tzschach, A. Phosphorus Sulfur Relat. Elem. 1985, 25, 345. |
| [13] | (a) Li, S.; Han, Z. S.; Viereck, P.; Lee, H.; Kurouski, D.; Senanayake, C. H.; Tsantrizos, Y. S. Org. Lett. 2017, 19, 894. |
| [13] | (b) Han, Z.S.; Wu, H.; Xu, Y.; Zhang, Y.; Qu, B.; Li, Z.; Caldwell, D. R.; Fandrick, K. R.; Zhang, L.; Roschangar, F.; Song, J.; Senanayake, C. H. Org. Lett. 2017, 19, 1796. |
| [14] | (a) Heinicke, J.; Tzschach, A. Z. Chem 1980, 20, 342. |
| [14] | (b) Washington, M. P.; Gudimetla, V. B.; Laughlin, F. L.; Deligonul, N.; He, S.; Payton, J. L.; Simpson, M. C.; Protasiewicz, J. D. J. Am. Chem. Soc. 2010, 132, 4566. |
| [14] | (c) Washington, M. P.; Payton, J. L.; Simpson, M. C.; Protasiewicz, J. D. Organometallics 2011, 30, 1975. |
| [14] | (d) Laughlin, F. Li; Deligonul, N.; Rheingold, A. L.; Golen, J. A.; Laughlin, B. J.; Smith, R. C.; Protasiewicz, J. D. Organometallics 2013, 32, 7116. |
| [14] | (e) Wu, S. S.; Rheingold, A. L.; Protasiewicz, J. D. Chem. Commun. 2014, 50, 11036. |
| [14] | (f) Laughlin, F. L.; Rheingold, A. L.; Deligonul, N.; Laughlin, B. J.; Smith, R. C.; Higham, L. J.; Protasiewicz, J. D. Dalton Trans. 2012, 41, 12016. |
| [14] | (g) Wu, S. S.; Deligonal, N.; Protasiewicz, J. D. Dalton Trans. 2013, 42, 14866. |
| [15] | Oehme, H.; Leissring, E. Tetrahedron 1981, 37, 753. |
| [16] | Huang, H.; Denne, J.; Yang, C.-H.; Wang, H.; Kang, J. Y. Angew. Chem., Int. Ed. 2018, 57, 6624. |
| [17] | (a) Melvin, L. S. Tetrahedron Lett. 1981, 22, 3375. |
| [17] | (b) Heinicke, J.; Böhle, I.; Tzschach, A. J. Organomet. Chem. 1986, 317, 11. |
| [17] | (c) Dhawan, B.; Redmore, D. J. Org. Chem. 1991, 56, 833. |
| [17] | (d) Li, S. S.; Wang, G. Q. Phosphorus Sulfur Relat. Elem. 1991, 61, 119. |
| [17] | (e) Paladino, J.; Guyard, C.; Thurieau, C.; Fauchère, J. - L. Helv. Chim. Acta 1993, 76, 2465. |
| [17] | (f) Taylor, C. M.; Watson, A. J. Curr. Org. Chem. 2004, 8, 623. |
| [17] | (g) Whisler, M. C.; MacNeil, S.; Snieckus, V.; Beak, P. Angew. Chem., Int. Ed. 2004, 43, 2206. |
| [17] | (h) Jayasundera, K. P.; Watson, A. J.; Taylor, C. M. Tetrahedron Lett. 2005, 46, 4311. |
| [17] | (i) Yilmaz, E.; Bier, D.; Guillory, X.; Briels, J.; Ruiz-Blanco, Y. B.; Sanchez-Garcia, E.; Ottmann, C.; Kaiser, M. Chem.-Eur. J. 2018, 24, 13807. |
| [17] | (j) Korb, M.; Lang, H. Chem. Soc. Rev. 2019, 48, 2829. |
| [17] | (k) Patel, J. J.; Blackburn, T.; Alessi, M.; Sawinski, H.; Snieckus, V. Org. Lett. 2020, 22, 3860. |
| [18] | (a) Kenny, N. P.; Rajendran, K. V.; Gilheany, D. G. Chem. Commun. 2015, 51, 16561. |
| [18] | (b) Huang, H.; Denne, J.; Yang, C. H.; Wang, H.; Kang, J. Y. Angew. Chem., Int. Ed. 2018, 57, 6624. |
| [18] | (c) Melvin, L. S. Tetrahedron Lett. 1981, 22, 3375. |
| [18] | (d) Yang, S. X.; Li, Y. G.; Wang, J. Chin. J. Org. Chem. 1984, 4, 271. (in Chinese) |
| [18] | ( 杨石先, 李玉桂, 王坚, 有机化学, 1984, 4, 271.) |
/
| 〈 |
|
〉 |