

芳基羧酸无痕导向官能化反应的研究进展
收稿日期: 2025-03-31
修回日期: 2025-04-08
网络出版日期: 2025-04-17
基金资助
国家自然科学基金(22071185)
国家自然科学基金(22271224)
中央高校基本科研业务专项资金(2042025kf0032)
Recent Progress in Traceless Directed Functionalization Reactions of Arylcarboxylic Acids
Received date: 2025-03-31
Revised date: 2025-04-08
Online published: 2025-04-17
Supported by
National Natural Science Foundation of China(22071185)
National Natural Science Foundation of China(22271224)
Fundamental Research Funds for the Central Universities(2042025kf0032)
Copyright
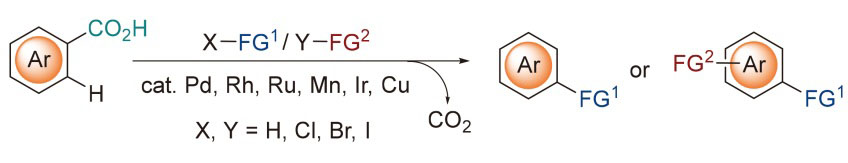
从简单、易得的原料高效构建复杂、高价值的有机分子是有机合成的核心目标. 近年来, 导向基团辅助的过渡金属催化的C—H键活化已成为实现位点选择性官能化的重要策略. 其中, 芳基羧酸因其结构多样性、稳定性和易获取性, 成为备受关注的合成原料. 特别是, 其羧基作为无痕导向基团, 有效避免了额外的导向基团引入和去除步骤, 显著提高了反应的原子和步骤经济性. 得益于这些优势, 过渡金属催化的芳基羧酸无痕导向C—H键单官能化反应已取得显著进展. 与之相比, 相应的双官能化转化在复杂分子构建中展现出重要的合成价值和应用前景, 但是这类反应研究进展相对滞后. 本综述总结了近年来羧基无痕导向的单官能化和双官能化的研究进展, 并探讨了该领域的挑战与未来发展方向.
陈明 , 张敬 . 芳基羧酸无痕导向官能化反应的研究进展[J]. 有机化学, 2025 , 45(8) : 2660 -2676 . DOI: 10.6023/cjoc202502006
Efficient construction of complex and high value organic molecules from simple and readily available starting materials is a core objetive of organic synhthesis. In recent years, transition metal-catalyzed C—H bond activation, facilitated by directing groups, has been demonstrated as a powerful strategy for achieving site-selective functionalization. Among various substrates, arylcarboxylic acids have gained significant attention as ideal starting materials due to their structural diversity, high stability, and easy accessibility. Notably, the carboxyl group can serve as a traceless directing group, eliminating the need for additional directing group installation and removal steps, thereby significantly enhancing atomic and step economy. Benefiting from these advantages, transition metal-catalyzed decarboxylative C—H bond mono-functionalization of aryl carboxylic acids has achieved remarkable progress. However, the development of difunctionalization remains underdeveloped, despite its significant synthetic value and application potential in rapidly constructing complex organic structures. This review summarizes the recent advances in traceless carboxyl-directed C—H monofunctionalization and difunctionalization, and discusses the challenges and future directions in this field.

| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
(余金权, 丁奎岭, 化学学报, 2015, 73, 1223.)
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
(付拯江, 曹晰晗, 尹健, 苟振宇, 伊学政, 蔡琥, 有机化学, 2022, 42, 67.)
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
(a)
(b)
(c)
(d)
|
| [58] |
|
| [59] |
(a)
(b)
(c)
(d)
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|
| [79] |
|
| [80] |
|
| [81] |
|
| [82] |
|
| [83] |
|
| [84] |
|
| [85] |
|
| [86] |
|
| [87] |
|
| [88] |
|
| [89] |
|
| [90] |
|
| [91] |
|
| [92] |
|
| [93] |
|
| [94] |
|
| [95] |
|
| [96] |
|
| [97] |
|
| [98] |
|
| [99] |
|
/
| 〈 |
|
〉 |