1 构建D-A框架的合成策略
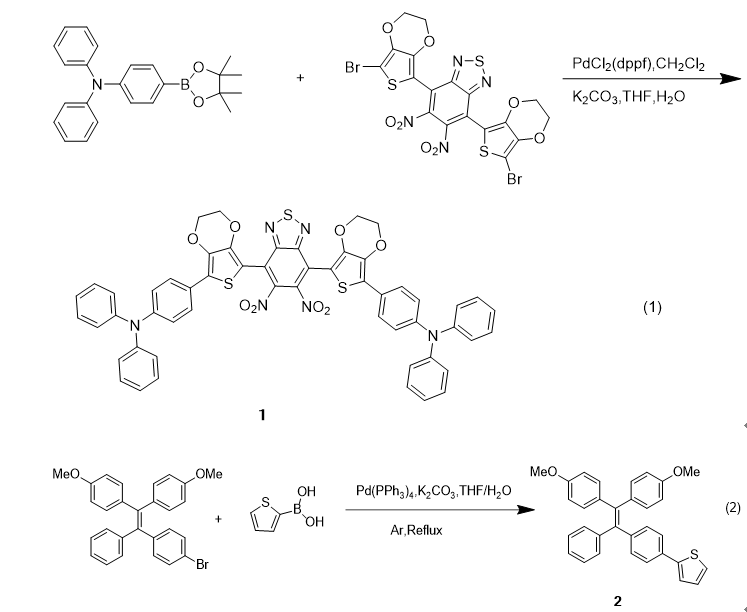
1.1 Suzuki-Miyaura偶联反应
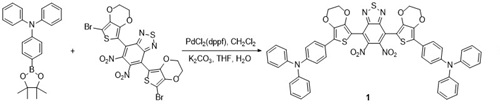
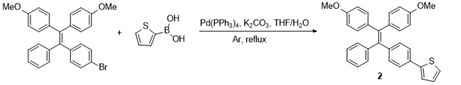
1.2 Stille偶联反应
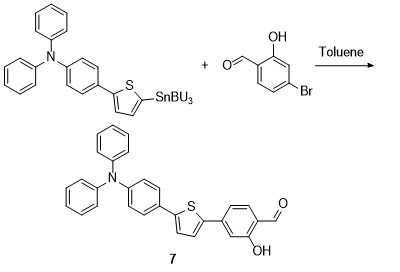
1.3 Buchwald-Hartwig偶联反应
1.4 Sonogashira偶联反应
1.5 Knoevenagel(脑文格)缩合反应
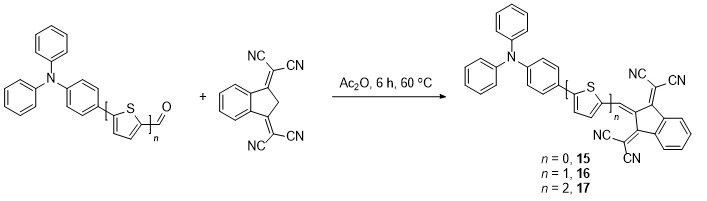
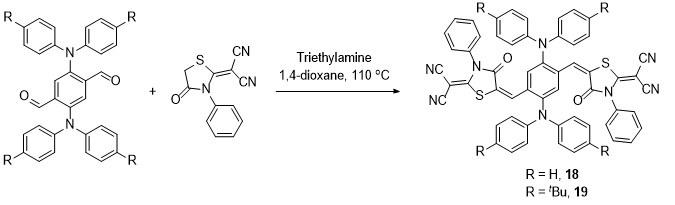
2 调控π共轭骨架的合成策略
2.1 Heck反应
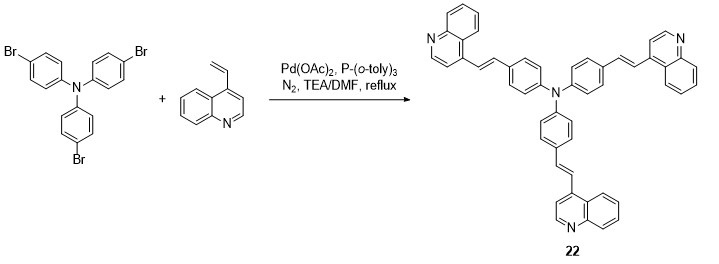
2.2 Vilsmeier-Haack反应
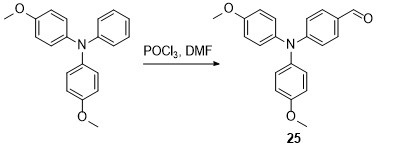
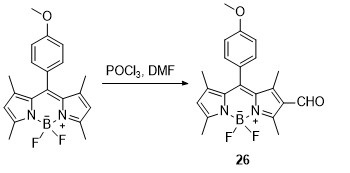
3 增强SOC的合成策略
3.1 Menshutkin反应
3.2 点击反应
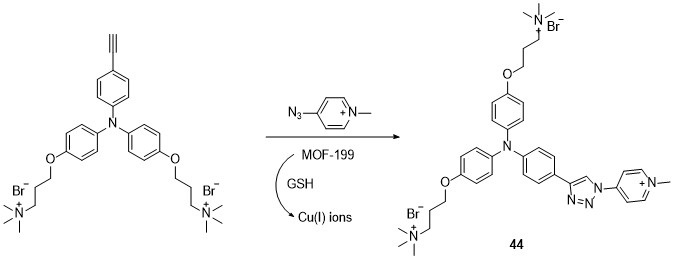

高效聚集诱导发光光敏剂的合成策略
收稿日期: 2025-03-03
修回日期: 2025-06-01
网络出版日期: 2025-06-19
基金资助
国家自然科学基金(22422401)
国家自然科学基金(22374007)
国家自然科学基金(22375002)
中央高校基本科研业务费专项资金(JD2507)
Strategies for the Synthesis of High-Efficiency Aggregation-Induced Emission Photosensitizers
Received date: 2025-03-03
Revised date: 2025-06-01
Online published: 2025-06-19
Supported by
National Natural Science Foundation of China(22422401)
National Natural Science Foundation of China(22374007)
National Natural Science Foundation of China(22375002)
Fundamental Research Funds for the Central Universities(JD2507)
聚集诱导发光(AIE)光敏剂即便处于高分子化或聚集态, 仍能维持强荧光特性且高效产生活性氧(ROS), 已成为新一代光动力治疗(PDT)候选材料. 围绕近年研究领域中分子电子结构与分子运动调控策略的相关进展, 重点梳理了构建供体-受体(D-A)框架的合成策略(如Suzuki-Miyaura偶联、Stille偶联、Buchwald-Hartwig偶联、Sonogashira偶联、Knoevenagel缩合), 调控π共轭骨架的合成策略(如Heck反应、Vilsmeier-Haac反应), 增强自旋轨道耦合(SOC)的合成策略(如Menshutkin反应、点击反应、金属配位反应), 以及分子运动限制策略(聚合物封装和纳米颗粒负载). 通过多维分子设计与材料工程协同, AIE光敏剂已在近红外成像与深部PDT疗效方面取得了显著进展. 展望未来, 可以借助机器学习辅助的分子筛选和多模态递送平台, 加速AIE光敏剂向临床深部实体瘤精准光疗的转化.
代鸿宇 , 孙红红 , 魏培发 , 管伟江 . 高效聚集诱导发光光敏剂的合成策略[J]. 有机化学, 2025 , 45(11) : 4128 -4142 . DOI: 10.6023/cjoc202503003
Aggregation-induced emission (AIE) photosensitizers have emerged as a new generation of candidates for photodynamic therapy (PDT) owing to their ability to maintain strong fluorescence and efficiently generate reactive oxygen species (ROS) in polymerized and aggregated states. Focusing on the recent research progress in molecular electronic structure and molecular motion regulation strategies, synthetic methodologies for constructing donor-acceptor (D-A) frameworks (such as Suzuki-Miyaura coupling, Stille coupling, Buchwald-Hartwig coupling, Sonogashira coupling, and Knoevenagel condensation), strategies for tuning π-conjugated backbones (such as the Heck reaction and Vilsmeier-Haack reaction), methods for enhancing spin-orbit coupling (SOC) including Menshutkin reactions, click chemistry, and metal coordination reaction, as well as motion-restricting strategies, including polymer encapsulation and nanoparticle loading, are mainly summarized. Through synergistic multidimensional molecular design and materials engineering, AIE photosensitizers have achieved significant improvements in near-infrared imaging and deep-tissue PDT efficacy. Looking forward, machine learning-assisted molecular screening and multimodal delivery platforms accelerate their clinical translation toward precision phototherapy of deep solid tumors.










| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
/
| 〈 |
|
〉 |