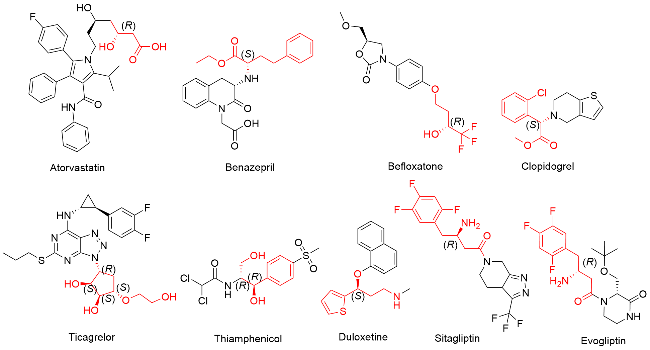
醇脱氢酶(Alcohol dehydrogenases, ADHs, 酶学编号EC 1.1.1.x)也称羰基还原酶(Carbonyl reductases, CRs)或酮还原酶(Ketoreductases, KREDs), 这类酶属于氧化还原酶家族, 依赖烟酰胺腺嘌呤二核苷酸(NAD
+/ NADH)或烟酰胺腺嘌呤二核苷酸磷酸酯(NADP
+/NADPH)辅酶作为电子供体或受体, 可催化醇羟基的脱氢氧化或其逆反应羰基还原
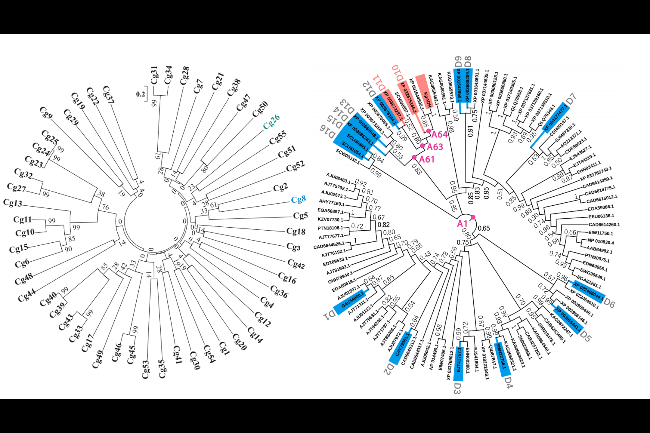
[8-9]. 根据结构与机制的不同, 目前将醇脱氢酶分为三个超家族(
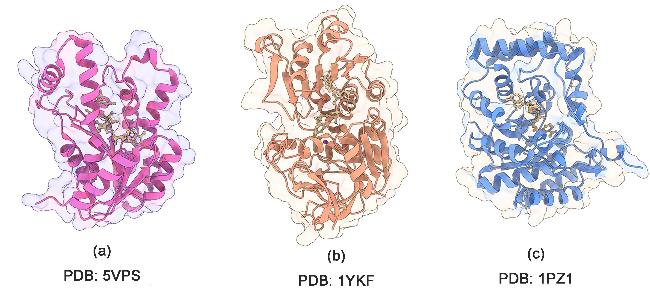
图2): (a)短链脱氢酶/还原酶(Short-chain dehydrogenase/reductases, SDRs), 其属于非金属依赖酶, 包括经典型和扩展型, 每条肽链一般含250或350个左右的氨基酸残基
[10], 短链脱氢酶通常以单体、二聚体、四聚体、八聚体或十聚体等同源多聚体的形式存在; (b)中链脱氢酶/还原酶(Medium- chain dehydrogenases/reductases, MDRs), 长度为350个左右的氨基酸
[11], 大都为锌离子依赖型, 中链脱氢酶一般是单聚体、二聚体或四聚体的形式存在; (c)醛酮还原酶(Aldo-keto reductases, AKRs), 每条链一般含385个左右的氨基酸, 少数含900个左右的氨基酸, 并大多以单体形式存在
[12]. NAD(P)
+依赖的醇脱氢酶催化醇(羰基)底物的不对称氧化(还原)反应遵循顺序反应机制. 首先, 辅因子与酶结合诱导蛋白由无序的状态形成适合底物分子结合的催化口袋, 成为全酶. 此后, 底物分子结合在活性口袋进一步诱导全酶形成合适的催化构象推动催化进行. 反应生成产物和氧化态或还原态的辅酶, 先释放产物, 最后释放辅酶
[11]. 醇脱氢酶催化前手性羰基化合物还原反应的过程简便, 理论收率可达100%, 故以醇脱氢酶催化合成手性醇的方案因应用前景广阔而备受学术界和产业界瞩目.