

蕊木属生物碱arboridinine和arborisidine的全合成研究进展
收稿日期: 2025-07-15
修回日期: 2025-09-04
网络出版日期: 2025-10-15
基金资助
国家自然科学基金(22401019)
Progress in the Total Synthesis of the Kopsia Alkaloids Arboridinine and Arborisidine
Received date: 2025-07-15
Revised date: 2025-09-04
Online published: 2025-10-15
Supported by
National Natural Science Foundation of China(22401019)
吲哚生物碱分布广泛、结构复杂, 并且具有丰富的药理活性, 是目前天然产物全合成领域的研究热点. 生物碱arboridinine和arborisidine是从马来西亚的蕊木属植物中分离得到的, 这两个生物碱特殊而高度复杂的笼状结构使其全合成研究极具挑战性, 因此得到了广泛关注. 本文总结了arboridinine和arborisidine的全合成研究进展, 以期为相关天然产物的全合成提供参考.
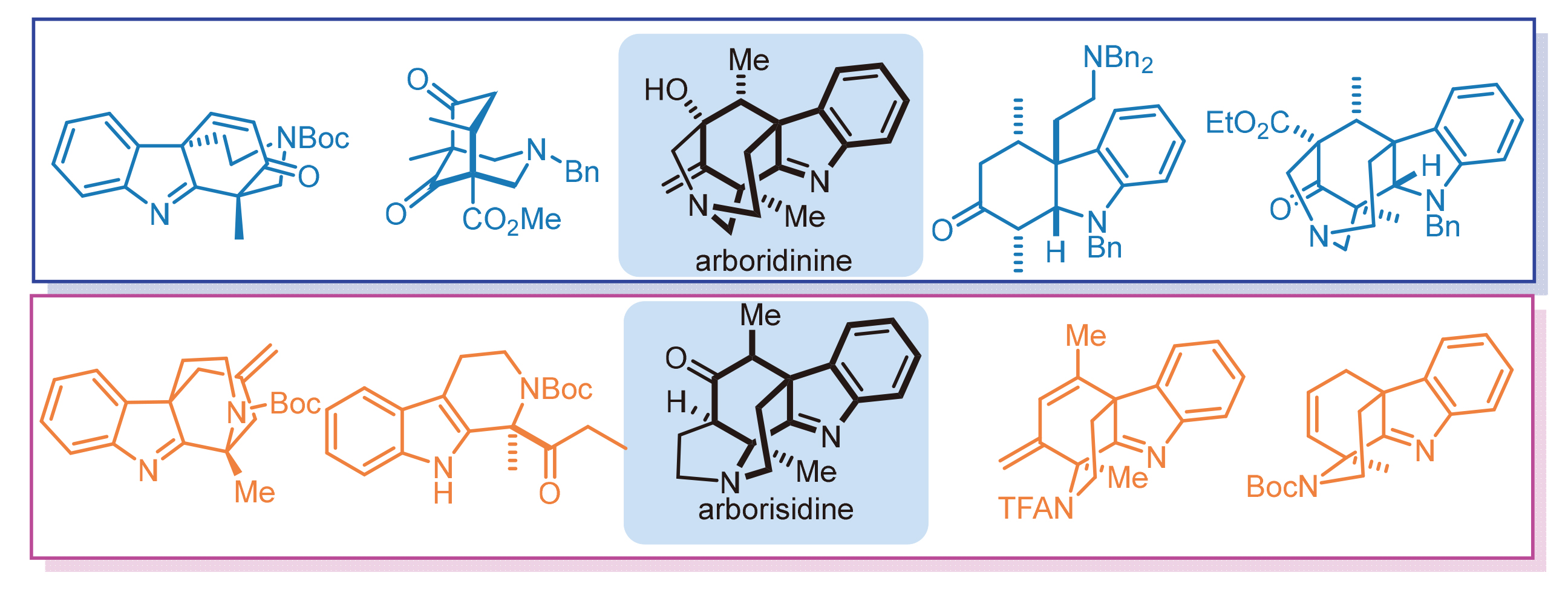
关键词: 生物碱; 全合成; arboridinine; arborisidine
何卫刚 , 段明月 , 闫帅 , 叶伟杰 , 徐雪园 , 孙先宇 . 蕊木属生物碱arboridinine和arborisidine的全合成研究进展[J]. 有机化学, 2026 , 46(2) : 443 -454 . DOI: 10.6023/cjoc202507021
Indole alkaloids are widely distributed in nature and have rich pharmacological activities, so many indole alkaloids have emerged as hot targets for the total synthesis of natural products. The alkaloids arboridinine and arborisidine were isolated from a plant of the Kopsia genus found in Malaysia by Kam and co-workers in 2015 and 2016, respectively. These two pentacyclic monoterpenoid indole alkaloids have unique caged skeleton with multiple chiral centers. The highly complex cage structure of these alkaloids has brought great challenges to their total synthesis research. In addition, arborisidine combined with pimelautide exhibits clear anti-gastric cancer activity. The complex and attractive chemical structure and potential pharmacological activity, together with an extremely low natural abundance make their total synthesis extremely attractive. Soon after the isolation, their total synthesis has received extensive and sustained attention. Up to now, the total synthesis of arboridinine has be achieved by the Snyder, Ma, Zhai and Li groups, and the total synthesis of arborisidine by the Snyder, Ma, Zhu, Jiao, She and Gao groups. This review summarizes the research progress of total synthesis of arboridinine and arborisidine, in order to provide reference for the total synthesis of the related natural products.

Key words: alkaloids; total synthesis; arboridinine; arborisidine
| [1] |
|
| [2] |
(a)
(涂永强, 科学观察, 2012, 7, 59.)
(b)
(郭瑞霞, 李力更, 王于方, 霍长虹, 付炎, 王磊, 史清文, 中草药, 2015, 46, 2019.)
|
| [3] |
|
| [4] |
(a)
(b)
|
| [5] |
|
| [6] |
|
| [7] |
(刘小宇, 肖涛, 秦勇, 化学进展, 2018, 30, 578.)
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
(a)
(陈志涛, 博士论文, 重庆大学, 重庆, 2019.)
(b)
(陈志涛, 肖涛, 宋颢, 秦勇, 有机化学, 2018, 38, 2427.)
|
| [29] |
|
| [30] |
|
| [31] |
(a)
(b)
|
| [32] |
(a)
(b)
|
| [33] |
|
/
| 〈 |
|
〉 |