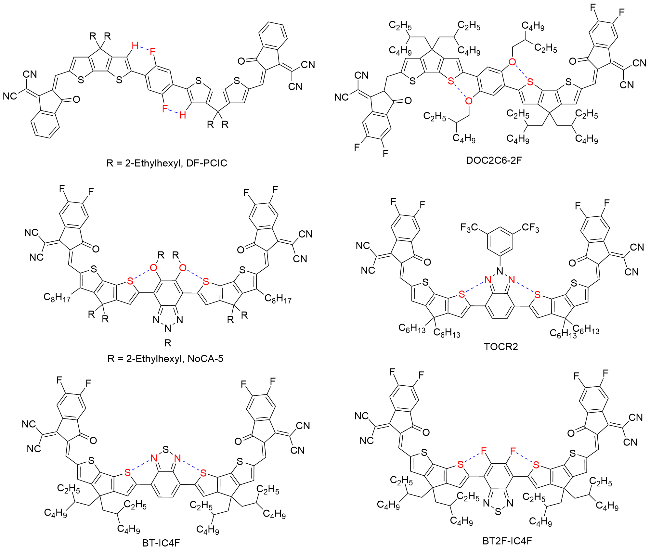
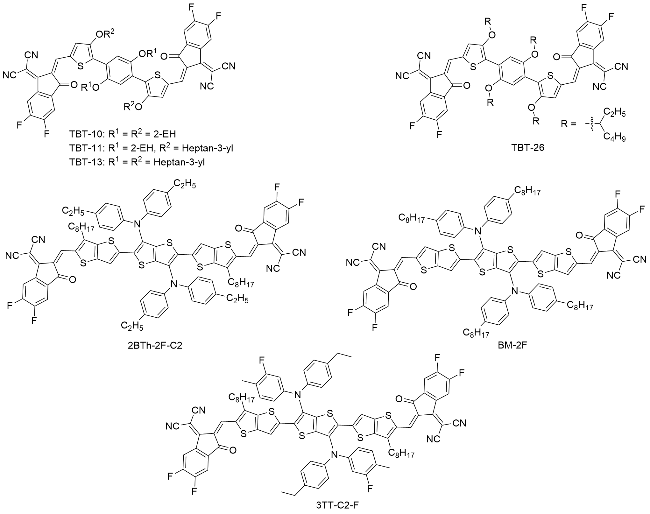
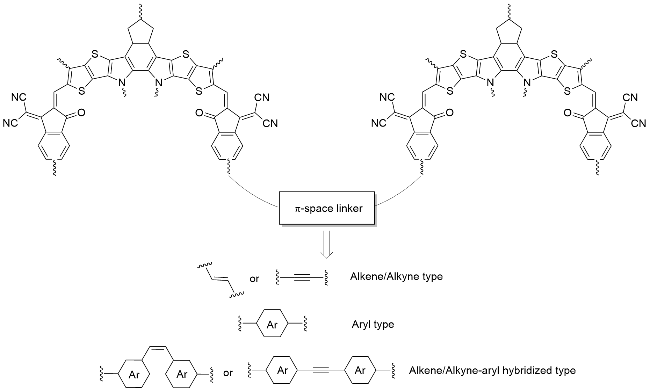
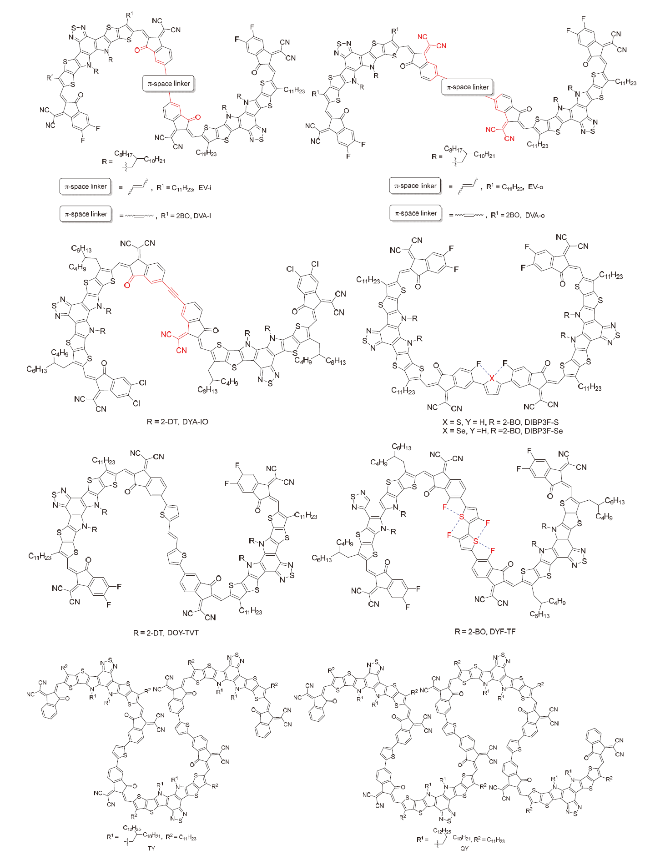
随着全球能源需求持续增长与环境问题日益严峻, 开发清洁、可再生且低成本的能源转换技术成为21世纪科学研究的重要议题. 在众多可再生能源中, 太阳能因其资源丰富、分布广泛的特点, 被视为最具潜力的解决方案之一. 作为新型清洁能源技术, 有机太阳能电池(Organic Solar Cells, OSCs)因其质量轻、柔性、可溶液制备和可卷对卷大面积印刷等优点, 受到科研工作者的广泛关注. 其中, 活性层中的给受体材料是决定有机光伏器件效率的关键
[1-3]. 某种程度上, OSCs的发展史也是一部受体材料的创新史. 从早期的富勒烯衍生物到如今的高性能非富勒烯受体(Non-fullerene acceptors, NFAs,
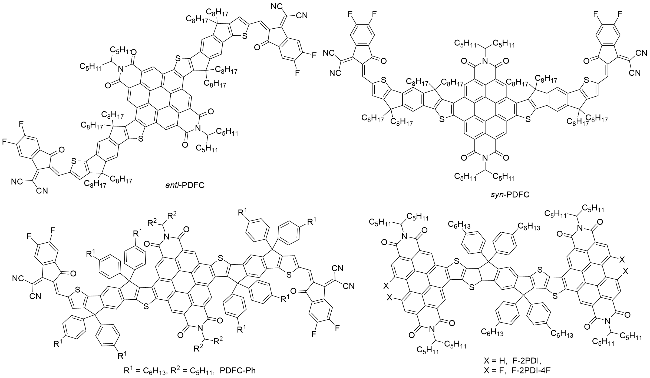
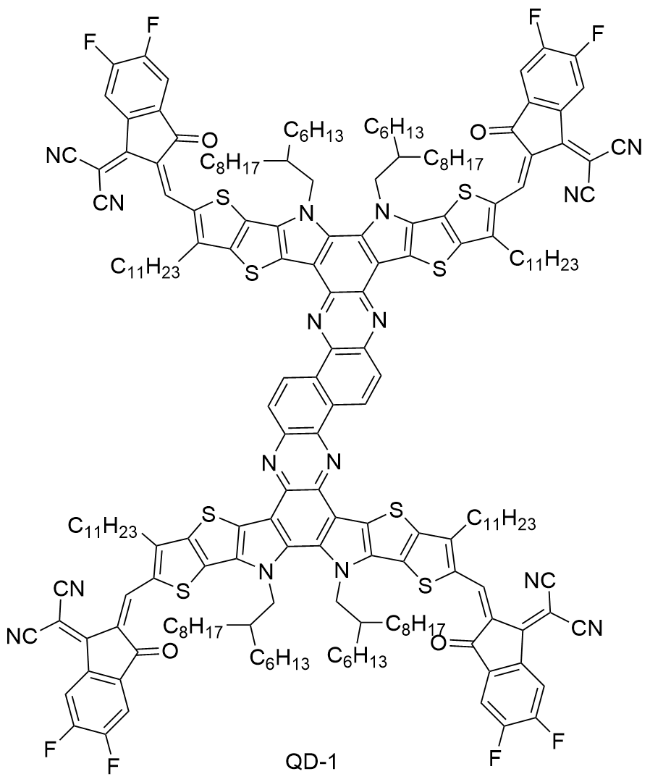
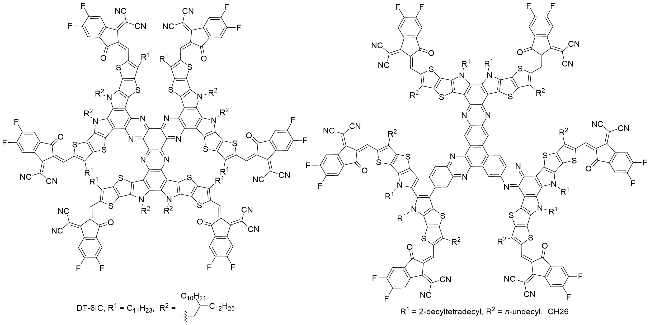
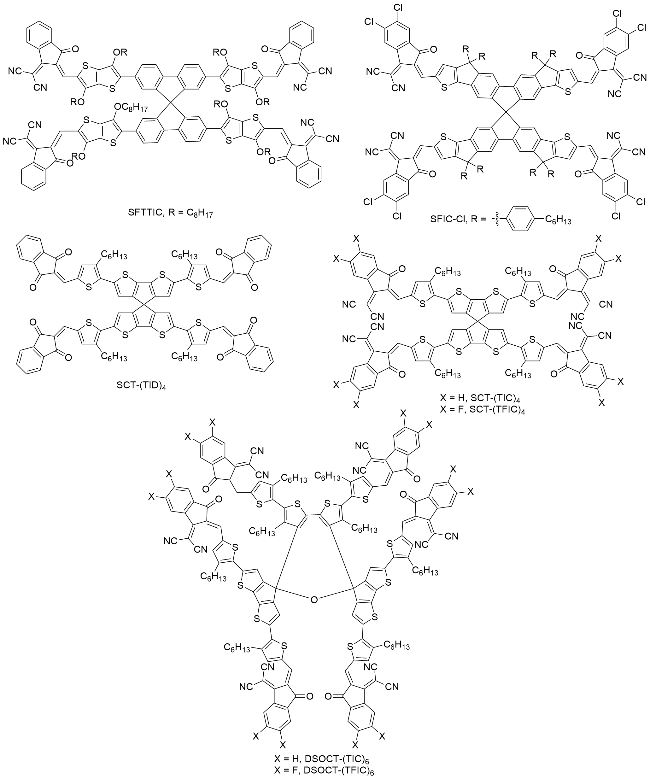
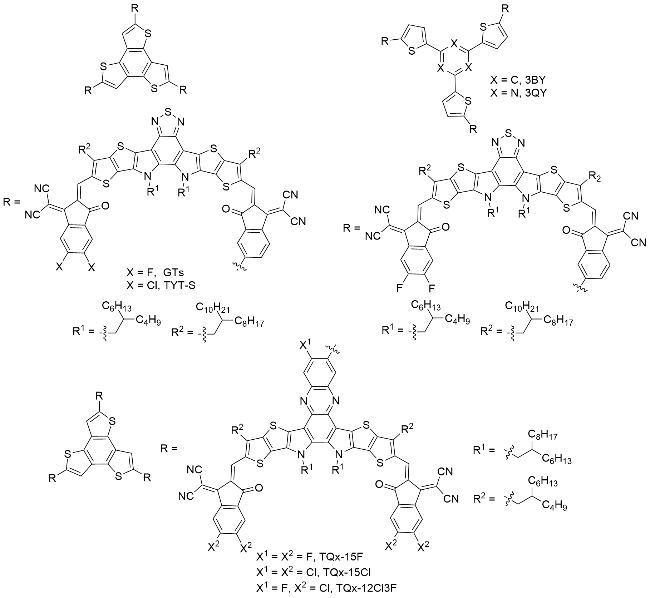
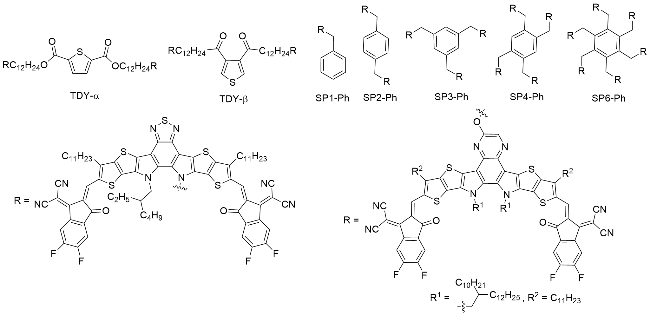
图1), 受体材料的每一次革新都大幅提升了OSCs的光电转换效率(Power conversion efficiencies, PCEs)和稳定性, 并推动了其从实验室研究走向商业化应用.
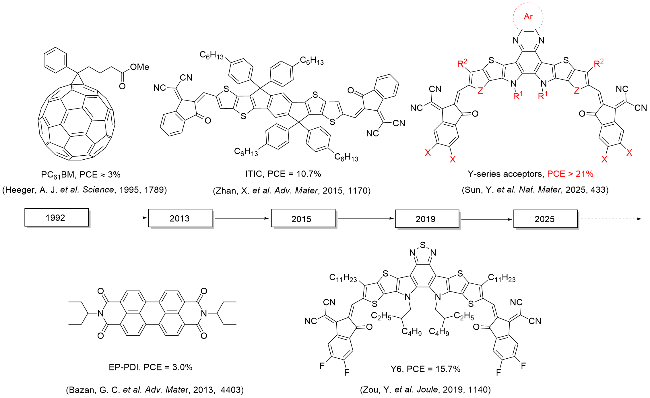
1992年, Wudl等
[4]发现C
60可以作为电子受体, 与共轭聚合物聚[4-亚苯基亚乙烯基](MEH-PPV)形成光诱导电荷转移, 奠定了有机光伏(OPV)的基本工作原理. 1995年, Heeger等
[5]提出“体异质结(Bulk Hetero Junction, BHJ)”的概念, 将共轭聚合物MEH-PPV与可溶性富勒烯衍生物PC
61BM共混, 大幅提升激子分离效率, 使OSCs器件效率接近3%. 在之后的10~15年时间里, 富勒烯衍生物因其较高的电子亲和势以及电荷传输的各向同性, 在受体材料中占主导地位
[6-9]. 然而其在可见光和近红外区的吸收偏弱, 合成分离过程繁琐, 结构可修饰性差, 带隙难以调节以及溶解性差等问题, 阻碍了OSCs领域进一步发展, 目前基于富勒烯受体的光伏器件最高效率仅为11.3%
[10]. 作为替代富勒烯受体的初步尝试, 苝二酰亚胺(Perylene Diimide, PDI)类小分子因其庞大的刚性π共轭体系拓宽了分子吸收
[11-14], 弥补了富勒烯在可见光区吸收不足的缺点, 提升了材料的光热稳定性和载流子迁移率. 但由于未解决其相分离尺寸过大的形貌问题, 器件性能依旧没能得到根本改善. 2010年前后, 基于寡聚噻吩类
[15]、苯并二噻吩类(BDT)
[16]和茚并二噻吩类(IDT)
[17]等A-D-A型柔性小分子给体材料的出现, 与富勒烯类受体获得了良好的能级匹配与形貌兼容, 从而帮助基于富勒烯受体的光伏器件实现了超10%的转换效率. 得益于小分子给体的设计思路, 研究人员发现这类小分子的吸收带普遍由D核的π-π*跃迁和D到A核的分子内电荷转移(Intramolecular Charge Transfer, ICT)跃迁组成. 其中封端A核的缺电子程度决定着小分子材料ICT效应的强度, 进而影响到分子的带隙和能级. 换言之, A核的缺电子特性越强, 分子的能级(尤其是LUMO能级)越低, 带隙越窄, 电荷分离的驱动力越大. 当通过增强A核的缺电子效应, 使这些低能级、窄带隙的共轭小分子与富勒烯类受体的能级与带隙接近, 甚至更低时, 便形成了NFAs. 而柔性侧链则解决了传统富勒烯和PDI类受体可溶液加工性能差的问题. 2015年, 占肖卫课题组
[18]首次以对称的茚并二噻吩[3,2-
b]噻吩(IDTT)为D核, 强缺电子的3-(二氰基亚甲基)茚-1-酮(IC)为封端A单元, 开发了窄带隙非富勒烯受体3,9-双(2-亚甲基-(3-(1,1-二氰基亚甲基)-茚酮))-5,5,11,11-四(4-己基苯基)-二噻吩并[3'-d']-s-茚并[6-b']二噻吩(ITIC), 实现了超800 nm吸收边的宽吸收光谱和突破10%的器件效率, 奠定了基于NFAs有机太阳能电池的基础. 羰基和丙二腈两个强吸电子官能团的引入使IC及其衍生结构, 包括2-(5,6-二氟-3-氧代-2,3-二氢-1
H-茚-1-亚基)丙二腈(2F-IC)、2-(3-氧代-2,3-二氢-1
H-环戊并[
b]萘-1-亚基)丙二腈(NC)等均表现出强烈的缺电子特性, 对拓宽分子吸收至近红外区, 增强分子间的π-π堆积, 提升电荷迁移率起到了至关重要的作用, 也是目前大多数高效NFAs所采用的端基类型. 2019年, 邹应萍组
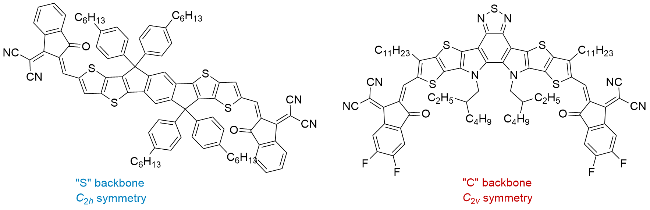
[19]开发出吸收超过900 nm, 效率接近16%的A-DA'D-A型受体Y6, 彻底改变了OSCs领域的竞争格局. Y6一方面继承了ITIC受体原有的梯形稠环结构, 一方面打破了ITIC的
C2h对称性“S”型骨架, 实现了
C2v对称性“C”型骨架的结构创新, 并直接推动后续衍生物, 如L8-BO
[20]、BTP-eC9
[21]等高效NFAs材料的出现, 因而“C”型骨架被认为是高效NFAs的必备分子结构, 并被广泛应用于Y6衍生物(以下称作Y系列受体)的构型优化. 截至本文发表, 基于Y系列受体的小面积器件效率已经达到了令人惊叹的20%
[22], 大面积器件效率达到了18%
[23], 标志着OSCs商业化进程的加速.
从共轭分子电子态调控调节材料特性的角度出发,对上述分子进行共轭单元、端基推拉电子单元、分子侧链单元等进行分子结构修饰, 可以有效改性材料特性, 进而开发出光电性能更为优异的非富勒烯受体材料. 包西昌
[24]以及He
[25]等分别从Y系列受体的改性修饰, 对该类分子的研究进展进行了综合论述. 除此之外, 詹传郎等从分子硒吩工程的角度, 对NFAs的分子结构设计进行了相关的综述
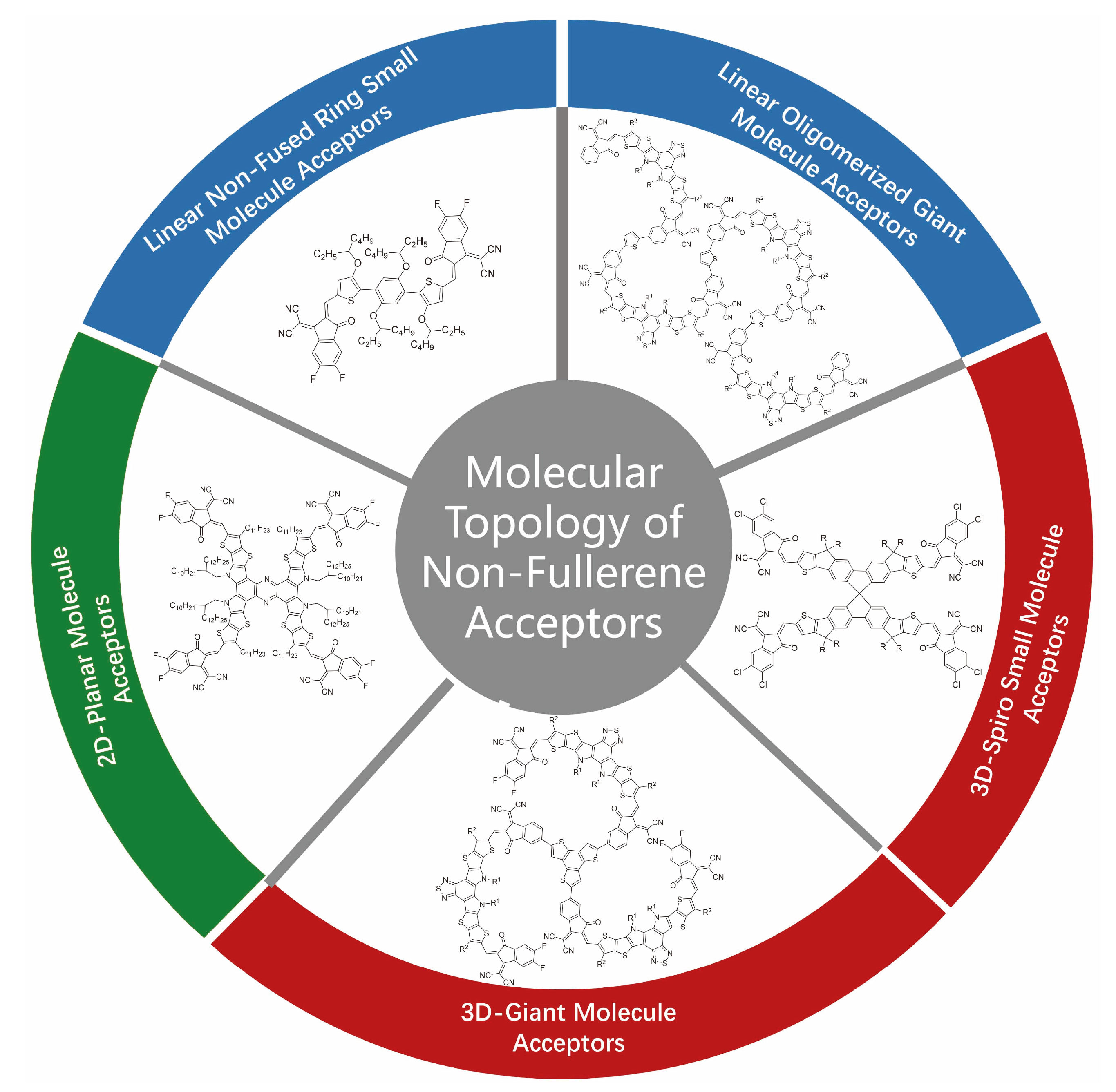
[26]. 以上这些综述对Y系列分子的构效关系以及未来的分子结构设计提出了明确的方向.除了化学键结构与类型对器件性能的影响外, 分子的空间构象也对材料特性及器件性能产生巨大影响. 因此, 近年来的分子设计方面也从分子的空间构型角度进行了较多的研究工作, 形成了较为系统的分子结构拓扑工程(Molecular Topology Engineering, MTE). 具体来说, 分子结构拓扑工程是一种通过精准设计分子空间结构及其连接方式, 构建出分别具有一维线性、二维平面以及空间三维扩展的新型共轭分子, 进而调控分子间相互作用、电子传输路径和材料性能. 如
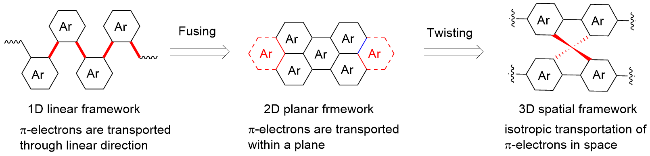
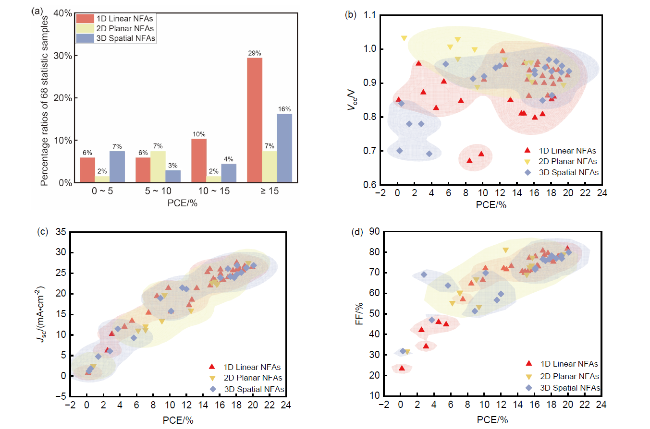
图2所示, 一维分子是指其共轭骨架主要沿着一个空间方向延伸的一类共轭分子, 由若干个芳香亚单元通过C—C单键相连形成, π电子沿线性方向传输
[27]; 二维分子则是指其共轭骨架在一个二维平面内扩展和离域的一类共轭分子. 其平坦、刚性的结构容易使二维平面分子之间存在强烈的面对面π-π堆积作用, 形成高度有序的结晶性薄膜, 有利于分子间的电荷传输
[28]. 现实中, 由于分子内大基团间的空间位阻, 往往使分子骨架弯曲形成一定的夹角, 完全平面化的二维NFAs几乎没有. 因此在本文中分子内夹角不超过30º的NFAs, 均近似认为是二维平面结构. 类似地, 三维分子是指其共轭骨架通过立体化学设计向三维空间扩展的共轭分子, 这类分子的核心特征是空间维度的突破. 通过引入空间位阻迫使分子结构发生巨大扭曲, 其π电子离域和电荷传输路径不再是线性的或面性的, 而是倾向于形成各向同性的三维网络
[29]. 基于共轭分子空间结构成为新型NFAs开发的新发展趋势, 本综述从共轭分子空间结构拓扑扩展的角度出发, 总结了具有一维线性、二维平面型和三维空间型分子的结构特征、分子设计思路、研究进展及其相应的结构-性能关系, 并对后续的分子设计创新进行了展望.