有机化学 ›› 2023, Vol. 43 ›› Issue (7): 2492-2498.DOI: 10.6023/cjoc202212025 上一篇 下一篇
研究论文
收稿日期:2022-12-19
修回日期:2023-01-22
发布日期:2023-03-17
通讯作者:
范威
基金资助:Received:2022-12-19
Revised:2023-01-22
Published:2023-03-17
Contact:
Wei Fan
Supported by:文章分享
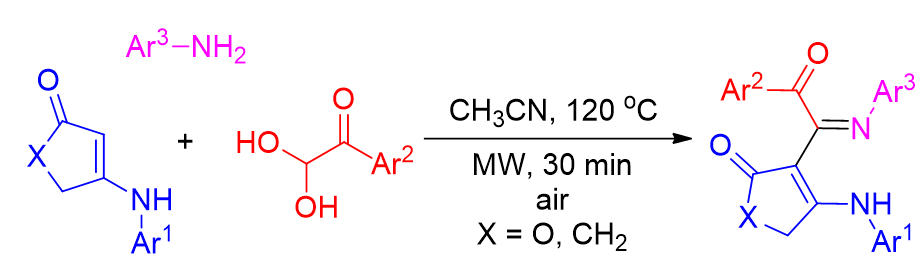
报道了一个O2促进下五元环烯胺的C—H亚胺化反应. 在微波辐射下, 季酮酸或1,3-环戊二酮衍生的烯胺酮、芳酮醛水合物和芳胺三组分参与的无金属催化反应进展顺利, 以良好的产率和完全的立体选择性得到了一系列α-烯胺基-α-芳酰基亚胺衍生物. 在该反应过程中, 空气充当绿色氧化剂, 水是唯一的副产物.
范威. O2促进下五元环烯胺的C—H亚胺化[J]. 有机化学, 2023, 43(7): 2492-2498.
Wei Fan. O2-Enabled C—H Imination of Five-Membered Cyclic Enamines[J]. Chinese Journal of Organic Chemistry, 2023, 43(7): 2492-2498.
| Entry | Solvent | Temp./℃ | Yieldb/% |
|---|---|---|---|
| 1 | EA | 100 | 27 |
| 2 | EtOH | 100 | 29 |
| 3 | DCE | 100 | 33 |
| 4 | Benzene | 100 | Trace |
| 5 | 1,4-Dioxane | 100 | 43 |
| 6 | THF | 100 | 58 |
| 7 | MeCN | 100 | 68 |
| 8 | MeCN | 110 | 70 |
| 9 | MeCN | 115 | 71 |
| 10 | MeCN | 120 | 73 |
| 11 | MeCN | 125 | 72 |
| 12 | MeCN | 130 | 71 |
| 13 | MeCN | 120 | 73c |
| 14 | MeCN | 120 | NDd |
| Entry | Solvent | Temp./℃ | Yieldb/% |
|---|---|---|---|
| 1 | EA | 100 | 27 |
| 2 | EtOH | 100 | 29 |
| 3 | DCE | 100 | 33 |
| 4 | Benzene | 100 | Trace |
| 5 | 1,4-Dioxane | 100 | 43 |
| 6 | THF | 100 | 58 |
| 7 | MeCN | 100 | 68 |
| 8 | MeCN | 110 | 70 |
| 9 | MeCN | 115 | 71 |
| 10 | MeCN | 120 | 73 |
| 11 | MeCN | 125 | 72 |
| 12 | MeCN | 130 | 71 |
| 13 | MeCN | 120 | 73c |
| 14 | MeCN | 120 | NDd |
| [1] |
(a) Hadjipavlou-Litina, D. J.; Geronikaki, A. A. Drug Des. Discovery 1998, 15, 199.
pmid: 18850749 |
|
(b) Adams, J. P. J. Chem. Soc., Perkin Trans. 1 2000, 125.
pmid: 18850749 |
|
|
(c) Gawronski, J.; Wascinska, N.; Gajewy, J. Chem. Rev. 2008, 108, 5227.
doi: 10.1021/cr800421c pmid: 18850749 |
|
|
(d) Patil, R. D.; Adimurthy, S. Asian J. Org. Chem. 2013, 2, 726.
doi: 10.1002/ajoc.v2.9 pmid: 18850749 |
|
| [2] |
(a) Eguchi, S. ARKIVOC 2005, 2005, 98.
|
|
(b) Palacios, F.; Alonso, C.; Aparicio, D.; Rubiales, G.; de los Santos, J. M. Tetrahedron 2007, 63, 523.
doi: 10.1016/j.tet.2006.09.048 |
|
|
(c) Palacios, F.; Aparicio, D.; Rubiales, G.; Alonso, C.; de los Santos, J. M. Curr. Org. Chem. 2009, 13, 810.
doi: 10.2174/138527209788167196 |
|
| [3] |
Li, H.; Lupp, D.; Das, P. K.; Yang, L.; Gonçalves, T. P.; Huang, M.-H.; Hajoui, M. E.; Liang, L.-C.; Huang, K.-W. ACS Catal. 2021, 11, 4071.
doi: 10.1021/acscatal.1c00379 |
| [4] |
(a) Ell, A. H.; Samec, J. S. M.; Brasse, C.; Baeckvall, J.-E. Chem. Commun. 2002, 1144.
pmid: 17992680 |
|
(b) Largeron, M.; Chiaroni, A.; Fleury, M.-B. Chem.-Eur. J. 2008, 14, 996.
pmid: 17992680 |
|
|
(c) Jiang, G.; Chen, J.; Huang, J.-S.; Che, C.-M. Org. Lett. 2009, 11, 4568.
doi: 10.1021/ol9018166 pmid: 17992680 |
|
|
(d) Su, F.; Mathew, S. C.; Moehlmann, L.; Antonietti, M.; Wang, X.; Blechert, S. Angew. Chem., Int. Ed. 2011, 50, 657.
pmid: 17992680 |
|
|
(e) Chen, B.; Wang, L.; Gao, S. ACS Catal. 2015, 5, 5851.
doi: 10.1021/acscatal.5b01479 pmid: 17992680 |
|
|
(f) Ray, R.; Chandra, S.; Yadav, V.; Mondal, P.; Maiti, D.; Lahiri, G. K. Chem. Commun. 2017, 53, 4006.
doi: 10.1039/C6CC10200J pmid: 17992680 |
|
| [5] |
(a) Blackburn, L.; Taylor, R. J. K. Org. Lett. 2001, 3, 1637.
pmid: 26924231 |
|
(b) Gnanaprakasam, B.; Zhang, J.; Milstein, D. Angew. Chem., Int. Ed. 2010, 49, 1468.
doi: 10.1002/anie.200907018 pmid: 26924231 |
|
|
(c) Maggi, A.; Madsen, R. Organometallics 2012, 31, 451.
doi: 10.1021/om201095m pmid: 26924231 |
|
|
(d) Zhang, G.; Hanson, S. K. Org. Lett. 2013, 15, 650.
doi: 10.1021/ol303479f pmid: 26924231 |
|
|
(e) Saha, B.; Wahidur Rahaman, S. M.; Daw, P.; Sengupta, G.; Bera, J. K. Chem.-Eur. J. 2014, 20, 6542.
doi: 10.1002/chem.v20.21 pmid: 26924231 |
|
|
(f) Tamura, M.; Tomishige, K. Angew. Chem., Int. Ed. 2015, 54, 864.
doi: 10.1002/anie.201409601 pmid: 26924231 |
|
|
(g) Mukherjee, A.; Nerush, A.; Leitus, G.; Shimon, L. J. W.; Ben-David, Y.; Espinosa Jalapa, N. A.; Milstein, D. J. Am. Chem. Soc. 2016, 138, 4298.
doi: 10.1021/jacs.5b13519 pmid: 26924231 |
|
|
(h) Esteruelas, M. A.; Lezaun, V.; Martinez, A.; Olivan, M.; Onate, E. Organometallics 2017, 36, 2996.
doi: 10.1021/acs.organomet.7b00521 pmid: 26924231 |
|
| [6] |
(a) Johnson, J. S.; Bergman, R. G. J. Am. Chem. Soc. 2001, 123, 2923.
pmid: 11456996 |
|
(b) Li, Y.; Shi, Y.; Odom, A. L. J. Am. Chem. Soc. 2004, 126, 1794.
doi: 10.1021/ja038320g pmid: 11456996 |
|
|
(c) Ryken, S. A.; Schafer, L. L. Acc. Chem. Res. 2015, 48, 2576.
doi: 10.1021/acs.accounts.5b00224 pmid: 11456996 |
|
|
(d) Mir, R.; Dudding, T. J. Org. Chem. 2016, 81, 2675.
doi: 10.1021/acs.joc.6b00241 pmid: 11456996 |
|
| [7] |
Srimani, D.; Feller, M.; Ben-David, Y.; Milstein, D. Chem. Commun. 2012, 48, 11853.
doi: 10.1039/c2cc36639h |
| [8] |
(a) Lee, S.-H.; Nikonov, G. I. ChemCatChem 2015, 7, 107.
doi: 10.1002/cctc.v7.1 |
|
(b) Kim, D.; Kang, B.; Hong, S. H. Org. Chem. Front. 2016, 3, 475.
doi: 10.1039/C5QO00378D |
|
| [9] |
(a) Zerecero-Silva, P.; Jimenez-Solar, I.; Crestani, M. G.; Arevalo, A.; Barrios-Francisco, R.; Garcia, J. J. Appl. Catal. A 2009, 363, 230.
doi: 10.1016/j.apcata.2009.05.027 |
|
(b) Chakraborty, S.; Berke, H. ACS Catal. 2014, 4, 2191.
doi: 10.1021/cs5004646 |
|
|
(c) Choi, J.-H.; Prechtl, M. H. G. ChemCatChem 2015, 7, 1023.
doi: 10.1002/cctc.201403047 |
|
|
(d) Chakraborty, S.; Milstein, D. ACS Catal. 2017, 7, 3968.
doi: 10.1021/acscatal.7b00906 |
|
| [10] |
(a) For selected reviews, see: a Elassara, A.-Z., A.; El-Khairb, A. A. Tetrahedron 2003, 59, 8463.
doi: 10.1016/S0040-4020(03)01201-8 pmid: 15137796 |
|
(b) Stanovnik, B.; Svete, J. Chem. Rev. 2004, 104, 2433.
pmid: 15137796 |
|
|
(c) Cao, S.; Jing, Y.; Liu, Y.; Wan, J.-P. Chin. J. Org. Chem. 2014, 34, 876 (in Chinese).
doi: 10.6023/cjoc201312016 pmid: 15137796 |
|
|
(曹硕, 景艳锋, 刘云云, 万结平, 有机化学, 2014, 34, 876.)
doi: 10.6023/cjoc201312016 pmid: 15137796 |
|
|
(d) Wan, J.-P.; Gao, Y. Chem. Rec. 2016, 16, 1164.
doi: 10.1002/tcr.201500296 pmid: 15137796 |
|
|
(e) Gaber, H. M.; Bagley, M. C.; Muhammada, Z. A.; Gomha, S. M. RSC Adv. 2017, 7, 14562.
doi: 10.1039/C7RA00683G pmid: 15137796 |
|
|
(f) Fu, L.; Wan, J.-P. Asian J. Org. Chem. 2019, 8, 767.
doi: 10.1002/ajoc.v8.6 pmid: 15137796 |
|
|
(g) Wang, Z.; Zhao, B.; Liu, Y.; Wan, J.-P. Adv. Synth. Catal. 2022, 364, 1508.
doi: 10.1002/adsc.v364.9 pmid: 15137796 |
|
| [11] |
(a) Liu, X.; Cheng, R.; Zhao, F.; Zhang-Negrerie, D.; Du, Y.; Zhao, K. Org. Lett. 2012, 14, 5480.
doi: 10.1021/ol3025583 pmid: 29419306 |
|
(b) Wang, F.; Sun, W.; Wang, Y.; Jiang, Y.; Loh, T.-P. Org. Lett. 2018, 20, 1256.
doi: 10.1021/acs.orglett.8b00222 pmid: 29419306 |
|
|
(c) Guo, Y.; Xiang, Y.; Wei, L.; Wan, J.-P. Org. Lett. 2018, 20, 3971.
doi: 10.1021/acs.orglett.8b01536 pmid: 29419306 |
|
| [12] |
(a) Sun, J.; Zhang-Negrerie, D.; Du, Y. Adv. Synth. Catal. 2016, 358, 2035.
doi: 10.1002/adsc.v358.13 pmid: 31457578 |
|
(b) Rafique, J.; Saba, S.; Schneider, A. R.; Franco, M. S.; Silva, S. M.; Braga, A. L. ACS Omega 2017, 2, 2280.
doi: 10.1021/acsomega.7b00445 pmid: 31457578 |
|
|
(c) Shang, Z.; Chen, Q.; Xing, L.; Zhang, Y.; Wait, L.; Du, Y. Adv. Synth. Catal. 2019, 361, 4926.
doi: 10.1002/adsc.v361.21 pmid: 31457578 |
|
| [13] |
(a) C—H Arylation: Ge, H.; Niphakis, M. J.; Georg, G. I. J. Am. Chem. Soc. 2008, 130, 3708.
doi: 10.1021/ja710221c |
|
(b) Wurtz, S.; Rakshit, S.; Neumann, J. J.; Droge, T.; Glorius, F. Angew. Chem., Int. Ed. 2008, 47, 7230.
doi: 10.1002/anie.v47:38 |
|
|
(c) Yu, W.; Du, Y.; Zhao, K. Org. Lett. 2009, 11, 2417.
doi: 10.1021/ol900576a |
|
|
(d) Yu, Y.-Y.; Bi, L. Georg, G. I. J. Org. Chem. 2013, 78, 6163.
doi: 10.1021/jo400830t |
|
|
(e) Wan, J.-P.; Tu, Z.; Wang, Y. Chem.-Eur. J. 2019, 25, 6907.
doi: 10.1002/chem.v25.28 |
|
|
(f) Mkrtchyan, S.; Laroshenko, V. O. Chem. Commun. 2020, 56, 2606.
doi: 10.1039/C9CC09945J |
|
| [14] |
(a) Yu, Y.; Niphakis, M. J.; Georg, G. I. Org. Lett. 2011, 13, 5932.
doi: 10.1021/ol202677g |
|
(b) Fu, L.; Xu, Z.; Wan, J.-P.; Liu, Y. Org. Lett. 2020, 22, 9518.
doi: 10.1021/acs.orglett.0c03548 |
|
|
(c) Fu, L.; Liu, Y.; Wan, J.-P. Org. Lett. 2021, 23, 4363.
doi: 10.1021/acs.orglett.1c01301 |
|
| [15] |
(a) Jiang, Y.; Liang, G.; Zhang, C.; Loh, T.-P. Eur. J. Org. Chem. 2016, 2016, 3326.
doi: 10.1002/ejoc.v2016.20 |
|
(b) Wan, J.-P.; Zhong, S.; Xie, L.; Cao, X.; Liu, Y.; Wei, L. Org. Lett. 2016, 18, 584.
doi: 10.1021/acs.orglett.5b03608 |
|
|
(c) Gao, Y.; Hu, C.; Wen, C.; Wan, J.-P. ACS Omega 2017, 2, 7784.
doi: 10.1021/acsomega.7b01422 |
|
|
(d) Gao, Y.; Liu, Y.; Wan, J.-P. J. Org. Chem. 2019, 84, 2243.
doi: 10.1021/acs.joc.8b02981 |
|
| [16] |
(a) Wan, J.-P.; Zhong, S.; Guo, Y.; Wei, L. Eur. J. Org. Chem. 2017, 2017, 4401.
doi: 10.1002/ejoc.v2017.30 |
|
(b) Tian, L.; Wan, J.-P.; Sheng, S. ChemCatChem 2020, 12, 2533.
doi: 10.1002/cctc.v12.9 |
|
|
(c) Yu, Q.; Liu, Y.; Wan, J.-P. Chin. Chem. Lett. 2021, 32, 3514.
doi: 10.1016/j.cclet.2021.04.037 |
|
| [17] |
(a) Jiang, H.; Huang, W.; Yu, Y.; Yi, S.; Li, J.; Wu, W. Chem. Commun. 2017, 53, 7473.
doi: 10.1039/C7CC03125D |
|
(b) Xiang, H.; Zhao, Q.; Tang, Z.; Xiao, J.; Xia, P.; Wang, C.; Yang, C.; Chen, X.; Yang, H. Org. Lett. 2017, 19, 146.
doi: 10.1021/acs.orglett.6b03441 |
|
|
(c) Sun, J.; Zhen, X.; Ge, H.; Zhang, G. An, X.; Du, Y. Beilstein J. Org. Chem. 2018, 14, 1452.
doi: 10.3762/bjoc.14.123 |
|
|
(d) Yu, Q.; Liu, Y.; Wan, J.-P. Org. Chem. Front. 2020, 7, 2770.
doi: 10.1039/D0QO00855A |
|
| [18] |
Zhang, Y.; Zhao, X.; Zhuang, C.; Wang, S.; Zhang-Negrerie, D.; Du, Y. Adv. Synth. Catal. 2018, 360, 2107.
doi: 10.1002/adsc.v360.11 |
| [19] |
(a) Yuan, J.; Zhang, Q.; Yu, M.; Huang, P.; Zhang, R.; Dong, D. Org. Lett. 2015, 17, 5012.
doi: 10.1021/acs.orglett.5b02485 pmid: 25658698 |
|
(b) Sun, X.; Lyu, Y.; Zhang-Negrerie, D.; Du, Y.; Zhao, K. Org. Lett. 2013, 15, 6222.
doi: 10.1021/ol4030716 pmid: 25658698 |
|
|
(c) Luo, T.; Wan, J.-P.; Liu, Y. Org. Chem. Front. 2020, 7, 1107.
doi: 10.1039/D0QO00065E pmid: 25658698 |
|
|
(d) Yuan, Y.; Hou, W.; Zhang-Negrerie, D.; Zhao, K.; Du, Y. Org. Lett. 2014, 16, 5410.
doi: 10.1021/ol5026525 pmid: 25658698 |
|
|
(e) Zheng, C.; Wang, Y.; Fan, R. Org. Lett. 2015, 17, 916.
doi: 10.1021/acs.orglett.5b00026 pmid: 25658698 |
|
|
(f) Duan, X.; Li, H.; Li, W.; Wang, J.; Liu, N. ChemistrySelect 2021, 6, 6478.
doi: 10.1002/slct.v6.25 pmid: 25658698 |
|
| [20] |
(a) Zhang, H.; Xu, J.; Ouyang, Y.; Yue, X.; Zhou, C.; Ni, Z.; Li, W. Chin. Chem. Lett. 2022, 33, 2036.
doi: 10.1016/j.cclet.2021.09.069 pmid: 26027938 |
|
(b) Gonzalez-de-Castro, A.; Xiao, J. J. Am. Chem. Soc. 2015, 137, 8206.
doi: 10.1021/jacs.5b03956 pmid: 26027938 |
|
|
(c) Cheng, Z.; Jin, W.; Liu, C. Org. Chem. Front. 2019, 6, 841.
doi: 10.1039/c8qo01412d pmid: 26027938 |
|
|
(d) Xu, J.; Yue, X.; He, L.; Shen, J.; Ouyang, Y.; Liang, C.; Li, W. ACS Sustainable Chem. Eng. 2022, 10, 14119.
doi: 10.1021/acssuschemeng.1c06755 pmid: 26027938 |
|
|
(e) Liu, K.-J.; Deng, J.-H.; Zeng, T.-Y.; Chen, X.-J.; Huang, Y.; Cao, Z.; Lin, Y.-W.; He, W.-M. Chin. Chem. Lett. 2020, 31, 1868.
doi: 10.1016/j.cclet.2020.01.036 pmid: 26027938 |
|
|
(f) Xu, J.; He, L.; Liang, C.; Yue, X.; Ouyang, Y.; Zhang, P. ACS Sustainable Chem. Eng. 2021, 9, 13663.
doi: 10.1021/acssuschemeng.1c05237 pmid: 26027938 |
|
|
(g) Zhang, Y.; Hatami, N.; Lange, N. S.; Ronge, E.; Schilling, W.; Jooss, C.; Das, S. Green Chem. 2020, 22, 4516.
doi: 10.1039/D0GC01187H pmid: 26027938 |
|
|
(h) Xu, J.; Huang, L.; He, L.; Liang, C.; Ouyang, Y.; Shen, J.; Jiang, M.; Li, W. Green Chem. 2021, 23, 6632.
doi: 10.1039/D1GC01899J pmid: 26027938 |
|
|
(i) Huang, L.; Xu, J.; He, L.; Liang, C.; Ouyang, Y.; Yu, Y.; Li, W.; Zhang, P. Chin. Chem. Lett. 2021, 32, 3627.
doi: 10.1016/j.cclet.2021.04.016 pmid: 26027938 |
|
|
(j) Li, W.; Li, S.; Luo, L.; Ge, Y.; Xu, J.; Zheng, X.; Yuan, M.; Li, R.; Chen, H.; Fu, H. Green Chem. 2021, 23, 3649.
doi: 10.1039/D1GC00716E pmid: 26027938 |
| [1] | 李靖鹏, 黄顺桃, 杨棋, 李伟强, 刘腾, 黄超. 利用连续流动技术合成(Z)-N-乙烯基取代N,O-缩醛[J]. 有机化学, 2023, 43(4): 1550-1558. |
| [2] | 曾成富, 何媛, 李清, 董琳. Ir(III)催化新型三组分串联三氟乙氧基化反应并一锅法构建复杂酰胺化合物[J]. 有机化学, 2023, 43(3): 1115-1123. |
| [3] | 陈东平, 杨春红, 李明, 赵国孝, 王文鹏, 王喜存, 权正军. 芳炔参与的三组分芳基化反应进展[J]. 有机化学, 2023, 43(2): 503-525. |
| [4] | 徐勇, 张永兴, 胡佳, 陈宬, 原晔, Francis Verpoort. ZnO/离子液体体系催化常压二氧化碳合成β-羰基氨基甲酸酯[J]. 有机化学, 2022, 42(8): 2542-2550. |
| [5] | 乔辉杰, 杨利婷, 陈雅, 王嘉琳, 孙武轩, 董昊博, 王云威. 温和条件下高效合成咪唑并杂环-肼类衍生物的三组分串联反应[J]. 有机化学, 2022, 42(4): 1188-1197. |
| [6] | 王明亮, 尹刘燕, 温甜甜, 张晓, 高杰, 王兰芝. 多官能团化的1,5-苯并二氮杂䓬类化合物的绿色合成[J]. 有机化学, 2022, 42(1): 160-171. |
| [7] | 许振丽, 张宗雪, 孟晨湘, 张萧雅, 许凯, 刘澜涛, 王涛, 徐海云, 毛国梁. 无配体条件钯催化内炔的氢膦酰化反应合成(E)-烯烃膦酸酯类化合物[J]. 有机化学, 2021, 41(8): 3264-3271. |
| [8] | 祝改革, 赖晓辉, 王思雨, 林彩霞, 袁耀锋. 铜催化合成2-亚氨基-1,2-二氢喹啉化合物[J]. 有机化学, 2021, 41(7): 2810-2819. |
| [9] | 王翔, 陈平, 支三军, 胡华友, 阚玉和, 唐果东, 张载超. 利用三组分串联反应合成3-苯并[d]咪唑啉取代的吡喃并[3,2-c]色烯-2-酮衍生物[J]. 有机化学, 2021, 41(3): 1241-1245. |
| [10] | 韩超, 聂磊, 韩晓, 张岩, 孙克磊, 石磊, 崔广华, 孟伟. “一锅”三组分合成新型1,5-苯并二氮杂䓬类化合物与抗牛病毒性腹泻病毒(BVDV)活性[J]. 有机化学, 2021, 41(2): 819-825. |
| [11] | 石瑛, 秦富文, 王捷, 闫艳梅. 无金属参与的连续的Ugi三组分/炔烃-叠氮环加成反应一锅合成[1,2,3]三唑并[1,5- a]喹喔啉[J]. 有机化学, 2021, 41(1): 297-302. |
| [12] | 郑茜茜, 刘云云, 万结平. N-磺基脒类化合物合成研究进展[J]. 有机化学, 2020, 40(7): 1891-1900. |
| [13] | 史大鹏, 段中余. 可回收铜纳米颗粒在无溶剂下催化三组分偶联反应合成炔丙基胺[J]. 有机化学, 2020, 40(5): 1316-1322. |
| [14] | 丁雨昕, 马永敏, 陈静. 无溶剂无催化剂条件下三组分一锅合成2,4,6-三芳基嘧啶衍生物的新方法[J]. 有机化学, 2020, 40(12): 4357-4363. |
| [15] | 张梦烨, 王宁, 徐文韬, 黄志斌, 史达清. 色烯并[4,3-d]吡唑并[3,4-b]吡啶衍生物的三组分合成及荧光性质研究[J]. 有机化学, 2019, 39(4): 1085-1094. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||
