有机化学 ›› 2025, Vol. 45 ›› Issue (4): 1379-1385.DOI: 10.6023/cjoc202407001 上一篇 下一篇
研究论文
收稿日期:2024-07-01
修回日期:2024-08-18
发布日期:2024-09-30
基金资助:
Zheng Wang( ), Yuqin Lan, Zhiyi Zhou, Yingzi Tan, Zongcheng Wang(
), Yuqin Lan, Zhiyi Zhou, Yingzi Tan, Zongcheng Wang( )
)
Received:2024-07-01
Revised:2024-08-18
Published:2024-09-30
Contact:
* E-mail: Supported by:文章分享
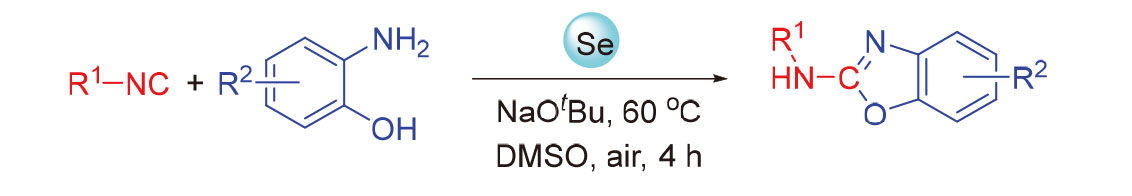
报道了一种硒粉介导下异腈与邻氨基苯酚进行环化反应合成2-胺基苯并噁唑的方法. 该反应简单地采用硒粉为促进剂, 叔丁醇钠为碱, 在温和条件下实现了多种2-胺基苯并噁唑的绿色、高效构建. 该反应具有操作简便和无金属污染的优点. 该方法还可以实现2-胺基苯并噻唑和2-胺基苯并咪唑的合成.
王峥, 兰羽琴, 周芷怡, 谭英姿, 王宗成. 硒介导异腈与邻氨基苯酚环化反应合成2-胺基苯并噁唑[J]. 有机化学, 2025, 45(4): 1379-1385.
Zheng Wang, Yuqin Lan, Zhiyi Zhou, Yingzi Tan, Zongcheng Wang. Selenium Mediated Cyclization Reaction of Isonitriles with o-Aminophenols to Synthesize 2-Aminobenzoxazoles[J]. Chinese Journal of Organic Chemistry, 2025, 45(4): 1379-1385.
| Entry | Base (equiv.) | Solvent | T/℃ | Yieldb/% |
|---|---|---|---|---|
| 1 | K2CO3 (1) | DCM | 25 | 23 |
| 2 | Cs2CO3 (1) | DCM | 25 | 5 |
| 3 | Na2CO3 (1) | DCM | 25 | 25 |
| 4 | K3PO4 (1) | DCM | 25 | 26 |
| 5 | tBuONa (1) | DCM | 25 | 65 |
| 6 | DABCO (1) | DCM | 25 | 33 |
| 7 | Et3N (1) | DCM | 25 | 26 |
| 8 | DBU (1) | DCM | 25 | 21 |
| 9 | tBuONa (1) | EtOH | 25 | 30 |
| 10 | tBuONa (1) | DMF | 25 | 61 |
| 11 | tBuONa (1) | 1,4-Dioxane | 25 | 20 |
| 12 | tBuONa (1) | CH3CN | 25 | 56 |
| 13 | tBuONa (1) | EtOAc | 25 | 0 |
| 14 | tBuONa (1) | Toluene | 25 | 0 |
| 15 | tBuONa (1) | DMSO | 25 | 76 |
| 16 | tBuONa (0.2) | DMSO | 25 | 38 |
| 17 | — | DMSO | 25 | trace |
| 18 | tBuONa (1) | DMSO | 60 | 88 |
| 19 | tBuONa (1) | DMSO | 80 | 86 |
| 20 | tBuONa (1) | DMSO | 60 | 62c |
| 21 | tBuONa (1) | DMSO | 60 | 21d |
| 22 | tBuONa (1) | DMSO | 60 | 0e |
| Entry | Base (equiv.) | Solvent | T/℃ | Yieldb/% |
|---|---|---|---|---|
| 1 | K2CO3 (1) | DCM | 25 | 23 |
| 2 | Cs2CO3 (1) | DCM | 25 | 5 |
| 3 | Na2CO3 (1) | DCM | 25 | 25 |
| 4 | K3PO4 (1) | DCM | 25 | 26 |
| 5 | tBuONa (1) | DCM | 25 | 65 |
| 6 | DABCO (1) | DCM | 25 | 33 |
| 7 | Et3N (1) | DCM | 25 | 26 |
| 8 | DBU (1) | DCM | 25 | 21 |
| 9 | tBuONa (1) | EtOH | 25 | 30 |
| 10 | tBuONa (1) | DMF | 25 | 61 |
| 11 | tBuONa (1) | 1,4-Dioxane | 25 | 20 |
| 12 | tBuONa (1) | CH3CN | 25 | 56 |
| 13 | tBuONa (1) | EtOAc | 25 | 0 |
| 14 | tBuONa (1) | Toluene | 25 | 0 |
| 15 | tBuONa (1) | DMSO | 25 | 76 |
| 16 | tBuONa (0.2) | DMSO | 25 | 38 |
| 17 | — | DMSO | 25 | trace |
| 18 | tBuONa (1) | DMSO | 60 | 88 |
| 19 | tBuONa (1) | DMSO | 80 | 86 |
| 20 | tBuONa (1) | DMSO | 60 | 62c |
| 21 | tBuONa (1) | DMSO | 60 | 21d |
| 22 | tBuONa (1) | DMSO | 60 | 0e |
| [1] |
(a) Alper-Hayta, S.; Arisoy, M.; Temiz-Arpaci, Ö.; Yildiz, I.; Aki, E.; Özkan, S.; Kaynak, F. Eur. J. Med. Chem. 2008, 43, 2568.
doi: 10.1016/j.ejmech.2007.12.019 pmid: 1560442 |
|
(b) Safak, C.; Erdogan, H.; Palaska, E.; Sunal, R.; Duru, S. J. Med. Chem. 1992, 35, 1296.
pmid: 1560442 |
|
|
(c) Feng, M. H.; Tang, B. Q.; Liang, S. H.; Jiang, X. F. Curr. Top. Med. Chem. 2016, 16, 1200.
pmid: 1560442 |
|
|
(d) Hal, I. H.; Peaty, N. J.; Henry, J. R.; Easmon, J.; Heinisch, G.; Pürstinger, G. Arch. Pharm. 1999, 332, 115.
pmid: 1560442 |
|
|
(e) Hou, J.-C.; Ji, H.-T.; Lu, Y.-H.; Wang, J.-S.; Xu, Y.-D.; Zeng, Y.-Y.; He, W.-M. Chin. Chem. Lett. 2024, 35, 109514.
pmid: 1560442 |
|
|
(f) Chen, X.; Ouyang, W.-T.; Li, X.; He, W.-M. Chin. J. Org. Chem. 2023, 43, 4213 (in Chinese).
pmid: 1560442 |
|
|
(陈祥, 欧阳文韬, 李潇, 何卫民, 有机化学, 2023, 43, 4213.)
doi: 10.6023/cjoc202307026 pmid: 1560442 |
|
| [2] |
(a) Pochetti, G.; Mitro, N.; Lavecchia, A.; Gilardi, F.; Besker, N.; Scotti, E.; Aschi, M.; Re, N.; Fracchiolla, G.; Laghezza, A.; Tortorella, P.; Montanari, R.; Novellino, E.; Mazza, F.; Crestani, M.; Loiodice, F. J. Med. Chem. 2010, 53, 4354.
doi: 10.1021/jm9013899 pmid: 20462215 |
|
(b) Kohler, P. C.; Ritschel, T.; Schweizer, W. B.; Klebe, G.; Diederich, F. Chem.-Eur. J. 2009, 15, 10809.
pmid: 20462215 |
|
| [3] |
Chai, J.-Y.; Jung, B.-K.; Hong, S.-J. Korean J. Parasitol. 2021, 59, 189.
|
| [4] |
Liu, K. G.; Lo, J. R.; Comery, T. A.; Zhang, G. M.; Zhang, J. Y.; Kowal, D. M.; Smith, D. L.; Di, L.; Kerns, E. H.; Schechter, L. E.; Robichaud, A. J. Bioorg. Med. Chem. Lett. 2009, 19, 1115.
|
| [5] |
Muro, F.; Iimura, S.; Yoneda, Y.; Chiba, J.; Watanabe, T.; Setoguchi, M.; Takayama, G.; Yokoyama, M.; Takashi, T.; Nakayama, A.; Machinaga, N. Bioorg. Med. Chem. 2009, 17, 1232.
|
| [6] |
Kablaoui, N.; Patel, S.; Shao, J.; Demian, D.; Hoffmaster, K.; Berlioz, F.; Vazquez, M. L.; Moore, W. M.; Nugent, R. A. Bioorg. Med. Chem. Lett. 2013, 23, 907.
doi: 10.1016/j.bmcl.2012.10.040 pmid: 23266122 |
| [7] |
Seregin, I.; Gevorgyan, V. Chem. Soc. Rev. 2007, 36, 1173.
doi: 10.1039/b606984n pmid: 17576484 |
| [8] |
You, L.; Yuan, J.; Yang, L.; Xiao, Y.; Mao, P. Chin. J. Org. Chem. 2016, 36, 2634 (in Chinese).
|
|
(游利琴, 袁金伟, 杨亮茹, 肖咏梅, 毛璞, 有机化学, 2016, 36, 2634.)
doi: 10.6023/cjoc201604044 |
|
| [9] |
(a) Vardhan Reddy, K. H.; Anil Kumar, B. S. P.; Prakash Reddy, V.; Uday Kumar, R.; Nageswar, Y. V. D. RSC Adv. 2014, 4, 45579.
|
|
(b) Yamato, M.; Takeuchi, Y.; Hattori, K.; Hashigaki, K. Chem. Pharm. Bull. 1984, 32, 3053.
|
|
|
(c) Saladino, R.; Crestini, C.; Occhionero, F.; Nicoletti, R. Synth. Commun. 1996, 26, 3241.
|
|
|
(d) Kövér, J.; Tímár, T.; Tompa, J. Synthesis 1994, 1124.
|
|
|
(e) Gu, J.; Cai, C. Synlett 2015, 26, 639.
|
|
| [10] |
(a) Wu, Y. Q.; Limburg, D. C.; Wilkinson, D. E.; Hamilton, G. S. J. Heterocycl. Chem. 2003, 40, 191.
|
|
(b) El-Faham, A.; Chebbo, M.; Abdul-Ghani, M.; Younes, G. Heterocycl. Chem. 2006, 43, 599.
|
|
|
(c) Cioffi, C. L.; Lansing, J. J.; Yüksel, H. J. Org. Chem. 2010, 75, 7942.
|
|
|
(d) Zhang, X. Y.; Jia, X. F.; Wang, J. J.; Fan, X. S. Green Chem. 2011, 13, 413.
|
|
|
(e) Kasthuri, M.; Sharath Babu, H.; Shiva Kumar, C.; Nagendra Kumar, P. V. Synlett 2015, 26, 897.
|
|
|
(f) Lin, C. C.; Hsieh, T. H.; Liao, P. Y.; Liao, Z. Y.; Chang, C. W.; Shih, Y. C.; Yeh, W. H.; Chien, T. C. Org. Lett. 2014, 16, 892.
|
|
| [11] |
(a) Kim, J. Y.; Cho, S. H.; Joseph, J.; Chang, S. Angew. Chem.,Int. Ed. 2010, 49, 9899.
pmid: 19254040 |
|
(b) Li, Y. M.; Liu, J.; Xie, Y. S.; Zhang, R.; Jin, K.; Wang, X. N.; Duan, C. Y. Org. Biomol. Chem. 2012, 10, 3715.
pmid: 19254040 |
|
|
(c) Li, Y. M.; Xie, Y. S.; Zhang, R.; Jin, K.; Wang, X. N.; Duan, C. Y. J. Org. Chem. 2011, 76, 5444.
pmid: 19254040 |
|
|
(d) Monguchi, D.; Fujiwara, T.; Furukawa, H.; Mori, A. Org. Lett. 2009, 11, 1607.
doi: 10.1021/ol900298e pmid: 19254040 |
|
|
(e) Pal, P.; Giri, A. K.; Singh, H.; Ghosh, S. C.; Panda, A. B. Chem. Asian J. 2014, 9, 2392.
pmid: 19254040 |
|
|
(f) Xie, Y. J.; Qian, B.; Xie, P.; Huang, H. M. Adv. Synth. Catal. 2013, 355, 1315.
pmid: 19254040 |
|
|
(g) Gao, W. J.; Li, W. C.; Zeng, C. C.; Tian, H. Y.; Hu, L. M.; Little, R. D. J. Org. Chem. 2014, 79, 9613.
pmid: 19254040 |
|
| [12] |
(a) Gilchrist, T. L.; John Harris, C.; King, F. D.; Peek, M. E. J. Chem. Soc., 1988, 2169.
pmid: 25641711 |
|
(b) Morofuji, T.; Shimizu, A.; Yoshida, J. Chem.-Eur. J. 2015, 21, 3211.
doi: 10.1002/chem.201406398 pmid: 25641711 |
|
| [13] |
(a) Wang, H.; Xu, B. Chin. J. Org. Chem. 2015, 35, 588 (in Chinese).
|
|
(王浩, 许斌, 有机化学, 2015, 35, 588.)
doi: 10.6023/cjoc201411035 |
|
|
(b) Lv, Y.; Bao, P.; Yue, H.; Li, J-S.; Wei, W. Green Chem. 2019, 21, 6051.
|
|
|
(c) Ma, C.; Li, X.; Chen, X.; He, X.; Zhang, S-T.; Jiang, Y-Q.; Yu, B. Org. Lett., 2023, 25, 8016.
|
|
| [14] |
(a) Zhu, T.-H.; Wang, S.-Y.; Wang, G.-N.; Ji, S.-J. Chem.-Eur. J. 2013, 19, 5850.
|
|
(b) Zhu, T.-H.; Wang, S.-Y.; Wang, G.-N.; Ji, S.-J. Adv. Synth. Catal. 2014, 356, 509.
|
|
| [15] |
Liu, J.; Hoover, J. M. Org. Lett. 2019, 21, 4510.
|
| [16] |
Liu, B.; Yin, M.; Gao, H.; Wu, W.; Jiang, H. J. Org. Chem. 2013, 78, 3009.
|
| [17] |
Vlaar, T.; Cioc, R. C.; Mampuys, P.; Maes, B. U. W.; Orru, R. V. A.; Ruijter, E. Angew. Chem., Int. Ed. 2012, 51, 13058.
|
| [18] |
Wang, G.-N.; Zhu, T.-H.; Wang, S.-Y.; Wei, T.-Q.; Ji, S.-J. Tetrahedron 2014, 70, 8079.
|
| [19] |
(a) Ji, H.-T.; Jiang, J.; He, W.-B.; Lu, Y.-H.; Liu, Y.-Y.; Li, X.; He, W-M. J. Org. Chem. 2024, 89, 4113.
pmid: 12027681 |
|
(b) Ji, H.-T.; Luo, Q.-X.; Wang, K.-L.; Ouyang, W.-T.; Li, H.-X.; He, W.-M. Green Chem. 2023, 25, 7983.
pmid: 12027681 |
|
|
(c) Kihlberg, T.; Karimi, F.; Långström, B. J. Org. Chem. 2002, 67, 3687.
pmid: 12027681 |
|
| [20] |
(a) Fei, N.; Wang, Y.; Gu, Y.; Wang, Z.; Zhu, Y.; Li, Y. J. Org. Chem. 2023, 88, 13042.
|
|
(b) Lin, J.-X.; Liu, G.-H.; Liu, L.-Q.; Wang, Y.-C.; He, Y. J. Org. Chem. 2024, 89, 101.
|
|
|
(c) Zhong, W.; Li, M.; Jin, Y.; Jiang, H.; Wu, W. Chem. Commun. 2022, 58, 6522.
|
|
|
(d) Shao, L.; Li, Y.; Lu, J.; Jiang, X. Org. Chem. Front. 2019, 6, 2999.
|
|
| [21] |
(a) Duangkamol, C.; Phakhodeea, W.; Pattarawarapan, M. Synthesis 2020, 52, 1981.
|
|
(b) Tran, D. T.; Huynh, T. N.; Nguyen, P. C.; Phan, N. T. S.; Nguyen, T. T. Tetrahedron Lett. 2023, 122, 154510.
|
|
|
(c) Xu, Y.; Li, F.; Zhao, N.; Su, J.; Wang, C.; Wang, C.; Li, Z.; Wang, L. Green Chem. 2021, 23, 8047.
|
| [1] | 冯书晓, 钟轩, 陈嘉豪, 张宗洛, 谷广娜, 王俊岭, 郭亚菲, 马军营, 张守仁. 纳米氧化铜催化单质硒与芳基碘“一锅法”合成对称二硒化物[J]. 有机化学, 2025, 45(7): 2425-2434. |
| [2] | 马豪杰, 周风院, 何雨蒙, 周小强, 孙洲, 张玉琦. 碘促进分子间环化合成2-苯基喹唑啉[J]. 有机化学, 2025, 45(6): 2157-2162. |
| [3] | 夏登鹏, 吴奇, 蔡志华, 杜广芬. 无催化条件下吲哚选择性硒化制备3-硒代吲哚[J]. 有机化学, 2025, 45(1): 349-357. |
| [4] | 蒋镓西, 刘全忠. 乙烯基重氮化合物非金属卡宾机制参与的反应[J]. 有机化学, 2024, 44(9): 2640-2657. |
| [5] | 高宇珅, 高媛媛, 张安安, 李路, 耿巍芝, 张凤华, 李飞, 刘澜涛. BF3•OEt2介导2-炔基苯胺的分子内环化反应合成3-硫醚吲哚化合物[J]. 有机化学, 2024, 44(9): 2785-2795. |
| [6] | 丁柔, 石思雨, 马超, 魏伟, 吕玉芬. 非金属1,8-二氮杂双环[5.4.0]十一碳-7-烯介导下乙缩醛酸与异硫氰酸酯反应合成α-缩醛基酰胺[J]. 有机化学, 2024, 44(7): 2216-2222. |
| [7] | 田永盛, 魏斓枫, 黄嘉为, 韦玉, 徐亮, 刘帅. 四丁基三溴化铵促进的有机硼酸在无过渡金属条件下的脱硼硒化、溴化和羟基化反应[J]. 有机化学, 2024, 44(6): 1987-1997. |
| [8] | 陈栋栋, 杨旭锋. 苄叉丙酮、硒粉和硼氢化钠一锅法构建四氢-2H-硒吡喃衍生物[J]. 有机化学, 2024, 44(5): 1641-1648. |
| [9] | 冯淼, 吕兰兰, 郭一佳, 刘建全, 王香善. 银催化邻羟基苯基炔丙醇5-exo-dig环化反应构筑2-亚甲基-2,3-二氢苯并呋喃-3-醇[J]. 有机化学, 2024, 44(4): 1218-1225. |
| [10] | 雍达明, 田杰, 杨瑞洪, 吴启超, 张旭. 氧化锆负载硒催化苯酚氧化反应[J]. 有机化学, 2024, 44(4): 1343-1347. |
| [11] | 雍达明, 左婷婷, 吴启超, 张旭. 氧化锆负载硒催化苯胺氧化聚合反应[J]. 有机化学, 2024, 44(11): 3392-3398. |
| [12] | 赵茜帆, 陈永正, 张世明. 碳基非金属催化剂在有机合成领域的应用及机理研究[J]. 有机化学, 2024, 44(1): 137-147. |
| [13] | 张莹珍, 江丹丹, 李娟华, 王菁菁, 刘昆明, 刘晋彪. 高选择性硒代半胱氨酸荧光探针的构建策略及成像[J]. 有机化学, 2024, 44(1): 41-53. |
| [14] | 冯莹珂, 王贺, 崔梦行, 孙然, 王欣, 陈阳, 李蕾. 可见光诱导的新型官能化芳基异腈化合物的二氟烷基化环化反应[J]. 有机化学, 2023, 43(8): 2913-2925. |
| [15] | 徐忠荣, 万结平, 刘云云. 基于热、光以及电化学过程的无过渡金属碳-氢键硫氰化和硒氰化反应[J]. 有机化学, 2023, 43(7): 2425-2446. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||