有机化学 ›› 2021, Vol. 41 ›› Issue (3): 934-946.DOI: 10.6023/cjoc202008017 上一篇 下一篇
所属专题: 有机电合成虚拟专辑
综述与进展
收稿日期:2020-09-11
修回日期:2020-09-22
发布日期:2020-10-15
通讯作者:
许颖
基金资助:
Yingjie Liu1, Yinghui Han1, Liqing Lin1, Ying Xu1,*( )
)
Received:2020-09-11
Revised:2020-09-22
Published:2020-10-15
Contact:
Ying Xu
About author:Supported by:文章分享
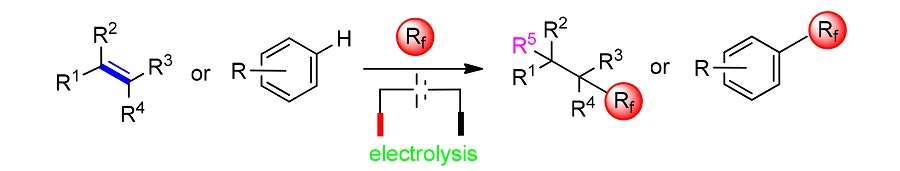
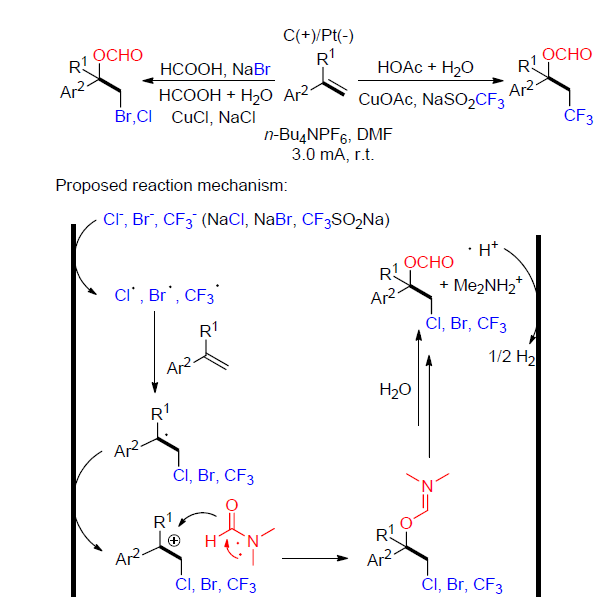
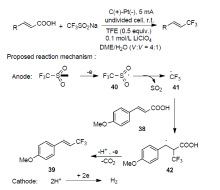
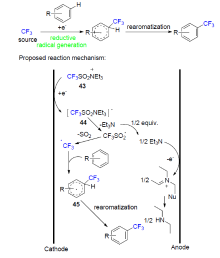
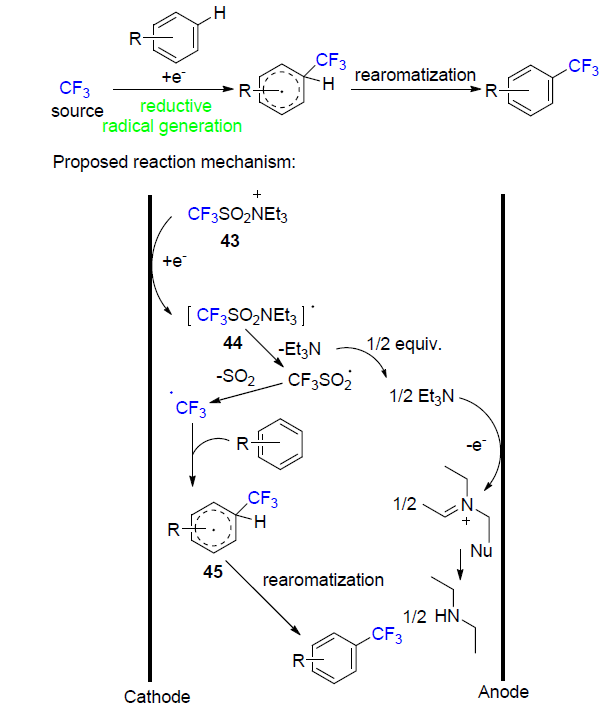
氟化学已经在各行各业受到广泛应用, 氟化学和有机化学的结合也遍地生花. 由于将氟原子或氟基团引入到药物中具有重要意义, 因此寻求一种有效的氟烷基化途径至关重要. 随着电化学的发展, 人们将电化学和氟烷基化反应进行了巧妙地结合. 进而得到了更加安全、经济、环保并且高效的氟烷基化途径. 在电化学指导下的氟烷基化反应途径, 不仅在反应方式方面进行了革新, 同样在底物普适性方面也具有优势. 针对不饱和脂肪族化合物及其衍生物和芳香族化合物的电化学催化下的氟烷基化反应已经有诸多报道. 根据底物的性质及其反应机理总结了电催化下氟烷基化方法的进展.
刘颖杰, 韩莹徽, 林立青, 许颖. 电化学催化下的多氟烷基化反应研究进展[J]. 有机化学, 2021, 41(3): 934-946.
Yingjie Liu, Yinghui Han, Liqing Lin, Ying Xu. Research Progress of Polyfluoroalkylation Reaction under Electrochemical Catalysis[J]. Chinese Journal of Organic Chemistry, 2021, 41(3): 934-946.

| [1] |
He, S. C.; Tian, D. Z.; Guo, B. H.; Chen, H. C. Zhejiang Chem. Ind. 2014, 45, 1. (in Chinese)
|
|
(何双材, 田端正, 郭本辉, 陈慧闯, 浙江化工, 2014, 45, 1.)
|
|
| [2] |
Kochervinskii, V. V.; Shoranova, L. O.; Shakirzyanov, R. I. Pharm. Sci. Technol. Today 2016,27266.
|
| [3] |
Tomilenko, A. A.; Bul'bak, T. A.; Pokhilenko, L. N. Dokl. Akad. Nauk 2016, 469, 82.
|
| [4] |
Müller, K.; Faeh, C.; Diederich, F. Science 2007, 317, 1881.
pmid: 17901324 |
| [5] |
Hagmann, W. K. J. Med. Chem. 2008, 51, 4359.
pmid: 18570365 |
| [6] |
Kirk, K. L. Org. Process Res. Dev. 2008, 12, 305.
doi: 10.1021/op700134j |
| [7] |
Purser, S.; Moore, P. R.; Swallow, S.; Gouverneur, V. Chem. Soc. Rev. 2008, 37, 320.
doi: 10.1039/b610213c pmid: 18197348 |
| [8] |
Tomashenko, O. A.; Grushin, V. V. Chem. Rev. 2011, 111, 4475.
pmid: 21456523 |
| [9] |
Zhou, Y.; Wang, J.; Gu, Z, N.; Wang, S. N.; Zhu, W. Chem. Rev. 2016, 116, 422.
pmid: 26756377 |
| [10] |
Wang, J.; Sanchez-Roselló, M.; Acenã, J. L.; del Pozo, C.; Sorochinsky, A. E.; Fustero, S.; Soloshonok, V. A.; Liu, H. Chem. Rev. 2014, 114, 2432.
pmid: 24299176 |
| [11] |
(a) Li, G. B.; Zhang, C.; Song, C.; Ma, Y. D. Beilstein J. Org. Chem. 2018, 14, 155.
doi: 10.3762/bjoc.14.11 pmid: 25635524 |
|
(b) Alonso, C.; Marigorta, E. M.; Rubiale, G.; Palacios, F. Chem. Rev. 2015, 115, 1847.
pmid: 25635524 |
|
|
(c) Studer, A. Angew. Chem.. Int. Ed. 2012, 51, 8950.
pmid: 25635524 |
|
| [12] |
(a) Nagib, D. A.; MacMillan, D. W. Nature 2011, 480, 224.
pmid: 21844378 |
|
(b) Ji, Y.; Brueckl, T.; Baxter, R.; Baxter, R. D.; Fujiwara, Y.; Seiple, I. B.; Su, S.; Blackmond, D. G.; Baran, P. S. Proc. Natl. Acad. Sci. U. S. A. 2011, 108, 14411.
pmid: 21844378 |
|
|
(c) Brien, A. G.; Maruyama, A.; Inokuma, Y.; Fujita, M.; Baran, P. S.; Blackmond, D. G. Angew. Chem.. Int. Ed. 2014, 53, 11868.
pmid: 21844378 |
|
| [13] |
(a) Sladojevich, F.; McNeill, E.; Borgel, J.; Zheng, S. L.; Ritter, T. Angew. Chem.. Int. Ed. 2015, 54, 3712.
|
|
(b) Cui, L.; Matusaki, Y.; Tada, N.; Miura, T.; Uno, B.; Itoh, A. Adv. Synth. Catal. 2013, 355, 2203.
|
|
| [14] |
Cho, E. J.; Senecal, T. D.; Kinzel, T.; Zhang, Y.; Watson, D. A.; Buchwald, S. L. Science 2010, 328, 1679.
pmid: 20576888 |
| [15] |
(a) Oishi, M.; Kondo, H.; Amii, H. Chem. Commun. 2009,1909.
pmid: 22624669 |
|
(b) Shimizu, R.; Egami, H.; Nagi, T.; Chae, J.; Hamashima, Y.; Sodeoka, M. Tetrahedron Lett. 2010, 51, 5947.
pmid: 22624669 |
|
|
(c) Liu, T.; Shen, Q. Org. Lett. 2011, 13, 2342.
doi: 10.1021/ol2005903 pmid: 22624669 |
|
|
(d) Ye, Y.; Sanford, M. S. J. Am. Chem. Soc. 2012, 134, 9034.
pmid: 22624669 |
|
| [16] |
(a) Sawada, H.; Nakayama, M.; Yoshida, T. J. Fluorine Chem. 1990, 46, 423.
|
|
(b) Langlois, B. R.; Laurent, E.; Roidot, N. Tetrahedron Lett. 1991, 32, 7525.
|
|
|
(c) Kino, T.; Nagase, Y.; Ohtsuka, Y.; Yamamoto, K.; Uraguchi, D.; Tokuhisa, K.; Yamakawa, T. J. Fluorine Chem. 2010, 131, 98.
|
|
| [17] |
Wang, X.; Truesdale, L.; Yu, J.-Q. J. Am. Chem. Soc. 2010, 132, 3648.
pmid: 20184319 |
| [18] |
He, L.; Natte, K.; Rabeah, J.; Taeschler, C.; Neumann, H.; Bruckner, A.; Beller, M. Angew. Chem., Int. Ed. 2015, 54, 4320.
|
| [19] |
Mohle, S.; Zirbes, M.; Rodrigo, E.; Gieshoff, T.; Wiebe, A.; Waldvogel, S. R. Angew. Chem., Int. Ed. 2018, 57, 6018.
|
| [20] |
Frontana-Uribe, B. A.; Little, R. D.; Ibanez, J. G.; Palma, A.; Vasquez-Medrano, R. Green Chem. 2010, 12, 2099.
|
| [21] |
Moeller, K. D. Tetrahedron 2000, 56, 9527.
|
| [22] |
Sperry, J. B.; Wright, D. L. Chem. Soc. Rev. 2006, 35, 605.
pmid: 16791332 |
| [23] |
(a) Yoshida, J.-I.; Kataoka, K.; Horcajada, R.; Nagaki, A. Chem. Rev. 2008, 108, 2265.
pmid: 28991454 |
|
(b) Yan, M.; Kawamata, Y.; Baran, P. S. Chem. Rev. 2017, 117, 13230.
pmid: 28991454 |
|
| [24] |
Herzog, G. Chromatographia 2016, 79, 521.
|
| [25] |
Zhang, Y.; Petersen, J. L.; Milsmann, C. J. Am. Chem. Soc. 2016, 138, 13115.
pmid: 27643820 |
| [26] |
Yeung, K. T.; To, W. P.; Sun, C.; Cheng, G.; Ma, C.; Tong, G. S. M.; Yang, C.; Che, C. M. Angew. Chem., Int. Ed. 2017, 56, 133.
|
| [27] |
Gazi, S.; Ng, W. K. H.; Ganguly, R.; Moeljadi, A. M. P.; Hirao, H.; Soo, H. S. Chem. Sci. 2015, 6, 7130.
pmid: 29861949 |
| [28] |
Uneyama, K. Tetrahedron 1991, 47, 555.
|
| [29] |
Arai, K.; Watts, K.; Wirth, T. ChemistryOpen 2013, 3, 23.
pmid: 24688891 |
| [30] |
Jud, W.; Kappe, C. O.; Cantillo, D. Chem.-Eur. J. 2018, 24, 17234.
pmid: 30285302 |
| [31] |
Gregory, S. S.; Lin, S. ACS Catal. 2018, 8, 5175.
|
| [32] |
Zhang, L. L.; Zhang, G. T.; Wang, P.; Li, Y. L.; Lei, A. W. Org. Lett. 2018, 20, 7396.
pmid: 30461286 |
| [33] |
Guan, Z. P.; Wang, H. M.; Huang, Y. G.; Wang, Y. K.; Wang, S. C.; Lei, A. W. Org. Lett. 2019, 21, 4619.
pmid: 31145632 |
| [34] |
Sun, X.; Ma, H. X.; Mei, T. S.; Fang, P.; Hu, Y. L. Org. Lett. 2019, 21, 3167.
pmid: 30995058 |
| [35] |
Zou, Z. L.; Zhang, W. G.; Wang, Y.; Kong, L. Y.; Karotsis, G.; Wang, Y. Org. Lett. 2019, 21, 1857.
pmid: 30817165 |
| [36] |
(a) Zhang, Y. C.; Han, X. L.; Zhao, J. Q.; Qian, Z. J.; Li, T. M.; Tang, Y. Q.; Zhang, H. Y. Adv. Synth. Catal. 2018, 360, 2659.
pmid: 27304228 |
|
(b) Wu, Z.; Wang, D. P.; Liu, Y.; Huan, L. T.; Zhu, C. J. Am. Chem. Soc. 2017, 139, 1388.
pmid: 27304228 |
|
|
(c) Ye, K. Y.; Pombar, G.; Fu, N. K.; Sauer, G. S.; Keresztes, I.; Lin, S. J. Am. Chem. Soc. 2018, 140, 2438.
doi: 10.1021/jacs.7b13387 pmid: 27304228 |
|
|
(d) Sauer, G. S.; Lin, S. ACS Catal. 2018, 8, 5175.
pmid: 27304228 |
|
|
(e) Yang, Y. D.; Lwamoto, K.; Tokunaga, E.; Shibata, N. Chem. Commun. 2013, 49, 5510.
pmid: 27304228 |
|
|
(f) Sakamoto, R.; Kashiwagi, H.; Selvakumar, S.; Moteki, S.; Maruoka, K. Org. Biomol. Chem. 2016, 14, 6417.
pmid: 27304228 |
|
| [37] |
Wang, H.; Xu, Q.; Yu, S. Y. Org. Chem. Front. 2018, 5, 2224.
|
| [38] |
Jung, H. I.; Kim, Y.; Kim, Y. D. Org. Biomol. Chem. 2019, 17, 25.
|
| [39] |
(a) Wu, Q. Y.; Ao, G. Z. Org. Chem. Front. 2018, 5, 2061.
pmid: 30730146 |
|
(b) Ye, K. Y.; Pombar, N. F.; Sauer, G. S.; Keresztes, I.; Lin, S. J. Am. Chem. Soc. 2018, 140, 2438.
pmid: 30730146 |
|
|
(c) Jiang, Y. Y.; Dou, G. Y.; Xu, K.; Zeng, C. C. Org. Chem. Front. 2018, 5, 2573.
pmid: 30730146 |
|
|
(d) Ye, K. Y.; Song, Z.; Sauer, S.; Harenberg, H.; Fu, N.; Lin, S. Chem.-Eur. J. 2018, 24, 12274.
pmid: 30730146 |
|
|
(e) Jud, W.; Kappe, C. O.; Cantillo, D. Chem.-Eur. J. 2018, 24, 17234.
pmid: 30730146 |
|
|
(f) Zhang, L.; Zhang, G.; Wang, Y.; Lei, A. Org. Lett. 2018, 20, 7396.
doi: 10.1021/acs.orglett.8b03081 pmid: 30730146 |
|
|
(g) Yingchao, J. W.; Guillot, D. R.; Kouklovsky, C.; Vencent, G. J. Am. Chem. Soc. 2019, 141, 2831.
pmid: 30730146 |
|
|
(h) Zhang, Z.; Zhang, Y.; Cao, F. L.; Bai, G.; Yang, Y.; Mo, F. Org. Lett. 2019, 21, 761.
pmid: 30730146 |
|
|
(i) Ruan, Z.; Huang, Z.; Xu, Z.; Tian, M. X.; Yu, X. Y.; Ackermann, L. Org. Lett. 2019, 21, 1237.
pmid: 30730146 |
|
| [40] |
Li, Z.; Jiao, L. C.; Sun, Y. H.; He, Z. Y.; Wei, Z. L.; Liao, W. W. Angew. Chem. 2020, 132, 7333.
|
| [41] |
(a) Majumdar, K. C.; Mondal, S. Chem. Rev. 2011, 111, 7749.
doi: 10.1021/cr1003776 pmid: 30229794 |
|
(b) Iwanrjko, J.; Wojaczynska, E. Org. Biomol. Chem. 2018, 16, 7296.
pmid: 30229794 |
|
| [42] |
Dhanak, D.; Duffy, K. J.; Johnston, V. K.; Goerke, J. L.; Darcy, M.; Shaw, A. N.; Gu, B.; Silverman, C.; Gates, A. T.; Nonnemacher, M. R.; Earnshaw, D. L.; Casper, D. J.; Kaura, A.; Baker, A.; Greenwood, C.; Gutshall, L. L.; Maley, D.; Delvecchio, A.; Ricardo, M.; Hofmann, G. A.; Alnoah, Z.; Cheng, H. Y.; Chan, G.; Khandekar, S.; Keenan, R. M.; Sarisky, R. T. J. Biol. Chem. 2002, 277, 38322.
pmid: 12167642 |
| [43] |
(a) Zheng, J.; Zhang, D. Y.; Cui, S. Adv. Synth. Catal. 2016, 358, 746.
doi: 10.1002/adsc.201500965 |
|
(b) Chen, D.; Ji, M.; Zhu, C. Chem. Commun. 2019, 55, 7796.
|
|
| [44] |
Kang, J. C.; Tu, Y. Q.; Dong, J. W.; Chen, C.; Zhou, J.; Ding, T. M.; Zai, J. T.; Chen, Z. M.; Zhang, S. Y. Org. Lett. 2019, 21, 2536.
pmid: 30945551 |
| [45] |
Zhang, Z. X.; Zhang, L.; Cao, Y.; Li, F.; Bai, G. C.; Liu, G. Q.; Yang, Y.; Mo, F. Y. Org. Let. 2019, 21, 762.
|
| [46] |
Xiong, P.; Xu, H. H.; Song, J. S.; Xu, H. C. J. Am. Chem. Soc. 2018, 140, 2460.
pmid: 29406700 |
| [47] |
(a) Studer, A. Angew. Chem., Int. Ed. 2012, 51, 8950.
doi: 10.1002/anie.201202624 pmid: 26178870 |
|
(b) Ni, C. F.; Hu, M. Y.; Hu, J. B. Chem. Rev. 2015, 115, 765.
pmid: 26178870 |
|
|
(c) Alonso, C.; Marigorta, E. M.; Rubiales, G.; Palacios, F. Chem. Rev. 2015, 115, 1847.
pmid: 26178870 |
|
|
(d) Belhomme, M. C.; Besset, T.; Poisson, T.; Pannecoucke, X. Chem.-Eur. J. 2015, 21, 12836.
pmid: 26178870 |
|
|
(e) Rong, J.; Ni, C. F.; Hu, J. B. J. Org. Chem. 2017, 6, 139.
pmid: 26178870 |
|
| [48] |
Taniguchi, T.; Idota, A.; Ishibashi, H. Org. Biomol. Chem. 2011, 9, 3151.
pmid: 21437319 |
| [49] |
Zhang, S.; Li, L. J.; Zhang, J. J.; Xue, M. Y.; Xu, K. Chem. Sci. 2019, 10, 3181.
pmid: 30996899 |
| [50] |
Li, F. Y.; lin, D. Z.; He, T. J.; Zhong, W. Q.; Huang, J. M. ChemCatChem 2019, 119, 2350.
|
| [51] |
Zhao, Y.; Lai, Y. L.; Du, K. S.; Lin, D. Z.; Huang, J. M. J. The J. Org. Chem. 2017, 82, 9655.
|
| [52] |
(a) Huang, J. M.; Lin, Z. Q.; Chen, D. S. Org. Lett. 2011, 141, 22.
pmid: 30783088 |
|
(b) Gong, M.; Huang, J. M. Chem.-Eur. J. 2016, 22, 14293.
pmid: 30783088 |
|
|
(c) Huang, H. B.; Huang, J. M. Adv. Synth. Catal. 2016, 358, 1975.
doi: 10.1002/adsc.v358.12 pmid: 30783088 |
|
|
(d) Lai, Y. L.; Huang, J. M. Org. Lett. 2017, 19, 2022.
pmid: 30783088 |
|
|
(e) Du, K. S.; Huang, J. M. Org. Lett. 2018, 20, 2911.
pmid: 30783088 |
|
|
(f) Lin, D. Z.; Huang, J. M. Org. Lett. 2018, 20, 2112.
pmid: 30783088 |
|
|
(g) Lai, Y. L.; Ye, J. S.; Huang, J. M. Chem.-Eur. J. 2016, 22, 5425.
pmid: 30783088 |
|
|
(h) He, T. J.; Ye, Z.; Ke, Z.; Huang, J. M. Nat. Commun. 2019, 10, 833.
pmid: 30783088 |
|
| [53] |
Brien, A. G. O.; Inokuma, M. Y.; Fujita, M.; Baran, P. S.; Blackmond, D. G. Angew. Chem. 2014, 53, 11868.
|
| [54] |
Qian, P.; Bi, M.; Su, J.; Zha, Z.; Wang, Z. J. Org. Chem. 2016, 81, 4876.
pmid: 27175916 |
| [55] |
Dudkina, Y. B.; Khrizanforov, M. N.; Gryazonova, T. V.; Budnikova, Y. H. J. Organomet. Chem. 2014, 751, 301.
doi: 10.1016/j.jorganchem.2013.10.012 |
| [56] |
Dubinina, G. G.; Brennessel, W. W.; Miller, J. L.; Vicic, D. A. Organometallics 2008, 27, 3933.
doi: 10.1021/om800300k |
| [57] |
Hossain, M. J.; Ono, T.; Wakiya, K.; Hisaeda, Y. J. Chem. Commun. 2017, 53, 10878.
|
| [58] |
Cui, L. X.; Ono, T.; Morita, Y.; Hisaede, Y. Dalton Trans. 2020, 22, 7546.
|
| [59] |
Jud, W.; Maljuric, S.; Kappe, C. O.; Cantillo, D. Org. Lett. 2019, 21, 7970.
pmid: 31513422 |
| [60] |
Rodrigo, S.; Um, C.; Mixdorf, J. C.; Gunasekera, D.; Nguyen, H. M.; Luo, L. Org. Lett. 2020, 22, 6719.
doi: 10.1021/acs.orglett.0c01906 pmid: 32658484 |
| [61] |
Brien, A. G. O.; Inokuma, M.Y. Fujita, M.; Baran, P. S.; Blackmond, D. G. Angew. Chem. 2014, 53, 11868.
|
| [62] |
Beryl, J. R.; Raj, X. J. Orient. J. Chem. 2018, 34, 2098.
|
| [63] |
Dou, G. Y.; Jiang, Y. Y.; Xu, K.; Zeng, C. C. Org. Chem. Front. 2019, 6, 2392.
|
| [64] |
Jiang, Y. Y.; Dou, G. Y.; Xu, K.; Zeng, C. C. Org. Chem. Front. 2018, 5, 2573.
|
| [1] | 李思达, 崔鑫, 舒兴中, 吴立朋. 钛催化的烯烃制备1,1-二硼化合物[J]. 有机化学, 2024, 44(2): 631-637. |
| [2] | 徐利军, 李宗军, 韩福社, 高翔. N,N-二甲基甲酰胺促进的富勒烯稠合噁唑啉衍生物的合成[J]. 有机化学, 2024, 44(1): 242-250. |
| [3] | 张建涛, 张聪, 莫诺琳, 罗佳婷, 陈莲芬, 刘卫兵. 氯仿参与的烯烃自由基加成反应的研究进展[J]. 有机化学, 2023, 43(9): 3098-3106. |
| [4] | 岁丹丹, 岑南楠, 龚若蕖, 陈阳, 陈文博. 无支持电解质条件下连续流电化学合成三氟甲基化氧化吲哚[J]. 有机化学, 2023, 43(9): 3239-3245. |
| [5] | 钟赟哲, 陈颖, 俞磊, 周宏伟. 电化学介导羧酸与醇的酯化反应[J]. 有机化学, 2023, 43(8): 2855-2863. |
| [6] | 刘露, 张曙光, 胡仁威, 赵晓晓, 崔京南, 贡卫涛. 基于多羟基柱[5]芳烃的酚醛多孔聚合物合成及CO2催化转化[J]. 有机化学, 2023, 43(8): 2808-2814. |
| [7] | 卢凯, 屈浩琦, 陈樨, 秋慧, 郑晶, 马猛涛. 无催化剂、无溶剂条件下炔烃和烯烃与儿茶酚硼烷的硼氢化反应[J]. 有机化学, 2023, 43(6): 2197-2205. |
| [8] | 刘铃, 浩涛涛, 伍晚花, 杨成. 利用超分子策略构筑具有聚集诱导发光(AIE)功能的二苯乙烯型分子开关[J]. 有机化学, 2023, 43(6): 2189-2196. |
| [9] | 陆晓雨, 孙晓梅, 钮亚琴, 王俊超, 殷文婧, 高梦婷, 刘孜, 韦正桓, 陶庭骅. 铜催化氟代丙烯酸与氧杂吖丙啶的脱羧交叉偶联反应[J]. 有机化学, 2023, 43(6): 2110-2119. |
| [10] | 张周, 郭钰, 羊静, 吴丹, 王佳昕, 洪欣玥, 蔡佩君, 荣良策. 电化学促进咪唑并[1,2-a]吡啶与二氯(溴)乙烷及碘仿的卤化反应[J]. 有机化学, 2023, 43(6): 2104-2109. |
| [11] | 李思达, 舒兴中, 吴立朋. 锆、钛介导的烯烃、炔烃硼氢化[J]. 有机化学, 2023, 43(5): 1751-1760. |
| [12] | 张祎, 杜呈卓, 李继坤, 王小野. 基于硼氮杂稠环芳烃的多重共振热活化延迟荧光材料研究进展[J]. 有机化学, 2023, 43(5): 1645-1690. |
| [13] | 张俊颖, 赵晓静, 李干鹏, 何永辉. 室温下电化学合成保护型有机硼酸RB(dan)[J]. 有机化学, 2023, 43(5): 1815-1823. |
| [14] | 杜琳琳, 张华. 芳烃与烷烃化合物参与的光化学与电化学硼化反应[J]. 有机化学, 2023, 43(5): 1726-1741. |
| [15] | 徐晓阳, 刘美艳, 李成龙, 刘旭光. 1,2-硼氮杂芳烃在中国的研究进展[J]. 有机化学, 2023, 43(5): 1611-1644. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||