化学学报 ›› 2019, Vol. 77 ›› Issue (9): 803-813.DOI: 10.6023/A19060201 上一篇 下一篇
所属专题: 有机自由基化学
综述
投稿日期:2019-06-08
发布日期:2019-08-13
通讯作者:
陆良秋,肖文精
E-mail:luliangqiu@mail.ccnu.edu.cn;wxiao@mail.ccnu.edu.cn
作者简介:路福东, 1995年出生于山东安丘, 2017年在华中农业大学获得学士学位, 目前在肖文精教授和陆良秋教授指导下攻读硕士学位. 研究兴趣是可见光催化的不对称反应.|姜烜, 1994年出生于浙江江山, 2016年在武汉理工大学获得学士学位, 目前在肖文精教授和陆良秋教授指导下攻读硕士学位. 研究兴趣是可见光催化的脱氨基偶联反应.|陆良秋教授1982年出生于浙江绍兴, 2005年和2011年在华中师范大学化学学院先后获得学士和博士学位(导师: 肖文精教授), 随后留校工作. 2011年至2013年以洪堡学者身份赴德国莱布尼茨催化所Matthias Beller教授课题组进行博士后研究. 2015年6月, 破格晋升为教授. 其研究兴趣主要是过渡金属催化的偶极环化反应与可见光促进的有机光化学合成研究.|肖文精教授1965年出生于湖北公安, 1984年和1990年在华中师范大学化学系先后获得学士和硕士学位. 1997年至2000年在加拿大渥太华大学化学系学习并获得博士学位(导师: Howard Alper教授). 2001年至2002年在美国加州理工学院化学与化学工程系David W. C. MacMillan教授课题组从事博士后研究. 2003年加入华中师范大学化学学院. 其研究兴趣主要是发展新的方法学合成具有潜在生物活性的碳杂环化合物.
基金资助:
Lu, Fu-Donga, Jiang, Xuana, Lu, Liang-Qiua*( ), Xiao, Wen-Jingab*(
), Xiao, Wen-Jingab*( )
)
Received:2019-06-08
Published:2019-08-13
Contact:
Lu, Liang-Qiu,Xiao, Wen-Jing
E-mail:luliangqiu@mail.ccnu.edu.cn;wxiao@mail.ccnu.edu.cn
Supported by:文章分享
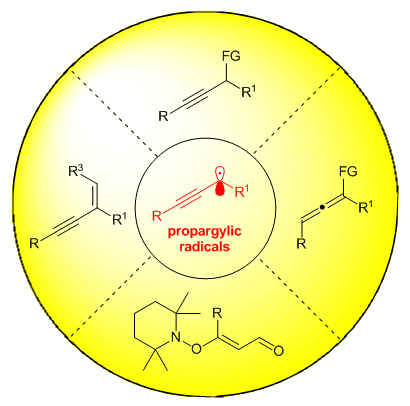
炔烃的合成与转化一直是有机合成化学的一个重要研究内容. 其中, 炔丙位官能化是实现炔烃合成与转化的一个重要途径. 相对于经历阳离子中间体途径的炔丙位官能化反应, 自由基途径的炔丙位官能化反应在最近十年才得以发展, 且与前者也已形成互补之势. 该类炔丙基自由基既能够通过炔丙位的碳杂键断裂生成, 又可通过自由基对1,3-烯炔的加成生成. 同时, 由于炔丙基自由基存在自由基与炔烃的共轭结构, 使得该自由基既能够直接对金属物种加成参与炔丙位的官能化反应, 又能够异构成联烯自由基后对金属物种加成, 继而参与联烯化合物的合成. 此外, 炔丙基自由基还可以被进一步氧化成炔丙基阳离子后参与后续的有机转化. 本综述根据炔丙基自由基所参与的反应类型, 对近年来炔丙位自由基参与的有机反应进行了简要总结.
路福东, 姜烜, 陆良秋, 肖文精. 炔丙基自由基在有机合成化学中的应用[J]. 化学学报, 2019, 77(9): 803-813.
Lu, Fu-Dong, Jiang, Xuan, Lu, Liang-Qiu, Xiao, Wen-Jing. Application of Propargylic Radicals in Organic Synthesis[J]. Acta Chimica Sinica, 2019, 77(9): 803-813.
| [1] |
(a) Trost, B. M.; Li, C.-J. Modern Alkyne Chemistry: Catalytic and Atom-Economic Transformations, Wiley-VCH, New York, 2014.
doi: 10.1021/cr400357r |
|
(b) Trotuş, I. T.; Zimmermann, T.; Schüth, F . Chem. Rev. 2014, 114, 1761.
doi: 10.1021/cr400357r |
|
|
(c) Tiwari, V. K.; Mishra, B. B.; Mishra, K. B.; Mishra, N.; Singh, A. S.; Chen, X. Chem. Rev. 2016, 116, 3086.
doi: 10.1021/cr400357r |
|
|
(d) Huang, D.; Liu, Y.; Qin, A.-J.; Tang, B.-Z. Polym. Chem. 2018, 9, 2853.
doi: 10.1021/cr400357r |
|
| [2] |
Ding, C.-H.; Hou, X.-L . Chem. Rev. 2011, 111, 1914.
doi: 10.1021/cr100284m |
| [3] |
(a) Nicholas, K. M.; Pettit, R. Tetrahedron Lett. 1971, 37, 3475.
doi: 10.1016/0040-4039(96)00594-1 |
|
(b) Nicholas, K. M.; Pettit, R. J. Organomet. Chem. 1972, 44, 21.
doi: 10.1016/0040-4039(96)00594-1 |
|
| [4] |
Melikyan, G. G . Acc. Chem. Res. 2015, 48, 1065.
doi: 10.1021/ar500365v |
| [5] | Geri, R.; Oilizzi, C.; Lardicci, L.; Caporusso, A. M. Gazz. Chim. Ital. 1994, 124, 241. |
| [6] |
(a) Miyake, Y.; Uemura, S.; Nishibayashi, Y. ChemCatChem 2009, 1, 342.
doi: 10.1002/cctc.v1:3 |
|
(b) Zhang, D.-Y.; Hu, X.-P. Tetrahedron Lett. 2015, 56, 283.
doi: 10.1002/cctc.v1:3 |
|
|
(c) Xiao, Y.-L.; Pan, Q.; Zhang, X.-G. Acta Chim. Sinica 2015, 73, 383 (in Chinese).
doi: 10.1002/cctc.v1:3 |
|
|
(肖玉兰, 潘强, 张新刚, 化学学报, 2015, 73, 383).
doi: 10.1002/cctc.v1:3 |
|
| [7] | Bruneau, C.; Dixneuf, P. H . Metal Vinylidenes and Allenylidenes in Catalysis, Wiley-VCH, Weinheim, 2008. |
| [8] |
(a) Kropf, H.; SchrÖder, R.; FÖlsing, R. Synthesis 1977,894.
doi: 10.1016/j.apcata.2007.02.045 |
|
(b) Alvarez, L. X.; Christ, M. L.; Sorokin, A. B. Appl. Catal. A: Gen. 2007, 325, 303.
doi: 10.1016/j.apcata.2007.02.045 |
|
| [9] |
Smith, S. W.; Fu, G. C. J. Am. Chem. Soc. 2008, 130, 12645.
doi: 10.1021/ja805165y |
| [10] |
Oelke, A. J.; Sun, J.-W.; Fu, G. C. J. Am. Chem. Soc. 2012, 134, 2966.
doi: 10.1021/ja300031w |
| [11] |
Pelphrey, P. M.; Popov, V. M.; Joska, T. M.; Beierlein, J. M.; Bolstad, E. S. D.; Fillingham, Y. A.; Wright, D. L.; Anderson, A. C. J. Med. Chem. 2007, 50, 940.
doi: 10.1021/jm061027h |
| [12] |
Schley, N. D.; Fu, G. C. J. Am. Chem. Soc. 2014, 136, 16588.
doi: 10.1021/ja508718m |
| [13] | Domingo-Legarda, P.; Soler-Yanes, R.; Quirós-López, M. T.; Buñuel, E.; Cárdenas, D. J. Eur. J. Org. Chem. 2018, 35, 4900. |
| [14] |
An, L.; Tong, F.-F.; Zhang, X.-G . Acta Chim. Sinica 2018, 76, 977 (in Chinese).
doi: 10.6023/A18080314 |
|
( 安伦, 童非非, 张新刚, 化学学报, 2018, 76, 977).
doi: 10.6023/A18080314 |
|
| [15] |
Lu, F.-D.; Liu, D.; Zhu, L.; Lu, L.-Q.; Yang, Q.; Zhou, Q.-Q.; Wei, Y.; Lan, Y.; Xiao, W.-J. J. Am. Chem. Soc. 2019, 141, 6167.
doi: 10.1021/jacs.9b02338 |
| [16] |
Cheng, J.-K.; Loh, T.-P. J. Am. Chem. Soc. 2015, 137, 42.
doi: 10.1021/ja510635k |
| [17] |
Andia, A. A.; Miner, M. R.; Woerpel, K. A. Org. Lett. 2015, 17, 2704.
doi: 10.1021/acs.orglett.5b01120 |
| [18] | Miner, M. R.; Woerpel, K. A . Eur. J. Org. Chem. 2016,1860. |
| [19] |
Cheng, J.-K.; Shen, L.; Wu, L.-H.; Hu, X.-H.; Loh, T.-P . Chem. Commun. 2017, 53, 12830.
doi: 10.1039/C7CC08074C |
| [20] |
(a) Chen, Z.-Y.; Zhou, D.-S.; Zhou, J.-Y.;Wu, S.-H. Acta Chim. Sinica 1997, 55, 1138 (in Chinese).
doi: 10.1021/cr020024j |
|
( 陈招银, 周大顺, 周景尧, 吴世晖 , 化学学报, 1997, 55, 1138).
doi: 10.1021/cr020024j |
|
|
(b) Ma, S.-M. Chem. Rev. 2005, 105, 2829.
doi: 10.1021/cr020024j |
|
|
(c) Lo, V. K.; Wong, M.; Che, C. Org. Lett. 2008, 10, 517.
doi: 10.1021/cr020024j |
|
|
(d) Yang, L.-J.; Ma, J.-A. Acta Chim. Sinica 2016, 74, 130 (in Chinese)
doi: 10.1021/cr020024j |
|
|
(杨丽军, 马军安, 化学学报, 2016, 74, 130)
doi: 10.1021/cr020024j |
|
|
(e) Huang, X.; Ma, S.-M. Acc. Chem. Res. 2019, 52, 1301.
doi: 10.1021/cr020024j |
|
| [21] |
(a) Wartenberg, F.-H.; Junga, H.; Blechert, S . Tetrahedron Lett. 1993, 34, 5251.
doi: 10.1016/j.tetlet.2005.11.154 |
|
(b) Alameda-Angulo, C.; Quiclet-Sire, B.; Zard, S. Z. Tetrahedron Lett. 2006, 47, 913.
doi: 10.1016/j.tetlet.2005.11.154 |
|
| [22] |
Soler-Yanes, R.; Arribas-Álvarez, I.; Guisán-Ceinos, M.; Buñuel, E.; Cárdenas, D. J. Chem. Eur. J. 2017, 23, 1584.
doi: 10.1002/chem.v23.7 |
| [23] |
Wang, F.; Wang, D.-H.; Zhou, Y.; Liang, L.; Lu, R.-H.; Chen, P.-H.; Lin, Z.-Y.; Liu, G.-S. Angew. Chem., Int. Ed. 2018, 57, 7140.
doi: 10.1002/anie.v57.24 |
| [24] |
Zhu, X.; Deng, W.; Chiou, M.-F.; Ye, C.; Jian, W.; Zeng, Y.; Jiao, Y.; Ge, L.; Li, Y.; Zhang, X.; Bao, H. J. Am. Chem. Soc. 2019, 141, 548.
doi: 10.1021/jacs.8b11499 |
| [25] |
Ye, C.-Q.; Li, Y.-J.; Zhu, X.-T.; Hu, S.-M.; Yuan, D.-Q.; Bao, H.-L . Chem. Sci. 2019, 10, 3632.
doi: 10.1039/C8SC05689G |
| [26] |
Zhang, K.-F.; Bian, K.-J.; Li, C.; Sheng, J.; Li, Y.; Wang, X.-S. Angew. Chem. Int. Ed. 2019, 58, 5069.
doi: 10.1002/anie.201813184 |
| [27] |
Ye, C.-Q.; Qian, B.; Li, Y.-J.; Su, M.; Li, D.-L.; Bao, H.-L . Org. Lett. 2018, 20, 3202.
doi: 10.1021/acs.orglett.8b01043 |
| [28] |
Kang, Y.-W.; Choi, Y.-J.; Jang, H.-Y . Org. Lett. 2014, 16, 4842.
doi: 10.1021/ol502341f |
| [29] |
Horn, E. J.; Rosen, B. R.; Chen, Y.; Tang, J.; Chen, K.; Eastgate, M. D.; Baran, P. S . Nature 2016, 533, 77.
doi: 10.1038/nature17431 |
| [1] | 黄涎廷, 韩洪亮, 肖婧, 王帆, 柳忠全. I2O5/KSCN介导的炔烃碘硫氰化反应[J]. 化学学报, 2024, 82(1): 5-8. |
| [2] | 黄家翩, 刘飞, 吴劼. 二氟环丙烯参与的有机反应研究进展★[J]. 化学学报, 2023, 81(5): 520-532. |
| [3] | 韩明亮, 徐丽华. 过渡金属催化的硫酯的交叉偶联反应研究进展[J]. 化学学报, 2023, 81(4): 381-392. |
| [4] | 刘霞, 匡春香, 苏长会. 过渡金属催化的1,2,3-三氮唑导向的C—H键官能团化反应研究进展[J]. 化学学报, 2022, 80(8): 1135-1151. |
| [5] | 徐云芳, 李阳, 付梓桐, 林绍艳, 祝洁, 吴磊. 钯催化选择性构筑(Z)-[3]戟烯反应研究[J]. 化学学报, 2022, 80(10): 1369-1375. |
| [6] | 白云平, 崔春明. 硅卡宾铁(0)氮气配合物催化的炔烃选择性硼氢化反应[J]. 化学学报, 2020, 78(8): 763-766. |
| [7] | 张洪浩, 俞寿云. 过渡金属与光氧化还原协同催化的烯丙基取代反应的研究进展[J]. 化学学报, 2019, 77(9): 832-840. |
| [8] | 杨启亮, 王向阳, 翁信军, 杨祥, 徐学涛, 童晓峰, 方萍, 伍新燕, 梅天胜. 电氧化促进的钯催化的芳烃C(sp 2)—H键氯代反应[J]. 化学学报, 2019, 77(9): 866-873. |
| [9] | 王强, 顾庆, 游书力. 过渡金属催化不对称C—H键官能团化反应构建轴手性联芳基化合物研究进展[J]. 化学学报, 2019, 77(8): 690-704. |
| [10] | 鲁鸿, 刘金宇, 李红玉, 许鹏飞. 氮杂环卡宾与过渡金属共催化反应研究进展[J]. 化学学报, 2018, 76(11): 831-837. |
| [11] | 张毛毛, 骆元元, 陆良秋, 肖文精. 过渡金属与有机小分子协同催化的不对称烯丙基取代反应研究进展[J]. 化学学报, 2018, 76(11): 838-849. |
| [12] | 周锵, 陆平. 手性路易斯碱和过渡金属协同催化反应的进展[J]. 化学学报, 2018, 76(11): 825-830. |
| [13] | 孙国峰, 苏敏, 方洁, Borzov Maxim, 聂万丽. 有机胺盐/硼烷体系与炔烃的硼氢化加成反应机理研究[J]. 化学学报, 2017, 75(8): 824-830. |
| [14] | 李娅琼, 黄志真. 过渡金属催化和有机小分子参与的α,β-不饱和酮与烯丙醇的Morita-Baylis-Hillman反应[J]. 化学学报, 2017, 75(3): 280-283. |
| [15] | 温志国, 田冲, Borzov Maxim V., 聂万丽. 有机胺盐酸盐/B(C6F5)3催化的酸与炔烃选择性加成反应研究[J]. 化学学报, 2016, 74(6): 498-502. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||