有机化学 ›› 2024, Vol. 44 ›› Issue (11): 3335-3344.DOI: 10.6023/cjoc202403024 上一篇 下一篇
综述与进展
方霄龙a,*( ), 张钰a, 王韬a, 李斌b, 段宁a, 张峰君a
), 张钰a, 王韬a, 李斌b, 段宁a, 张峰君a
收稿日期:2024-03-19
修回日期:2024-05-07
发布日期:2024-05-30
基金资助:
Xiaolong Fanga,*( ), Yu Zhanga, Tao Wanga, Bin Lib, Ning Duana, Fengjun Zhanga
), Yu Zhanga, Tao Wanga, Bin Lib, Ning Duana, Fengjun Zhanga
Received:2024-03-19
Revised:2024-05-07
Published:2024-05-30
Contact:
*E-mail:Supported by:文章分享
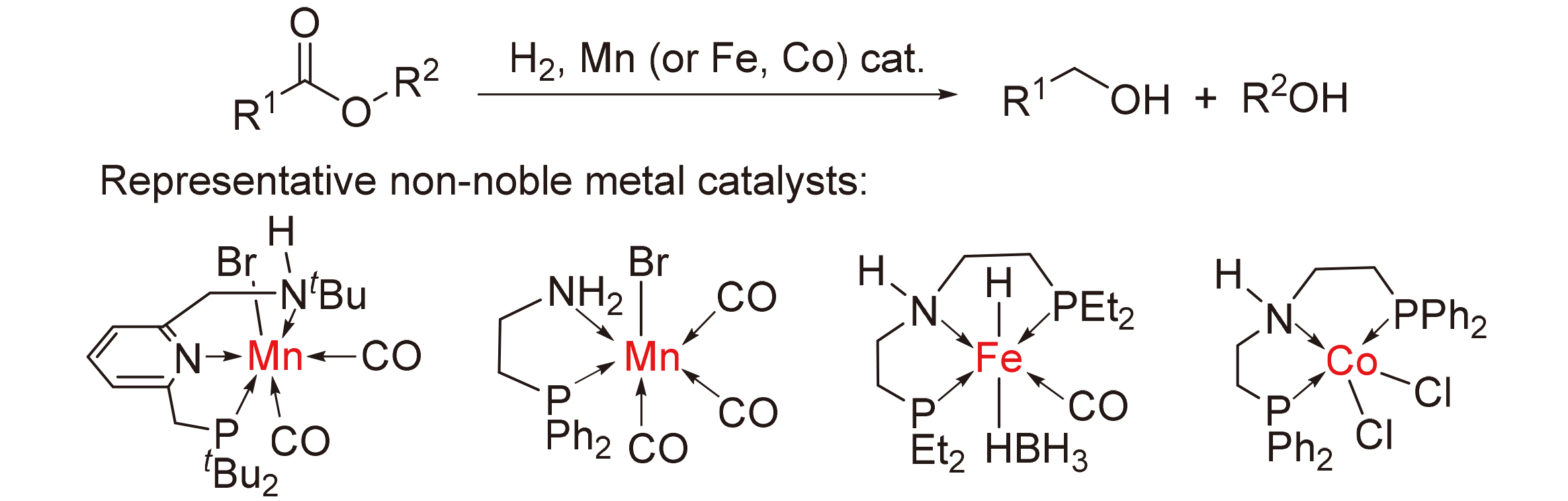
酯类分子的催化加氢还原是一种绿色、可持续和原子经济的制备醇类化合物的方法. 近20年来, Ru(II)、Ir(III)、Os(II)等贵金属配合物应用于均相催化酯加氢制醇的研究取得了显著的进展, 将贵金属替代为储量丰富且环境友好的廉价金属已经成为当下的研究热点. 总结了近年来Fe(II)、Co(II)、Mn(I)等廉价金属配合物应用于均相催化酯加氢制醇的研究进展, 围绕配合物结构与性能的关联以及催化加氢反应机理, 探讨了影响配合物性能的关键因素, 为进一步设计开发性能优异的廉价金属配合物催化剂提供参考.
方霄龙, 张钰, 王韬, 李斌, 段宁, 张峰君. 廉价金属配合物应用于均相催化酯加氢制醇的研究进展[J]. 有机化学, 2024, 44(11): 3335-3344.
Xiaolong Fang, Yu Zhang, Tao Wang, Bin Li, Ning Duan, Fengjun Zhang. Advances in Homogeneous Hydrogenation of Esters to Alcohols by Non-noble Metal Complexes[J]. Chinese Journal of Organic Chemistry, 2024, 44(11): 3335-3344.
| Entry | Cat. | Cat./mol% | Temp./℃ | p(H2)/MPa | Time/h | Conv./% | Yield/% | Ref. |
|---|---|---|---|---|---|---|---|---|
| 1 | 6 | 1 | 60 | 5.0 | 6 | 52 | 49 | [ |
| 2 | 7 | 1 | 60 | 3.0 | 6 | 99 | 99 | [ |
| 3 | 8 | 2 | 110 | 3.0 | 24 | >99 | 97 | [ |
| 4 | 9 | 2 | 110 | 2.0 | 23 | >99 | 97 | [ |
| 5 | 10 | 2 | 120 | 5.5 | 20 | 45 | 26 | [ |
| 6 | 11 | 5 | 120 | 5.0 | 6 | >99 | 99 | [ |
| 7 | 12 | 5 | 140 | 5.0 | 48 | 65 | 46 | [ |
| 8 | 13 | 5 | 140 | 5.0 | 48 | 67 | 45 | [ |
| 9 | 15 | 0.2 | 100 | 5.0 | 48 | — | 61 | [ |
| 10 | 16 | 1 | 60 | 5.0 | 16 | — | 97 | [ |
| 11 | 18 | 4 | 130 | 5.0 | 48 | — | 65 | [ |
| 12 | 19 | 1 | 100 | 2.0 | 50 | 99 | 98 | [ |
| 13 | 21 | 0.001 | 100 | 10.1 | 96 | — | 45 | [ |
| 14 | Co(BF4)2•6H2O+ MeC(CH2PPh2)3 | 10 | 100 | 8.0 | 5 | 98 | 95 | [ |
| 15 | 24 | 0.2 | 100 | 5.0 | 16 | 95 | 87 | [ |
| 16 | 24 | 1 | 100 | 5.0 | 20 | 99 | 98 | [ |
| 17 | 25 | 1 | 100 | 5.0 | 20 | 43 | 24 | [ |
| 18 | 26 | 1 | 100 | 5.0 | 20 | 13 | 3 | [ |
| 19 | 30 | 1 | 100 | 5.0 | 24 | 96 | 96 | [ |
| Entry | Cat. | Cat./mol% | Temp./℃ | p(H2)/MPa | Time/h | Conv./% | Yield/% | Ref. |
|---|---|---|---|---|---|---|---|---|
| 1 | 6 | 1 | 60 | 5.0 | 6 | 52 | 49 | [ |
| 2 | 7 | 1 | 60 | 3.0 | 6 | 99 | 99 | [ |
| 3 | 8 | 2 | 110 | 3.0 | 24 | >99 | 97 | [ |
| 4 | 9 | 2 | 110 | 2.0 | 23 | >99 | 97 | [ |
| 5 | 10 | 2 | 120 | 5.5 | 20 | 45 | 26 | [ |
| 6 | 11 | 5 | 120 | 5.0 | 6 | >99 | 99 | [ |
| 7 | 12 | 5 | 140 | 5.0 | 48 | 65 | 46 | [ |
| 8 | 13 | 5 | 140 | 5.0 | 48 | 67 | 45 | [ |
| 9 | 15 | 0.2 | 100 | 5.0 | 48 | — | 61 | [ |
| 10 | 16 | 1 | 60 | 5.0 | 16 | — | 97 | [ |
| 11 | 18 | 4 | 130 | 5.0 | 48 | — | 65 | [ |
| 12 | 19 | 1 | 100 | 2.0 | 50 | 99 | 98 | [ |
| 13 | 21 | 0.001 | 100 | 10.1 | 96 | — | 45 | [ |
| 14 | Co(BF4)2•6H2O+ MeC(CH2PPh2)3 | 10 | 100 | 8.0 | 5 | 98 | 95 | [ |
| 15 | 24 | 0.2 | 100 | 5.0 | 16 | 95 | 87 | [ |
| 16 | 24 | 1 | 100 | 5.0 | 20 | 99 | 98 | [ |
| 17 | 25 | 1 | 100 | 5.0 | 20 | 43 | 24 | [ |
| 18 | 26 | 1 | 100 | 5.0 | 20 | 13 | 3 | [ |
| 19 | 30 | 1 | 100 | 5.0 | 24 | 96 | 96 | [ |
| [1] |
(a) Dub P. A.; Ikariya T. ACS Catal. 2012, 2, 1718.
|
|
(b) Clarke M. L. Catal. Sci. Technol. 2012, 2, 2418.
|
|
|
(c) Li W.; Xie J.-H.; Yuan M. L.; Zhou Q. L. Green. Chem. 2014, 16, 4081.
|
|
|
(d) Gu X.; Li X.; Xie J.; Zhou Q. Acta Chim. Sinica 2019, 77, 598 (in Chinese).
|
|
|
(顾雪松, 李校根, 谢建华, 周其林, 化学学报, 2019, 77, 598.)
doi: 10.6023/A19050166 |
|
| [2] |
Ohkuma T.; Ooka H.; Ikariya T.; Noyori R. J. Am. Chem. Soc. 1995, 117, 10417.
|
| [3] |
(a) Noyori R.; Ohkuma T. Angew. Chem., Int. Ed. 2001, 40, 40.
|
|
(b) Noyori R. Angew. Chem., Int. Ed. 2002, 41, 2008.
|
|
|
(c) Sandoval C. A.; Ohkuma T.; Muñiz K.; Noyori R. J. Am. Chem. Soc. 2003, 125, 13490.
|
|
|
(d) Zhao B.; Han Z.; Ding K. Angew. Chem., Int. Ed. 2013, 52, 4744.
|
|
|
(e) Werkmeister S.; Junge K.; Beller M. Org. Process Res. Dev. 2014, 18, 289.
|
|
| [4] |
Zhang J.; Leitus G.; Ben-David Y.; Milstein D. Angew. Chem., Int. Ed. 2006, 45, 1113.
|
| [5] |
Saudan L. A.; Saudan C. M.; Debieux C.; Wyss P. Angew. Chem., Int. Ed. 2007, 46, 7473.
|
| [6] |
Kuriyama W.; Matsumoto T.; Ogata O.; Ino Y.; Aoki K.; Tanaka S.; Ishida K.; Kobayashi T.; Sayo N.; Saito T. Org. Process Res. Dev. 2012, 16, 166.
|
| [7] |
(a) Sun Y.; Koehler C.; Tan R.; Annibale V. T.; Song D. Chem. Commun. 2011, 47, 8349.
pmid: 25741992 |
|
(b) Spasyuk D.; Gusev D. G. Organometallics 2012, 31, 5239.
pmid: 25741992 |
|
|
(c) Spasyuk D.; Smith S.; Gusev D. G. Angew. Chem., Int. Ed. 2012, 51, 2772.
pmid: 25741992 |
|
|
(d) Yue H.; Zhao Y.; Ma X.; Gong J. Chem. Soc. Rev. 2012, 41, 4218.
pmid: 25741992 |
|
|
(e) Chen T.; Li H.; Qu S.; Zheng B.; He L.; Lai Z.; Wang Z. X.; Huang K. W. Organometallics 2014, 33, 4152.
pmid: 25741992 |
|
|
(f) Spasyuk D.; Vicent C.; Gusev D. G. J. Am. Chem. Soc. 2015, 137, 3743.
doi: 10.1021/ja512389y pmid: 25741992 |
|
|
(g) Tan X.; Wang Y.; Liu Y.; Wang F.; Shi L.; Lee K.-H.; Lin Z.; Lv H.; Zhang X. Org. Lett. 2015, 17, 454.
pmid: 25741992 |
|
|
(h) Wang F.; Tan X.; Lv H.; Zhang X. Chem.-Asian J. 2016, 11, 2103.
pmid: 25741992 |
|
| [8] |
(a) Clarke Z. E.; Maragh P. T.; Dasgupta T. P.; Gusev D. G.; Lough A. J.; Abdur-Rashid K. Organometallics 2006, 25, 4113.
|
|
(b) Bertoli M.; Choualeb A.; Lough A. J.; Moore B.; Spasyuk D.; Gusev D. G. Organometallics 2011, 30, 3479.
|
|
|
(c) Acosta-Ramirez A.; Bertoli M.; Gusev D. G.; Schlaf M. Green Chem. 2012, 14, 1178.
|
|
|
(d) Otsuka T.; Ishii A.; Dub P. A.; Ikariya T. J. Am. Chem. Soc. 2013, 135, 9600.
|
|
|
(e) Junge K.; Wendt B.; Jiao H.; Beller M. ChemCatChem 2014, 6, 2810.
|
|
|
(f) Ogata O.; Nakayama Y.; Nara H.; Fujiwhara M.; Kayaki Y. Org. Lett. 2016, 18, 3894.
|
|
| [9] |
Werkmeister S.; Junge K.; Wendt B.; Alberico E.; Jiao H.; Baumann W.; Junge H.; Gallou F.; Beller M. Angew. Chem., Int. Ed. 2014, 53, 8722.
|
| [10] |
(a) Chakraborty S.; Dai H.; Bhattacharya P.; Fairweather N. T.; Gibson M. S.; Krause J. A.; Guan H. J. Am. Chem. Soc. 2014, 136, 7869.
doi: 10.1021/ja504034q pmid: 24846811 |
|
(b) Qu S.; Dai H.; Dang Y.; Song C.; Wang Z. X.; Guan H. ACS Catal. 2014, 4, 4377.
pmid: 24846811 |
|
| [11] |
Elangovan S.; Wendt B.; Topf C.; Bachmann S.; Scalone M.; Spannenberg A.; Jiao H.; Baumann W.; Junge K.; Beller M. Adv. Synth. Catal. 2016, 358, 820.
|
| [12] |
Elangovan S.; Garbe M.; Jiao H.; Spannenberg A.; Junge K.; Beller M. Angew. Chem., Int. Ed. 2016, 55, 15364.
|
| [13] |
Yuwen J.; Chakraborty S.; Brennessel W. W.; Jones W. D. ACS Catal. 2017, 7, 3735.
|
| [14] |
John J. M.; Takebayashi S.; Dabral N.; Miskolzie M.; Bergens S. H. J. Am. Chem. Soc. 2013, 135, 8578.
|
| [15] |
Junge K.; Wendt B.; Cingolani A.; Spannenberg A.; Wei Z.; Jiao H.; Beller M. Chem.-Eur. J. 2018, 24, 1046.
|
| [16] |
(a) Zhang G.; Hanson S. K. Org. Lett. 2013, 15, 650.
|
|
(b) Rösler S.; Ertl M.; Irrgang T.; Kempe R. Angew. Chem., Int. Ed. 2015, 54, 15046.
|
|
|
(c) Zhang G.; Yin Z.; Zheng S. Org. Lett. 2016, 18, 300.
|
|
|
(d) Mastalir M.; Tomsu G.; Pittenauer E.; Allmaier G.; Kirchner K. Org. Lett. 2016, 18, 3462.
|
|
| [17] |
Zhong R.; Wei Z.; Zhang W.; Liu S.; Liu Q. Chem 2019, 5, 1552.
doi: 10.1016/j.chempr.2019.03.010 |
| [18] |
Yang W.; Chernyshov I. Y.; van Schendel R. K.; Weber M.; Müller C.; Filonenko G. A.; Pidko E. A. Nat. Commun. 2021, 12, 12.
|
| [19] |
Yang W.; Kalavalapalli T. Y.; Krieger A. M.; Khvorost T. A.; Chernyshov I. Y.; Weber M.; Uslamin E. A.; Pidko E. A.; Filonenko G. A. J. Am. Chem. Soc. 2022, 144, 8129.
|
| [20] |
Wei Z.; Li H.; Wang Y.; Liu Q. Angew. Chem., Int. Ed. 2023, 62, e202301042.
|
| [21] |
(a) Gunanathan C.; Ben-David Y.; Milstein D. Science 2007, 317, 790.
|
|
(b) Gnanaprakasam B.; Zhang J.; Milstein D. Angew. Chem., Int. Ed. 2010, 49, 1468.
|
|
|
(c) Gunanathan C.; Gnanaprakasam B.; Iron M. A.; Shimon L. J.; Milstein D. J. Am. Chem. Soc. 2010, 132, 14763.
|
|
|
(d) Balaraman E.; Gunanathan C.; Zhang J.; Shimon L. J.; Milstein D. Nat. Chem. 2011, 3, 609.
|
|
| [22] |
Zell T.; Ben‐David Y.; Milstein D. Angew. Chem., Int. Ed. 2014, 53, 4685.
|
| [23] |
Srimani D.; Mukherjee A.; Goldberg A. F.; Leitus G.; Diskin‐ Posner Y.; Shimon L. J.; Ben David Y.; Milstein D. Angew. Chem., Int. Ed. 2015, 54, 12357.
|
| [24] |
Espinosa‐Jalapa N. A.; Nerush A.; Shimon L. J.; Leitus G.; Avram L.; Ben‐David Y.; Milstein D. Chem.-Eur. J. 2017, 23, 5934.
doi: 10.1002/chem.201604991 pmid: 27796060 |
| [25] |
(a) Widegren M. B.; Harkness G. J.; Slawin A. M.; Cordes D. B.; Clarke M. L. Angew. Chem., Int. Ed. 2017, 56, 5825.
pmid: 29671599 |
|
(b) Widegren M. B.; Clarke M. L. Org. Lett. 2018, 20, 2654.
doi: 10.1021/acs.orglett.8b00864 pmid: 29671599 |
|
| [26] |
Li X. G.; Li F.; Xu Y.; Xiao L. J.; Xie J. H.; Zhou Q. L. Adv. Synth. Catal. 2022, 364, 744.
|
| [27] |
Zubar V.; Lichtenberger N.; Schelwies M.; Oeser T.; Hashmi A. S. K.; Schaub T. ChemCatChem 2022, 14, e202101443.
|
| [28] |
Teunissen H. T.; Elsevier C. J. Chem. Commun. 1997, 667.
|
| [29] |
(a) Hanton M. J.; Tin S.; Boardman B. J.; Miller P. J. Mol. Catal. A: Chem. 2011, 346, 70.
pmid: 21786816 |
|
(b) Geilen F. M.; Engendahl B.; Hölscher M.; Klankermayer J.; Leitner W. J. Am. Chem. Soc. 2011, 133, 14349.
doi: 10.1021/ja2034377 pmid: 21786816 |
|
|
(c) Wesselbaum S.; Vom Stein T.; Klankermayer J.; Leitner W. Angew. Chem., Int. Ed. 2012, 51, 7499.
pmid: 21786816 |
|
|
(d) Vom Stein T.; Meuresch M.; Limper D.; Schmitz M.; Hölscher M.; Coetzee J.; Cole-Hamilton D. J.; Klankermayer J. R.; Leitner W. J. Am. Chem. Soc. 2014, 136, 13217.
pmid: 21786816 |
|
| [30] |
Korstanje T. J.; van der Vlugt J. I.; Elsevier C. J.; de Bruin B. Science 2015, 350, 298.
|
| [31] |
(a) Takebayashi S.; Bergens S. H. Organometallics 2009, 28, 2349.
|
|
(b) Kuriyama W.; Ino Y.; Ogata O.; Sayo N.; Saito T. Adv. Synth. Catal. 2010, 352, 92.
|
|
|
(c) Stempfle F.; Quinzler D.; Heckler I.; Mecking S. Macromolecules 2011, 44, 4159.
|
|
|
(d) Furst M. R.; Le Goff R.; Quinzler D.; Mecking S.; Botting C. H.; Cole-Hamilton D. J. Green Chem. 2012, 14, 472.
|
|
|
(e) Fang X.; Zhang C.; Chen J.; Zhu H.; Yuan Y. RSC Adv. 2016, 6, 45512.
|
|
|
(f) Fang X.; Li B.; Zheng J.; Wang X.; Zhu H.; Yuan Y. Dalton Trans. 2019, 48, 2290.
|
|
|
(g) Fang X. L.; Li B.; Jin J.; Duan N. Chin. J. Org. Chem. 2022, 42, 1407 (in Chinese).
|
|
|
(方霄龙, 李斌, 金杰, 段宁, 有机化学, 2022, 42, 1407.)
doi: 10.6023/cjoc202202034 |
|
| [32] |
Van Putten R.; Uslamin E. A.; Garbe M.; Liu C.; Gonzalez‐de‐Castro A.; Lutz M.; Junge K.; Hensen E. J.; Beller M.; Lefort L.; Pidko E. A. Angew. Chem., Int. Ed. 2017, 56, 7531.
|
| [33] |
(a) Hamilton R. J.; Bergens S. H. J. Am. Chem. Soc. 2006, 128, 13700.
pmid: 17044693 |
|
(b) Fang X.; Duan N.; Zhang M.; Zhang C.; Liu R.; Zhu H. Chin. J. Org. Chem. 2019, 39, 1450 (in Chinese).
pmid: 17044693 |
|
|
(方霄龙, 段宁, 章敏, 张春燕, 刘睿, 朱红平, 有机化学, 2019, 39, 1450.)
doi: 10.6023/cjoc201812014 pmid: 17044693 |
|
| [34] |
(a) Langer R.; Iron M. A.; Konstantinovski L.; Diskin‐Posner Y.; Leitus G.; Ben‐David Y.; Milstein D. Chem.-Eur. J. 2012, 18, 7196.
pmid: 26837422 |
|
(b) Hoyt J. M.; Shevlin M.; Margulieux G. W.; Krska S. W.; Tudge M. T.; Chirik P. J. Organometallics 2014, 33, 5781.
pmid: 26837422 |
|
|
(c) Lagaditis P. O.; Sues P. E.; Sonnenberg J. F.; Wan K. Y.; Lough A. J.; Morris R. H. J. Am. Chem. Soc. 2014, 136, 1367.
pmid: 26837422 |
|
|
(d) Thai T. T.; Mérel D. S.; Poater A.; Gaillard S.; Renaud J. L. Chem.-Eur. J. 2015, 21, 7066.
pmid: 26837422 |
|
|
(e) Gajewski P.; Renom‐Carrasco M.; Facchini S. V.; Pignataro L.; Lefort L.; de Vries J. G.; Ferraccioli R.; Piarulli U.; Gennari C. Eur. J. Org. Chem. 2015, 2015, 5526.
pmid: 26837422 |
|
|
(f) Rosas-Hernández A.; Alsabeh P. G.; Barsch E.; Junge H.; Ludwig R.; Beller M. Chem. Commun. 2016, 52, 8393.
pmid: 26837422 |
|
|
(g) Hodgkinson R.; Del Grosso A.; Clarkson G.; Wills M. Dalton Trans. 2016, 45, 3992.
doi: 10.1039/c5dt04610f pmid: 26837422 |
|
| [35] |
Gajewski P.; Gonzalez‐de‐Castro A.; Renom‐Carrasco M.; Piarulli U.; Gennari C.; de Vries J. G.; Lefort L.; Pignataro L. ChemCatChem 2016, 8, 3431.
|
| [36] |
Azouzi K.; Pedussaut L.; Pointis R.; Bonfiglio A.; Kumari Riddhi R.; Duhayon C.; Bastin S.; Sortais J. B. Organometallics 2023, 42, 1832.
|
| [1] | 李平, 张寅, 杨子琪, 郝文娟, 姜波. 利用碱促进环外1,3-二羰化合物的解构反应合成腙化的1,n-二羰化合物及其生物活性检测[J]. 有机化学, 2024, 44(9): 2777-2784. |
| [2] | 荀苗苗, 郭晶晶, 马文兵, 李宇强, 袁长春, 傅凯. BF3•Et2O促进的环丙烯基甲醇衍生物重排反应研究[J]. 有机化学, 2024, 44(9): 2760-2776. |
| [3] | 叶丹锋, 徐冰, 万云辉. 叔丁醇锂催化N-苄基-N-叔丁氧羰基酰胺与糖的酯化反应[J]. 有机化学, 2024, 44(9): 2924-2932. |
| [4] | 王华斌, 徐连华, 刘雄伟, 潘博文, 姚震, 黄强, 周英. N-溴代丁二酰亚胺促进的P(O)-H化合物参与的醇的直接磷酸化反应[J]. 有机化学, 2024, 44(9): 2847-2853. |
| [5] | 丁柔, 石思雨, 马超, 魏伟, 吕玉芬. 非金属1,8-二氮杂双环[5.4.0]十一碳-7-烯介导下乙缩醛酸与异硫氰酸酯反应合成α-缩醛基酰胺[J]. 有机化学, 2024, 44(7): 2216-2222. |
| [6] | 林雨, 付海峰, 曹华, 刘想. 碳酸亚乙烯酯: 有机合成化学中的多功能合成子[J]. 有机化学, 2024, 44(7): 2147-2173. |
| [7] | 胡懿鸣, 许嘉宇, 汤敏, 刘雅雯, 关丽萍, 金晴昊. 2-(1,3-二氧代异吲哚啉-2-基)-N-苯乙酰胺和2-(3,4-二氢异喹啉-1-基)异吲哚-1,3-二酮类单胺氧化酶(MAO)和胆碱酯酶(ChE)抑制剂的设计、合成和生物活性研究[J]. 有机化学, 2024, 44(6): 1907-1919. |
| [8] | 李文多, 魏娜娜, 冯楠. 硼自由基促进的C—C键形成反应构筑联芳基和苄基羧酸甲酯[J]. 有机化学, 2024, 44(6): 1853-1861. |
| [9] | 张倩, 应垚璐, 张泓银, 徐林博, 林新奎, 黄晓雷. 钯催化SO2插入的炔丙基乙酸酯和碘代芳烃的还原偶联反应[J]. 有机化学, 2024, 44(6): 2033-2040. |
| [10] | 王斌, 韩万仓, 代林林, 张永红, 夏昱, 金伟伟, 刘晨江. 吡唑啉酮与磺酰氯的直接磺酰化合成吡唑磺酸酯[J]. 有机化学, 2024, 44(6): 1998-2005. |
| [11] | 吉崇磊, 高得伟. 不对称催化合成手性1,2-双硼酸酯研究进展[J]. 有机化学, 2024, 44(5): 1385-1402. |
| [12] | 于兆锦, 张展, 王海洋, 王波, 付光明, 张瑛, 杨晓朋, 董爱君, 姬小明. 乙基麦芽酚丁二酸双酯的合成、热解及抗氧化研究[J]. 有机化学, 2024, 44(5): 1526-1534. |
| [13] | 万云辉, 杨福美, 陈明瀚, 孙德立, 叶丹锋. 无过渡金属催化的N-苄基-N-叔丁氧羰基酰胺与不饱和醇的酯化反应[J]. 有机化学, 2024, 44(4): 1293-1300. |
| [14] | 孙雪, 颜廷涛, 闫克鲁, 杨建静, 文江伟. 电化学促使α-重氮酯的磷酸化构筑亚膦酸腙[J]. 有机化学, 2024, 44(3): 1013-1020. |
| [15] | 李梦帆, 程旭. 烯丙基芳香化合物的电化学选择性氧化酯化[J]. 有机化学, 2024, 44(3): 1005-1012. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||