有机化学 ›› 2021, Vol. 41 ›› Issue (9): 3585-3592.DOI: 10.6023/cjoc202105010 上一篇 下一篇
研究论文
收稿日期:2021-05-07
修回日期:2021-06-07
发布日期:2021-07-12
通讯作者:
马仁超, 马永敏
基金资助:
Qinjiao Fu, Ruiqin Zhang, Huanyi Qiu, Renchao Ma( ), Yongmin Ma(
), Yongmin Ma( )
)
Received:2021-05-07
Revised:2021-06-07
Published:2021-07-12
Contact:
Renchao Ma, Yongmin Ma
Supported by:文章分享
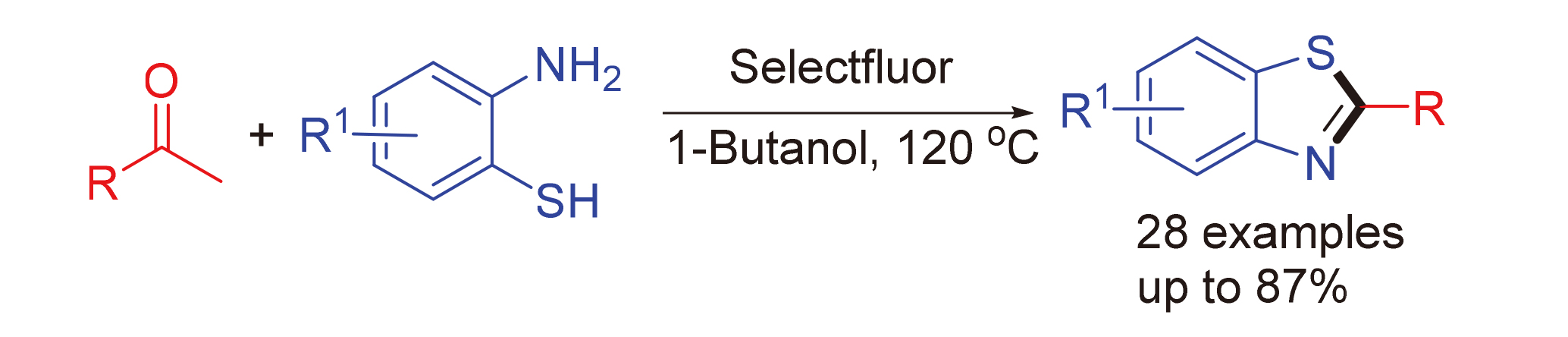
开发了一种以芳基甲基酮或脂肪酮和2-氨基苯硫酚为原料, 正丁醇为溶剂, 120 ℃条件下经Selectfluor氧化合成2-取代苯并噻唑类衍生物的方法. 通过改变底物芳基甲基酮上的取代基可以获得具有生物活性的药物中间体.
傅琴姣, 张瑞芹, 裘浣沂, 马仁超, 马永敏. Selectfluor氧化合成2-芳基苯并噻唑的新方法[J]. 有机化学, 2021, 41(9): 3585-3592.
Qinjiao Fu, Ruiqin Zhang, Huanyi Qiu, Renchao Ma, Yongmin Ma. A New Method for the Synthesis of 2-Arylbenzothiazoles Oxidized by Selectfluor[J]. Chinese Journal of Organic Chemistry, 2021, 41(9): 3585-3592.
| Entry | Solvent | Selectfluor/equiv. | T/℃ | Time/h | Yield/% |
|---|---|---|---|---|---|
| 1 | DMF | 2 | 120 | 12 | 0 |
| 2 | DMA | 2 | 120 | 12 | 0 |
| 3 | DMSO | 2 | 120 | 12 | Trace |
| 4 | THF | 2 | Reflux | 12 | 0 |
| 5 | 1,4-Dioxane | 2 | Reflux | 12 | Trace |
| 6 | PhCH3 | 2 | Reflux | 12 | Trace |
| 7 | PhCl | 2 | 120 | 12 | Trace |
| 8 | MeOH | 2 | Reflux | 12 | 17 |
| 9 | EtOH | 2 | Reflux | 12 | 20 |
| 10 | 1-Butanol | 2 | 120 | 12 | 75 |
| 11 | 1-Octanol | 2 | 120 | 12 | 70 |
| 12b | 1-Butanol | 2 | 120 | 12 | 73 |
| 13 | 1-Butanol | 1 | 120 | 12 | 66 |
| 14 | 1-Butanol | 0.5 | 120 | 12 | 42 |
| 15 | 1-Butanol | 0 | 120 | 24 | 0 |
| 16 | 1-Butanol | 2 | 120 | 6 | 50 |
| 17 | 1-Butanol | 2 | 120 | 2 | 10 |
| 18 | 1-Butanol | 2 | r.t. | 24 | 0 |
| 19 | 1-Butanol | 2 | 80 | 24 | 25 |
| Entry | Solvent | Selectfluor/equiv. | T/℃ | Time/h | Yield/% |
|---|---|---|---|---|---|
| 1 | DMF | 2 | 120 | 12 | 0 |
| 2 | DMA | 2 | 120 | 12 | 0 |
| 3 | DMSO | 2 | 120 | 12 | Trace |
| 4 | THF | 2 | Reflux | 12 | 0 |
| 5 | 1,4-Dioxane | 2 | Reflux | 12 | Trace |
| 6 | PhCH3 | 2 | Reflux | 12 | Trace |
| 7 | PhCl | 2 | 120 | 12 | Trace |
| 8 | MeOH | 2 | Reflux | 12 | 17 |
| 9 | EtOH | 2 | Reflux | 12 | 20 |
| 10 | 1-Butanol | 2 | 120 | 12 | 75 |
| 11 | 1-Octanol | 2 | 120 | 12 | 70 |
| 12b | 1-Butanol | 2 | 120 | 12 | 73 |
| 13 | 1-Butanol | 1 | 120 | 12 | 66 |
| 14 | 1-Butanol | 0.5 | 120 | 12 | 42 |
| 15 | 1-Butanol | 0 | 120 | 24 | 0 |
| 16 | 1-Butanol | 2 | 120 | 6 | 50 |
| 17 | 1-Butanol | 2 | 120 | 2 | 10 |
| 18 | 1-Butanol | 2 | r.t. | 24 | 0 |
| 19 | 1-Butanol | 2 | 80 | 24 | 25 |
| Entry | Product | Ar | R1 | Yield/% |
|---|---|---|---|---|
| 1 | 3aa | C6H5 | H | 75 (72b) |
| 2 | 3ba | 2-MeOC6H4 | H | 75 |
| 3 | 3ca | 2-ClC6H4 | H | 73 |
| 4 | 3da | 3-MeOC6H4 | H | 68 |
| 5 | 3ea | 3-ClC6H4 | H | 60 |
| 6 | 3fa | 4-ClC6H4 | H | 62 |
| 7 | 3ga | 4-CH3C6H4 | H | 78 |
| 8 | 3ha | 4-NH2C6H4 | H | 73 |
| 9 | 3ia | 3,5-(CH3O)2C6H3 | H | 73 |
| 10 | 3ja | 3,4-(CH3)2C6H3 | H | 76 |
| 11 | 3ka | 3,5-F2C6H3 | H | 70 |
| 12 | 3la | 2,4-(CH3)2C6H3 | H | 65 |
| 13 | 3ma | 3-MeO-4-HO-C6H3 | H | 56 |
| 14 | 3na | 4-O2NC6H4 | H | 0 |
| 15 | 3oa | 2-Thienyl | H | 58 |
| 16 | 3pa | 2-Benzothienyl | H | 55 |
| 17 | 3qa | 2-Benzofuryl | H | 40 |
| 18 | 3ra | 2-Naphthyl | H | 60 |
| 19 | 3sa | 4-CF3C6H4 | H | 74 |
| 20 | 3ab | C6H5 | 5-Cl | 79 |
| 21 | 3eb | 4-FC6H4 | 5-Cl | 75 |
| 22 | 3fb | 4-MeOC6H4 | 5-Cl | 66 |
| 23 | 3kb | 3,5-F2C6H3 | 5-Cl | 78 |
| 24 | 3lb | 2,4-(CH3)2C6H3 | 5-Cl | 70 |
| 25 | 3mb | 3-MeO-4-HO-C6H3 | 5-Cl | 67 |
| Entry | Product | Ar | R1 | Yield/% |
|---|---|---|---|---|
| 1 | 3aa | C6H5 | H | 75 (72b) |
| 2 | 3ba | 2-MeOC6H4 | H | 75 |
| 3 | 3ca | 2-ClC6H4 | H | 73 |
| 4 | 3da | 3-MeOC6H4 | H | 68 |
| 5 | 3ea | 3-ClC6H4 | H | 60 |
| 6 | 3fa | 4-ClC6H4 | H | 62 |
| 7 | 3ga | 4-CH3C6H4 | H | 78 |
| 8 | 3ha | 4-NH2C6H4 | H | 73 |
| 9 | 3ia | 3,5-(CH3O)2C6H3 | H | 73 |
| 10 | 3ja | 3,4-(CH3)2C6H3 | H | 76 |
| 11 | 3ka | 3,5-F2C6H3 | H | 70 |
| 12 | 3la | 2,4-(CH3)2C6H3 | H | 65 |
| 13 | 3ma | 3-MeO-4-HO-C6H3 | H | 56 |
| 14 | 3na | 4-O2NC6H4 | H | 0 |
| 15 | 3oa | 2-Thienyl | H | 58 |
| 16 | 3pa | 2-Benzothienyl | H | 55 |
| 17 | 3qa | 2-Benzofuryl | H | 40 |
| 18 | 3ra | 2-Naphthyl | H | 60 |
| 19 | 3sa | 4-CF3C6H4 | H | 74 |
| 20 | 3ab | C6H5 | 5-Cl | 79 |
| 21 | 3eb | 4-FC6H4 | 5-Cl | 75 |
| 22 | 3fb | 4-MeOC6H4 | 5-Cl | 66 |
| 23 | 3kb | 3,5-F2C6H3 | 5-Cl | 78 |
| 24 | 3lb | 2,4-(CH3)2C6H3 | 5-Cl | 70 |
| 25 | 3mb | 3-MeO-4-HO-C6H3 | 5-Cl | 67 |
| [1] |
(a) Zablotskaya, A.; Segal, I.; Geronikaki, A.; Eremkina, T.; Belyakov, S.; Petrova, M.; Shestakova, I.; Zvejniece, L.; Nikolajeva, V. Eur. J. Med. Chem. 2013, 70, 846.
doi: 10.1016/j.ejmech.2013.10.008 pmid: 24262377 |
|
(b) Cai, J.; Sun, M.; Wu, X.; Chen, J.; Wang, P.; Zong, X.; Ji, M. Eur. J. Med. Chem. 2013, 63, 702.
doi: 10.1016/j.ejmech.2013.03.013 pmid: 24262377 |
|
|
(c) Huang, S.-T.; Hsei, I. J.; Chen, C. Bioorg. Med. Chem. 2006, 14, 6106.
doi: 10.1016/j.bmc.2006.05.007 pmid: 24262377 |
|
| [2] |
(a) Diao, P.-C.; Lin, W.-Y.; Jian, X.-E.; Li, Y.-H.; You, W.-W.; Zhao, P.-L. Eur. J. Med. Chem. 2019, 179, 196.
doi: 10.1016/j.ejmech.2019.06.055 |
|
(b) Racane, L.; Pticek, L.; Fajdetic, G.; Tralic-Kulenovic, V.; Klobucar, M.; Pavelic, S. K.; Peric, M.; Paljetak, H. C.; Verbanac, D.; Starcevic, K. Bioorg. Chem. 2019, 95, 103537.
doi: 10.1016/j.bioorg.2019.103537 |
|
|
(c) Li, E.; Meng, Y.; Zhang, L.; Zhang, Y.; Zhou, R.; Liu, L.; Li, N.; Xin, J.; Zheng, J.; Shan, L.; Liu, H.; Zhang, Q. Chin. J. Org. Chem. 2020, 40, 417. (in Chinese).
doi: 10.6023/cjoc201907016 |
|
|
( 李二冬, 孟娅琪, 张路野, 张洋, 周蕊, 刘丽敏, 栗娜, 辛景超, 郑甲信, 单丽红, 刘宏民, 张秋荣, 有机化学, 2020, 40, 417.)
|
|
| [3] |
(a) Keri, R. S.; Patil, M. R.; Patil, S. A.; Budagumpi, S. Eur. J. Med. Chem. 2015, 89, 207.
doi: 10.1016/j.ejmech.2014.10.059 |
|
(b) Sumit, K. A.; Kumar, A.; Mishra, A. K. Mini-Rev. Med. Chem. 2020, 21, 314.
doi: 10.2174/1389557520666200820133252 |
|
| [4] |
(a) Huang, X.; Meggers, E. Acc. Chem. Res. 2019, 52, 833.
doi: 10.1021/acs.accounts.9b00028 |
|
(b) Lu, H.-Y.; Barve, I. J.; Selvaraju, M.; Sun, C.-M. ACS Comb. Sci. 2020, 22, 42.
doi: 10.1021/acscombsci.9b00161 |
|
|
(c) Huo, X.; Li, W.; Zhang, B.; Chen, X.; Zhou, Y.; Zhang, J.; Han, X.; Dai, B. Chin. J. Org. Chem. 2018, 38, 3356. (in Chinese).
doi: 10.6023/cjoc201805053 |
|
|
( 霍新玉, 李文斌, 张博雅, 陈晓飞, 周月婷, 张洁, 韩小强, 代斌, 有机化学, 2018, 38, 3356.)
|
|
|
(d) Jiang, K.; Cao, L.; Hao, Z.; Chen, M.; Cheng, J.; Li, X.; Xiao, P.; Chen, L.; Wang, Z. Chin. J. Org. Chem. 2017, 37, 2221. (in Chinese).
doi: 10.6023/cjoc201703041 |
|
|
( 蒋凯, 曹梁, 郝志峰, 陈美燕, 程洁銮, 李晓, 肖萍, 陈亮, 汪朝阳, 有机化学, 2017, 37, 2221.)
|
|
|
(e) Gabr, M. T.; El-Gohary, N. S.; El-Bendary, E. R.; El-Kerdawy, M. M.; Ni, N. Chin. Chem. Lett. 2016, 27, 380.
doi: 10.1016/j.cclet.2015.12.033 |
|
| [5] |
(a) Guria, U. N.; Gangopadhyay, A.; Ali, S. S.; Maiti, K.; Samanta, S. K.; Manna, S.; Ghosh, A. K.; Uddin, M. R.; Mandal, S.; Mahapatra, A. K. Anal. Methods 2019, 11, 5447.
doi: 10.1039/C9AY01622H |
|
(b) Maliyappa, M. R.; Keshavayya, J.; Mahanthappa, M.; Shivaraj, Y.; Basavarajappa, K. V. J. Mol. Struct. 2020, 1199, 126959.
doi: 10.1016/j.molstruc.2019.126959 |
|
| [6] |
(a) Zhang, F.; Xu, J.; Guo, X.; Yuan, B.; Huang, H.; Li, L. Appl. Surf. Sci. 2020, 501, 144054.
doi: 10.1016/j.apsusc.2019.144054 |
|
(b) Devi, A. S.; Aswathy, V. V.; Mary, Y. S.; Panicker, C. Y.; Armakovic, S.; Armakovic, S. J.; Ravindran, R.; Van Alsenoy, C. J. Mol. Struct. 2017, 1148, 282.
doi: 10.1016/j.molstruc.2017.07.065 |
|
|
(c) Dzulkharnien, N. S. F.; Salleh, N. M.; Yahya, R.; Karim, M. R. Soft Mater. 2017, 15, 292.
doi: 10.1080/1539445X.2017.1355816 |
|
| [7] |
Wang, Y.; Zhou, R.; Liu, W.; Liu, C.; Wu, P. Chin. Chem. Lett. 2020, 31, 2950.
doi: 10.1016/j.cclet.2020.01.023 |
| [8] |
(a) Zhang, J.; Liu, Y.; Zhang, Y.; Hu, L.; Han, S. Chin. J. Org. Chem. 2021, 41, 1053. (in Chinese).
doi: 10.6023/cjoc202007036 |
|
( 张俊, 刘雅菲, 张育榕, 呼亮, 韩世清, 有机化学, 2021, 41, 1053.)
|
|
|
(b) Dai, X.; Zhu, Y.; Wang, Z.; Weng, J. Chin. J. Org. Chem. 2017, 37, 1924. (in Chinese).
doi: 10.6023/cjoc201703034 |
|
|
( 戴小强, 朱亚波, 汪洲洋, 翁建全, 有机化学, 2017, 37, 1924.)
|
|
|
(c) Zhu, N.; Zhang, Z.; Gao, M.; Han, L.; Suo, Q.; Hong, H. Chin. J. Org. Chem. 2013, 33, 1423. (in Chinese).
doi: 10.6023/cjoc201212014 |
|
|
( 竺宁, 张志伟, 高敏, 韩利民, 索全伶, 洪海龙, 有机化学, 2013, 33, 1423.)
|
|
|
(d) Yang, W.; Li, B.; Zhang, M.; Wang, S.; Ji, Y.; Dong, S. Chin. Chem. Lett. 2020, 31, 1313.
doi: 10.1016/j.cclet.2019.10.022 |
|
|
(e) Wan, J.-P.; Zhou, Y.; Liu, Y.; Sheng, S. Green Chem. 2016, 18, 402.
doi: 10.1039/C5GC01821H |
|
|
(f) Singh, M.; Vaishali, Paul, A. K.; Singh, V. Org. Biomol. Chem. 2020, 18, 4459.
doi: 10.1039/D0OB00888E |
|
| [9] |
(a) Ferlin, F.; van der Hulst, M. K.; Santoro, S.; Lanari, D.; Vaccaro, L. Green Chem. 2019, 21, 5298.
doi: 10.1039/C9GC01641D |
|
(b) Fan, L.-Y.; Shang, Y.-H.; Li, X.-X.; Hua, W.-J. Chin. Chem. Lett. 2015, 26, 77.
doi: 10.1016/j.cclet.2014.10.017 |
|
|
(c) Samanta, S.; Das, S.; Biswas, P. J. Org. Chem. 2013, 78, 11184.
doi: 10.1021/jo401445j |
|
|
(d) Mali, J. K.; Mali, D. A.; Telvekar, V. N. Tetrahedron. Lett. 2016, 57, 2324.
doi: 10.1016/j.tetlet.2016.04.058 |
|
|
(e) Nagao, I.; Ishizaka, T.; Kawanami, H. Green Chem. 2016, 18, 3494.
doi: 10.1039/C6GC01195K |
|
|
(f) Sun, Y.; Jiang, H.; Wu, W.; Zeng, W.; Wu, X. Org. Lett. 2013, 15, 1598.
doi: 10.1021/ol400379z |
|
|
(g) Ma, R.; Ding, Y.; Chen, R.; Wang, Z.; Wang, L.; Ma, Y. J. Org. Chem. 2021, 86, 310.
doi: 10.1021/acs.joc.0c02095 |
|
|
(h) Sharma, H.; Singh, N.; Jang, D. O, Green Chem. 2014, 16, 4922.
doi: 10.1039/C4GC01142B |
|
|
(i) Li, Z.; Dong, J.; Chen, X.; Li, Q.; Zhou, Y.; Yin, S.-F. J. Org. Chem. 2015, 80, 9392.
doi: 10.1021/acs.joc.5b00937 |
|
|
(j) Liu, J.; Wang, C.; Ma, X.; Shi, X.; Wang, X.; Li, H.; Xu, Q. Catal. Lett. 2016, 146, 2139.
doi: 10.1007/s10562-016-1818-2 |
|
|
(k) Shi, X.; Guo, J. Liu, J.; Ye, M.; Xu, Q. Chem.-Eur. J. 2015, 21, 9988.
doi: 10.1002/chem.201501184 |
|
| [10] |
(a) Xu, Y.; Li, B.; Zhang, X.; Fan, X. J. Org. Chem. 2017, 82, 9637.
doi: 10.1021/acs.joc.7b01683 pmid: 30943366 |
|
(b) Mishra, N.; Singh, A. S.; Agrahari, A. K.; Singh, S. K.; Singh, M.; Tiwari, V. K. ACS Comb. Sci. 2019, 21, 389.
doi: 10.1021/acscombsci.9b00004 pmid: 30943366 |
|
|
(c) Urzúa, J. I.; Contreras, R.; Salas, C. O.; Tapia, R. A. RSC Adv. 2016, 6, 82401.
doi: 10.1039/C6RA18510J pmid: 30943366 |
|
| [11] |
Ma, D.; Xie, S.; Xue, P.; Zhang, X.; Dong, J.; Jiang, Y. Angew. Chem., Int. Ed. 2009, 48, 4222.
doi: 10.1002/anie.v48:23 |
| [12] |
(a) Zhu, Y.-P.; Jia, F.-C.; Liu, M.-C.; Wu, A.-X. Org. Lett. 2012, 14, 4414.
doi: 10.1021/ol301921t |
|
(b) Zhu, Y.-P.; Lian, M.; Jia, F.-C.; Liu, M.-C.; Yuan, J.-J.; Gao, Q.-H.; Wu, A.-X. Chem. Commun. 2012, 48, 9086.
doi: 10.1039/c2cc34561g |
|
| [13] |
(a) Liao, Y.; Qi, H.; Chen, S.; Jiang, P.; Zhou, W.; Deng, G.-J. Org. Lett. 2012, 14, 6004.
doi: 10.1021/ol302902e |
|
(b) Wang, J.; Zhang, X.-Z.; Chen, S.-Y.; Yu, X.-Q. Tetrahedron 2014, 70, 245.
doi: 10.1016/j.tet.2013.11.078 |
|
|
(c) Liu, S.; Chen, R.; Chen, H.; Deng, G.-J. Tetrahedron Lett. 2013, 54, 3838.
|
|
| [14] |
(a) Yu, X.-Y.; Chen, J.-R.; Xiao, W.-J. Chem. Rev. 2021, 121, 506.
doi: 10.1021/acs.chemrev.0c00030 |
|
(b) Wan, J.-P.; Gao, Y.; Wei, L. Chem.-Asian J. 2016, 11, 2092.
doi: 10.1002/asia.v11.15 |
|
|
Gan, L.; Yu, Q.; Liu, Y.; Wan, J.-P. J. Org. Chem. 2021, 86, 1231.
doi: 10.1021/acs.joc.0c02431 |
|
|
(d) Gan, Y.; Zhang, N.; Huang, S.; Liu, Y. Chin. J. Chem. 2020, 38, 1686.
doi: 10.1002/cjoc.v38.12 |
|
|
(e) Wang, G.; Guo, Y.; Wan, J. Chin. J. Org. Chem. 2020, 40, 645. (in Chinese).
doi: 10.6023/cjoc201912018 |
|
|
( 王国栋, 郭艳辉, 万结平, 有机化学, 2020, 40, 645.)
|
|
| [15] |
(a) Nyffeler, P. T.; Duron, S. G.; Burkart, M. D.; Vincent, S. P.; Wong, C.-H. Angew. Chem.,Int. Ed. 2004, 44, 192.
doi: 10.1002/anie.200400648 |
|
(b) Syvret, R. G.; Butt, K. M.; Nguyen, T. P.; Bulleck, V. L.; Rieth, R. D. J. Org. Chem. 2002, 67, 4487.
doi: 10.1021/jo020053u |
|
| [16] |
Lv, Y.; Sun, K.; Pu, W.; Mao, S.; Li, G.; Niu, J.; Chen, Q.; Wang, T. RSC Adv. 2016, 6, 93486.
doi: 10.1039/C6RA22653A |
| [17] |
Zhao, J.; Xiao, Q.; Chen, J.; Xu, J. Eur. J. Org. Chem. 2020, 2020, 5201.
doi: 10.1002/ejoc.v2020.32 |
| [18] |
Wang, H.; Ren, S.; Zhang, J.; Zhang, W.; Liu, Y. J. Org. Chem. 2015, 80, 6856.
doi: 10.1021/acs.joc.5b00857 |
| [19] |
(a) Shah, S.; Arshia; Javaid, K.; Zafar, H.; Khan, K. M.; Khalil, R.; Ul-Haq, Z.; Perveen, S.; Choudhary, M. I. Bioorg. Chem. 2018, 78, 269.
doi: 10.1016/j.bioorg.2018.02.013 pmid: 31698294 |
|
(b) Ghannam, I. A. Y.; Abd El-Meguid, E. A.; Ali, I. H.; Sheir, D. H.; El Kerdawy, A. M. Bioorg. Chem. 2019, 93, 103373.
doi: S0045-2068(19)31378-1 pmid: 31698294 |
|
| [20] |
(a) Deligeorgiev, T. G.; Kaloyanova, S.; Vasilev, A.; Vaquero, J. J., Phosphorus, Sulfur Silicon Relat. Elem. 2010, 185, 2292.
pmid: 18947183 |
|
(b) Fawzia, A. Q.; Ramadan, A. M.; Kamal, U. S. Molecules 2008, 13, 2908.
doi: 10.3390/molecules13112908 pmid: 18947183 |
|
|
(c) Kiyofumi, I.; Chisa, H.; Kou, H.; Takayuki, D. Org. Lett. 2008, 10, 5147.
doi: 10.1021/ol802033p pmid: 18947183 |
|
|
(d) Wang, Z.; Tang, R.; Li, J. Chin. J. Chem. 2011, 29, 314.
doi: 10.1002/cjoc.201190084 pmid: 18947183 |
|
|
(e) Das, K.; Mondal, A.; Srimani, D. Chem. Commun. 2018, 54, 10582.
doi: 10.1039/C8CC05877F pmid: 18947183 |
|
|
(f) Xu, Z.-M.; Li, H.-X.; Young, D. J.; Zhu, D.-L.; Li, H.-Y.; Lang, J.-P. Org. Lett. 2019, 21, 237.
doi: 10.1021/acs.orglett.8b03679 pmid: 18947183 |
|
|
(g) Song, Q.; Feng, Q.; Zhou, M. Org. Lett. 2013, 15, 5990.
doi: 10.1021/ol402871f pmid: 18947183 |
| [1] | 孟宪强, 杨艺, 梁万洁, 王靖涛, 张荣葵, 刘会. 钯催化联烯胺区域选择性芳基酚氧化反应[J]. 有机化学, 2024, 44(1): 224-231. |
| [2] | 董江湖, 宣良明, 王池, 赵晨熙, 王海峰, 严琼姣, 汪伟, 陈芬儿. 无过渡金属或无光催化剂条件下可见光促进喹喔啉酮C(3)—H官能团化研究进展[J]. 有机化学, 2024, 44(1): 111-136. |
| [3] | 岁丹丹, 岑南楠, 龚若蕖, 陈阳, 陈文博. 无支持电解质条件下连续流电化学合成三氟甲基化氧化吲哚[J]. 有机化学, 2023, 43(9): 3239-3245. |
| [4] | 归春明, 周潼瑶, 王海峰, 严琼姣, 汪伟, 黄锦, 陈芬儿. 可见光氧化还原催化炔基化反应的研究进展[J]. 有机化学, 2023, 43(8): 2647-2663. |
| [5] | 刘长俊, 胡慧玲, 刘宬宏, 朱超杰, 唐天地. 介孔ETS-10沸石担载Pd高效催化内炔氧化制备1,2-二酮[J]. 有机化学, 2023, 43(8): 2953-2960. |
| [6] | 吴文倩, 陈春霞, 彭进松, 李占宇. 羰基α-位胺化反应研究进展[J]. 有机化学, 2023, 43(8): 2743-2763. |
| [7] | 赵婷, 农旭华, 王佳莉, 许宽毓, 唐敏敏, 易继凌, 韩长日, 陈光英. 长花龙血树茎中抗氧化活性的木脂素类成分研究[J]. 有机化学, 2023, 43(8): 2968-2972. |
| [8] | 张晓雨, 李欣燕, 崔冰, 邵志晖, 赵铭钦. 四氢-β-咔啉衍生物的设计、合成及抗氧化性能研究[J]. 有机化学, 2023, 43(8): 2885-2894. |
| [9] | 廖旭, 王泽宇, 唐武飞, 林金清. 多孔有机聚合物用于化学固定二氧化碳的研究进展[J]. 有机化学, 2023, 43(8): 2699-2710. |
| [10] | 刘露, 张曙光, 胡仁威, 赵晓晓, 崔京南, 贡卫涛. 基于多羟基柱[5]芳烃的酚醛多孔聚合物合成及CO2催化转化[J]. 有机化学, 2023, 43(8): 2808-2814. |
| [11] | 吴敏, 刘博, 袁佳龙, 付强, 汪锐, 娄大伟, 梁福顺. 可见光媒介的C—S键构建反应研究进展[J]. 有机化学, 2023, 43(7): 2269-2292. |
| [12] | 高艳华, 张银潘, 张妍, 宋涛, 杨勇. 可见光驱动表面富含氧空位Nb2O5催化醇氧化反应[J]. 有机化学, 2023, 43(7): 2572-2579. |
| [13] | 李宜芳, 王耀, 牛华伟, 陈秀金, 李兆周, 王永国. 线粒体靶向的二氧化硫荧光探针研究进展[J]. 有机化学, 2023, 43(6): 1952-1962. |
| [14] | 罗诚, 尹艳丽, 江智勇. P-手性膦氧化物的不对称合成研究进展[J]. 有机化学, 2023, 43(6): 1963-1976. |
| [15] | 宋姿洁, 刘俊, 白赢, 厉嘉云, 彭家建. 利用硅氢加成反应催化转化二氧化碳研究进展[J]. 有机化学, 2023, 43(6): 2068-2080. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||