有机化学 ›› 2023, Vol. 43 ›› Issue (6): 2068-2080.DOI: 10.6023/cjoc202210024 上一篇 下一篇
所属专题: 二氧化碳虚拟合辑
综述与进展
收稿日期:2022-10-22
修回日期:2022-11-25
发布日期:2023-01-05
通讯作者:
白赢, 彭家建
基金资助:
Zijie Song, Jun Liu, Ying Bai*( ), Jiayun Li, Jiajian Peng*(
), Jiayun Li, Jiajian Peng*( )
)
Received:2022-10-22
Revised:2022-11-25
Published:2023-01-05
Contact:
E-mail: Supported by:文章分享
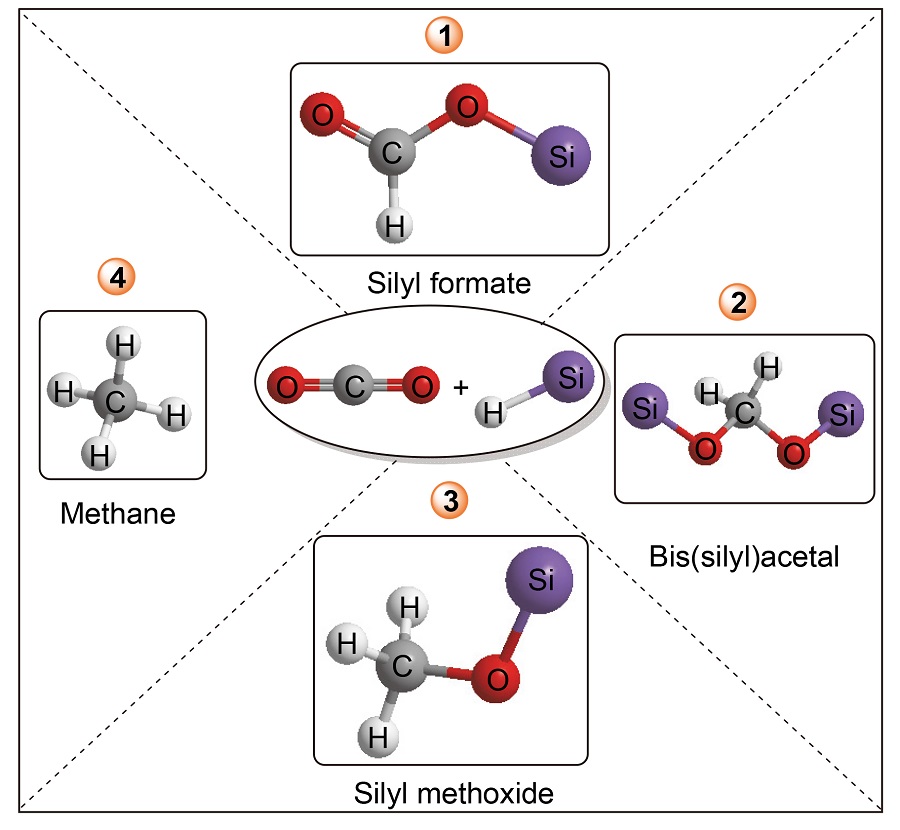
减少CO2的排放和转化利用空气中的CO2一直以来都是科研工作者研究的一个热点. CO2具有无毒、丰富及易得的特点, 是合成有机化合物的理想原料. 近年来, 硅氢化还原反应已经发展成为一种有效转化CO2的方法, 可以在较温和的反应条件下将CO2还原转化为甲酸盐、甲醛、甲醇和甲烷等具有利用价值的化学产品, 大大促进了CO2的转化和利用. 总结了用于催化CO2硅氢化还原反应催化体系的设计、合成与催化性能研究进展, 讨论了CO2硅氢化还原的反应机理, 分析了各种催化剂体系的优势和缺点, 并对该领域未来的研究方向进行了展望.
宋姿洁, 刘俊, 白赢, 厉嘉云, 彭家建. 利用硅氢加成反应催化转化二氧化碳研究进展[J]. 有机化学, 2023, 43(6): 2068-2080.
Zijie Song, Jun Liu, Ying Bai, Jiayun Li, Jiajian Peng. Progress in Catalysis Transformation of Carbon Dioxide through Hydrosilylation[J]. Chinese Journal of Organic Chemistry, 2023, 43(6): 2068-2080.



| [1] |
Chen, J.; McGraw, M.; Chen, E. Y.-X. ChemSusChem 2019, 12, 4543.
doi: 10.1002/cssc.v12.20 |
| [2] |
Maeda, C.; Miyazaki, Y.; Ema, T. Catal. Sci. Technol. 2014, 4, 1482.
doi: 10.1039/c3cy00993a |
| [3] |
Centi, G.; Quadrelli, E. A.; Perathoner, S. Energy Environ. Sci. 2013, 6, 1711.
doi: 10.1039/c3ee00056g |
| [4] |
Liu, X.-F.; Li, X.-Y.; Qiao, C.; He, L.-N. Synlett 2018, 29, 548.
doi: 10.1055/s-0036-1591533 |
| [5] |
Liu, X.-F.; Li, X.-Y.; He, L.-N. Eur. J. Org. Chem. 2019, 2019, 2437.
doi: 10.1002/ejoc.201801833 |
| [6] |
Fernandez-Alvarez, F. J.; Aitani, A. M.; Oro, L. A. Catal. Sci. Technol. 2014, 4, 611.
doi: 10.1039/C3CY00948C |
| [7] |
Pramudita, R. A.; Motokura, K. Green Chem, 2018, 20, 4834.
doi: 10.1039/C8GC02052C |
| [8] |
Zhang, Y.; Zhang, T.; Das, S. Green Chem. 2020, 22, 1800.
doi: 10.1039/C9GC04342J |
| [9] |
Huang, Y.; Deng, W.; Lin, B.-L. Chin. Chem. Lett. 2020, 31, 111.
doi: 10.1016/j.cclet.2019.04.064 |
| [10] |
Cabrero-Antonino, J. R.; Adam, R.; Beller, M. Angew. Chem., Int. Ed. 2019, 58, 12820.
doi: 10.1002/anie.v58.37 |
| [11] |
Li, Y.; Cui, X.; Dong, K.; Junge, K.; Beller, M. ACS Catal. 2017, 7, 1077.
doi: 10.1021/acscatal.6b02715 |
| [12] |
Süss-Fink, G.; Reiner, J. J. Organomet. Chem. 1981, 221, C36.
doi: 10.1016/S0022-328X(00)88383-7 |
| [13] |
Koinuma, H.; Kawakami, F.; Kato, H.; Hirai, H. J. Chem. Soc., Chem. Commun. 1981, 213.
|
| [14] |
Parks, D. J.; Piers, W. E. J. Am. Chem. Soc. 1996, 118, 9440.
doi: 10.1021/ja961536g |
| [15] |
Eisenschmid, T. C.; Eisenberg, R. Organometallics 1989, 8, 1822.
doi: 10.1021/om00109a041 |
| [16] |
Park, S.; Bezier, D.; Brookhart, M. J. Am. Chem. Soc. 2012, 134, 11404.
doi: 10.1021/ja305318c |
| [17] |
Lalrempuia, R.; Iglesias, M.; Polo, V.; Sanz Miguel, P. J.; Fernandez-Alvarez, F. J.; Perez-Torrente, J. J.; Oro, L. A. Angew. Chem., Int. Ed. 2012, 51, 12824.
doi: 10.1002/anie.201206165 |
| [18] |
Jaseer, E. A.; Akhtar, M. N.; Osman, M.; Al-Shammari, A.; Oladipo, H. B.; Garces, K.; Fernandez-Alvarez, F. J.; Al-Khattaf, S.; Oro, L. A. Catal. Sci. Technol. 2015, 5, 274.
doi: 10.1039/C4CY00815D |
| [19] |
Oladipo, H. B.; Jaseer, E. A.; Julian, A.; Fernandez-Alvarez, F. J.; Al-Khattaf, S.; Oro, L. A. J. CO2 Util. 2015, 12, 21.
|
| [20] |
Julián, A.; Jaseer, E. A.; Garces, K.; Fernandez-Alvarez, F. J.; Garcia-Orduna, P.; Lahoz, F. J.; Oro, L. A. Catal. Sci. Technol. 2016, 6, 4410.
doi: 10.1039/C5CY02139A |
| [21] |
Julián, A.; Guzman, J.; Jaseer, E. A.; Fernandez-Alvarez, F. J.; Royo, R.; Polo, V.; Garcia-Orduna, P.; Lahoz, F. J.; Oro, L. A. Chem.-Eur. J. 2017, 23, 11898.
doi: 10.1002/chem.201702246 |
| [22] |
Guzman, J.; Garcia-Orduna, P.; Polo, V.; Lahoz, F. J.; Oro, L. A.; Fernandez-Alvarez, F. J. Catal. Sci. Technol. 2019, 9, 2858.
doi: 10.1039/C8CY02353K |
| [23] |
Nguyen, T. V. Q.; Yoo, W. J.; Kobayashi, S. Angew. Chem., Int. Ed. 2015, 54, 9209.
doi: 10.1002/anie.201504072 |
| [24] |
Rios, P.; Diez, J.; Lopez-Serrano, J.; Rodriguez, A.; Conejero, S. Chem.-Eur. J. 2016, 22, 16791.
doi: 10.1002/chem.v22.47 |
| [25] |
Takaya, J.; Iwasawa, N. J. Am. Chem. Soc. 2017, 139, 6074.
doi: 10.1021/jacs.7b02553 pmid: 28423896 |
| [26] |
Steinhoff, P.; Paul, M.; Schroers, J. P.; Tauchert, M. E. Dalton Trans. 2019, 48, 1017.
doi: 10.1039/c8dt03777a pmid: 30574969 |
| [27] |
Wang, G.; Jiang, M.; Ji, M.; Sun, Z.; Ma, L.; Li, C.; Du, H.; Yan, L.; Ding, Y. Catalysts 2021, 11, 220.
doi: 10.3390/catal11020220 |
| [28] |
Matsuo, T.; Kawaguchi, H. J. Am. Chem. Soc. 2006, 128, 12362.
doi: 10.1021/ja0647250 |
| [29] |
Metsaenen, T. T.; Oestreich, M. Organometallics 2015, 34, 543.
doi: 10.1021/om501279a |
| [30] |
LeBlanc, F. A.; Piers, W. E.; Parvez, M. Angew. Chem., Int. Ed. 2014, 53, 789.
doi: 10.1002/anie.201309094 |
| [31] |
Wang, M.; Wang, N.; Liu, X.; Qiao, C.; He, L. Green Chem. 2018, 20, 1564.
doi: 10.1039/C7GC03416D |
| [32] |
Chang, K.; del Rosal, I.; Zheng, X.; Maron, L.; Xu, X. Dalton Trans. 2021, 50, 7804.
doi: 10.1039/D1DT01074C |
| [33] |
Scheuermann, M. L.; Semproni, S. P.; Pappas, I.; Chirik, P. J. Inorg. Chem. 2014, 53, 9463.
doi: 10.1021/ic501901n pmid: 25171221 |
| [34] |
Cramer, H. H.; Chatterjee, B.; Weyhermueller, T.; Werle, C.; Leitner, W. Angew. Chem., Int. Ed. 2020, 59, 15674.
doi: 10.1002/anie.v59.36 |
| [35] |
Cramer, H. H.; Ye, S.; Neese, F.; Werle, C.; Leitner, W. JACS Au 2021, 1, 2058.
doi: 10.1021/jacsau.1c00350 pmid: 34849511 |
| [36] |
Hlatshwayo, Z. T.; Doremus, J. G.; McGrier, P. L. ChemCatChem 2022, 14, e202200783.
|
| [37] |
Gonzalez-Sebastian, L.; Flores-Alamo, M.; Garcia, J. J. Organometallics 2013, 32, 7186.
doi: 10.1021/om400876j |
| [38] |
Singh, V.; Sakaki, S.; Deshmukh, M. M. Organometallics 2018, 37, 1258.
doi: 10.1021/acs.organomet.8b00011 |
| [39] |
Ríos, P.; Curado, N.; Lopez-Serrano, J.; Rodriguez, A. Chem. Commun. 2016, 52, 2114.
doi: 10.1039/C5CC09650B |
| [40] |
Li, H.; Goncalves, T. P.; Zhao, Q.; Gong, D.; Lai, Z.; Wang, Z.; Zheng, J.; Huang, K. Chem. Commun. 2018, 54, 11395.
doi: 10.1039/C8CC05948A |
| [41] |
Li, H.; Castro, L. C. M.; Zheng, J.; Roisnel, T.; Dorcet, V.; Sortais, J. B.; Darcel, C. Angew. Chem., Int. Ed. 2013, 52, 8045.
doi: 10.1002/anie.v52.31 |
| [42] |
Frogneux, X.; Jacquet, O.; Cantat, T. Catal. Sci. Technol. 2014, 4, 1529.
doi: 10.1039/C4CY00130C |
| [43] |
Jurado-Vazquez, T.; Garcia, J. J. Catal. Lett. 2018, 148, 1162.
doi: 10.1007/s10562-018-2305-8 |
| [44] |
Gopakumar, A.; Akçok, I.; Lombardo, L.; Formal, F. L.; Magrez, A.; Sivula, K.; Dyson, P. J. ChemistrySelect 2018, 3, 10271.
doi: 10.1002/slct.201802646 |
| [45] |
Li, W.; Zhu, D.; Li, G.; Chen, J.; Xia, J. Adv. Synth. Catal. 2019, 361, 5098.
doi: 10.1002/adsc.v361.22 |
| [46] |
Li, W.; Chen, J.; Zhu, D.; Xia, J. Chin. J. Chem. 2021, 39, 614.
doi: 10.1002/cjoc.v39.3 |
| [47] |
Bertini, F.; Glatz, M.; Stoger, B.; Peruzzini, M.; Veiros, L. F.; Kirchner, K.; Gonsalvi, L. ACS Catal. 2019, 9, 632.
doi: 10.1021/acscatal.8b04106 |
| [48] |
Huang, Z.; Jiang, X.; Zhou, S.; Yang, P.; Du, C.; Li, Y. ChemSusChem 2019, 12, 3054.
doi: 10.1002/cssc.v12.13 |
| [49] |
Deshmukh, M. M.; Sakaki, S. Inorg. Chem. 2014, 53, 8485.
doi: 10.1021/ic501058j |
| [50] |
Rauch, M.; Parkin, G. J. Am. Chem. Soc. 2017, 139, 18162.
doi: 10.1021/jacs.7b10776 |
| [51] |
Luo, R.; Lin, X.; Lu, J.; Zhou, X.; Ji, H. Chin. J. Catal. 2017, 38, 1382.
doi: 10.1016/S1872-2067(17)62877-8 |
| [52] |
Feng, G.; Du, C.; Xiang, L.; Rosal, I. D.; Li, G.; Leng, X.; Chen, E. Y.-X.; Maron, L.; Chen, Y. ACS Catal. 2018, 8, 4710.
doi: 10.1021/acscatal.8b01033 |
| [53] |
Zhang, Q.; Fukaya, N.; Fujitani, T.; Choi, J, C. Bull. Chem. Soc. Jpn. 2019, 92, 1945.
doi: 10.1246/bcsj.20190203 |
| [54] |
Baalbaki, Hassan A.; Shu, J.; Nyamayaro, K.; Jung, H.; Mehrkhodavandi, P. Chem. Commun. 2022, 58, 6192.
doi: 10.1039/D2CC01498J |
| [55] |
Cao, Q.; Zhang, L.; Zhou, C.; He, J.; Marcomini, A.; Lu, J. Appl. Catal. B 2021, 294, 120238.
doi: 10.1016/j.apcatb.2021.120238 |
| [56] |
Wang, P.; He, Q.; Zhang, H.; Sun, Q.; Cheng, Y.; Gan, T.; He, X.; Ji, H. Catal. Commun. 2021, 149, 106195.
doi: 10.1016/j.catcom.2020.106195 |
| [57] |
Lin, X.; Matsumoto, K.; Maegawa, Y.; Takeuchi, K.; Fukaya, N.; Sato, K.; Inagaki, S.; Choi, J.-C. New J. Chem. 2021, 45, 9501.
doi: 10.1039/D1NJ01204E |
| [58] |
Ruccolo, S.; Sambade, D.; Shlian, D.; Amemiya, E.; Parkin, G. Dalton Trans. 2022, 51, 5868.
doi: 10.1039/D1DT04156H |
| [59] |
Chen, J.; Falivene, L.; Caporaso, L.; Cavallo, L.; Chen, E. Y.-X. J. Am. Chem. Soc. 2016, 138, 5321.
doi: 10.1021/jacs.6b01497 |
| [60] |
Saleh, M.; Powell, D. R.; Wehmschulte, R. J. Organometallics 2017, 36, 4810.
doi: 10.1021/acs.organomet.7b00716 |
| [61] |
Bolley, A.; Specklin, D.; Dagorne, S. Polyhedron 2021, 194, 114956.
doi: 10.1016/j.poly.2020.114956 |
| [62] |
Motokura, K.; Kashiwame, D.; Miyaji, A.; Baba, T. Org. Lett. 2012, 14, 2642.
doi: 10.1021/ol301034j pmid: 22540994 |
| [63] |
Motokura, K.; Kashiwame, D.; Takahashi, N.; Miyaji, A.; Baba, T. Chem.-Eur. J. 2013, 19, 10030.
doi: 10.1002/chem.201300935 pmid: 23776009 |
| [64] |
Motokura, K.; Takahashi, N.; Miyaji, A.; Sakamoto, Y.; Yamaguchi, S.; Baba, T. Tetrahedron 2014, 70, 6951.
doi: 10.1016/j.tet.2014.07.089 |
| [65] |
Zhang, S.; Mei, Q.; Liu, H.; Liu, H.; Zhang, Z.; Han, B. RSC Adv. 2016, 6, 32370.
doi: 10.1039/C6RA05199E |
| [66] |
Li, X.; Xia, S.; Chen, K.; Liu, X.; Li, H.; He, L. Green Chem. 2018, 20, 4853.
doi: 10.1039/C8GC02280A |
| [67] |
Zhang, L.; Cheng, J.; Hou, Z. Chem. Commun. 2013, 49, 4782.
doi: 10.1039/c3cc41838c |
| [68] |
Tani, Y.; Kuga, K.; Fujihara, T.; Terao, J.; Tsuji, Y. Chem. Commun. 2015, 51, 13020.
doi: 10.1039/C5CC03932K |
| [69] |
Yang, Z.; Yu, B.; Zhang, H.; Zhao, Y.; Ji, G.; Ma, Z.; Gao, X.; Liu, Z. Green Chem. 2015, 17, 4189.
doi: 10.1039/C5GC01386K |
| [70] |
Liu, X.; Li, X.; Qiao, C.; Fu, H.; He, L. Ange. Chem., Int. Ed. 2017, 56, 7425.
|
| [71] |
Frogneux, X.; Blondiaux, E.; Thuery, P.; Cantat, T. ACS Catal. 2015, 5, 3983.
doi: 10.1021/acscatal.5b00734 |
| [72] |
Bobbink, F. D.; Das, S.; Dyson, P. J. Nat. Protoc. 2017, 12, 417.
doi: 10.1038/nprot.2016.175 pmid: 28125103 |
| [73] |
Chong, C.; Kinjo, R. Angew. Chem., Int. Ed. 2015, 54, 12116.
doi: 10.1002/anie.201505244 |
| [74] |
Yu, Z.; Li, Z.; Zhang, L.; Zhu, K.; Wu, H.; Li, H.; Yang, S. Green Chem. 2021, 23, 5759.
doi: 10.1039/D1GC01897C |
| [75] |
Li, G.; Chen, J.; Zhu, D.; Chen, Y.; Xia, J. Adv. Synth. Catal. 2018, 360, 2364.
doi: 10.1002/adsc.201800140 |
| [76] |
Motokura, K.; Naijo, M.; Yamaguchi, S.; Miyaji, A.; Baba, T. Chem. Lett. 2015, 44, 1217.
doi: 10.1246/cl.150510 |
| [77] |
Fang, C.; Lu, C.; Liu, M.; Zhu, Y.; Fu, Y.; Lin, B.-L. ACS Catal. 2016, 6, 7876.
doi: 10.1021/acscatal.6b01856 |
| [78] |
Wu, S.; Huang, Z.; Jiang, X.; Yan, F.; Li, Y.; Du, C. ChemSusChem 2021, 14, 1763.
doi: 10.1002/cssc.v14.7 |
| [79] |
Jiang, X.; Huang, Z.; Makha, M.; Du, C.-X.; Zhao, D.; Wang, F.; Li, Y. Green Chem. 2020, 22, 5317.
doi: 10.1039/D0GC01741H |
| [80] |
Zhu, D.; Fang, L.; Han, H.; Wang, Y.; Xia, J. Org. Lett. 2017, 19, 4259.
doi: 10.1021/acs.orglett.7b01906 |
| [81] |
Zhu, D.; Li, W.; Yang, C.; Chen, J.; Xia, J. Org. Lett. 2018, 20, 3282.
doi: 10.1021/acs.orglett.8b01155 |
| [82] |
Nicholls, R. L.; McManus, J. A.; Rayner, C. M.; Morales-Serna, J. A.; White, A. J. P.; Nguyen, B. N. ACS Catal. 2018, 8, 3678.
doi: 10.1021/acscatal.7b04108 |
| [83] |
Mu, Z.; Ding, X.; Chen, Z.; Han, B. ACS Appl. Mater. Interfaces 2018, 10, 41350.
doi: 10.1021/acsami.8b14671 |
| [84] |
Zhu, A.; Bai, S.; Li, L.; Wang, M.; Wang, J. Catal. Lett. 2015, 145, 1089.
doi: 10.1007/s10562-015-1487-6 |
| [85] |
Zhao, W.; Chi, X.; Li, H.; He, J.; Long, J.; Xua, Y.; Yang, S. Green Chem. 2019, 21, 567.
doi: 10.1039/C8GC03549K |
| [86] |
Gopakumar, A.; Lombardo, L.; Fei, Z. F.; Shyshkanov, S.; Vasilyev, D.; Chidambaram, A.; Stylianou, K.; Züttel, A.; Dyson, P. J. J. CO2 Util. 2020, 101240.
|
| [87] |
Pramudita, R. A.; Nakagawa, C.; Manaka, Y.; Motokura, K. Chem. Lett. 2019, 48, 1417.
doi: 10.1246/cl.190649 |
| [88] |
Shen, Q.; Chen, X.; Tan, Y.; Chen, J.; Chen, L.; Tan, S. ACS Appl. Mater. Interfaces 2019, 11, 38838.
doi: 10.1021/acsami.9b14509 |
| [89] |
Zhai, G.; Liu, Q.; Ji, J.; Wu, Y.; Geng, J.; Hu, X. J. CO2 Util. 2022, 61, 102052.
|
| [1] | 邹发凯, 王能中, 姚辉, 王慧, 刘明国, 黄年玉. 1β-/3R-芳基硫代糖的区域与立体选择性合成[J]. 有机化学, 2024, 44(2): 593-604. |
| [2] | 刘继宇, 李圣玉, 陈款, 朱茵, 张元. 三苯胺功能化有序介孔聚合物作为无金属光催化剂用于二硫化物合成[J]. 有机化学, 2024, 44(2): 605-612. |
| [3] | 杨爽, 房新强. 氮杂环卡宾催化实现的动力学拆分近期研究进展[J]. 有机化学, 2024, 44(2): 448-480. |
| [4] | 李路瑶, 贺忠文, 张振国, 贾振华, 罗德平. 三芳基碳正离子在有机合成中的应用[J]. 有机化学, 2024, 44(2): 421-437. |
| [5] | 陈宛婷, 钟雄威, 邢佳乐, 吴昌书, 高杨. C—N轴手性化合物的不对称催化合成研究进展[J]. 有机化学, 2024, 44(2): 349-377. |
| [6] | 黄净, 杨毅华, 张占辉, 刘守信. 酰胺键的绿色高效构建方法与技术进展[J]. 有机化学, 2024, 44(2): 409-420. |
| [7] | 梅青刚, 李清寒. 可见光促进C(3)(杂)芳硫基吲哚化合物的合成研究进展[J]. 有机化学, 2024, 44(2): 398-408. |
| [8] | 李洋, 董亚楠, 李跃辉. 经由N-硼基酰胺中间体的酰胺高效转化合成腈类化合物[J]. 有机化学, 2024, 44(2): 638-643. |
| [9] | 李思达, 崔鑫, 舒兴中, 吴立朋. 钛催化的烯烃制备1,1-二硼化合物[J]. 有机化学, 2024, 44(2): 631-637. |
| [10] | 童红恩, 郭宏宇, 周荣. 可见光促进惰性碳-氢键对羰基的加成反应进展[J]. 有机化学, 2024, 44(1): 54-69. |
| [11] | 董江湖, 宣良明, 王池, 赵晨熙, 王海峰, 严琼姣, 汪伟, 陈芬儿. 无过渡金属或无光催化剂条件下可见光促进喹喔啉酮C(3)—H官能团化研究进展[J]. 有机化学, 2024, 44(1): 111-136. |
| [12] | 李梦竹, 孟博莹, 兰文捷, 傅滨. 邻亚甲醌与硫叶立德反应合成2,3-二取代苯并二氢呋喃化合物[J]. 有机化学, 2024, 44(1): 195-203. |
| [13] | 孟宪强, 杨艺, 梁万洁, 王靖涛, 张荣葵, 刘会. 钯催化联烯胺区域选择性芳基酚氧化反应[J]. 有机化学, 2024, 44(1): 224-231. |
| [14] | 朱彦硕, 王红言, 舒朋华, 张克娜, 王琪琳. 烷氧自由基引发1,5-氢原子转移实现C(sp3)—H键官能团化的研究进展[J]. 有机化学, 2024, 44(1): 1-17. |
| [15] | 姜权彬. 经由氮杂邻联烯醌中间体合成轴手性化合物的研究进展[J]. 有机化学, 2024, 44(1): 159-172. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||