有机化学 ›› 2024, Vol. 44 ›› Issue (2): 644-649.DOI: 10.6023/cjoc202308010 上一篇 下一篇
研究简报
高宝昌a,b,*( ), 石雨b, 田媛b, 张治国b, 张婧如b, 孙宇峰b, 毛国梁a, 戴凌燕c,*(
), 石雨b, 田媛b, 张治国b, 张婧如b, 孙宇峰b, 毛国梁a, 戴凌燕c,*( )
)
收稿日期:2023-08-12
修回日期:2023-10-13
发布日期:2023-11-07
基金资助:
Baochang Gaoa,b( ), Yu Shib, Yuan Tianb, Zhiguo Zhangb, Jingru Zhangb, Yufeng Sunb, Guoliang Maoa, Lingyan Daic(
), Yu Shib, Yuan Tianb, Zhiguo Zhangb, Jingru Zhangb, Yufeng Sunb, Guoliang Maoa, Lingyan Daic( )
)
Received:2023-08-12
Revised:2023-10-13
Published:2023-11-07
Contact:
E-mail: Supported by:文章分享

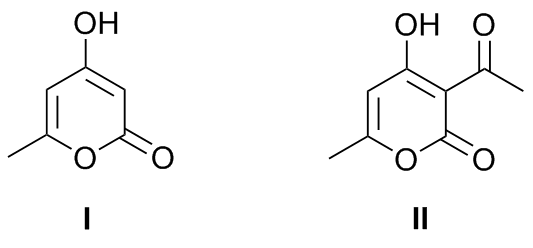
2-吡喃酮衍生物在药物领域表现出了巨大的应用潜力, 已有很多该类骨架结构用作合成药物活性分子前体. 因此, 探索新型2-吡喃酮衍生物的合成方法非常重要. 以β-酮酰胺衍生物和氰基乙酸乙酯为原料一步反应合成了2-吡喃酮衍生物, 具有产物收率高(82%~93%)、反应条件温和产物后处理方便等优点, 为2-吡喃酮生物的合成提供了新策略.
高宝昌, 石雨, 田媛, 张治国, 张婧如, 孙宇峰, 毛国梁, 戴凌燕. 4-甲基-2-氧代-6-芳氨基-二氢-吡喃-3-腈衍生物的合成[J]. 有机化学, 2024, 44(2): 644-649.
Baochang Gao, Yu Shi, Yuan Tian, Zhiguo Zhang, Jingru Zhang, Yufeng Sun, Guoliang Mao, Lingyan Dai. Synthesis of 4-Methyl-2-oxo-6-arylamino-2H-pyran-3-carbonitrile Derivatives[J]. Chinese Journal of Organic Chemistry, 2024, 44(2): 644-649.
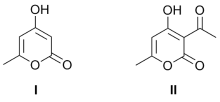
| Entry | Base (equiv.) | Solvent | Temp./℃ | Yield/% |
|---|---|---|---|---|
| 1 | NaOH (1) or KOH (1) | DMF | r.t. | 0 or 0 |
| 2 | NaOH (1) or KOH (1) | DMF | 80 | Mixture or mixture |
| 3 | CsCO3 (1) | C2H5OH | 50 or reflux | Mixture or 17 |
| 4 | LiOH (1) | CH3OH | 50 or reflux | Mixture or 20 |
| 5 | Pyridine (1) | C2H5OH | r.t. or 50 | 0 or mixture |
| 6 | Pyridine (1 or 2) | CH2Cl2 | r.t. | 0 or 0 |
| 7 | DBU (1) | DMF | r.t. or 70 | Mixture or mixture |
| 8 | DABCO (1) | C2H5OH | r.t. or 50 | Mixture or mixture |
| 9 | DABCO (2) | CH3OH | reflux | Mixture |
| 10 | K2CO3 (1) | DMF | r.t. or 50 | Mixture or mixture |
| 11 | K2CO3 (2) | DMF | 80 or 110 | 23 or 31 |
| 12 | K2CO3 (1) | C2H5OH | r.t. or reflux | Mixture or 68 |
| 13 | K2CO3 (2) | C2H5OH | reflux | 67 |
| 14 | tBuOK (1) | DMF or C2H5OH | 80 | 31 or 44 |
| 15 | CH3ONa (1) | CH3OH | r.t. or 50 | 25 or 47 |
| 16 | CH3ONa (1) | CH3OH | reflux | 52 |
| 17 | C2H5ONa (1) | C2H5OH | r.t. or 50 | Mixture or 66 |
| 18 | C2H5ONa (1) | C2H5OH | reflux | 89 |
| 19 | C2H5ONa (0.5 or 2) | C2H5OH | reflux | 57 or 85 |
| 20 | C2H5ONa (1) | C2H5OH | reflux | 90b |
| Entry | Base (equiv.) | Solvent | Temp./℃ | Yield/% |
|---|---|---|---|---|
| 1 | NaOH (1) or KOH (1) | DMF | r.t. | 0 or 0 |
| 2 | NaOH (1) or KOH (1) | DMF | 80 | Mixture or mixture |
| 3 | CsCO3 (1) | C2H5OH | 50 or reflux | Mixture or 17 |
| 4 | LiOH (1) | CH3OH | 50 or reflux | Mixture or 20 |
| 5 | Pyridine (1) | C2H5OH | r.t. or 50 | 0 or mixture |
| 6 | Pyridine (1 or 2) | CH2Cl2 | r.t. | 0 or 0 |
| 7 | DBU (1) | DMF | r.t. or 70 | Mixture or mixture |
| 8 | DABCO (1) | C2H5OH | r.t. or 50 | Mixture or mixture |
| 9 | DABCO (2) | CH3OH | reflux | Mixture |
| 10 | K2CO3 (1) | DMF | r.t. or 50 | Mixture or mixture |
| 11 | K2CO3 (2) | DMF | 80 or 110 | 23 or 31 |
| 12 | K2CO3 (1) | C2H5OH | r.t. or reflux | Mixture or 68 |
| 13 | K2CO3 (2) | C2H5OH | reflux | 67 |
| 14 | tBuOK (1) | DMF or C2H5OH | 80 | 31 or 44 |
| 15 | CH3ONa (1) | CH3OH | r.t. or 50 | 25 or 47 |
| 16 | CH3ONa (1) | CH3OH | reflux | 52 |
| 17 | C2H5ONa (1) | C2H5OH | r.t. or 50 | Mixture or 66 |
| 18 | C2H5ONa (1) | C2H5OH | reflux | 89 |
| 19 | C2H5ONa (0.5 or 2) | C2H5OH | reflux | 57 or 85 |
| 20 | C2H5ONa (1) | C2H5OH | reflux | 90b |
| Entry | 1 | R | 2 | Time/h | Yield/% |
|---|---|---|---|---|---|
| 1 | 1a | Ph | 2a | 4 | 89a, 90b |
| 2 | 1b | 4-ClC6H4 | 2b | 4.5 | 91a, 87b |
| 3 | 1c | 2-MeC6H4 | 2c | 5 | 93a, 91b |
| 4 | 1d | 2-MeOC6H4 | 2d | 4 | 84a, 82b |
| 5 | 1e | 2,4-Me2C6H3 | 2e | 4 | 82a, 85b |
| 6 | 1f | 4-MeOC6H4 | 2f | 4.5 | 87a, 84b |
| 7 | 1g | 2-ClC6H4 | 2g | 5 | 86a, 81b |
| 8 | 1h | 4-MeC6H4 | 2h | 4 | 90a, 92b |
| 9 | 1i | 2,5-(MeO)2-4-ClC6H2 | 2i | 5 | 83a, 84b |
| 10 | 1j | CH3 | 2j | 5 | 0 |
| Entry | 1 | R | 2 | Time/h | Yield/% |
|---|---|---|---|---|---|
| 1 | 1a | Ph | 2a | 4 | 89a, 90b |
| 2 | 1b | 4-ClC6H4 | 2b | 4.5 | 91a, 87b |
| 3 | 1c | 2-MeC6H4 | 2c | 5 | 93a, 91b |
| 4 | 1d | 2-MeOC6H4 | 2d | 4 | 84a, 82b |
| 5 | 1e | 2,4-Me2C6H3 | 2e | 4 | 82a, 85b |
| 6 | 1f | 4-MeOC6H4 | 2f | 4.5 | 87a, 84b |
| 7 | 1g | 2-ClC6H4 | 2g | 5 | 86a, 81b |
| 8 | 1h | 4-MeC6H4 | 2h | 4 | 90a, 92b |
| 9 | 1i | 2,5-(MeO)2-4-ClC6H2 | 2i | 5 | 83a, 84b |
| 10 | 1j | CH3 | 2j | 5 | 0 |
| [1] |
(a) Vara Prasad, J. V. N.; Para, K. S.; Lunney, E. A.; Ortwine, D. F.; Dunbar, J. B., Jr.; Ferguson, D.; Tummino, P. J.; Hupe, D.; Tait, B. D.; Domagala, J. M.; Humblet, C.; Bhat, T. N.; Liu, B.; Guerin, D. M. A.; Baldwin, E. T.; Erickon, J. W.; Swayer, T. K. J. Am. Chem. Soc. 1994, 116, 6989.
doi: 10.1021/ja00094a085 pmid: 9371233 |
|
(b) Douglas, C. J.; Sklenicka, H. M.; Shen, H. C.; Mathias, D. S.; Degen, S. I.; Golding, G. M.; Morgan, C. D.; Shih, R. A.; Mueller, K. L.; Seurer, I. M.; Johnson, E. W.; Hsung, R. P. Tetrahedro. 1999, 55, 13683.
doi: 10.1016/S0040-4020(99)00847-9 pmid: 9371233 |
|
|
(c) Hagen, S. E.; Vara Prasad, J. V. N.; Boyer, F. E.; Domagala, J. M.; Ellsworth, E. L.; Gjda, C.; Hamilton, H. W.; Markkoski, L. J.; Steinbangh, B. A.; Tit, B. D.; Lunney, E. A.; Tummino, P. J.; Fergnson, D.; Hupe, D.; Nouhan, C.; Gracheck, S. J.; Saunders, J. M.; Vander Roest, S. J. Med. Chem. 1997, 40, 3707.
pmid: 9371233 |
|
| [2] |
(a) Claydon, N.; Allan, M. Trans. Br. Mycol. Soc. 1987, 88, 503.
doi: 10.1016/S0007-1536(87)80034-7 |
|
(b) Simon, A.; Dunlop, R. W.; Ghisalberti, E. L.; Silvasithamparam, K. Soil Biol. Biochem. 1988, 20, 263.
doi: 10.1016/0038-0717(88)90050-8 |
|
|
(c) You, X. K.; Lin, Z. L.; Zhang, X. L.; Gao, Y. Chin. J. Org. Chem. 2012, 32, 156 (in Chinese).
doi: 10.6023/cjoc1104071 |
|
|
(游新奎, 林志兰, 张雪利, 高原, 有机化学. 2012, 32, 156.)
doi: 10.6023/cjoc1104071 |
|
| [3] |
Liu, Z.; Meinwald, J. J. Org. Chem. 1996, 61, 6693.
doi: 10.1021/jo951394t |
| [4] |
Aytemir, M. D.; Calis, U.; Ozalp, M. Arch. Pharm. Med. Chem. 2004, 337, 281.
doi: 10.1002/ardp.v337:5 |
| [5] |
(a) Yao, T.; Larock, R. C. J. Org. Chem. 2003, 68, 5936.
doi: 10.1021/jo034308v |
|
(b) Fairlamb, I. J. S.; Marrison, L. R.; Dickinson, J. M.; Lu, F. J.; Schmidt, J. P. Bioorg. Med. Chem. 2004, 12, 4285.
doi: 10.1016/j.bmc.2004.01.051 |
|
| [6] |
Shi, X.; Leal, W. S.; Liu, Z.; Schrader, E.; Meinwald, J. Tetrahedron Lett. 1995, 36, 71.
doi: 10.1016/0040-4039(94)02214-V |
| [7] |
Allen M. Chem. Br. 1996, May, 35.
|
| [8] |
Kondoh, M.; Usui, T.; Kobayashi, S.; Tsuchiya, K.; Nishikawa, K.; Nishikiori, T.; Mayumi, T.; Osada, H. Cancer Lett. 1998, 126, 29.
pmid: 9563645 |
| [9] |
Kobayashi, S.; Tsuchiya, K.; Kurokawa, T.; Nakagawa, T.; Shimada, N.; Iitaka, Y. J. Antibiot. 1994, 47, 703.
pmid: 7794417 |
| [10] |
Tsuchiya, K.; Kobayashi, S.; Nishikiori, T.; Nakagawa, T.; Tatsuta, K. J. Antibiot. 1997, 50, 259.
pmid: 9127198 |
| [11] |
(a) Ichihara, A.; Tazaki, H.; Sakamura, S. Tetrahedron Lett. 1983, 48, 5373.
|
|
(b) Chmielewski, M.; Jurczak, J. J. Org. Chem. 1981, 46, 2230.
doi: 10.1021/jo00324a008 |
|
|
(c) Hernandez-Galan, R. J.; Salva, R.; Massannet, G. M.; Collado, I. G. Tetrahedro. 1993, 49, 1701.
|
|
| [12] |
Atul, G.; Vishnu, J. R. Tetrahedro. 2009, 65, 7865.
doi: 10.1016/j.tet.2009.06.031 |
| [13] |
Xu, M. M.; Cai, Q. Chin. J. Org. Chem. 2022, 42, 698 (in Chinese).
doi: 10.6023/cjoc202109025 |
|
(徐萌萌, 蔡泉, 有机化学. 2022, 42, 698.)
doi: 10.6023/cjoc202109025 |
|
| [14] |
(a) Benetti, S.; Romagnoli, R.; De Risi, C.; Spalluto, G.; Zanirato, V. Chem. Rev. 1995, 95, 1065.
doi: 10.1021/cr00036a007 |
|
(b) Bonne, D.; Coquerel, Y.; Constantieux, T.; Rodriguez, J. Tetrahedron: Asymmetr. 2010, 21, 1085.
doi: 10.1016/j.tetasy.2010.04.045 |
|
|
(c) del Duque, M. M. S.; Allais, C.; Isambert, N.; Constantieux, T.; Rodriguez, J. In Synthesis of Heterocycles via Multicomponent Reactions I, Eds.: Orru, R. V. A.; Ruijter, E.,Springer Berlin Heidelberg, 2010, p. 227.
|
|
|
(d) Liang, Y. J.; Huang, P.; Zhang, R.; Dong, D. W. Chin. J. Org. Chem. 2014, 34, 1037 (in Chinese).
doi: 10.6023/cjoc201403006 |
|
|
(梁永久, 黄鹏, 张睿, 董德文, 有机化学. 2014, 34, 1037.)
doi: 10.6023/cjoc201403006 |
|
| [15] |
(a) Zhang Z. Ph.D. Dissertation. Northeast Normal University, Changchun, 2010 (in Chinese).
pmid: 21391701 |
|
(张志国, 博士论文,东北师范大学, 长春, 2010.)
pmid: 21391701 |
|
|
(b) Xiang, D.; Wang, K.; Liang, Y.; Zhou, G.; Dong, D. Org. Lett. 2008, 10, 345.
doi: 10.1021/ol702846t pmid: 21391701 |
|
|
(c) Zhang, Z.; Zhang, Q.; Sun, S.; Xiong, T.; Liu, Q. Angew. Chem.. Int. Ed. 2007, 46, 1726.
doi: 10.1002/anie.v46:10 pmid: 21391701 |
|
|
(d) Wang, K.; Xiang, D.; Liu, J.; Pan, W.; Dong, D. Org. Lett. 2008, 10, 1691.
doi: 10.1021/ol800178x pmid: 21391701 |
|
|
(e) Zhang, R.; Liang, Y.; Zhou, G.; Wang, K.; Dong, D. J. Org. Chem. 2008, 73, 8089.
doi: 10.1021/jo801289p pmid: 21391701 |
|
|
(f) Xiang, D.; Yang, Y.; Zhang, R.; Liang, Y.; Pan, W.; Huang, J.; Dong, D. J. Org. Chem. 2007, 72, 8593.
doi: 10.1021/jo7015482 pmid: 21391701 |
|
|
(g) Zhang, R.; Zhang, D.; Guo, Y.; Zhou, G.; Jiang, Z.; Dong, D. J. Org. Chem. 2008, 73, 9504.
doi: 10.1021/jo801959j pmid: 21391701 |
|
|
(h) Zhang, R.; Zhang, D.; Liang, Y.; Zhou, G.; Dong, D. J. Org. Chem. 2011, 76, 2880.
doi: 10.1021/jo101949y pmid: 21391701 |
|
| [16] |
(a) Gao, B. C.; Sun, Y. F.; Wang, J.; Zu, L. W.; Zhang, X.; Liu, W. B. J. Heterocycl. Chem. 2018, 55, 2732.
doi: 10.1002/jhet.v55.12 |
|
(b) Gao, B. C.; Sun, Y. F.; Wang, J.; Chang, C.; Yuan, Z. G.; Tian, Y.; Shi, Y.Liu. W. B. J. Heterocycl. Chem. 2019, 56, 2281.
doi: 10.1002/jhet.v56.8 |
|
|
(c) Gao, B. C.; Sun Y. F. Wang, J.; Yuan, Z. G.; Zu, L. W.; Zhang, X.; Liu, W. B. RSC Adv. 2018, 8, 33625.
doi: 10.1039/C8RA05709E |
|
|
(d) Peter, Z.; Cheuk, K. L. Synlet. 2003, 215.
|
|
|
(e) Atul, G.; Fateh, V. S.; Ashoke, S.; Prakas, R. M. Synlett. 2005, 623.
|
|
|
(f) Vishnu, K. T.; Hardesh, K. M.; Balendu, K.; Brijesh, K.; Vishnu, J. R. Synlet. 2009, 2992.
|
|
| [17] |
Zhou, Q. F.; Zhao, S.; Wang, X.; Lu, T. Chin. J. Org. Chem. 2010, 30, 1652 (in Chinese).
|
|
(周庆发, 赵慎, 王珣, 陆涛, 有机化学. 2010, 30, 1652.)
|
|
| [18] |
(a) Wang, D. P.; Zhang, X. D.; Liang, Y.; Li, J. H. Chin. J. Org. Chem. 2006, 26, 19 (in Chinese).
doi: 10.1002/cjoc.v26:1 |
|
(王德平, 张旭东, 梁云, 李金恒, 有机化学. 2006, 26, 19.)
|
|
|
(b) Lee, J. H.; Kim, W. S.; Lee, Y. Y.; Cho, C. G. Tetrahedron Lett. 2002, 43, 5779.
doi: 10.1016/S0040-4039(02)01182-6 |
|
|
(c) Kim, W. S.; Kim, H. J.; Cho, C. G. J. Am. Chem. Soc. 2003, 125, 14288.
doi: 10.1021/ja037043a |
|
| [19] |
(a) Wang, Y. F.; Deng, W.; Liu, L.; Guo, Q. X. Chin. J. Org. Chem. 2005, 25, 8 (in Chinese).
pmid: 16557307 |
|
(王晔峰, 邓伟, 刘磊, 郭庆祥, 有机化学. 2005, 25, 8.)
pmid: 16557307 |
|
|
(b) Jin, X. Y.; Xiao, Q.; Ju, Y. Chin. J. Org. Chem. 2009, 29, 44 (in Chinese).
pmid: 16557307 |
|
|
(靳玄烨, 肖强, 巨勇, 有机化学. 2009, 29, 44.)
pmid: 16557307 |
|
|
(c) Fairlamb, I. J. S.; Lee, A. F.; Loe-Mie, F. E. M.; Niemelä, E. H.; O'Brien, C. T.; Whitwood, A. C. Tetrahedro. 2005, 61, 9827.
doi: 10.1016/j.tet.2005.07.102 pmid: 16557307 |
|
|
(d) Fairlamb, I. J. S.; O'Brien, C. T.; Lin, Z.; Lam, K. C. Org. Biomol. Chem. 2006, 4, 1213.
pmid: 16557307 |
|
| [20] |
(a) Cerezo, S.; Moreno-Maňas, M.; Pleixats, R. Tetrahedro. 1998, 54, 7813.
doi: 10.1016/S0040-4020(98)00415-3 |
|
(b) Afarinkia, K.; Berna-Canovas, J. Tetrahedron Lett. 2000, 41, 4955.
doi: 10.1016/S0040-4039(00)00744-9 |
|
| [21] |
(a) Mochida, S.; Hirano, K.; Satoh, T.; Miura, M. J. Org. Chem. 2009, 74, 6295.
doi: 10.1021/jo901077r |
|
(b) Luo, T.; Schreiber, S. L. Angew. Chem.. Int. Ed. 2007, 46, 8250.
doi: 10.1002/anie.v46:43 |
|
| [22] |
(a) Zhu, X. F.; Henry, C. E.; Wang, J.; Dudding, T.; Kwon, O. Org. Lett. 2005, 7, 1387.
doi: 10.1021/ol050203y pmid: 18537252 |
|
(b) Dudding, T.; Kwon, O.; Mercier, E. Org. Lett. 2006, 8, 3643.
doi: 10.1021/ol061095y pmid: 18537252 |
|
|
(c) Usachev, B. I.; Obydennov, D. L.; Röschenthaler, G. V.; Sosnovskikh, V. Y. Org. Lett. 2008, 10, 2857.
doi: 10.1021/ol800992z pmid: 18537252 |
| [1] | 刘杰, 韩峰, 李双艳, 陈天煜, 陈建辉, 徐清. 无过渡金属参与甲基杂环化合物与醇的选择性有氧烯基化反应[J]. 有机化学, 2024, 44(2): 573-583. |
| [2] | 贝文峰, 潘健, 冉冬梅, 刘伊琳, 杨震, 冯若昆. 基于钴催化吲哚酰胺与二炔和单炔的[4+2]环化反应合成γ-咔啉酮[J]. 有机化学, 2023, 43(9): 3226-3238. |
| [3] | 唐菁, 罗文坤, 周俊. 氮杂螺[4.5]三烯酮衍生物的合成研究进展[J]. 有机化学, 2023, 43(9): 3006-3034. |
| [4] | 樊思捷, 董武恒, 梁彩云, 王贵超, 袁瑶, 尹作栋, 张兆国. 可见光诱导的自由基环化反应构建4-芳基-1,2-二氢萘类化合物[J]. 有机化学, 2023, 43(9): 3277-3286. |
| [5] | 冯莹珂, 王贺, 崔梦行, 孙然, 王欣, 陈阳, 李蕾. 可见光诱导的新型官能化芳基异腈化合物的二氟烷基化环化反应[J]. 有机化学, 2023, 43(8): 2913-2925. |
| [6] | 张素珍, 张文文, 杨慧, 顾庆, 游书力. 铑催化2-烯基苯酚与炔烃的对映体选择性螺环化反应[J]. 有机化学, 2023, 43(8): 2926-2933. |
| [7] | 陈玉琢, 孙红梅, 王亮, 胡方芝, 李帅帅. 基于α-氢迁移策略构建杂环骨架的研究进展[J]. 有机化学, 2023, 43(7): 2323-2337. |
| [8] | 蔡荣斌, 李冰, 周琪, 朱隆懿, 罗军. 4,8,9,10-四官能化的2-氮杂金刚烷及其2-氮杂原金刚烷骨架异构体的合成[J]. 有机化学, 2023, 43(6): 2217-2225. |
| [9] | 孙李星, 孙婷婷, 王海清, 吴淑芳, 王小烨, 刘天雅, 张宇辰. Lewis酸催化下3-烷基-2-吲哚烯与α,β-不饱和N-磺酰基亚胺的[2+4]环化反应[J]. 有机化学, 2023, 43(6): 2178-2188. |
| [10] | 任志军, 罗维纬, 周俊. 银介导的N-芳基丙烯酰胺串联环化反应研究进展[J]. 有机化学, 2023, 43(6): 2026-2039. |
| [11] | 孔德亮, 戴闻, 赵怡玲, 陈艺林, 朱红平. 脒基胺硼基硅宾与单酮和二酮的氧化环加成反应研究[J]. 有机化学, 2023, 43(5): 1843-1851. |
| [12] | 李靖鹏, 黄顺桃, 杨棋, 李伟强, 刘腾, 黄超. 利用连续流动技术合成(Z)-N-乙烯基取代N,O-缩醛[J]. 有机化学, 2023, 43(4): 1550-1558. |
| [13] | 南江, 黄冠杰, 胡岩, 王波. 钌催化喹唑啉酮与碳酸亚乙烯酯的C—H [4+2]环化反应[J]. 有机化学, 2023, 43(4): 1537-1549. |
| [14] | 曾成富, 何媛, 李清, 董琳. Ir(III)催化新型三组分串联三氟乙氧基化反应并一锅法构建复杂酰胺化合物[J]. 有机化学, 2023, 43(3): 1115-1123. |
| [15] | 王海清, 杨爽, 张宇辰, 石枫. 邻羟基苄醇参与的催化不对称反应研究进展[J]. 有机化学, 2023, 43(3): 974-999. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||