有机化学 ›› 2021, Vol. 41 ›› Issue (2): 582-593.DOI: 10.6023/cjoc202006050 上一篇 下一篇
综述与进展
余述燕a,*( ), 高丽宏a, 闫溢哲b, 尹志刚a, 商永嘉c,*(
), 高丽宏a, 闫溢哲b, 尹志刚a, 商永嘉c,*( )
)
收稿日期:2020-06-23
修回日期:2020-07-28
发布日期:2020-08-19
通讯作者:
余述燕, 商永嘉
作者简介:基金资助:
Shuyan Yua,*( ), Lihong Gaoa, Yizhe Yanb, Zhigang Yina, Yongjia Shangc,*(
), Lihong Gaoa, Yizhe Yanb, Zhigang Yina, Yongjia Shangc,*( )
)
Received:2020-06-23
Revised:2020-07-28
Published:2020-08-19
Contact:
Shuyan Yu, Yongjia Shang
Supported by:文章分享
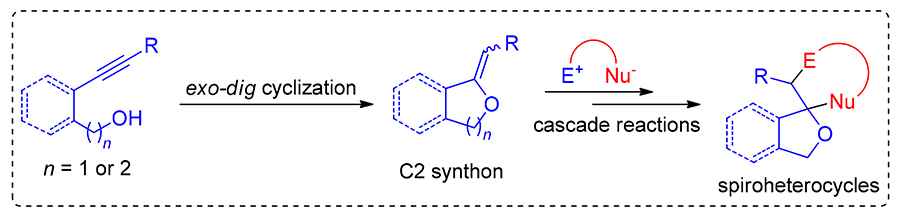
螺杂环化合物独特的立体结构和丰富的理化特性, 激发了研究工作者对其高效合成方法的持续关注. 炔醇在过渡金属作用下经exo-dig式分子内环化可原位形成环外烯醇醚, 其作为一类高活性的C2合成子, 能够与同时具有亲电和亲核特性的“双亲性底物”发生串联反应, 实现螺杂环骨架的快速构建. 综述了近年来炔醇分子内环化促发的串联反应在螺杂环化合物合成中的应用进展, 以期激发更多相关研究工作的设计与报道. 按照参与螺环构建的“双亲性底物”原子数目的不同进行分类, 重点阐述了反应采用的催化体系和反应机制, 分析了目前该领域存在的挑战, 并对未来的发展进行了展望.
余述燕, 高丽宏, 闫溢哲, 尹志刚, 商永嘉. 炔醇分子内环化促发的串联反应在螺杂环化合物合成中的应用[J]. 有机化学, 2021, 41(2): 582-593.
Shuyan Yu, Lihong Gao, Yizhe Yan, Zhigang Yin, Yongjia Shang. Application of Cascade Reactions in the Synthesis of Sprio-hetero- cycles Initiated by Intramolecular Cyclization of Alkynols[J]. Chinese Journal of Organic Chemistry, 2021, 41(2): 582-593.
| [1] |
Krapcho, A.P. Synthesis 1974, 383.
|
|
Lovering, F.; Bikker, J.; Humblet, C. J. Med. Chem. 2009, 52,6752.
doi: 10.1021/jm901241e |
|
|
Nai, G.X.; Dai, R.Q. Technol. Dev. Chem. Ind. 2012, 41, 6. (in Chinese)
|
|
|
赖谷仙, 戴日强, 化工技术与开发,2012, 41, 6.).
|
|
|
Zou, L.; Wang, C.S.; Liang, B. New Chem. Mater. 2013, 41, 12. (in Chinese)
|
|
|
邹琳, 王长松, 梁兵, 化工新型材料,2013, 41, 12.).
|
|
|
Fan, K.Q.; Wang, X.B.; Ma, Y.P.; Yang, H.R.; Han, G.L.; Zhou, L.M.; Fang, S.M. New J. Chem. 2020, 44, 8351.
doi: 10.1039/D0NJ01269F |
|
| [2] |
Wei, R.B.; Liang, Y. Chin. J. Org. Chem. 2008, 28, 1501. (in Chinese)
|
|
魏荣宝, 梁娅, 有机化学,2008, 28, 1501.).
|
|
|
Li, F.F.; Wang, L.; Chen, S.Y.; Zhu, H.M.; Ouyang, G.P. Chem. Res. Appl. 2012, 24, 1181. (in Chinese)
|
|
|
李飞飞, 王磊, 陈舒忆, 朱红梅, 欧阳贵平, 化学研究与应用,2012, 24, 1181.).
|
|
|
Wei, R.B.; Zhang, D.W.; Liu, B.; Liu, Y.; Jia, C.X. Chin. J. Org. Chem. 2009, 29, 517. (in Chinese)
|
|
|
魏荣宝, 张大为, 刘博, 刘洋, 李文丽, 贾辰熙, 有机化学,2009, 29, 517.).
|
|
|
Michael, J.B. Carbon 1997, 35, 1.
doi: 10.1016/S0008-6223(96)00119-4 |
|
| [3] |
Rios, R. Chem. Soc. Rev. 2012, 41, 1060.
doi: 10.1039/C1CS15156H |
| [4] |
Kotha, S.; Panguluri, N.R.; Ali, R. Eur. J. Org. Chem. 2017, 5316.
|
| [5] |
Li, X.F. Ph. D. Dissertation, Tianjing University, Tianjing, 2003. (in Chinese)
|
|
李筱芳, 博士论文, 天津大学, 天津,2003. ).
|
|
| [6] |
Alcaide, B.; Almendros, P.; Alonso, J.M. Molecules 2011, 16, 7815.
doi: 10.3390/molecules16097815 pmid: 22143545 |
|
Zeng, X.M. Chem. Rev. 2013, 113, 6864.
doi: 10.1021/cr400082n pmid: 22143545 |
|
|
Alcaide, B.; Almendros, P. Acc. Chem. Res. 2014, 47, 939.
doi: 10.1021/ar4002558 pmid: 22143545 |
|
| [7] |
Solomon, V.R.; Lee, H. Curr. Med. Chem. 2011, 18, 1488.
doi: 10.2174/092986711795328382 |
|
Afzal, O.; Kumar, S.; Haider, M.R.; Ali, M.R.; Kumar, R.; Jaggi, M.; Bawa, S. Eur. J. Med. Chem. 2015, 97, 871.
doi: 10.1016/j.ejmech.2014.07.044 |
|
| [8] |
Kouznetsov, V.V.; Mendez, L. Y. V.; Gomez, C. M. M. Curr. Org. Chem. 2005, 9, 141.
doi: 10.2174/1385272053369196 |
|
Kouznetsov, V.V. Tetrahedron 2009, 65, 2721.
doi: 10.1016/j.tet.2008.12.059 |
|
|
Fochi, M.; Caruana, L.; Bernardi, L. Synthesis 2014, 46, 135.
doi: 10.1055/s-00000084 |
|
| [9] |
Barluenga, J.; Mendoza, A.; Rodríguez, F.; Fañanás, F.J. Angew. Chem. Int. Ed. 2008, 47, 7044.
doi: 10.1002/anie.v47:37 |
| [10] |
Wang, L.; Liu, L.Y.; Chang, W.X.; Li, J. J. Org. Chem. 2018, 83, 7799.
doi: 10.1021/acs.joc.8b00691 |
| [11] |
Aho, J.E.; Pihko, P.M.; Rissa, T.K. Chem. Rev. 2005, 105, 4406.
doi: 10.1021/cr050559n |
| [12] |
Uckun, F.M.; Mao. C.; Vassilev, A.O.; Huang, H.; Jan, S.T. Bioorg. Med. Chem. Lett. 2000, 10, 541.
pmid: 10741549 |
|
Barun, O.; Kumar, K.; Sommer, S.; Langerak, A.; Mayer, T.U.; Muller, O.; Waldman, H. Eur. J. Org. Chem. 2005, 4773.
pmid: 10741549 |
|
| [13] |
Mead, K.T.; Brewer, B.N. Curr. Org. Chem. 2003, 7, 227.
doi: 10.2174/1385272033372969 |
| [14] |
Barluenga, J.; Mendoza, A.; Rodríguez, F.; Fañanás, F.J. Angew. Chem. Int. Ed. 2009, 48, 1644.
doi: 10.1002/anie.200805519 |
| [15] |
Wu, H.; He, Y.P.; Gong, L.Z. Org. Lett. 2013, 15, 460.
doi: 10.1021/ol303188u |
| [16] |
Liang, M. M.S. Thesis, Shangdong University, Jinan, 2018. (in Chinese)
|
|
梁曼, 硕士论文, 山东大学, 济南,2018. ).
|
|
| [17] |
Wang, X.H.; Dong, S.L.; Yao, Z.L.; Feng, L.; Daka, P.; Wang, H.; Xu, Z.H. Org. Lett. 2014, 16, 22.
doi: 10.1021/ol4033286 |
| [18] |
Li, J.; Lin, L.; Hu, B.; Lian, X.; Wang, G.; Liu, X; Feng, X. Angew. Chem. Int. Ed. 2016, 55, 6075.
doi: 10.1002/anie.v55.20 |
| [19] |
Gong, J.; Wan, Q.; Kang, Q. Adv. Synth. Catal. 2018, 360, 4031.
doi: 10.1002/adsc.v360.21 |
| [20] |
Willis, N.J.; Bray, C.D. Chem .- Eur. J. 2012, 18, 9160.
doi: 10.1002/chem.v18.30 pmid: AF8C4C72-6A1E-427C-A6BD-D0AEDAA07AA8 |
|
Bai, W.J.; David, J.G.; Feng, Z.G.; Weaver, M. G. Wu, K. L.; Pettus, T. R. R. Acc. Chem. Res. 2014, 47, 3655.
doi: 10.1021/ar500330x pmid: AF8C4C72-6A1E-427C-A6BD-D0AEDAA07AA8 |
|
|
Caruana, L.; Fochi, M.; Bernardi, L. Molecules 2015, 20, 11733;.
doi: 10.3390/molecules200711733 pmid: AF8C4C72-6A1E-427C-A6BD-D0AEDAA07AA8 |
|
|
Ai, W.; Liao, D.; Lei, X. Chin. J. Org. Chem. 2015, 35, 1615. (in Chinese)
doi: 10.6023/cjoc201504031 pmid: AF8C4C72-6A1E-427C-A6BD-D0AEDAA07AA8 |
|
|
艾文英, 廖道红, 雷晓光, 有机化学,2015, 35, 1615.).
doi: 10.6023/cjoc201504031 pmid: AF8C4C72-6A1E-427C-A6BD-D0AEDAA07AA8 |
|
| [21] |
Liang, M.; Zhang, S.; Jia, J.; Tung, C.H.; Wang, J.W.; Xu, Z.H. Org. Lett. 2017, 19, 2526.
doi: 10.1021/acs.orglett.7b00804 |
| [22] |
Wang, C.S.; Cheng, Y.C.; Zhou, J.; Mei, G.J.; Wang, S.L.; Shi, F. J. Org. Chem. 2018, 83, 13861.
doi: 10.1021/acs.joc.8b02186 |
| [23] |
Gharpure, S.J.; Nanda, S.K.; Shelke, Y.G. Chem .- Eur. J. 2017, 23, 10007.
doi: 10.1002/chem.v23.42 |
| [24] |
Stierle, A.A.; Stierle, D.B.; Kelly, K. J. Org. Chem. 2006, 71, 5357.
pmid: 16808526 |
| [25] |
Arto, T.; Santa-Marĭa, I.S.; Chiara, M.D.; Fañanás, F.J.; Rodríguez, F. Eur. J. Org. Chem. 2016, 5876.
|
| [26] |
Elsharif, A.M. Orient. J. Chem. 2019, 35, 658.
doi: 10.13005/ojc |
|
de Fatima, A.; Braga, T.C.; Neto, L. D. S.; Terra, B.S.; Oliveira, B. G. F.; da Silva, D.L.; Modolo, L.V. J. Adv. Res. 2015, 6, 363.
doi: 10.1016/j.jare.2014.10.006 |
|
|
Wang, B.Z.; Xu, X.Y.; Tao, Y.C.; Ke, S.Y.; Qian, X.H.; Li, Z. Chin. J. Pestic. Sci. 2010, 12, 429. (in Chinese)
|
|
|
王宝珠, 徐晓勇, 陶玉成, 柯少勇, 钱旭红, 李忠, 农药学学报,2010, 12, 429.).
|
|
| [27] |
Kappe, C.O. Acc. Chem. Res. 2000, 33, 879.
doi: 10.1021/ar000048h |
|
Gong, L.Z.; Chen, X.H.; Xu, X.Y. Chem .- Eur. J. 2007, 13, 8920.
doi: 10.1002/(ISSN)1521-3765 |
|
|
Heravi, M.M.; Moradi, R.; Mohammadkhani, L.; Moradi, B. Mol. Diversity 2018, 22, 751.
doi: 10.1007/s11030-018-9841-4 |
|
| [28] |
Yu, S.Y.; Wu, J.X.; Lan, H.B.; Gao, L.H.; Qian, H.Y.; Fan, K.Q.; Yin, Z.G. Org. Lett. 2020, 22, 102.
doi: 10.1021/acs.orglett.9b04015 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
Yu, S.Y.; Gao, L.H.; Lan, H.B.; Qian, H.Y.; Yin, Z.G.; Shang, Y.J. Chin. J. Org. Chem. 2020, 40, 2714. (in Chinese)
doi: 10.6023/cjoc202004034 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
|
余述燕, 高丽宏, 兰宏兵, 钱恒玉, 尹志刚, 商永嘉, 有机化学,2020, 40, 2714.).
doi: 10.6023/cjoc202004034 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
|
Yu, S.Y.; Wu, J.X.; Lan, H.B.; Xu, H.W.; Shi, X.F.; Zhu, X.W.; Yin, Z.G. RSC Adv. 2018, 8, 33968.
doi: 10.1039/C8RA07212D pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
|
Yu, S.Y.; Gao, L.H.; Wu, J.X.; Lan, H.B.; Ma, Y.; Yin, Z.G. Chem. Pap. 2020, 74, 3303.
doi: 10.1007/s11696-020-01159-5 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
|
Yu, S.Y.; Wu, J.X.; He, X.W.; Shang, Y.J. Appl. Organomet. Chem. 2018, 32, e4156.
doi: 10.1002/aoc.v32.3 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
|
Yu, S.Y.; Zhang, Z.Q.; Yu, Z.Y.; Shang, Y.J. Appl. Organomet. Chem. 2014, 28, 657.
doi: 10.1002/aoc.3176 pmid: b44c991b-11cd-4d5b-b68e-805f7583b119 |
|
| [29] |
Yao, H.L.; Wang, J.; Tong, R.B. Chem. Rev. 2017, 17, 1109.
|
|
Wang, J.; Tong, R.B. J. Org. Chem. 2016, 81, 4325.
doi: 10.1021/acs.joc.6b00788 |
|
| [30] |
Cala, L.; Mendoza, A.; Fañanás, F.J.; Rodríguez, F. Chem. Commun. 2013, 49, 2715.
doi: 10.1039/c3cc00118k |
| [31] |
Kambale, D.A.; Thorat, S.S.; Pratapure, M.S.; Gonnade, R.G.; Kontham, R. Chem. Commun. 2017, 53, 6641.
doi: 10.1039/C7CC03668J |
| [32] |
Teng, Q.; Qi, J.L.; Zhou, L.; Xu, Z.H.; Tung, C.H. Org. Chem. Front. 2018, 5, 990.
doi: 10.1039/C7QO01005B |
| [33] |
Jackson, S.K.; Banfield, S.C, Kerr, M.A. Org. Lett. 2005, 7, 1215.
doi: 10.1021/ol047498k |
|
Uliana, M.P.; Servilha, B.M.; Alexopoulos, O.; de Oliveira, K.T.; Tormena, C.F.; Ferreira, M. A. B.; Brocksom, T.J. Tetrahedron 2014, 70, 6963.
doi: 10.1016/j.tet.2014.07.088 |
|
| [34] |
Liao, L.H.; Shu, C.; Zhang, M.M.; Liao, Y.J.; Hu, X.Y.; Zhang, Y.H.; Wu, Z.J.; Yuan, W.C.; Zhang, X.M. Angew. Chem. Int. Ed. 2014, 53, 10471.
doi: 10.1002/anie.201405689 |
|
Sun. X.X.; Zhang, H.H.; Li, G.H.; Meng, L.; Shi, F. Chem. Commun. 2016, 52, 2968.
doi: 10.1039/C5CC09145D |
|
|
Shu, C.; Liao, L.H; Liao. Y. J.; Hu, X.Y.; Zhang, Y.H.; Yuan, W.C.; Zhang, X.M. Eur. J. Org. Chem. 2014, 4467.
|
|
| [35] |
Jasper, A.; Schepmann, D.; Lehmkuhl, K.; Vela, J.M.; Buschmann, H.; Holenz, J.; Wünsch, B. Eur. J. Med. Chem. 2012, 53, 327.
doi: 10.1016/j.ejmech.2012.04.018 |
|
Strachan, J.; Farias, J.J.; Zhang, J.; Caldwell, W.S.; Bhatti, B.S. Bioorg. Med. Chem. Lett. 2012, 22, 5089.
doi: 10.1016/j.bmcl.2012.05.108 |
|
| [36] |
Sweeney, J.B. Chem. Soc. Rev. 2002, 31, 247.
pmid: 12357722 |
| [37] |
Huisgen, R.; Scheer, W.; Mäder, H. Angew. Chem. Int. Ed. 1969, 8, 602.
|
| [38] |
Lu, P.F. Tetrahedron 2010, 66, 2549.
doi: 10.1016/j.tet.2010.01.077 |
|
Pineschi, M. Eur. J. Org. Chem. 2006, 4979.
|
|
|
Schneider, C. Angew. Chem. Int. Ed. 2009, 48, 2082.
doi: 10.1002/anie.v48:12 |
|
| [39] |
Wang, B.; Liang, M.; Tang, J.; Deng, Y.T.; Zhao, J.H.; Sun, H.; Tung, C.H.; Jia, J.; Xu, Z.H. Org. Lett. 2016, 18, 4614.
doi: 10.1021/acs.orglett.6b02253 |
| [40] |
Wagner, B.; Hiller, W.; Ohno, H.; Krause, N. Org. Biomol. Chem. 2016, 14, 1579.
doi: 10.1039/C5OB02453F |
| [41] |
Sun, W.S.; Zhu, G.M.; Wu, C.Y.; Hong, L.; Wang, R. Chem .- Eur. J. 2012, 18, 6737.
doi: 10.1002/chem.201200478 |
|
Singh, K.; Pramanik, S.; Hamlin, T.A.; Mondal, B.; Das, D.; Saha, J. Chem. Commun. 2019, 55, 7069.
doi: 10.1039/C9CC03393A |
|
| [42] |
Kusama, H.; Ebisawa, M.; Funama, H.; Iwasawa, N. J. Am. Chem. Soc. 2009, 131, 45, 16352.
|
| [43] |
Yao, T.; Zhang, X.; Larock, R.C. J. Am. Chem. Soc. 2004, 126, 40, 11164.
doi: 10.1021/ja034986z |
| [44] |
Patil, N.T.; Wu, H.; Yamamoto, Y. J. Org. Chem. 2005, 70, 4531.
doi: 10.1021/jo050191u |
|
Oh, C.H.; Reddy, V.R.; Kim, A.; Rhim, C.Y. Tetrahedron Lett. 2006, 47, 5307.
doi: 10.1016/j.tetlet.2006.05.119 |
|
|
Liu, Y.H.; Zhou, S. Org. Lett. 2005, 6, 4609.
|
|
|
Liu, F. Ph. D. Dissertation, East China Normal University, Shanghai,2013. (in Chinese)
|
|
|
刘锋, 博士论文, 华东师范大学, 上海,2013. ).
|
|
|
Di, X.Y. Ph. D. Dissertation, East China Normal University, Shanghai,2019. (in Chinese)
|
|
|
底晓煜, 博士论文, 华东师范大学, 上海,2019. ).
|
|
| [45] |
Qi, J.L.; Teng, Q.; Thirupathi, N.; Tung, C.H.; Xu, Z.H. Org. Lett. 2019, 21, 692.
doi: 10.1021/acs.orglett.8b03880 |
| [46] |
Barluenga, J.; Calleja, J.; Mendoza, A.; Rodrígue, F.; Fañanás, F J. Chem .- Eur. J. 2010, 16, 7110.
doi: 10.1002/chem.201000515 |
| [47] |
Wang, X.; Yao, Z.; Dong, S.; Wei, F.; Wang, H.; Xu, Z.H. Org. Lett. 2013, 15, 2234.
doi: 10.1021/ol400803f |
| [1] | 曾成富, 何媛, 李清, 董琳. Ir(III)催化新型三组分串联三氟乙氧基化反应并一锅法构建复杂酰胺化合物[J]. 有机化学, 2023, 43(3): 1115-1123. |
| [2] | 李硕, 王明亮, 周来运, 王兰芝. 磁性纳米负载对甲苯磺酸催化串联合成稠合多环的1,5-苯并氧氮杂䓬类化合物[J]. 有机化学, 2023, 43(11): 3977-3988. |
| [3] | 石云, 肖婷, 夏冬, 杨文超. 三氟甲硫基自由基引发不饱和烃的串联反应[J]. 有机化学, 2022, 42(9): 2715-2727. |
| [4] | 赵晓正, 凌琴琴, 曹桂妍, 火星, 赵小龙, 苏瀛鹏. 炔丙醇类化合物参与的环化反应研究进展[J]. 有机化学, 2022, 42(9): 2605-2639. |
| [5] | 周旭煜, 张爱君, 张庆庆, 刘庆安, 宣俊. 可见光诱导4-色满酮合成: 醋酸碘苯促进的α-酮酸与邻-烯丙氧基芳醛的自由基串联环化反应[J]. 有机化学, 2022, 42(8): 2488-2495. |
| [6] | 侯金松, 杨高升. 三(邻二甲胺基苄基)钇催化脂肪胺对烯腈的插入串联反应[J]. 有机化学, 2022, 42(7): 2070-2078. |
| [7] | 袁飞, 赵艳, 郭青松, 尹福丹, 赖金荣, 念倍芳, 张明, 汤峨. 乙烯基硒盐参与的串联反应合成1-[1-(胺基)环丙基]酮化合物[J]. 有机化学, 2022, 42(6): 1759-1769. |
| [8] | 孙鑫, 屈超凡, 马超蕊, 赵筱薇, 柴国璧, 江智勇. 光氧化还原催化串联自由基加成反应构建1,4-二酮官能团化喹喔啉-2(1H)-酮衍生物[J]. 有机化学, 2022, 42(5): 1396-1406. |
| [9] | 肖立伟, 刘光仙, 任萍, 吴彤桐, 卢玉伟, 孔洁. 单质硫: 合成含硫杂环的优质硫源[J]. 有机化学, 2022, 42(4): 1002-1012. |
| [10] | 乔辉杰, 杨利婷, 陈雅, 王嘉琳, 孙武轩, 董昊博, 王云威. 温和条件下高效合成咪唑并杂环-肼类衍生物的三组分串联反应[J]. 有机化学, 2022, 42(4): 1188-1197. |
| [11] | 罗享豪, 谢益碧, 黄年玉, 王龙. 基于原位捕获异腈的Ugi四组分反应及其后修饰串联反应: 一锅法合成含氮杂环化合物[J]. 有机化学, 2022, 42(3): 838-846. |
| [12] | 洪科苗, 黄晶晶, 姚铭瀚, 徐新芳. 氮宾/炔烃复分解串联反应研究进展[J]. 有机化学, 2022, 42(2): 344-352. |
| [13] | 王明亮, 尹刘燕, 温甜甜, 张晓, 高杰, 王兰芝. 多官能团化的1,5-苯并二氮杂䓬类化合物的绿色合成[J]. 有机化学, 2022, 42(1): 160-171. |
| [14] | 郭钰钰, 陈祥杰, 李师伍, 蔡志华, 何林. 2-芳基乙烯苯并咪唑串联反应合成多取代二氢吡啶并[1,2-a]苯并咪唑衍生物[J]. 有机化学, 2021, 41(9): 3692-3700. |
| [15] | 杨凯, 刘美娟, 张毓娜, 占佳琦, 邓璐璇, 郑雪洁, 周永军, 汪朝阳. 基于2-卤苯甲酰胺合成苯并杂环化合物的研究进展[J]. 有机化学, 2021, 41(6): 2175-2187. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||