有机化学 ›› 2023, Vol. 43 ›› Issue (8): 2905-2912.DOI: 10.6023/cjoc202302023 上一篇 下一篇
研究论文
收稿日期:2023-02-23
修回日期:2023-03-23
发布日期:2023-04-13
基金资助:Received:2023-02-23
Revised:2023-03-23
Published:2023-04-13
Contact:
*E-mail: Supported by:文章分享
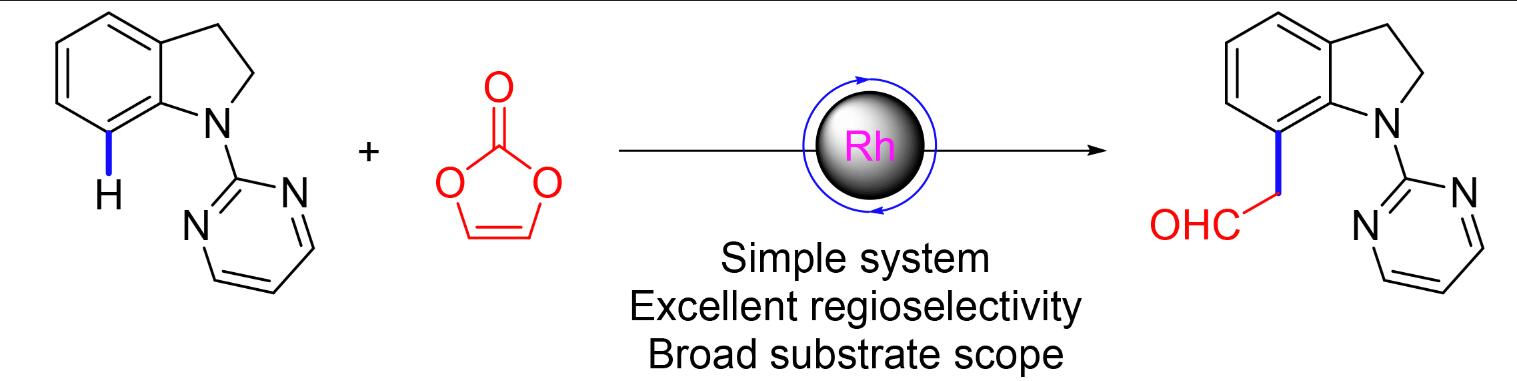
发展了一种铑催化碳酸亚乙烯酯与吲哚啉C(7)位C—H甲酰甲基化反应合成芳基乙醛化合物的高效方法. 该反应条件温和, 区域选择性专一, 底物官能团兼容性好, 产物收率较高.
张彦波, 孙萌. 铑催化碳酸亚乙烯酯与吲哚啉C(7)位C—H甲酰甲基化反应[J]. 有机化学, 2023, 43(8): 2905-2912.
Yanbo Zhang, Meng Sun. Rh(III)-Catalyzed C(7)—H Formylmethylation of Indoline with Vinylene Carbonate[J]. Chinese Journal of Organic Chemistry, 2023, 43(8): 2905-2912.
| Entry | Catalyst | Additive | Solvent | Yield/% |
|---|---|---|---|---|
| 1 | [Cp*RhCl2]2 | AgSbF6 | THF | 67 |
| 2 | [Cp*RhCl2]2 | AgSbF6 | DCE | 78 |
| 3 | [Cp*RhCl2]2 | AgSbF6 | Toluene | 92 |
| 4 | [Cp*RhCl2]2 | AgSbF6 | DME | 68 |
| 5 | [Cp*RhCl2]2 | AgSbF6 | Dioxane | 83 |
| 6 | [Cp*RhCl2]2 | AgSbF6 | TFE | n.r. |
| 7 | [Cp*RhCl2]2 | AgOTf | Toluene | 79 |
| 8 | [Cp*RhCl2]2 | AgNTf2 | Toluene | 85 |
| 9 | [Cp*RhCl2]2 | AgOAc | Toluene | n.r. |
| 10 | [Cp*RhCl2]2 | AgBF4 | Toluene | 81 |
| 11c | [Cp*RhCl2]2 | AgSbF6 | Toluene | 66 |
| 12d | [Cp*RhCl2]2 | AgSbF6 | Toluene | 80 |
| 13 | [Cp*RhCl2]2 | Toluene | n.r. | |
| 14 | AgSbF6 | Toluene | n.r. | |
| 15 | RhCl3 | AgSbF6 | Toluene | n.r. |
| 16 | Rh2(OAc)4 | AgSbF6 | Toluene | n.r. |
| Entry | Catalyst | Additive | Solvent | Yield/% |
|---|---|---|---|---|
| 1 | [Cp*RhCl2]2 | AgSbF6 | THF | 67 |
| 2 | [Cp*RhCl2]2 | AgSbF6 | DCE | 78 |
| 3 | [Cp*RhCl2]2 | AgSbF6 | Toluene | 92 |
| 4 | [Cp*RhCl2]2 | AgSbF6 | DME | 68 |
| 5 | [Cp*RhCl2]2 | AgSbF6 | Dioxane | 83 |
| 6 | [Cp*RhCl2]2 | AgSbF6 | TFE | n.r. |
| 7 | [Cp*RhCl2]2 | AgOTf | Toluene | 79 |
| 8 | [Cp*RhCl2]2 | AgNTf2 | Toluene | 85 |
| 9 | [Cp*RhCl2]2 | AgOAc | Toluene | n.r. |
| 10 | [Cp*RhCl2]2 | AgBF4 | Toluene | 81 |
| 11c | [Cp*RhCl2]2 | AgSbF6 | Toluene | 66 |
| 12d | [Cp*RhCl2]2 | AgSbF6 | Toluene | 80 |
| 13 | [Cp*RhCl2]2 | Toluene | n.r. | |
| 14 | AgSbF6 | Toluene | n.r. | |
| 15 | RhCl3 | AgSbF6 | Toluene | n.r. |
| 16 | Rh2(OAc)4 | AgSbF6 | Toluene | n.r. |
| [12] |
(e) Park, M. S.; Moon, K.; Oh, H.; Lee, J. Y.; Ghosh, P.; Kang, J. Y.; Park, J. S.; Mishra, N. K.; Kim, I. S. Org. Lett. 2021, 23, 5518.
|
|
(f) Wang, L.; Jiang, K.-C.; Zhang, N.; Zhang, Z.-H. Asian J. Org. Chem. 2021, 10, 1671.
|
|
|
(g) Huang, X.; Xu, Y.; Li, J.; Lai, R.; Luo, Y.; Wang, Q.; Yang, Z.; Wu, Y. Chin. Chem. Lett. 2021, 32, 3518.
|
|
|
(h) Wang, Z.-H.; Wang, H.; Wang, H.; Li, L.; Zhou, M.-D. Org. Lett. 2021, 23, 995.
|
|
|
(i) Wang, C.; Fan, X.; Chen, F.; Qian, P.-C.; Cheng, J. Chem. Commun. 2021, 57, 3929.
|
|
|
(j) Hu, Y.; Nan, J.; Yin, J.; Huang, G.; Ren, X.; Ma, Y. Org. Lett. 2021, 23, 8527.
|
|
|
(k) Kato, M.; Ghosh, K.; Nishii, Y.; Miura, M. Chem. Commun. 2021, 57, 8280.
|
|
|
(l) Hu, W.; Wang, X.; Yu, X.; Zhu, X.; Hao, X.-Q.; Song, M.-P. Asian J. Org. Chem. 2021, 10, 2557.
|
|
|
(m) Nan, J.; Ma, Q.; Yin, J.; Liang, C.; Tian, L.; Ma, Y. Org. Chem. Front. 2021, 8, 1764.
|
|
|
(n) Shen, B.; Liu, S.; Zhu, L.; Zhong, K.; Liu, F.; Chen, H.; Bai, R.; Lan, Y. Organometallics 2020, 39, 2813.
|
|
| [13] |
(a) Kato, M.; Ghosh, K.; Nishii, Y.; Miura, M. Chem. Commun. 2021, 57, 8280.
|
|
(b) Liu, M.; Yan, K. L.; Wen, J. W.; Shang, W. D.; Sui, X. L.; Wang, X. Adv. Synth. Catal. 2022, 364, 1580.
|
|
|
(c) Kumar, P.; Kapur, M. Chem. Commun. 2022, 58, 4476.
|
|
| [14] |
(a) Ackermann, L.; Lygin, A. V. Org. Lett. 2011, 13, 3332.
|
|
(b) Leitch, J. A.; McMullin, C. L.; Mahon, M. F.; Bhonoah, Y.; Frost, C. G. ACS Catal. 2017, 7, 2616.
|
|
| [1] |
(a) Ishikura, M.; Abe, T.; Choshi, T.; Hibino, S. Nat. Prod. Rep. 2013, 30, 694.
|
|
(b) Chang, L.; Podoll, J. D.; Wang, W.; Walls, S.; O'Rourke, C. P.; Wang, X. J. Med. Chem. 2014, 57, 3803.
|
|
|
(c) Ishikura, M.; Abe, T.; Choshi, T.; Hibino, S. Nat. Prod. Rep. 2015, 32, 1389.
|
|
|
(d) Manikandan, A.; Moharil, P.; Sathishkumar, M.; Muñoz-Garay, C.; Sivakumar, A. Eur. J. Med. Chem. 2017, 141, 417.
|
|
| [2] |
(a) Owa, T.; Yokoi, A.; Yamazaki, K.; Yoshimatsu, K.; Yamori, T.; Nagasu, T. J. Med. Chem. 2002, 45, 4913.
|
|
(b) Mohan, R.; Banerjee, M.; Ray, A.; Manna, T.; Wilson, L.; Owa, T.; Bhattacharyya, B.; Panda, D. Biochemistry 2006, 45, 5440.
|
|
|
(c) Ferandin, Y.; Bettayeb, K.; Kritsanida, M.; Lozach, O.; Polychronopoulos, P.; Magiatis, P.; Skaltsounis, A.-L.; Meijer, L. J. Med. Chem. 2006, 49, 4638.
|
|
|
(d) Burke, J. P.; Bian, Z.; Shaw, S.; Zhao, B.; Goodwin, C. M.; Belmar, J.; Browning, C. F.; Vigil, D.; Friberg, A.; Camper, D. V.; Rossanese, O. W.; Lee, T.; Olejniczak, E. T.; Fesik, S. W. J. Med. Chem. 2015, 58, 3794.
|
|
|
(e) Takahashi, K.; Kasai, M.; Ohta, M.; Shoji, Y.; Kunishiro, K.; Kanda, M.; Kurahashi, K.; Shirahase, H. J. Med. Chem. 2008, 51, 4823.
|
|
| [3] |
(a) Neufeldt, S. R.; Seigerman, C. K.; Sanford, M. S. Org. Lett. 2013, 15, 2302.
|
|
(b) Lee, S. H.; Jeong, T.; Kim, K.; Kwon, N. Y.; Pandey, A. K.; Kim, H. S.; Ku, J.-M.; Mishra, N. K.; Kim, I. S. J. Org. Chem. 2019, 84, 2307.
|
|
|
(c) Jagtap, R. A.; Samal, P. P.; Vinod, C. P.; Krishnamurty, S.; Punji, B. ACS Catal. 2020, 10, 7312.
|
|
|
(d) Zhou, X.; Yu, S.; Qi, Z.; Kong, L.; Li, X. J. Org. Chem. 2016, 81, 4869.
|
|
|
(e) Premi, C.; Dixit, A.; Jain, N. Org. Lett. 2015, 17, 2598.
|
|
|
(f) Hu, W.; Wang, X.; Yu, X.; Zhu, X.; Hao, X.-Q.; Song, M.-P. Asian J. Org. Chem. 2021, 10, 2557.
|
|
|
(g) Jo, H.; Park, J.; Choi, M.; Sharma, S.; Jeon, M.; Mishra, N. K.; Jeong, T.; Han, S.; Kim, I. S. Adv. Synth. Catal. 2016, 358, 2714.
|
|
|
(h) Ai, W.; Yang, X.; Wu, Y.; Wang, X.; Li, Y.; Yang, Y.; Zhou, B. Chem.-Eur. J. 2014, 20, 17653.
|
|
|
(i) Xu, X.; Zhou, G.; Ju, G.; Wang, D.; Li, B.; Zhao, Y. Chin. Chem. Lett. 2022, 33, 847.
|
|
| [4] |
(a) Urones, B.; Arrayás, R. G.; Carretero, J. C. Org. Lett. 2013, 15, 1120.
|
|
(b) Jiao, L.-Y.; Oestreich, M. Org. Lett. 2013, 15, 5374.
|
|
|
(c) Song, Z.; Samanta, R.; Antonchick, A. P. Org. Lett. 2013, 15, 5662.
|
|
|
(d) Pan, S.; Wakaki, T.; Ryu, N.; Shibata, T. Chem.-Asian J. 2014, 9, 1257.
|
|
|
(e) Wu, M.; Gao, H.; Xu, H.; Yi, W.; Zhou, Z. Chin. Chem. Lett. 2022, 33, 842.
|
|
|
(f) He, Y.; Tian, L.; Chang, X.; Qu, Z.; Huang, Y.; Huang, C.; Sun, Q.; Wang, H. Chin. Chem. Lett. 2022, 33, 2987.
|
|
| [5] |
(a) Wu, Y.; Yang, Y.; Zhou, B.; Li, Y. J. Org. Chem. 2015, 80, 1946.
|
|
(b) Yang, X.-F.; Hu, X.-H.; Feng, C.; Loh, T.-P. Chem. Commun. 2015, 51, 2532.
|
|
| [6] |
(a) Kalyani, D.; Deprez, N. R.; Desai, L. V.; Sanford, M. S. J. Am. Chem. Soc. 2005, 127, 7330.
|
|
(b) Nishikata, T.; Abela, A. R.; Huang, S.; Lipshutz, B. H. J. Am. Chem. Soc. 2010, 132, 4978.
|
|
|
(c) De, P. B.; Pradhan, S.; Banerjee, S.; Punniyamurthy, T. Chem. Commun. 2018, 54, 2494.
|
|
| [7] |
(a) Kim, M.; Mishra, N. K.; Park, J.; Han, S.; Shin, Y.; Sharma, S.; Lee, Y.; Lee, E.-K.; Kwak, J. H.; Kim, I. S. Chem. Commun. 2014, 50, 14249.
|
|
(b) Suzuki, H.; Sasamori, F.; Matsuda, T. Org. Lett. 2022, 24 1141.
|
|
|
(c) Xie, G.; Zhao, Y.; Cai, C.; Deng, G.-J.; Gong, H. Org. Lett. 2021, 23, 410.
|
|
| [8] |
(a) Yan, Q.; Huang, H.; Zhang, H.; Li, M.-H.; Yang, D.; Song, M.-P.; Niu, J.-L. J. Org. Chem. 2020, 85, 11190.
|
|
(b) Kumar, M.; Raziullah; Khan, A. A.; Ahmad, A.; Dutta, H. S.; Kant, R.; Koley, D. J. Org. Chem. 2019, 84, 13624.
|
|
|
(c) Jeon, M.; Mishra, N. K.; De, U.; Sharma, S.; Oh, Y.; Choi, M.; Jo, H.; Sachan, R.; Kim, H. S.; Kim, I. S. J. Org. Chem. 2016, 81, 9878.
|
|
|
(d) Mishra, N. K.; Jeon, M.; Oh, Y.; Jo, H.; Park, J.; Han, S.; Sharma, S.; Han, S. H.; Jung, Y. H.; Kim, I. S. Org. Chem. Front. 2017, 4, 241.
|
|
|
(e) Li, H.; Jie, J.; Wu, S.; Yang, X.; Xu, H. Org. Chem. Front. 2017, 4, 250.
|
|
| [9] |
(a) Ahmad, A.; Dutta, H. S.; Kumar, M.; Khan, A. A.; Raziullah; Koley, D. Org. Lett. 2020, 22, 5870.
|
|
(b) Manisha; Gupta, S. S.; Dhiman, A. K.; Sharma, U. Eur. J. Org. Chem. 2021, 2021, 5443.
|
|
| [10] |
(a) Mishra, A.; Vats, T. K.; Nair, M. P.; Das, A.; Deb, I. J. Org. Chem. 2017, 82, 12406.
|
|
(b) Ahmad, A.; Dutta, H. S.; Khan, B.; Kant, R.; Koley, D. Adv. Synth. Catal. 2018, 360, 1644.
|
|
|
(c) De, P. B.; Banerjee, S.; Pradhan, S.; Punniyamurthy, T. Org. Biomol. Chem. 2018, 16, 5889.
|
|
| [11] |
(a) Li, B. S.; Guo, H. X.; Sun, W.; Sun, M. Tetrahedron Lett. 2022, 99, 153854.
|
|
(b) Mishra, N. K.; Sharma, S.; Park, J.; Han, S.; Kim, I. S. ACS Catal. 2017, 7, 2821.
|
|
| [12] |
(a) Ghosh, K.; Nishii, Y.; Miura, M. ACS Catal. 2019, 9, 11455.
|
|
(b) Ghosh, K.; Nishii, Y.; Miura, M. Org. Lett. 2020, 22, 3547.
|
|
|
(c) Mihara, G.; Ghosh, K.; Nishii, Y.; Miura, M. Org. Lett. 2020, 22, 5706.
|
|
|
(d) Li, X.; Huang, T.; Song, Y.; Qi, Y.; Li, L.; Li, Y.; Xiao, Q.; Zhang, Y. Org. Lett. 2020, 22, 5925.
|
| [1] | 文思, 丁宇浩, 田青于, 葛进, 程国林. 铑(III)催化苯甲亚胺酸乙酯和CF3-亚胺氧锍叶立德C—H 活化/环化反应合成CF3-1H-苯并[de][1,8]萘吡啶[J]. 有机化学, 2024, 44(1): 291-300. |
| [2] | 高晓阳, 翟锐锐, 陈训, 王烁今. 碳酸亚乙烯酯参与C—H键活化反应的研究进展[J]. 有机化学, 2023, 43(9): 3119-3134. |
| [3] | 汤振, 皮超, 吴养洁, 崔秀灵. 铑催化2-芳基-2H-吲唑与硫叶立德的酰甲基化/串联环化反应高效构建6-芳基吲唑并[2,3-a]喹啉类衍生物[J]. 有机化学, 2023, 43(3): 1187-1196. |
| [4] | 刘晓洁, 徐必平, 苏伟平. 铑催化羧酸原位生成酰氟的脱羰Suzuki-Miyaura偶联[J]. 有机化学, 2022, 42(7): 2184-2191. |
| [5] | 庞丽萍, 杨昌杰, 林洪敏, 李心宇, 唐海涛, 潘英明. 多孔有机膦配体聚合物作为可回收配体用于异吲哚啉酮类化合物的合成[J]. 有机化学, 2022, 42(7): 2117-2123. |
| [6] | 王家状, 滕丽果, 熊绍棋, 肖铁波, 江玉波. Rh催化N-磺酰腙的偕-二氟烯丙基化反应[J]. 有机化学, 2022, 42(11): 3658-3667. |
| [7] | 王璐, 邵莺, 陈帆, 钱鹏程, 成江. 铑催化定位基促进芳环C—H键和碳酸亚乙烯酯的缩合得到异香豆素[J]. 有机化学, 2022, 42(1): 242-248. |
| [8] | 马蔚青, 韩莹, 孙晶, 颜朝国. 三组分反应高效合成螺[环戊烷-1,3'-吲哚啉]衍生物[J]. 有机化学, 2021, 41(8): 3180-3191. |
| [9] | 唐灏, 张贝贝, 陈卫东, 骆钧飞. 空气条件下温和高效催化N-吡啶吲哚啉的氧化脱氢[J]. 有机化学, 2021, 41(3): 1131-1137. |
| [10] | 戴雨倩, 李兴伟, 刘丙贤. 三价铑催化通过环己二酮高效构建异香豆素类化合物[J]. 有机化学, 2021, 41(11): 4476-4483. |
| [11] | 赵森, 李淳朴, 许斌, 柳红. 铑催化碳氢二氟烯丙基化/N-碘代丁二酰亚胺介导的环化反应构建含氟3,4-二氢嘧啶并[1,6-a]吲哚-1(2H)-酮衍生物[J]. 有机化学, 2020, 40(6): 1549-1562. |
| [12] | 李文兰, 孙一茼, 姚永超, 许颖, 李鹏, 刘颖杰, 梁德强. 无金属催化非活化烯烃的多氯甲基化/芳基化自由基反应合成含多氯甲基吲哚啉[J]. 有机化学, 2019, 39(6): 1727-1734. |
| [13] | 郝云鹏, 解正峰, 包万睿, 王馨, 石伟. 一种新型比色荧光增强型CN-探针的合成与性能研究[J]. 有机化学, 2018, 38(8): 2109-2115. |
| [14] | 张倩倩, 丁群山, 宋传君, 常俊标. N-叔丁氧羰基吲哚啉-2-羧酸甲酯的不对称合成[J]. 有机化学, 2018, 38(1): 221-227. |
| [15] | 王志惠, 张振锋, 刘燕刚, 张万斌. 烯醇酯的不对称催化氢化研究进展[J]. 有机化学, 2016, 36(3): 447-459. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||
