有机化学 ›› 2024, Vol. 44 ›› Issue (4): 1124-1150.DOI: 10.6023/cjoc202309012 上一篇 下一篇
综述与进展
郭凯杰a, 符昕姝a, 李靖a, 陈艳a, 胡美丽a, 堵锡华a, 谢屿阳b,*( ), 何燕a,*(
), 何燕a,*( )
)
收稿日期:2023-09-11
修回日期:2023-12-06
发布日期:2023-12-15
基金资助:
Kaijie Guoa, Xinshu Fua, Jing Lia, Yan Chena, Meili Hua, Xihua Dua, Yuyang Xieb( ), Yan Hea(
), Yan Hea( )
)
Received:2023-09-11
Revised:2023-12-06
Published:2023-12-15
Contact:
E-mail: Supported by:文章分享

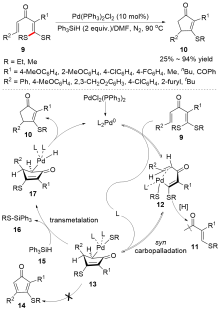
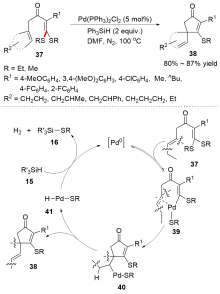
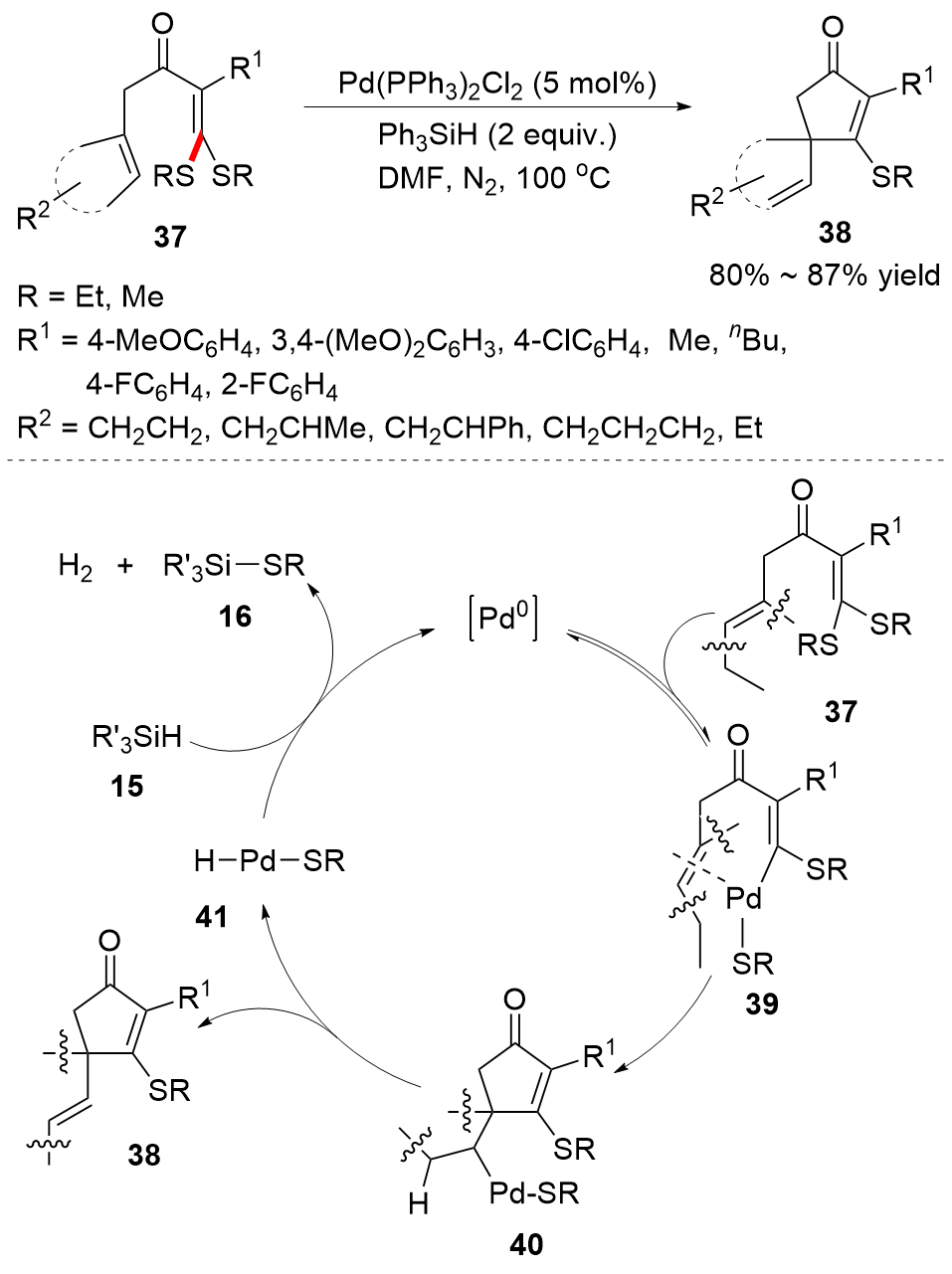
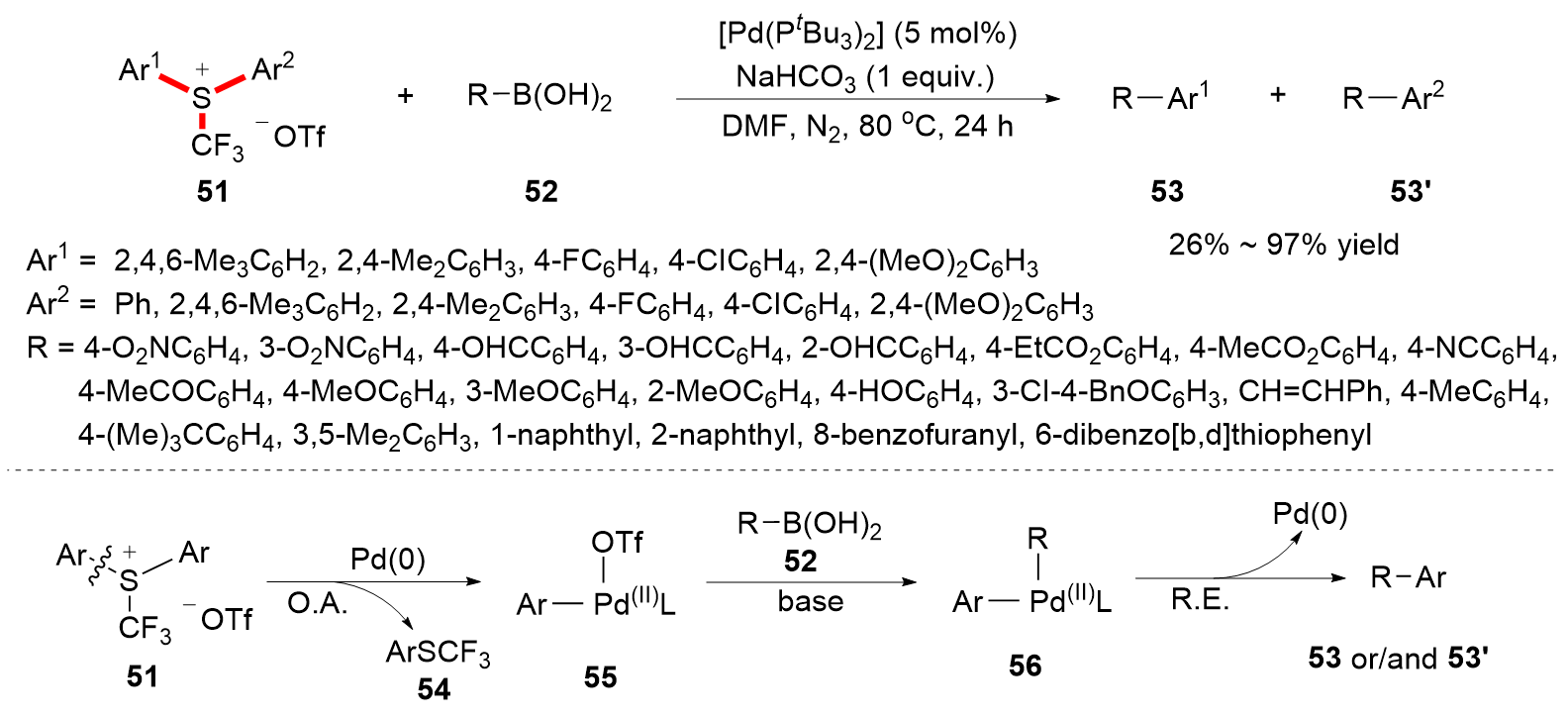
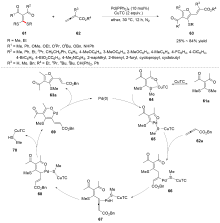
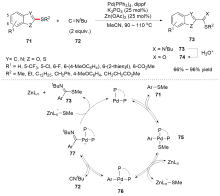
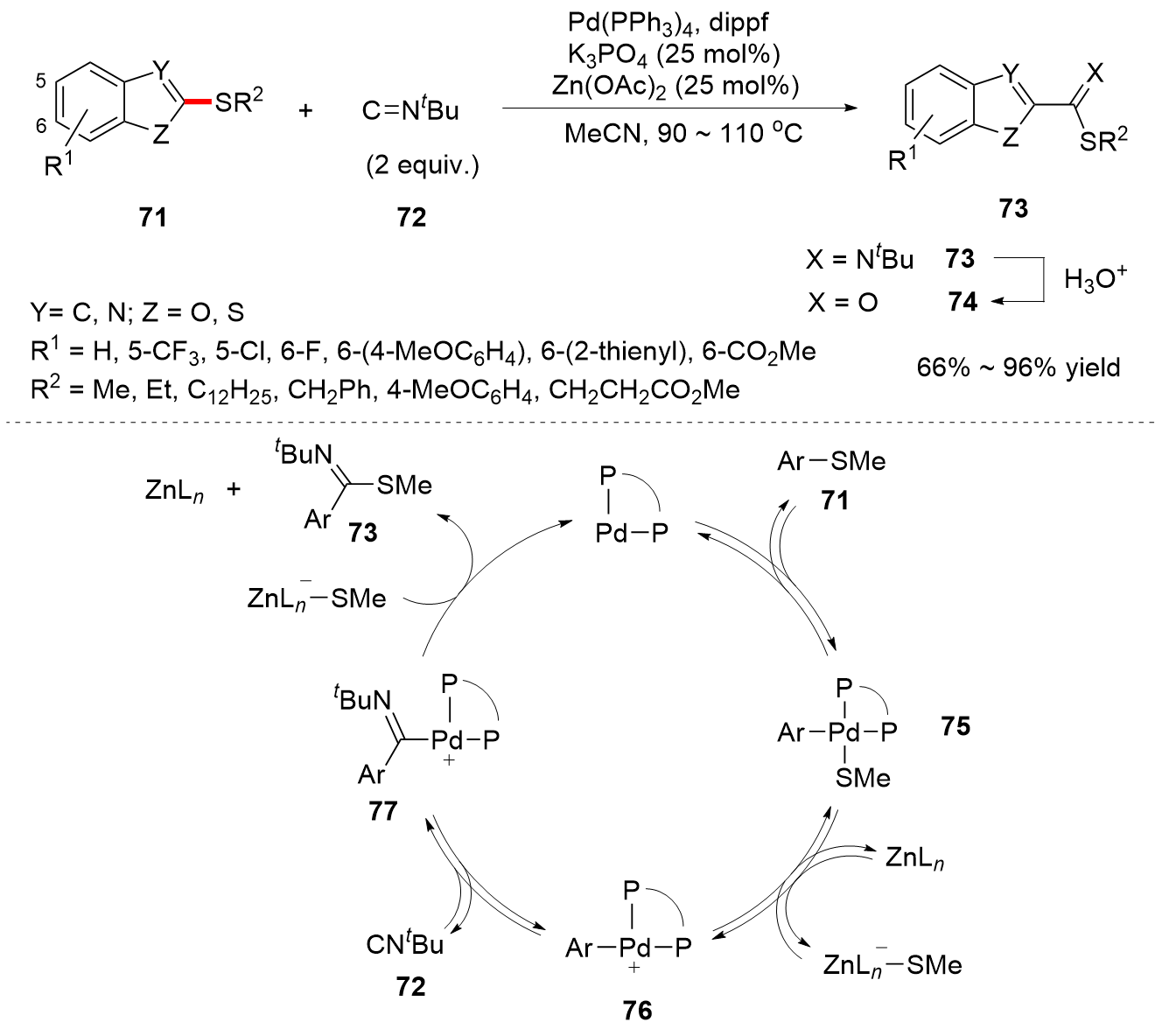
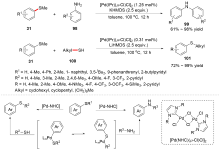
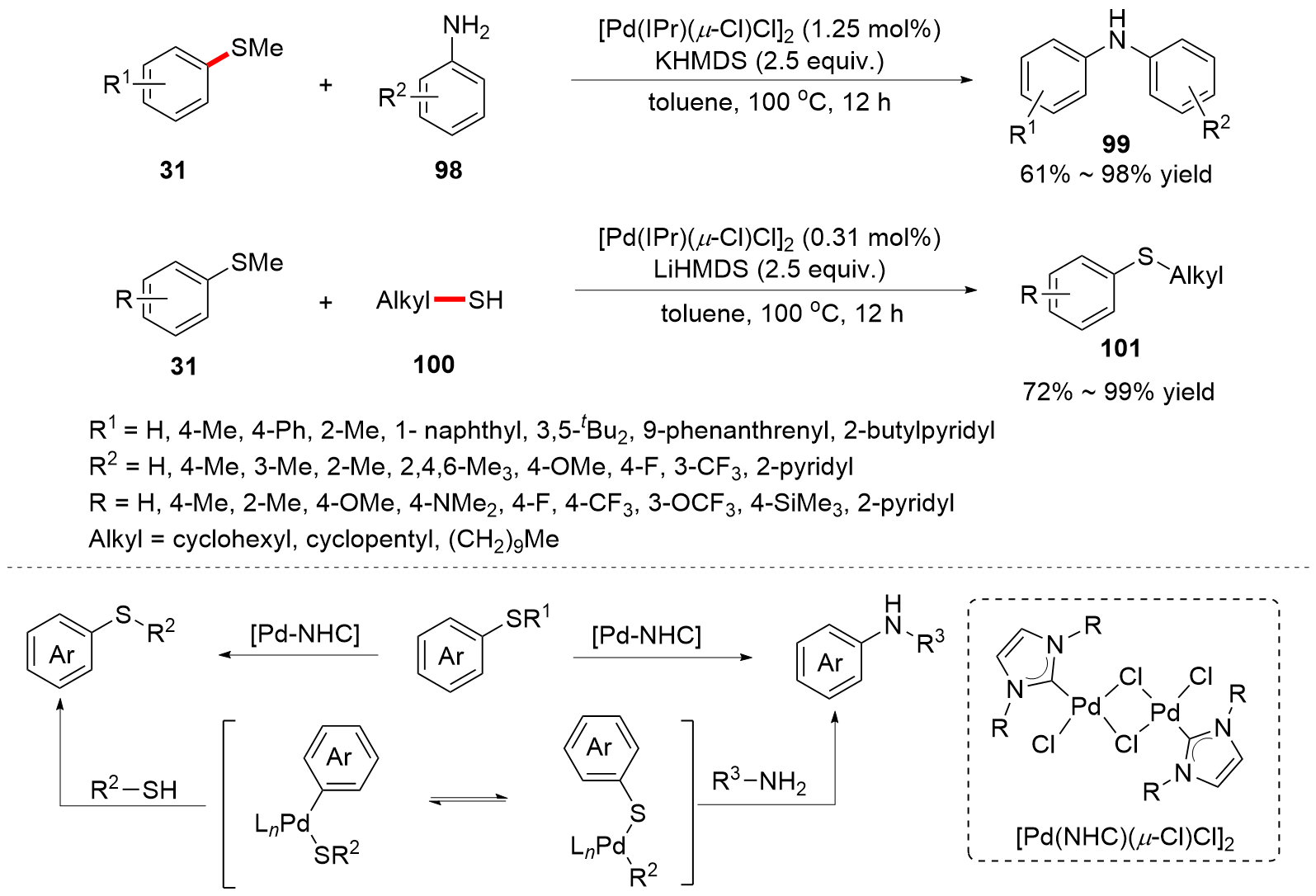
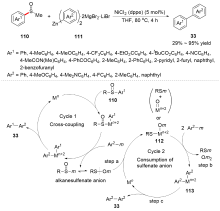
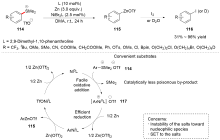
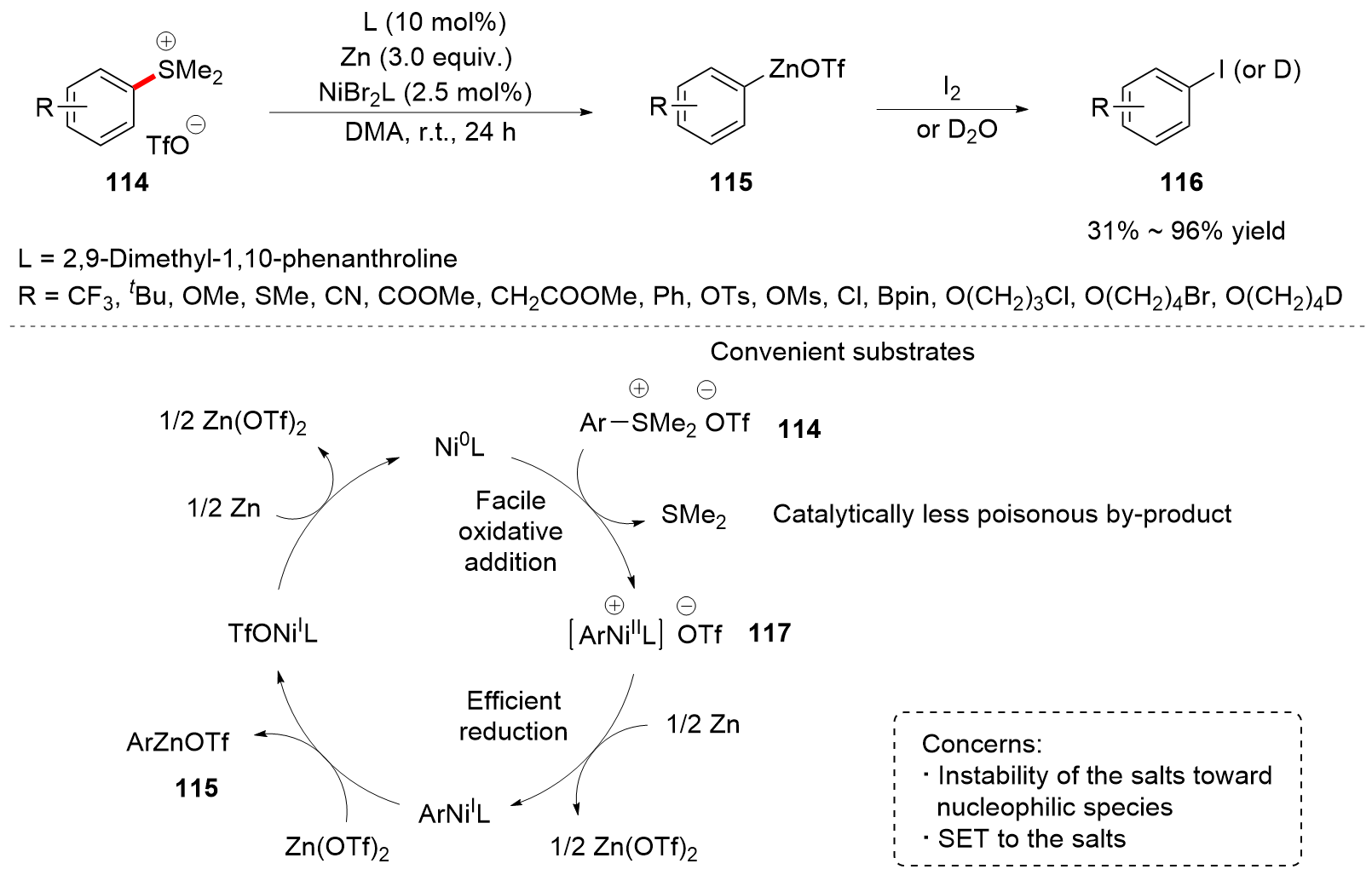
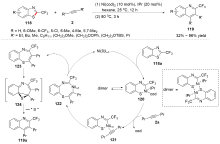
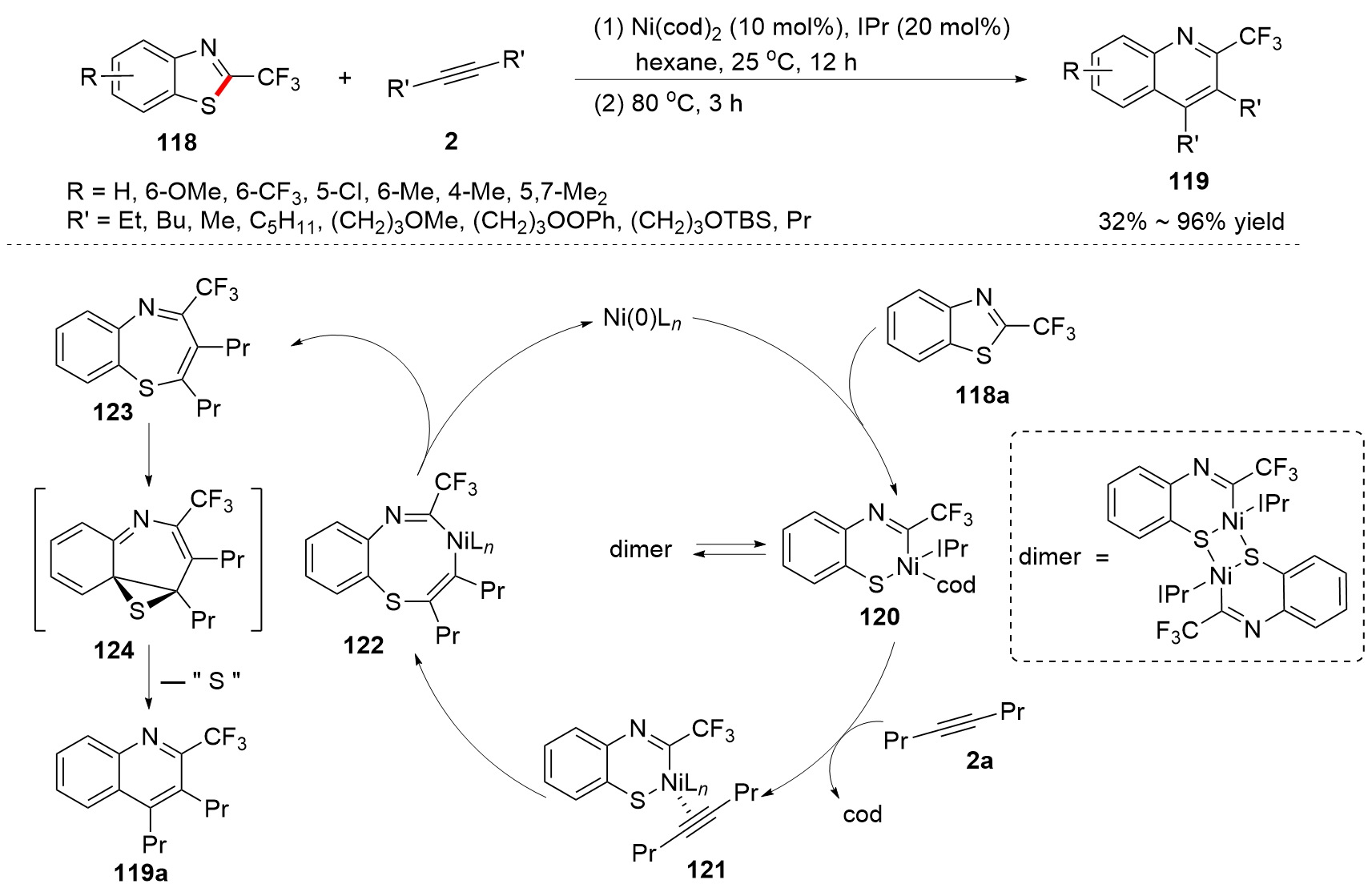
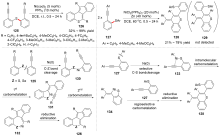
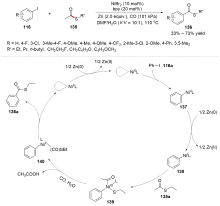
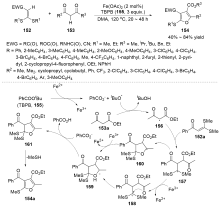
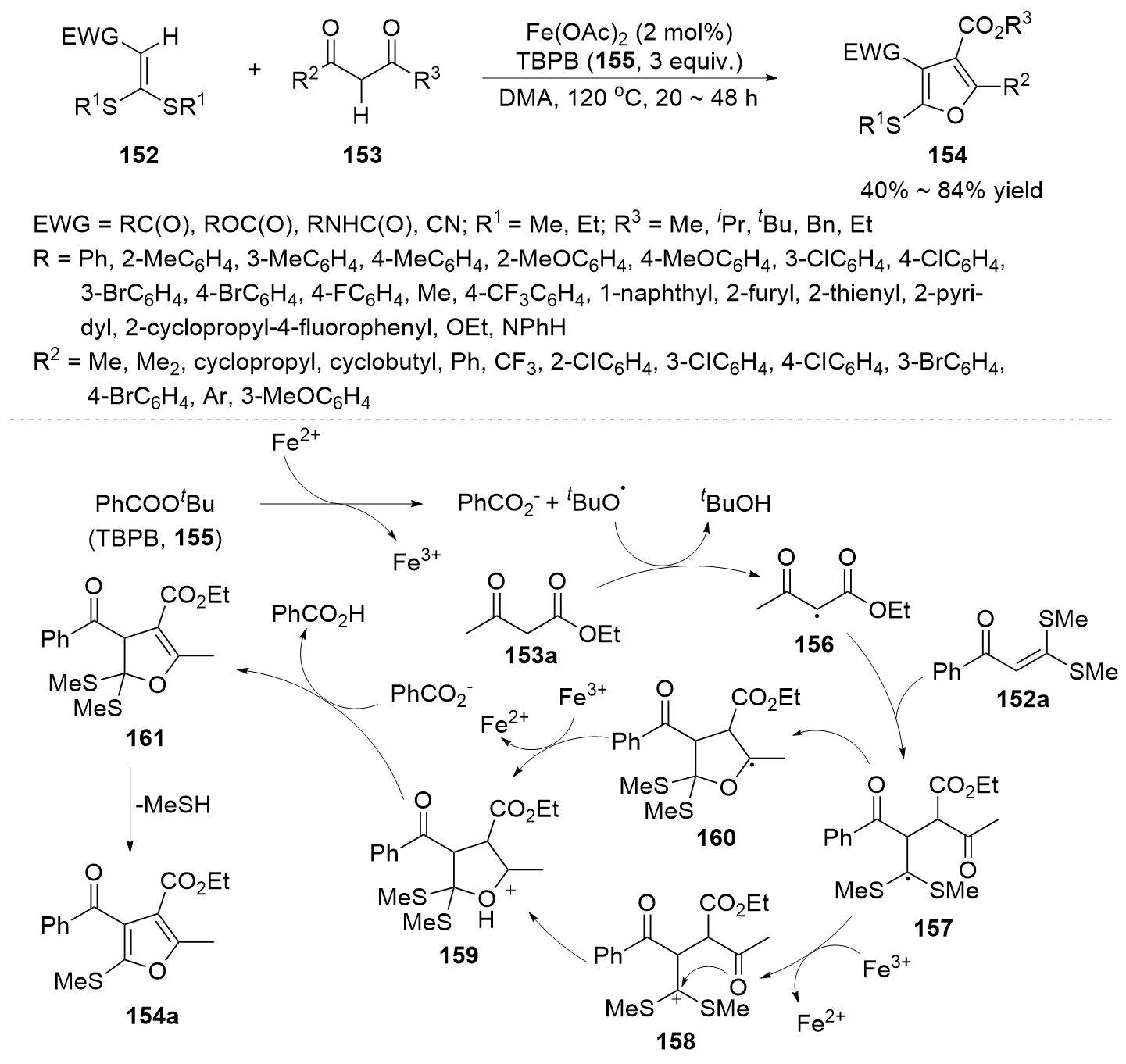
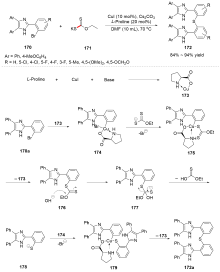
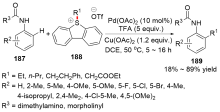
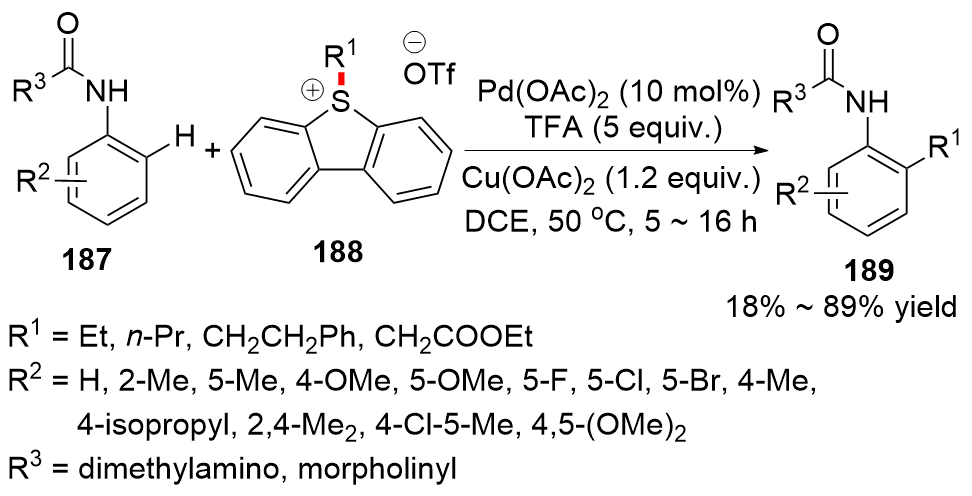
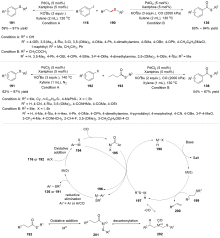
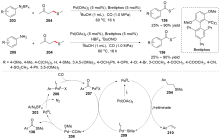
C—S键的活化, 对于药物分子、高性能聚合物和复合材料的制备以及生物医学、环境保护等领域具有重要作用, 过渡金属催化C—S键的活化与转化更是具有广泛的应用前景. 根据有机硫化物中碳原子的杂化类型进行分类, 综述了近十年来过渡金属催化C(sp)/C(sp2)/C(sp3)—S键活化与转化的研究进展, 采用不同的过渡金属催化剂, 着重讨论了底物适用性和反应机理, 并对该领域存在的挑战以及未来发展趋势进行了讨论和展望.
郭凯杰, 符昕姝, 李靖, 陈艳, 胡美丽, 堵锡华, 谢屿阳, 何燕. 过渡金属催化C—S键活化与转化研究进展[J]. 有机化学, 2024, 44(4): 1124-1150.
Kaijie Guo, Xinshu Fu, Jing Li, Yan Chen, Meili Hu, Xihua Du, Yuyang Xie, Yan He. Recent Advances in Transition-Metal-Catalyzed C—S Bond Activation and Transformations[J]. Chinese Journal of Organic Chemistry, 2024, 44(4): 1124-1150.
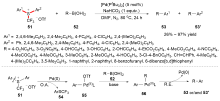





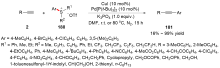




| [1] |
(a) Wächtershäuser G. Trans. R. Soc. B 2006, 361, 1787.
doi: 10.1098/rstb.2006.1904 pmid: 20704269 |
|
(b) Harpp D. N.; Vines S. M.; Montillier J. P.; Chan T. H. J. Org. Chem. 1976, 41, 3987.
doi: 10.1021/jo00887a012 pmid: 20704269 |
|
|
(c) Grochowski M. R.; Li T.; Brennessel W. W.; Jones W. D. J. Am. Chem. Soc. 2010, 132, 12412.
doi: 10.1021/ja104158h pmid: 20704269 |
|
| [2] |
(a) Boyd D. A. Angew. Chem., Int. Ed. 2016, 55, 15486.
doi: 10.1002/anie.v55.50 |
|
(b) Liu J.; Yang J.; Yang Q.; Wang G.; Li Y. Adv. Funct. Mater. 2005, 15, 1297.
doi: 10.1002/(ISSN)1616-3028 |
|
|
(c) Dondoni A. Angew. Chem., Int. Ed. 2008, 120, 9133.
doi: 10.1002/ange.v120:47 |
|
| [3] |
(a) Natarajan A.; Guo Y.; Harbinski F.; Fan Y.-H.; Chen H.; Luus L.; Diercks J.; Aktas H.; Chorev M.; Halperin J. A. J. Med. Chem. 2004, 47, 4979.
pmid: 19588965 |
|
(b) Cole D. C.; Lennox W. J.; Lombardi S.; Ellingboe J. W.; Bernotas R. C.; Tawa G. J.; Mazandarani H.; Smith D. L.; Zhang G.; Coupet J.; Schechter L. E. J. Med. Chem. 2005, 48, 353.
doi: 10.1021/jm049243i pmid: 19588965 |
|
|
(c) Banerjee M.; Poddar A.; Mitra G.; Surolia A.; Owa T.; Bhattacharyya B. J. Med. Chem. 2005, 48, 547.
pmid: 19588965 |
|
|
(d) Feng E.; Huang H.; Zhou Y.; Ye D.; Jiang H.; Liu H. J. Comb. Chem. 2010, 12, 422.
doi: 10.1021/cc9001839 pmid: 19588965 |
|
|
(e) Gao G.-Y.; Colvin A. J.; Chen Y.; Zhang X. P. J. Org. Chem. 2004, 69, 8886.
doi: 10.1021/jo048552d pmid: 19588965 |
|
|
(f) Inamoto K.; Hasegawa C.; Hiroya K.; Doi T. Org. Lett. 2008, 10, 5147.
doi: 10.1021/ol802033p pmid: 19588965 |
|
|
(g) Jegelka M.; Plietker B. Org. Lett. 2009, 11, 3462.
doi: 10.1021/ol901297s pmid: 19588965 |
|
|
(h) Niu P.; Kang J.; Tian X.; Song L.; Liu H.; Wu J.; Yu W.; Chang J. J. Org. Chem. 2015, 80, 1018.
doi: 10.1021/jo502518c pmid: 19588965 |
|
| [4] |
(a) Fang R.; Xu J.; Wang D.-W. Energy Environ. Sci. 2020, 13, 432.
doi: 10.1039/C9EE03408K |
|
(b) Shi F.; Yu J.; Chen C.; Lau S. P.; Lv W.; Xu Z.-L. J. Mater. Chem. A 2022, 10, 19412.
doi: 10.1039/D2TA02217F |
|
|
(c) Li M.; Chen H.; Wang Y.; Chen X.; Wu J.; Su J.; Wang M.; Li X.; Li C.; Ma L.; Li X.; Chen Y. J. Mater. Chem. A 2023, 11, 11721.
doi: 10.1039/D3TA01803B |
|
| [5] |
(a) Luque R. Curr. Org. Synth. 2011, 8, 1.
doi: 10.2174/157017911794407665 |
|
(b) Ornellas S. D.; Storr T. E.; Williams T. J.; Baumann C. G.; Fairlamb I. J. S. Curr. Org. Synth. 2011, 8, 79.
doi: 10.2174/157017911794407656 |
|
|
(c) Wang L.; He W.; Yu Z. Chem. Soc. Rev. 2013, 42, 599.
doi: 10.1039/C2CS35323G |
|
|
(d) Modha S. G.; Mehta V. P.; Eycken E. V. Chem. Soc. Rev. 2013, 42, 5042.
doi: 10.1039/c3cs60041f |
|
|
(e) Lou J.; Wang Q.; Wu P.; Wang H.; Zhou Y. G.; Yu Z. Chem. Soc. Rev. 2020, 49, 4307.
doi: 10.1039/C9CS00837C |
|
|
(f) Huang S.; Wang M.; Jiang X. Chem. Soc. Rev. 2022, 51, 8351.
doi: 10.1039/D2CS00553K |
|
|
(g) Otsuka S.; Nogi K.; Yorimitsu H. Top. Curr. Chem. 2018, 376, 13.
|
|
| [6] |
(a) Li Y.; Wang H.; Wang Z.; Alhumade H.; Huang Z.; Lei A. Chem. Sci. 2023, 14, 372.
doi: 10.1039/D2SC05507D |
|
(b) Tyagi A.; Taneja N.; Khan J.; Hazra C. K. Adv. Synth. Catal. 2023, 365, 1247.
doi: 10.1002/adsc.v365.8 |
|
|
(c) Liang D.; Wang M.; Bekturhun B.; Xiong B.; Liu Q. Adv. Synth. Catal. 2010, 352, 1593.
doi: 10.1002/adsc.v352:10 |
|
|
(d) Liu Y.; Wang M.; Yuan H.; Liu Q. Adv. Synth. Catal. 2010, 352, 884.
doi: 10.1002/adsc.v352:5 |
|
|
(e) Liu Y.; Liu J.; Wang M.; Liu J.; Liu Q. Adv. Synth. Catal. 2012, 354, 2678.
doi: 10.1002/adsc.v354.14/15 |
|
|
(f) Yu H.; Yu Z. Angew. Chem. 2009, 121, 2973.
doi: 10.1002/ange.v121:16 |
|
|
(g) Dong Y.; Wang M.; Liu J.; Ma W.; Liu Q. Chem. Commun. 2011, 47, 7380.
doi: 10.1039/c1cc11382h |
|
|
(h) Verma R. K.; Verma G. K.; Shukla G.; Singh M. S. RSC Adv. 2012, 2, 2413.
doi: 10.1039/c2ra00987k |
|
|
(i) Jin W.; Du W.; Yang Q.; Yu H.; Chen J.; Yu Z. Org. Lett. 2011, 13, 4272.
doi: 10.1021/ol201620g |
|
| [7] |
Yang K.; Li Q.; Li Z.; Sun X. Chem. Commun. 2023, 59, 5343.
doi: 10.1039/D3CC00377A |
| [8] |
Liebeskind L. S.; Srogl J.; Savarin C.; Polanco C. Pure Appl. Chem. 2002, 74, 115.
doi: 10.1351/pac200274010115 |
| [9] |
Iwasaki M.; Fujino D.; Wada T.; Kondoh A.; Yorimitsu H.; Oshima K. Chem. Asian J. 2011, 6, 3190.
doi: 10.1002/asia.v6.12 |
| [10] |
Arisawa M.; Igarashi Y.; Tagami Y.; Yamaguchi M.; Kabuto C. Tetrahedron Lett. 2011, 52, 920
doi: 10.1016/j.tetlet.2010.12.065 |
| [11] |
Shibata T.; Mitake A.; Akiyamac Y.; Stephen K. K. Chem. Commun. 2017, 53, 9016.
doi: 10.1039/C7CC04997H |
| [12] |
Beletskaya I. P.; Ananikov V. P. Chem. Rev. 2022, 122, 16110.
doi: 10.1021/acs.chemrev.1c00836 pmid: 36112510 |
| [13] |
(a) Beletskaya I. P.; Alonso F.; Tyurin V. Coord Chem. Rev. 2019, 385, 137.
doi: 10.1016/j.ccr.2019.01.012 |
|
(b) Buchspies J.; Szostak M. Catalysts 2019, 9, 53.
doi: 10.3390/catal9010053 |
|
|
(c) Das P.; Linert W. Coord. Chem. Rev. 2016, 311, 1.
doi: 10.1016/j.ccr.2015.11.010 |
|
|
(d) Han F.-S. Chem. Soc. Rev. 2013, 42, 5270.
doi: 10.1039/c3cs35521g |
|
|
(e) Hooshmand S. E.; Heidari B.; Sedghi R.; Varma R. S. Green chem. 2019, 21, 381.
doi: 10.1039/c8gc02860e |
|
|
(f) Lennox A. J. J.; Lloyd-Jones G. C. Chem. Soc. Rev. 2014, 43, 412.
doi: 10.1039/C3CS60197H |
|
|
(g) Lamblin M.; Nassar-Hardy L.; Hierso J.-C.; Fouquet E.; Felpin F.-X. Adv. Synth. Catal. 2010, 352, 33.
doi: 10.1002/adsc.v352:1 |
|
| [14] |
Liu B.; Zheng G.; Liu X.; Xu C.; Liu J.; Wang M. Chem. Commun. 2013, 49, 2201.
doi: 10.1039/c3cc37571d |
| [15] |
Liu J.; Liu Y.; Du W.; Dong Y.; Liu J.; Wang M. J. Org. Chem. 2013, 78, 7293.
doi: 10.1021/jo400984h |
| [16] |
Dong Y.; Liu B.; Chen P.; Liu Q.; Wang M. Angew. Chem. 2014, 126, 3510.
doi: 10.1002/ange.v126.13 |
| [17] |
Otsuka S.; Fujino D.; Murakami K.; Yorimitsu H.; Osuka A. Chem. Eur. J. 2014, 20, 13146.
doi: 10.1002/chem.v20.41 |
| [18] |
Vasu D.; Yorimitsu H.; Osuka A. Synthesis 2015, 47, 3286.
doi: 10.1055/s-00000084 |
| [19] |
Liu B.; Chang J.; Zheng G.; Song X.; Wang M. Eur. J. Org. Chem. 2015, 4611.
|
| [20] |
Chang J.; Liu B.; Yang Y.; Wang M. Org. Lett. 2016, 18, 3984.
doi: 10.1021/acs.orglett.6b01780 pmid: 27498923 |
| [21] |
Wang S.-M.; Wang X.-Y.; Qin H.-L.; Zhang C.-P. Chem. Eur. J. 2016, 22, 6542.
doi: 10.1002/chem.v22.19 |
| [22] |
Iwasaki M.; Topolovčan N.; Hu H.; Nishimura Y.; Gagnot G.; Na nakorn R.; Yuvacharaskul R.; Nakajima K.; Nishihara Y. Org. Lett. 2016, 18, 1642.
doi: 10.1021/acs.orglett.6b00503 |
| [23] |
Wang Q.; Liu Z.; Lou J.; Yu Z. Org. Lett. 2018, 20, 6007.
doi: 10.1021/acs.orglett.8b02253 |
| [24] |
Otsuka S.; Nogi K.; Yorimitsu H. Angew. Chem., Int. Ed. 2018, 57, 6653.
doi: 10.1002/anie.v57.22 |
| [25] |
Minami H.; Nogi K.; Yorimitsu H. Org. Lett. 2019, 21, 2518.
doi: 10.1021/acs.orglett.9b00067 |
| [26] |
Uno D.; Nogi K.; Yorimitsu H. Org. Lett. 2019, 21, 8295.
doi: 10.1021/acs.orglett.9b03056 |
| [27] |
Xu J.-X.; Zhao F.; Wu X.-F. Org. Biomol. Chem. 2020, 18, 9796.
doi: 10.1039/D0OB02043E |
| [28] |
Delcaillau T.; Schmitt H. L.; Boehm P.; Falk E.; Morandi B. ACS Catal. 2022, 12, 6081.
doi: 10.1021/acscatal.2c01178 |
| [29] |
Yang S.; Yu X.; Poater A.; Cavallo L.; Cazin C. S. J.; Nolan S. P.; Szostak M. Org. Lett. 2022, 24, 9210.
doi: 10.1021/acs.orglett.2c03717 |
| [30] |
Mond J.; Langer C.; Quincke F. J. Chem. Soc., Trans. 1890, 57, 749.
doi: 10.1039/CT8905700749 |
| [31] |
Wilke G. Angew. Chem., Int. Ed. 1988, 27, 185.
|
| [32] |
Stephan Enthaler, C. I. S. M. W. Catal. Lett. 2013, 143, 424.
doi: 10.1007/s10562-013-0979-5 |
| [33] |
Yamamoto K.; Otsuka S.; Nogi K.; Yorimitsu H. ACS Catal. 2017, 7, 7623.
doi: 10.1021/acscatal.7b02347 |
| [34] |
Yamada K.; Yanagi T.; Yorimitsu H. Org. Lett. 2020, 22, 9712.
doi: 10.1021/acs.orglett.0c03782 pmid: 33300805 |
| [35] |
Inami T.; Kurahashi T.; Matsubara S. Synlett 2021, 32, 1948.
doi: 10.1055/s-0037-1610785 |
| [36] |
Shibata T.; Sekine A.; Akino M.; Ito M. Chem. Commun., 2021, 57, 9048.
doi: 10.1039/D1CC03226G |
| [37] |
Mai W.-P.; Sui H.-D.; Lv M.-X.; Lu K. J. Chem. Res. 2021, 45, 890.
doi: 10.1177/17475198211028114 |
| [38] |
Pan F.; Wang H.; Shen P.-X.; Zhao J.; Shi Z.-J. Chem. Sci. 2013, 4, 1573.
doi: 10.1039/c3sc22242j |
| [39] |
Uetake Y.; Niwa T.; Hosoya T. Org. Lett. 2016, 18, 2758.
doi: 10.1021/acs.orglett.6b01250 pmid: 27210907 |
| [40] |
(a) Sherry B. D.; Fürstner A. Acc. Chem. Res. 2008, 41, 1500.
doi: 10.1021/ar800039x |
|
(b) Czaplik W. M.; Mayer M.; Cvengros, Wangelin, J.; A. Jacobi von. ChemSusChem 2009, 2, 396.
doi: 10.1002/cssc.v2:5 |
|
|
(c) Piontek A.; Bisz E.; Szostak M. Angew. Chem., Int. Ed. 2018, 57, 11116.
doi: 10.1002/anie.v57.35 |
|
| [41] |
Blanksby S. J.; Ellison G. B. Acc. Chem. Res. 2003, 36, 255.
doi: 10.1021/ar020230d |
| [42] |
Lou J.; Wang Q.; Wu K.; Wu P.; Yu Z. Org. Lett. 2017, 19, 3287.
doi: 10.1021/acs.orglett.7b01431 |
| [43] |
Chen S.; Guo X.; Hou H.; Geng S.; Liu Z.; He Y.; Xue X.-S.; Feng Z. Angew. Chem., Int. Ed. 2023, 62, e202303470.
doi: 10.1002/anie.v62.25 |
| [44] |
Zhang Y.; Li T.-J.; Lv L.; Liu J.-Q.; Wang X.-S. J. Heterocyclic. Chem. 2022, 59, 67.
doi: 10.1002/jhet.v59.1 |
| [45] |
Tian Z.-Y.; Wang S.-M.; Jia S.-J.; Song H.-X.; Zhang C.-P. Org. Lett. 2017, 19, 5454.
doi: 10.1021/acs.orglett.7b02764 |
| [46] |
Li Y.; Wang H.; Wang Z.; Alhumade H.; Huang Z.; Lei A. Chem. Sci. 2023, 14, 372.
doi: 10.1039/D2SC05507D |
| [47] |
Nambo M.; Crudden C. M. Angew. Chem., Int. Ed. 2014, 53, 742.
doi: 10.1002/anie.v53.3 |
| [48] |
Simkó D. C.; Elekes P.; Pázmándi V.; Novák Z. Org. Lett. 2018, 20, 676.
doi: 10.1021/acs.orglett.7b03813 |
| [49] |
Li Y.; Bao G.; Wu X.-F. Chem. Sci. 2020, 11, 2187.
doi: 10.1039/C9SC05532K |
| [50] |
Tian Q.; Xu S.; Zhang C.; Liu X.; Wu X.; Li Y. J.Org. Chem. 2021, 86, 8797.
doi: 10.1021/acs.joc.1c00665 |
| [51] |
Yu H.; Zhao L.; Diao Q.; Li T.; Liao P.; Hou D.; Xin G. Synlett 2017, 28, 1828.
doi: 10.1055/s-0036-1588982 |
| [52] |
Zhang X.-S.; Zhang Y.-F.; Li Z.-W.; Luo F.-X.; Shi Z.-J. Angew. Chem., Int. Ed. 2015, 54, 5478.
doi: 10.1002/anie.v54.18 |
| [53] |
Ming X.-X.; Wu S.; Tian Z.-Y.; Song J.-W.; Zhang C.-P. Org. Lett. 2021, 23, 6795.
doi: 10.1021/acs.orglett.1c02379 |
| [1] | 万云辉, 杨福美, 陈明瀚, 孙德立, 叶丹锋. 无过渡金属催化的N-苄基-N-叔丁氧羰基酰胺与不饱和醇的酯化反应[J]. 有机化学, 2024, 44(4): 1293-1300. |
| [2] | 李晨龙, 余志祥. 一氧化碳参与的过渡金属催化的插羰环加成反应研究进展[J]. 有机化学, 2024, 44(4): 1045-1068. |
| [3] | 鞠国栋, 周冠宇, 赵应声. 三异丙基硅烷(TIPS)保护苯酚的无过渡金属催化区域选择性硫氰化反应[J]. 有机化学, 2024, 44(4): 1327-1336. |
| [4] | 彭天凤, 赵玉祥, 浦绍健, 罗娟, 刘腾, 缪应纯, 沈先福. 过渡金属催化的关键反应在异戊烯基吲哚生物碱全合成中的研究进展[J]. 有机化学, 2024, 44(4): 1160-1180. |
| [5] | 高淳, 刘欣, 王明慧, 刘淑贤, 朱婷婷, 张怡康, 郝二军, 杨启亮. 电化学不对称合成反应的研究进展[J]. 有机化学, 2024, 44(3): 673-727. |
| [6] | 赵红琼, 于淼, 宋冬雪, 贾琦, 刘颖杰, 季宇彬, 许颖. 羧酸脱羧羟基化反应研究进展[J]. 有机化学, 2024, 44(1): 70-84. |
| [7] | 高晓阳, 翟锐锐, 陈训, 王烁今. 碳酸亚乙烯酯参与C—H键活化反应的研究进展[J]. 有机化学, 2023, 43(9): 3119-3134. |
| [8] | 陈新强, 张敬. 伯醇的脱羟甲基反应的研究进展[J]. 有机化学, 2023, 43(8): 2711-2719. |
| [9] | 徐光利, 许静, 徐海东, 崔香, 舒兴中. 过渡金属催化烯烃和炔烃合成1,3-共轭二烯化合物研究进展[J]. 有机化学, 2023, 43(6): 1899-1933. |
| [10] | 户晓兢, 郭斐翔, 朱润青, 周柄棋, 张涛, 房立真. 对烷氧基酚的合成及其去芳构化后的合成应用[J]. 有机化学, 2023, 43(6): 2239-2244. |
| [11] | 庞明杨, 常宏宏, 冯璋, 张娟. 过渡金属催化吲哚的串联去芳构化反应研究进展[J]. 有机化学, 2023, 43(4): 1271-1291. |
| [12] | 贾海瑞, 邱早早. 过渡金属催化硼-氢键活化合成含硼-杂原子键邻碳硼烷衍生物的研究进展[J]. 有机化学, 2023, 43(3): 1045-1068. |
| [13] | 段康慧, 唐俊龙, 伍婉卿. 稠杂环化合物的合成及其抗肿瘤活性研究进展[J]. 有机化学, 2023, 43(3): 826-854. |
| [14] | 吴孔川, 卢铠洪, 林建斌, 张慧君. 莱啉酰亚胺类化合物的邻位C—H键功能化研究进展[J]. 有机化学, 2023, 43(3): 1000-1011. |
| [15] | 蒙玲, 汪君. 硫代黄烷酮类衍生物的合成研究进展[J]. 有机化学, 2023, 43(3): 873-891. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||