有机化学 ›› 2021, Vol. 41 ›› Issue (10): 4050-4058.DOI: 10.6023/cjoc202105044 上一篇 下一篇
所属专题: 南开大学化学学科创立100周年; 热点论文虚拟合集
研究论文
收稿日期:2021-05-25
修回日期:2021-06-22
发布日期:2021-07-05
通讯作者:
王浩, 陈弓
基金资助:
Fangfang Song, Shiyang Zhu, Hao Wang( ), Gong Chen(
), Gong Chen( )
)
Received:2021-05-25
Revised:2021-06-22
Published:2021-07-05
Contact:
Hao Wang, Gong Chen
Supported by:文章分享

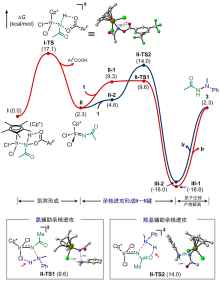
报道了一类铱催化下异羟肟酸衍生物作为酰基氮宾前体参与的分子间N—N偶联合成酰肼化合物的反应. 与之前报道的二噁唑酮参与的反应不同, 该类氮宾前体不仅可以合成N-酰基肼类化合物, 又可以用于N-氧酰基肼类化合物的合成. 计算化学研究说明分子内氢键辅助N—O键断裂脱酸形成金属酰基氮宾中间体可能是决速步, 随后芳胺在氢键辅助下亲核进攻金属酰基氮宾形成N—N键.
宋方方, 朱士阳, 王浩, 陈弓. 铱催化异羟肟酸衍生物参与的分子间N—N键偶联反应合成酰肼[J]. 有机化学, 2021, 41(10): 4050-4058.
Fangfang Song, Shiyang Zhu, Hao Wang, Gong Chen. Iridium-Catalyzed Intermolecular N—N Coupling for Hydrazide Synthesis Using N-Benzoyloxycarbamates as Acyl Nitrene Precursor[J]. Chinese Journal of Organic Chemistry, 2021, 41(10): 4050-4058.
| Entry | Variation from the standard conditions | Yielda/% |
|---|---|---|
| 1 | Standard condition | 97 (94)b |
| 2 | No [Cp*IrCl2]2 | No reaction |
| 3 | Solvent free | 92 |
| 4 | [1]=0.1 mol/L | 95 |
| 5 | 1.2 equiv. 2e was added | 82 |
| 6 | HFIP as solvent | No reaction |
| 7 | DCE as solvent | 93 |
| 8 | Ar atmosphere | 92 |
| 9 | FeCl2•4H2O (5 mol%) as catalyst | No reaction |
| 10 | T=60 ℃ | 77 |
| 11 | AgSbF6 (5 mol%) | 15 |
| Entry | Variation from the standard conditions | Yielda/% |
|---|---|---|
| 1 | Standard condition | 97 (94)b |
| 2 | No [Cp*IrCl2]2 | No reaction |
| 3 | Solvent free | 92 |
| 4 | [1]=0.1 mol/L | 95 |
| 5 | 1.2 equiv. 2e was added | 82 |
| 6 | HFIP as solvent | No reaction |
| 7 | DCE as solvent | 93 |
| 8 | Ar atmosphere | 92 |
| 9 | FeCl2•4H2O (5 mol%) as catalyst | No reaction |
| 10 | T=60 ℃ | 77 |
| 11 | AgSbF6 (5 mol%) | 15 |

| [1] |
(a) Ke, S.; Sun, T.; Liang, Y.; Yang, Z. Chin. J. Org. Chem. 2010, 30, 1820. (in Chinese)
|
|
(柯少勇, 孙婷婷, 梁英, 杨自文, 有机化学, 2010, 30, 1820.)
|
|
|
(b) Blair, L. M.; Sperry, J. J. Nat. Prod. 2013, 76, 794.
doi: 10.1021/np400124n |
|
|
(c) Chen, L.; Deng, Z.; Zhao, C. ACS Chem. Biol. 2021, 16, 559.
doi: 10.1021/acschembio.1c00052 |
|
| [2] |
(a) Okuhara, M.; Kuroda, Y.; Goto, T.; Okamoto, M.; Terano, H.; Kohsaka, M.; Aoki, H.; Imanaka, H. J. Antibiot. 1980, 33, 13.
pmid: 16441076 |
|
(b) Ogita, T.; Gunji, S.; Fukazawa, Y.; Terahara, A.; Kinoshita, T.; Nagaki, H.; Beppu, T. Tetrahedron Lett. 1983, 24, 2283.
doi: 10.1016/S0040-4039(00)81904-8 pmid: 16441076 |
|
|
(c) Broberg, A.; Menkis, A.; Vasiliauskas, R. J. Nat. Prod. 2006, 69, 97.
pmid: 16441076 |
|
|
(d) Wang, K.-K. A.; Ng, T. L.; Wang, P.; Huang, Z.; Balskus, E. P.; van der Donk, W. A. Nat. Commun. 2018, 9, 3687.
doi: 10.1038/s41467-018-06083-7 pmid: 16441076 |
|
| [3] |
Forquet, V.; Sabaté, C. M.; Jacob, G.; Guelou, Y.; Delalu, H.; Darwich, C. Chem.-Asian J. 2015, 10, 1668.
doi: 10.1002/asia.v10.8 |
| [4] |
Diccianni, J. B.; Hu, C.; Diao, T. Angew. Chem.,Int. Ed. 2016, 55, 7534.
doi: 10.1002/anie.v55.26 |
| [5] |
(a) Ragnarsson, U. Chem. Soc. Rev. 2001, 30, 205.
doi: 10.1039/b010091a pmid: 11700143 |
|
(b) Wolter, M.; Klapars, A.; Buchwald, S. L. Org. Lett. 2001, 3, 3803.
pmid: 11700143 |
|
| [6] |
(a) Evans, D. A.; Johnson, D. S. Org. Lett. 1999, 1, 595.
pmid: 10823188 |
|
(b) Feng, G.; Wang, X.; Jin, J. Eur. J. Org. Chem. 2019, 6728.
pmid: 10823188 |
|
|
(c) Chen, J.; Shen, X.; Lu, Z. J. Am. Chem. Soc. 2020, 142, 14455.
doi: 10.1021/jacs.0c07258 pmid: 10823188 |
|
| [7] |
Guo, Q.; Lu, Z. Synthesis 2017, 49, 3835.
doi: 10.1055/s-0036-1588512 |
| [8] |
(a) Rosen, B. R.; Werner, E. W.; O'Brien, A. G.; Baran, P. S. J. Am. Chem. Soc. 2014, 136, 5571.
doi: 10.1021/ja5013323 pmid: 33974802 |
|
(b) Pandit, P.; Yamamoto, K.; Nakamura, T.; Nishimura, K.; Kurashige, Y.; Yanai, T.; Nakamura, G.; Masaoka, S.; Furukawa, K.; Yakiyama, Y.; Kawano, M.; Higashibayashi, S. Chem. Sci. 2015, 6, 4160.
doi: 10.1039/C5SC00946D pmid: 33974802 |
|
|
(c) Ryan, M. C.; Martinelli, J. R.; Stahl, S. S. J. Am. Chem. Soc. 2018, 140, 9074.
doi: 10.1021/jacs.8b05245 pmid: 33974802 |
|
|
(d) Feng, N.; Hou, Z.; Xu, H. Chin. J. Org. Chem. 2019, 39, 1424. (in Chinese)
doi: 10.6023/cjoc201812007 pmid: 33974802 |
|
|
(冯恩祺, 侯中伟, 徐海超, 有机化学, 2019, 39, 1424.)
doi: 10.6023/cjoc201812007 pmid: 33974802 |
|
|
(e) Yin, D.; Jin, J. Eur. J. Org. Chem. 2019, 2019, 5646.
doi: 10.1002/ejoc.201900763 pmid: 33974802 |
|
|
(f) Ryan, M. C.; Kim, Y. J.; Gerken, J. B.; Wang, F.; Aristov, M. M.; Martinelli, J. R.; Stahl, S. S. Chem. Sci. 2020, 11, 1170.
doi: 10.1039/C9SC04305E pmid: 33974802 |
|
|
(g) Vemuri, P. Y.; Patureau, F. W. Org. Lett. 2021, 23, 3902.
doi: 10.1021/acs.orglett.1c01034 pmid: 33974802 |
|
| [9] |
(a) Wallace, R. G. Aldrichim. Acta 1980, 13, 3.
|
|
(b) Vidal, J.; Hannachi, J. C.; Hourdin, G.; Mulatier, J. C.; Collet, A. Tetrahedron Lett. 1998, 39, 8845.
doi: 10.1016/S0040-4039(98)01983-2 |
|
|
(c) Kang, C. W.; Sarnowski, M. P.; Elbatrawi, Y. M.; Del Valle, J. R. J. Org. Chem. 2017, 82, 1833.
doi: 10.1021/acs.joc.6b02718 |
|
|
(d) Lei, L.; Li, C.; Mo, D. Chin. J. Org. Chem. 2019, 39, 2989. (in Chinese)
doi: 10.6023/cjoc201904037 |
|
|
(雷禄, 李承璟, 莫冬亮, 有机化学, 2019, 39, 2989.)
doi: 10.6023/cjoc201904037 |
|
|
(e) Zhang, Y.; He, J.; Song, P.; Wang, Y.; Zhu, S. CCS Chem. 2020, 2, 2259.
|
|
| [10] |
(a) Li, J.; Cisar, J. S.; Zhou, C.-Y.; Vera, B.; Williams, H.; Rodríguez, A. D.; Cravatt, B. F.; Romo, D. Nat. Chem. 2013, 5, 510.
doi: 10.1038/nchem.1653 |
|
(b) Kono, M.; Harada, S.; Nemoto, T. Chem.-Eur. J. 2019, 25, 3119.
|
|
|
(c) Maestre, L.; Dorel, R.; Pablo, O.; Escofet, I.; Sameera, W. M. C.; Alvarez, E.; Maseras, F.; Diaz-Requejo, M. M.; Echavarren, A. M.; Perez, P. J. J. Am. Chem. Soc. 2017, 139, 2216.
doi: 10.1021/jacs.6b08219 |
|
|
(d) Dehghany, M.; Eshon, J.; Roberts, J. M.; Schomaker, J. M. In Silver Catalysis in Organic Synthesis, Vol. 4, Eds.: Li, C.-J.; Bi, X., John Wiley & Sons, Weinheim, 2019, Chapter 8, pp. 439-532.
|
|
| [11] |
(a) Shimbayashi, T.; Sasakura, K.; Eguchi, A.; Okamoto, K.; Ohe, K. Chem.-Eur. J. 2019, 25, 3156.
doi: 10.1002/chem.201803716 pmid: 30183111 |
|
(b) van Vliet, K. M.; de Bruin, B. ACS Catal. 2020, 10, 4751.
doi: 10.1021/acscatal.0c00961 pmid: 30183111 |
|
|
(c) Wang, Y.-C.; Lai, X.-J.; Huang, K.; Yadav, S.; Qiu, G.; Zhang, L.; Zhou, H. Org. Chem. Front. 2021, 8, 1677.
doi: 10.1039/D0QO01360A pmid: 30183111 |
|
|
(d) Hong, S. Y.; Hwang, Y.; Lee, M.; Chang, S. Acc. Chem. Res. 2021, 54, 2683.
doi: 10.1021/acs.accounts.1c00198 pmid: 30183111 |
|
|
(e) Wu, L.-Y.; Zhong, D.; Liu, W.-B. Chin. J. Org. Chem. 2021, 41, 4083. (in Chinese)
pmid: 30183111 |
|
|
(邬林洋, 钟大猷, 刘文博, 有机化学, 2021, 41, 4083.)
pmid: 30183111 |
|
| [12] |
(a) Ng, K.-H.; Chan, A. S. C.; Yu, W.-Y. J. Am. Chem. Soc. 2010, 132, 12862.
doi: 10.1021/ja106364r pmid: 30978019 |
|
(b) Grohmann, C.; Wang, H.; Glorius, F. Org. Lett. 2013, 15, 3014.
doi: 10.1021/ol401209f pmid: 30978019 |
|
|
(c) John, A.; Byun, J.; Nicholas, K. M. Chem. Commun. 2013, 49, 10965.
doi: 10.1039/c3cc46412a pmid: 30978019 |
|
|
(d) Zhou, B.; Du, J.; Yang, Y.; Feng, H.; Li, Y. Org. Lett. 2014, 16, 592.
doi: 10.1021/ol403477w pmid: 30978019 |
|
|
(e) Shi, J.; Zhao, G.; Wang, X.; Xu, H. E.; Yi, W. Org. Biomol. Chem. 2014, 12, 6831.
doi: 10.1039/C4OB00637B pmid: 30978019 |
|
|
(f) Huh, S.; Hong, S. Y.; Chang, S. Org. Lett. 2019, 21, 2808.
doi: 10.1021/acs.orglett.9b00791 pmid: 30978019 |
|
|
(g) Wang, H.; Park, Y.; Bai, Z. Q.; Chang, S.; He, G.; Chen, G. J. Am. Chem. Soc. 2019, 141, 7194.
doi: 10.1021/jacs.9b02811 pmid: 30978019 |
|
|
(h) Guo, Q.; Ren, X.; Lu, Z. Org. Lett. 2019, 21, 880.
doi: 10.1021/acs.orglett.8b03299 pmid: 30978019 |
|
|
(i) Jung, H.; Keum, H.; Kweon, J.; Chang, S. J. Am. Chem. Soc. 2020, 142, 5811.
doi: 10.1021/jacs.0c00868 pmid: 30978019 |
|
| [13] |
(a) Bräse, S.; Gil, C.; Knepper, K.; Zimmermann, V. Angew. Chem., nt. Ed. 2005, 44, 5188.
pmid: 32357006 |
|
(b) Clayden, J.; Donnard, M.; Lefranc, J.; Tetlow, D. J. Chem. Commun. 2011, 47, 4624.
doi: 10.1039/c1cc00049g pmid: 32357006 |
|
|
(c) Zhou, H.; Hong, J.; Huang, J.; Chen, Z. Asian J. Org. Chem. 2017, 6, 817.
doi: 10.1002/ajoc.v6.7 pmid: 32357006 |
|
|
(d) Li, W. H.; Dong, L. Adv. Synth. Catal. 2018, 360, 1104.
doi: 10.1002/adsc.v360.6 pmid: 32357006 |
|
|
(e) Bakhoda, A.; Jiang, Q.; Badiei, Y. M.; Bertke, J. A.; Cundari, T. R.; Warren, T. H. Angew. Chem., nt. Ed. 2019, 58, 3421.
pmid: 32357006 |
|
|
(f) Yoshitake, M.; Hayashi, H.; Uchida, T. Org. Lett. 2020, 22, 4021.
doi: 10.1021/acs.orglett.0c01373 pmid: 32357006 |
|
| [14] |
Wang, H.; Jung, H.; Song, F.; Zhu, S.; Bai, Z.; Chen, D.; He, G.; Chang, S.; Chen, G. Nat. Chem. 2021, 13, 378.
doi: 10.1038/s41557-021-00650-0 |
| [15] |
Ball, R. G.; Graham, W. A. G.; Heinekey, D. M.; Hoyano, J. K.; McMaster, A. D.; Mattson, B. M.; Michel, S. T. Inorg. Chem. 1990, 29, 2023.
doi: 10.1021/ic00335a051 |
| [16] |
Le Grel, P.; Salaün, A.; Mocquet, C.; Le Grel, B.; Roisnel, T.; Potel, M. J. Org. Chem. 2011, 76, 8756.
doi: 10.1021/jo201390b |
| [17] |
Han, S.; Shin, Y.; Sharma, S.; Mishra, N. K.; Park, J.; Kim, M.; Kim, M.; Jang, J.; Kim, I. S. Org. Lett. 2014, 16, 2494.
doi: 10.1021/ol500865j |
| [18] |
Zhan, F.; Liang, G. Angew. Chem., nt. Ed. 2013, 52, 1266.
|
| [1] | 蒋旺, 史壮志. 芳烃间/对位选择性碳氢硼化反应研究进展[J]. 有机化学, 2023, 43(5): 1691-1705. |
| [2] | 杨幸, 刘旭, 王丽佳. 导向基辅助的过渡金属催化C(sp3)—H键氮宾插入反应研究进展[J]. 有机化学, 2023, 43(3): 914-923. |
| [3] | 徐欢, 吴鸿飞, 张晓鸣, 路星星, 孙腾达, 亓悦, 林誉凡, 杨新玲, 张莉, 凌云. 含1,2,3,4-四氢异喹啉片段磺酰肼和酰肼类化合物的设计、合成及生物活性研究[J]. 有机化学, 2023, 43(2): 725-733. |
| [4] | 景智霞, 杜建喜, 蒋平, 阿布拉江•克依木. 四丁基碘化胺介导烷基酰胺与酰肼一锅法构建1,3,4-噁二唑衍生物[J]. 有机化学, 2023, 43(11): 3930-3938. |
| [5] | 洪科苗, 黄晶晶, 姚铭瀚, 徐新芳. 氮宾/炔烃复分解串联反应研究进展[J]. 有机化学, 2022, 42(2): 344-352. |
| [6] | 马豪杰, 周小强, 韩波, 李然, 侯雪艳, 姬星月, 张玉琦, 黄国生, 王记江. 无催化剂一锅法构建取代磺酰吡唑[J]. 有机化学, 2021, 41(9): 3710-3716. |
| [7] | 周进, 孙宏顺, 李玉龙, 蒋蕻, 郭成, 沈临江. 一种大环类双核非离子型磁共振对比剂的合成及弛豫性能[J]. 有机化学, 2021, 41(7): 2767-2773. |
| [8] | 马豪杰, 孙洲, 刘金磊, 张夏, 崔华莉, 张玉琦, 王记江. CBr4促进的分子间环化反应: 高效合成取代N-酰基吡唑[J]. 有机化学, 2021, 41(11): 4353-4360. |
| [9] | 邬林洋, 钟大猷, 刘文博. 无配体参与的铁催化分子内C(sp3)—H键胺化合成咪唑啉酮[J]. 有机化学, 2021, 41(10): 4083-4087. |
| [10] | 彭美, 郑扬帆, 黄浩, 叶佳, 邓兴国, 何纯莲. 可见光促进N-苯丙炔胺与磺酰肼的环化:在无碱和催化剂下快速合成3-磺酰基喹啉衍生物[J]. 有机化学, 2020, 40(7): 2078-2085. |
| [11] | 虎永琴, 黄丹凤, 王克虎, 赵转霞, 赵芳霞, 徐炜刚, 胡雨来. 三氟甲基酰腙与烯丙基硅或烯丙基硼试剂的烯丙基化反应研究[J]. 有机化学, 2020, 40(6): 1689-1696. |
| [12] | 徐炜刚, 黄丹凤, 王克虎, 赵芳霞, 赵转霞, 虎永琴, 苏瀛鹏, 胡雨来. 三氟甲基酰腙的氰基化反应研究[J]. 有机化学, 2020, 40(4): 922-929. |
| [13] | 王林, 杨丽丽, 欧云付, 徐石海, 林啟福, 杨定乔. 铂催化氧杂二环烯烃与芳基磺酰肼的顺式-立体控制开环反应[J]. 有机化学, 2020, 40(12): 4228-4236. |
| [14] | 李毅, 万结平. 磺酰肼和二硫缩烯酮区域选择性环化反应合成3-烷硫基取代吡唑[J]. 有机化学, 2020, 40(11): 3889-3894. |
| [15] | 田飞, 张键, 杨武林, 邓卫平. 协同催化模式在金属铱催化不对称烯丙基取代反应中的应用研究进展[J]. 有机化学, 2020, 40(10): 3262-3278. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||