有机化学 ›› 2022, Vol. 42 ›› Issue (12): 3979-3994.DOI: 10.6023/cjoc202209025 上一篇 下一篇
所属专题: 自由基化学专辑
综述与进展
收稿日期:2022-09-19
修回日期:2022-10-17
发布日期:2022-11-07
通讯作者:
钟建基
基金资助:
Qian Xiaoa, Qing-Xiao Tongb, Jian-Ji Zhongb( )
)
Received:2022-09-19
Revised:2022-10-17
Published:2022-11-07
Contact:
Jian-Ji Zhong
Supported by:文章分享

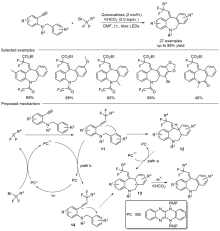
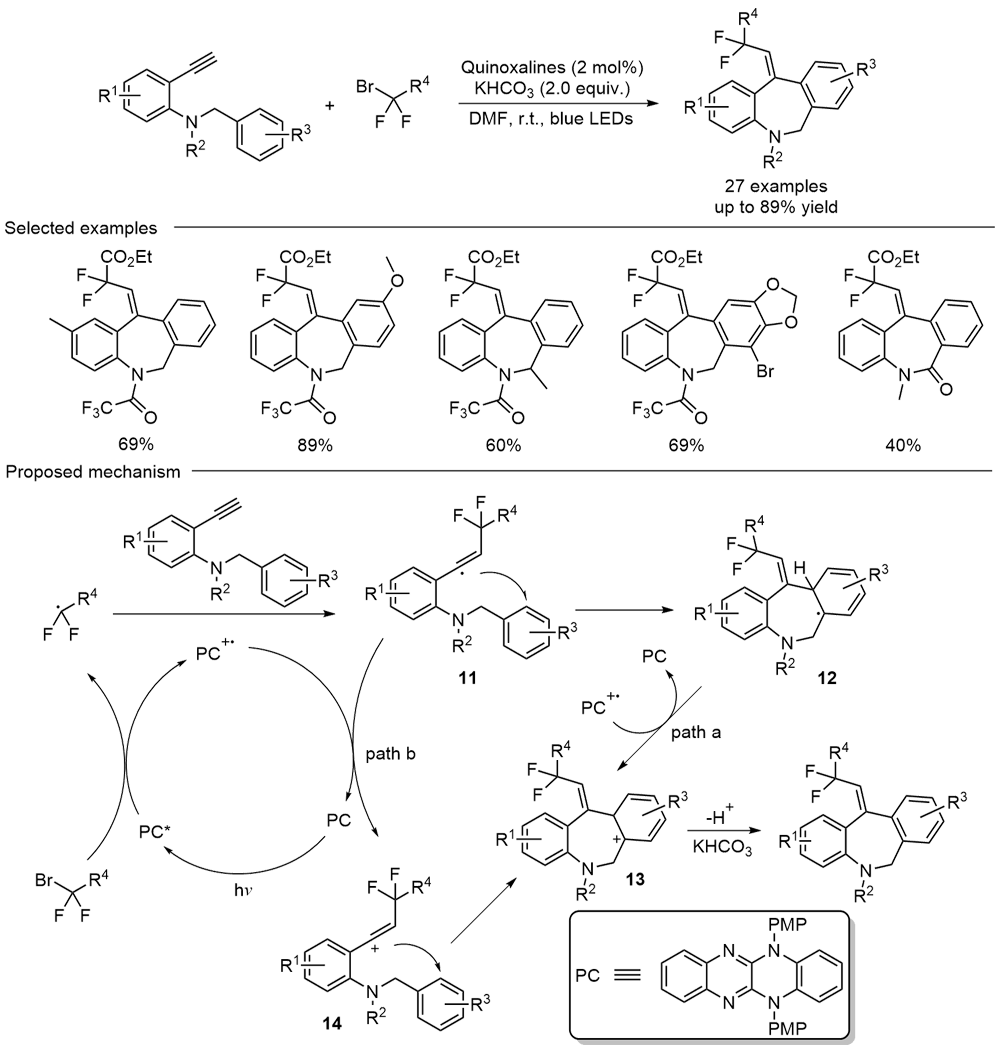
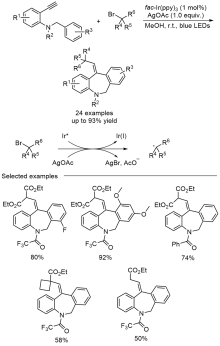
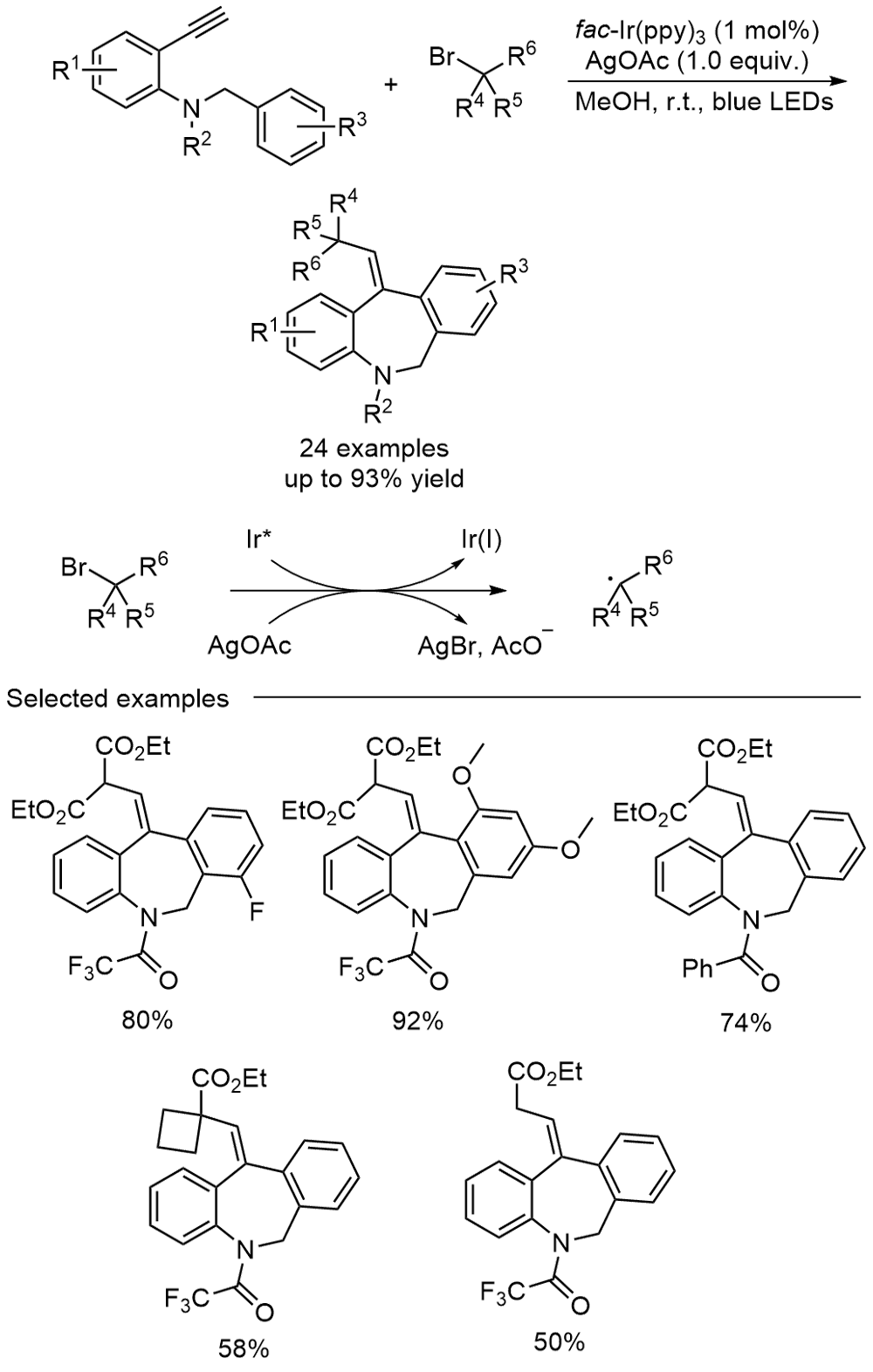
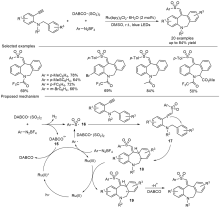
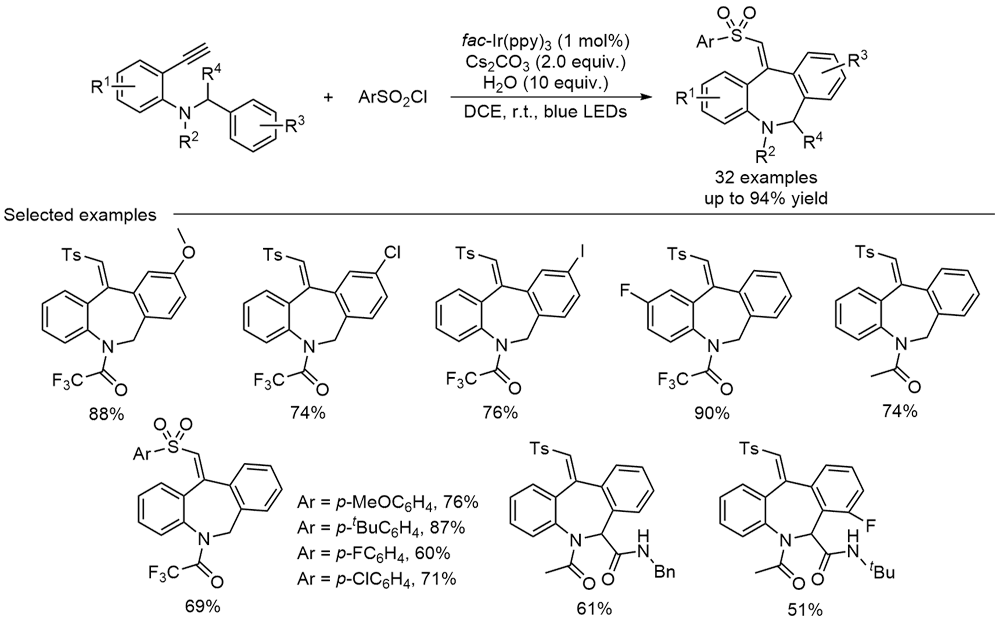
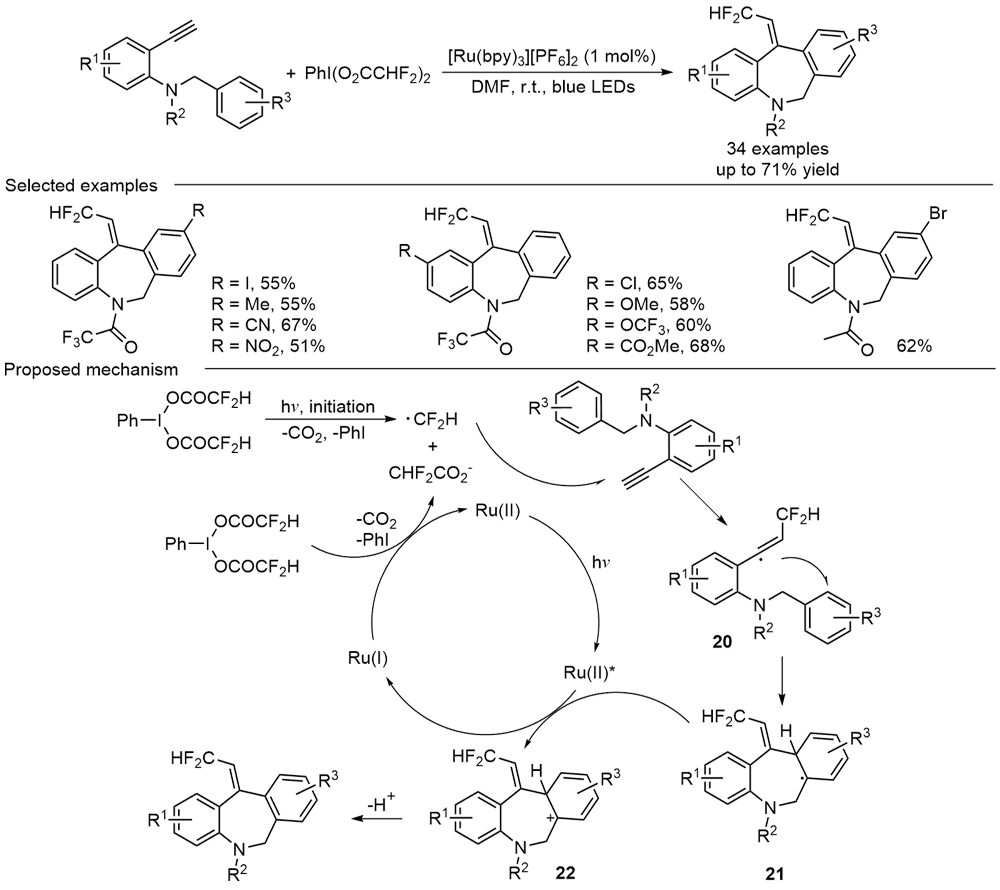
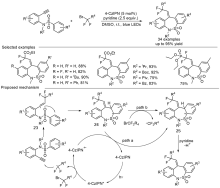
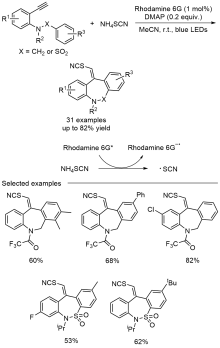
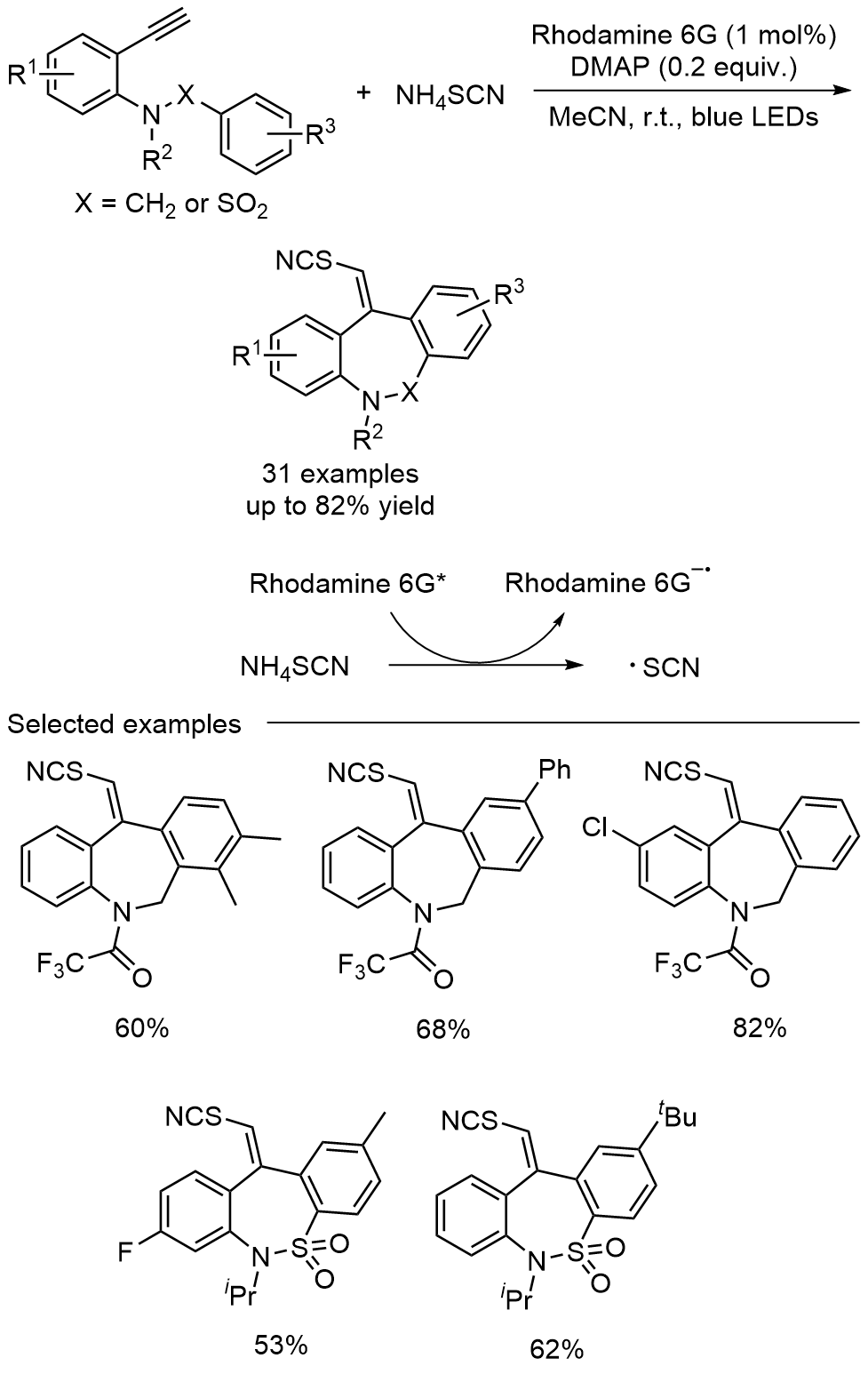
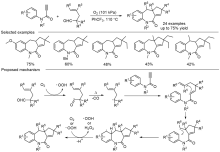
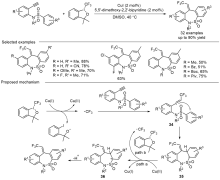
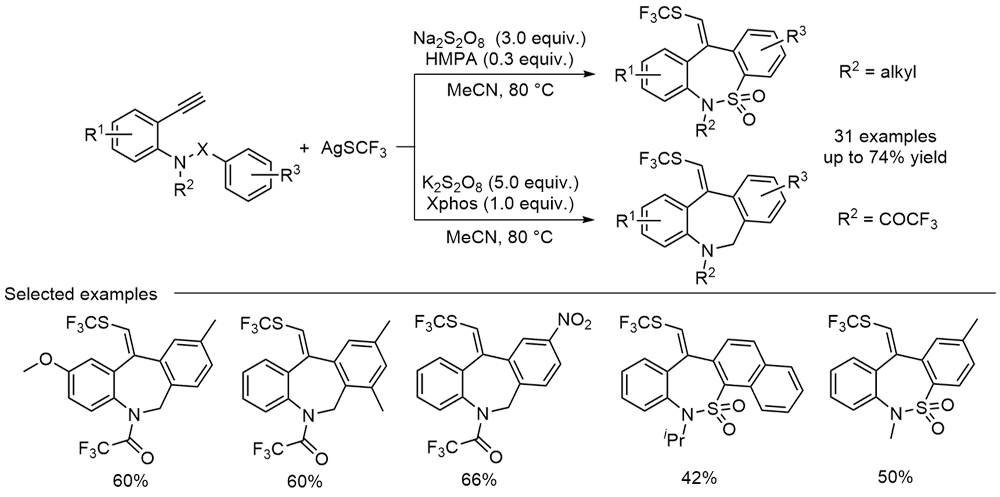
苯并吖庚因骨架衍生物是一类重要的七元含氮杂环化合物, 广泛存在于天然产物和药物分子中, 具有多样的生物活性. 因此, 开发绿色、高效的苯并吖庚因骨架衍生物合成方法备受关注. 近年来, 自由基参与的串联环化反应凭借其独特的优势已逐渐发展成为构建该类骨架化合物的一种强有力工具. 根据不同的反应驱动力, 从光化学、电化学和热化学三方面系统地概括了近五年来通过自由基串联环化反应制备苯并吖庚因骨架衍生物的研究进展.
肖潜, 佟庆笑, 钟建基. 基于自由基串联环化反应合成苯并吖庚因衍生物的研究进展[J]. 有机化学, 2022, 42(12): 3979-3994.
Qian Xiao, Qing-Xiao Tong, Jian-Ji Zhong. Recent Progress on the Synthesis of Benzazepine Derivatives via Radical Cascade Cyclization Reactions[J]. Chinese Journal of Organic Chemistry, 2022, 42(12): 3979-3994.










| [1] |
Lebegue, N.; Gallet, S.; Flouquet, N.; Carato, P.; Pfeiffer, B.; Renard, P.; Léonce, S.; Pierré, A.; Chavatte, P.; Berthelot, P. J. Med. Chem. 2005, 48, 7363.
doi: 10.1021/jm0503897 |
| [2] |
Gilleron, P.; Wlodarczyk, N.; Houssin, R.; Farce, A.; Laconde, G.; Goossens, J.-F.; Lemoine, A.; Pommery, N.; Hénichart, J.-P.; Millet, R. Bioorg. Med. Chem. Lett. 2007, 17, 5465.
pmid: 17827015 |
| [3] |
Srinivasa Rao, D. V. N.; Dandala, R.; Handa, V. K.; Sivakumaran, M.; Raghava Reddy, A. V.; Naidu, A. Org. Prep. Proced. Int. 2007, 39, 399.
doi: 10.1080/00304940709458595 |
| [4] |
Al-Qawasmeh, R. A.; Lee, Y.; Cao, M.-Y.; Gu, X.; Viau, S.; Lightfoot, J.; Wright, J. A.; Young, A. H. Bioorg. Med. Chem. Lett. 2009, 19, 104.
doi: 10.1016/j.bmcl.2008.11.001 pmid: 19027297 |
| [5] |
Aoyama, A.; Endo-Umeda, K.; Kishida, K.; Ohgane, K.; Noguchi- Yachide, T.; Aoyama, H.; Ishikawa, M.; Miyachi, H.; Makishima, M.; Hashimoto, Y. J. Med. Chem. 2012, 55, 7360.
doi: 10.1021/jm3002394 |
| [6] |
Watthey, J. W. H.; Stanton, J. L.; Desai, M.; Babiarz, J. E.; Finn, B. M. J. Med. Chem. 1985, 28, 1511.
pmid: 2995669 |
| [7] |
O’Grady, M. R.; O’Sullivan, M. L.; Minors, S. L.; Horne, R. J. Vet. Intern. Med. 2009, 23, 977.
doi: 10.1111/j.1939-1676.2009.0346.x |
| [8] |
ter Laak, A. M.; Venhorst, J.; Donne-Op den Kelder, G. M.; Timmerman, H. J. Med. Chem. 1995, 38, 3351.
pmid: 7650688 |
| [9] |
Wagstaff, A. J.; Ormrod, D.; Spencer, C. M. CNS Drugs 2001, 15, 231.
pmid: 11463130 |
| [10] |
Gassaway, M. M.; Rives, M.-L.; Kruegel, A. C.; Javitch, J. A.; Sames, D. Transl. Psychiatry 2014, 4, e411.
doi: 10.1038/tp.2014.30 |
| [11] |
Yang, B. H.; Buchwald, S. L. Org. Lett. 1999, 1, 35.
pmid: 10822529 |
| [12] |
Merten, S.; Fröhlich, R.; Kataeva, O.; Metz, P. Adv. Synth. Catal. 2005, 347, 754.
doi: 10.1002/adsc.200404372 |
| [13] |
Cao, H.; Vieira, T. O.; Alper, H. Org. Lett. 2011, 13, 11.
doi: 10.1021/ol102699a |
| [14] |
Roszkowski, P.; Maurin, J. K.; Czarnocki, Z. Beilstein J. Org. Chem. 2015, 11, 1509.
doi: 10.3762/bjoc.11.164 pmid: 26425208 |
| [15] |
Samineni, R.; Bandi, C. R. C.; Srihari, P.; Mehta, G. Org. Lett. 2016, 18, 6184.
pmid: 27934377 |
| [16] |
Snider, B. B. Chem. Rev. 1996, 96, 339.
pmid: 11848756 |
| [17] |
Xuan, J.; Studer, A. Chem. Soc. Rev. 2017, 46, 4329.
doi: 10.1039/c6cs00912c pmid: 28585948 |
| [18] |
Sun, K.; Wang, X.; Li, C.; Wang, H.; Li, L. Org. Chem. Front. 2020, 7, 3100.
doi: 10.1039/D0QO00849D |
| [19] |
Liao, J.; Yang, X.; Ouyang, L.; Lai, Y.; Huang, J.; Luo, R. Org. Chem. Front. 2021, 8, 1345.
doi: 10.1039/D0QO01453B |
| [20] |
Zhou, X.; Zhang, A.; Zhang, Q.; Liu, Q.; Xuan, J. Chin. J. Org. Chem. 2022, 42, 2488. (in Chinese)
doi: 10.6023/cjoc202204005 |
|
( 周旭煜, 张爱君, 张庆庆, 刘庆安, 宣俊, 有机化学, 2022, 42, 2488.)
doi: 10.6023/cjoc202204005 |
|
| [21] |
Chen, B.; Wu, L. Z.; Tung, C. H. Acc. Chem. Res. 2018, 51, 2512.
doi: 10.1021/acs.accounts.8b00267 |
| [22] |
Guo, W.; Tao, K.; Tan, W.; Zhao, M.; Zheng, L.; Fan, X. Org. Chem. Front. 2019, 6, 2048.
doi: 10.1039/C8QO01353E |
| [23] |
Zhang, H.; Xiao, Q.; Qi, X.-K.; Gao, X.-W.; Tong, Q.-X.; Zhong, J.-J. Chem. Commun. 2020, 56, 12530.
doi: 10.1039/D0CC05580H |
| [24] |
Yu, X.-Y.; Zhao, Q.-Q.; Chen, J.; Xiao, W.-J.; Chen, J.-R. Acc. Chem. Res. 2020, 53, 1066.
doi: 10.1021/acs.accounts.0c00090 |
| [25] |
Xiao, Q.; Zhang, H.; Li, J.-H.; Jian, J.-X.; Tong, Q.-X.; Zhong, J.-J. Org. Lett. 2021, 23, 3604.
doi: 10.1021/acs.orglett.1c00999 |
| [26] |
Bell, J. D.; Murphy, J. A. Chem. Soc. Rev. 2021, 50, 9540.
doi: 10.1039/D1CS00311A |
| [27] |
Lu, F.-D.; Chen, J.; Jiang, X.; Chen, J.-R.; Lu, L.-Q.; Xiao, W.-J. Chem. Soc. Rev. 2021, 50, 12808.
doi: 10.1039/D1CS00210D |
| [28] |
Yu, X.; Chen, J.; Xiao, W. Chem. Rev. 2021, 121, 506.
doi: 10.1021/acs.chemrev.0c00030 |
| [29] |
Yin, Y.; Zhao, X.; Jiang, Z. Chin. J. Org. Chem. 2022, 42, 1609. (in Chinese)
doi: 10.6023/cjoc202201047 |
|
( 尹艳丽, 赵筱薇, 江智勇, 有机化学, 2022, 42, 1609.)
doi: 10.6023/cjoc202201047 |
|
| [30] |
Xiao, Q.; Tong, Q.-X.; Zhong, J.-J. Molecules 2022, 27, 619.
doi: 10.3390/molecules27030619 |
| [31] |
Zhao, Y.; Chen, J.-R.; Xiao, W.-J. Org. Lett. 2018, 20, 224.
doi: 10.1021/acs.orglett.7b03588 pmid: 29257700 |
| [32] |
Qi, X.-K.; Zhang, H.; Pan, Z.-T.; Liang, R.-B.; Zhu, C.-M.; Li, J.-H.; Tong, Q.-X.; Gao, X.-W.; Wu, L.-Z.; Zhong, J.-J. Chem. Commun. 2019, 55, 10848.
doi: 10.1039/C9CC04977K |
| [33] |
Liu, D.; Jiao, M.-J.; Wang, X.-Z.; Xu, P.-F. Org. Lett. 2019, 21, 4745.
doi: 10.1021/acs.orglett.9b01629 |
| [34] |
Zhang, T.; Luo, M.; Teng, F.; Li, Y.; Hu, M.; Li, J. Adv. Synth. Catal. 2019, 361, 4645.
doi: 10.1002/adsc.201900776 |
| [35] |
Yao, Y.; Yin, Z.; He, F.-S.; Qin, X.; Xie, W.; Wu, J. Chem. Commun. 2021, 57, 2883.
doi: 10.1039/D0CC07927H |
| [36] |
Qu, C.; Song, G.; Ou, J.; Tang, D.; Xu, Z.; Chen, Z. Chin. J. Chem. 2021, 39, 2220.
doi: 10.1002/cjoc.202100194 |
| [37] |
Zhou, N.; Kuang, K.; Wu, M.; Wu, S.; Xia, Z.; Xu, Q.; Zhang, M. Org. Chem. Front. 2021, 8, 4095.
doi: 10.1039/D1QO00611H |
| [38] |
Li, J.; Huang, C.-Y.; Han, J.-T.; Li, C.-J. ACS Catal. 2021, 11, 14148.
doi: 10.1021/acscatal.1c04073 |
| [39] |
Wang, L.; Zhang, Y.; Zhu, T.; Wu, J. J. Org. Chem. 2022, 87, 7551.
doi: 10.1021/acs.joc.2c00584 |
| [40] |
Xiao, Q.; Lu, M.; Deng, Y.; Jian, J.-X.; Tong, Q.-X.; Zhong, J.-J. Org. Lett. 2021, 23, 9303.
doi: 10.1021/acs.orglett.1c03700 |
| [41] |
Zheng, X.; Shen, Q.; Yin, C.; Li, L.; Zhong, T.; Yu, C. Adv. Synth. Catal. 2022, 364, 1750.
doi: 10.1002/adsc.202200292 |
| [42] |
Chen, S.; Yan, Q.; Fan, J.; Gao, Y.; Yang, X.; Li, L.; Liu, Z.; Li, Z. Green Chem. 2022, 24, 4742.
doi: 10.1039/D2GC01276F |
| [43] |
Yuan, Y.; Lei, A. Acc. Chem. Res. 2019, 52, 3309.
doi: 10.1021/acs.accounts.9b00512 |
| [44] |
Xiong, P.; Xu, H.-C. Acc. Chem. Res. 2019, 52, 3339.
doi: 10.1021/acs.accounts.9b00472 |
| [45] |
Chen, N.; Xu, H. Chem. Rec. 2021, 21, 2306.
doi: 10.1002/tcr.202100048 |
| [46] |
Liu, Y.; Wang, Z.; Meng, J.; Li, C.; Sun, K. Chin. J. Org. Chem. 2022, 42, 100. (in Chinese)
doi: 10.6023/cjoc202106051 |
|
( 刘颖杰, 王智传, 孟建萍, 李晨, 孙凯, 有机化学, 2022, 42, 100.)
doi: 10.6023/cjoc202106051 |
|
| [47] |
Li, Y.; Hu, M.; Li, J.-H. ACS Catal. 2017, 7, 6757.
doi: 10.1021/acscatal.7b02061 |
| [48] |
Li, Y.; Li, J.-H. Org. Lett. 2018, 20, 5323.
doi: 10.1021/acs.orglett.8b02243 |
| [49] |
Pan, G.-A.; Li, Y.; Li, J.-H. Org. Chem. Front. 2020, 7, 2486.
doi: 10.1039/D0QO00651C |
| [50] |
Zhang, Z.-Q.; Xu, Y.-H.; Dai, J.-C.; Li, Y.; Sheng, J.; Wang, X.-S. Org. Lett. 2021, 23, 2194.
doi: 10.1021/acs.orglett.1c00344 |
| [51] |
Chen, X.; Pei, C.; Liu, B.; Li, J.; Zou, D.; Wu, Y.; Wu, Y. Chem. Commun. 2022, 1.
|
| [52] |
Ren, Y.; Yan, Q.; Li, Y.; Gao, Y.; Zhao, J.; Li, L.; Liu, Z.-Q.; Li, Z. J. Org. Chem. 2022, 87, 8773.
doi: 10.1021/acs.joc.2c00623 |
| [53] |
Xiong, P.; Xu, H.-H.; Song, J.; Xu, H.-C. J. Am. Chem. Soc. 2018, 140, 2460.
doi: 10.1021/jacs.8b00391 pmid: 29406700 |
| [1] | 黄芬, 罗维纬, 周俊. 基于C—H键断裂的多氯烷基化反应研究进展[J]. 有机化学, 2023, 43(7): 2368-2390. |
| [2] | 田钰, 张娟, 高文超, 常宏宏. 二甲亚砜作为甲基化试剂在有机合成中的应用[J]. 有机化学, 2023, 43(7): 2391-2406. |
| [3] | 任志军, 罗维纬, 周俊. 银介导的N-芳基丙烯酰胺串联环化反应研究进展[J]. 有机化学, 2023, 43(6): 2026-2039. |
| [4] | 李靖鹏, 黄顺桃, 杨棋, 李伟强, 刘腾, 黄超. 利用连续流动技术合成(Z)-N-乙烯基取代N,O-缩醛[J]. 有机化学, 2023, 43(4): 1550-1558. |
| [5] | 赵金晓, 魏彤辉, 柯森, 李毅. 可见光催化合成二氟烷基取代的多环吲哚化合物[J]. 有机化学, 2023, 43(3): 1102-1114. |
| [6] | 胡朝明, 吴纪红, 吴晶晶, 吴范宏. 直接三氟甲硒基化反应研究进展[J]. 有机化学, 2023, 43(1): 36-56. |
| [7] | 刘东汉, 鲁席杭, 柴张梦洁, 杨浩琦, 孙瑜琳, 余富朝. 构建2H-吡咯-2-酮骨架的研究进展[J]. 有机化学, 2023, 43(1): 57-73. |
| [8] | 宇世伟, 陈兆华, 陈淇, 林舒婷, 何金萍, 陶冠燊, 汪朝阳. 硫代磺酸酯的合成与应用研究进展[J]. 有机化学, 2022, 42(8): 2322-2330. |
| [9] | 张力之, 廖永剑, 陈宁, 黄磊, 周敏. 叔丁醇钾促进的环化和偶联反应[J]. 有机化学, 2022, 42(7): 1950-1959. |
| [10] | 李亚东, 吴鹏举, 杨志勇. 可见光催化苯并噁唑与α-酮酸合成芳基苯并噁唑[J]. 有机化学, 2022, 42(6): 1770-1777. |
| [11] | 乐柏佟, 吴新鑫, 朱晨. 烯基自由基参与的分子内氢原子转移反应的新进展[J]. 有机化学, 2022, 42(2): 458-470. |
| [12] | 孙亚敏, 李锡勇, 袁金伟, 余加琳, 刘帅楠. 温和条件下以芳基胺为原料CuI催化下区域选择性合成3-芳基香豆素[J]. 有机化学, 2022, 42(2): 631-640. |
| [13] | 许耀辉, 吴镇, 吴新鑫, 朱晨. 无过渡金属参与的醚、醛和酰胺C—H键自由基炔基化和烯丙基化反应[J]. 有机化学, 2022, 42(12): 4340-4349. |
| [14] | 高盼盼, 肖文精, 陈加荣. 可见光促进的烯烃合成研究进展[J]. 有机化学, 2022, 42(12): 3923-3943. |
| [15] | 张孟琪, 南光明, 赵晓辉, 魏伟. 可见光介导喹喔啉-2(1H)-酮C3-H缩醛化反应[J]. 有机化学, 2022, 42(12): 4315-4322. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||