有机化学 ›› 2024, Vol. 44 ›› Issue (9): 2658-2681.DOI: 10.6023/cjoc202402007 上一篇 下一篇
综述与进展
收稿日期:2024-02-07
修回日期:2024-04-09
发布日期:2024-05-16
通讯作者:
周俊
基金资助:
Zhaoyang Zhang, Weiwei Luo, Jun Zhou( )
)
Received:2024-02-07
Revised:2024-04-09
Published:2024-05-16
Contact:
Jun Zhou
Supported by:文章分享

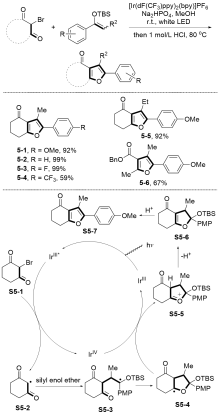
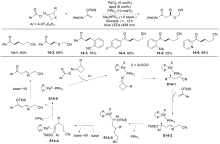
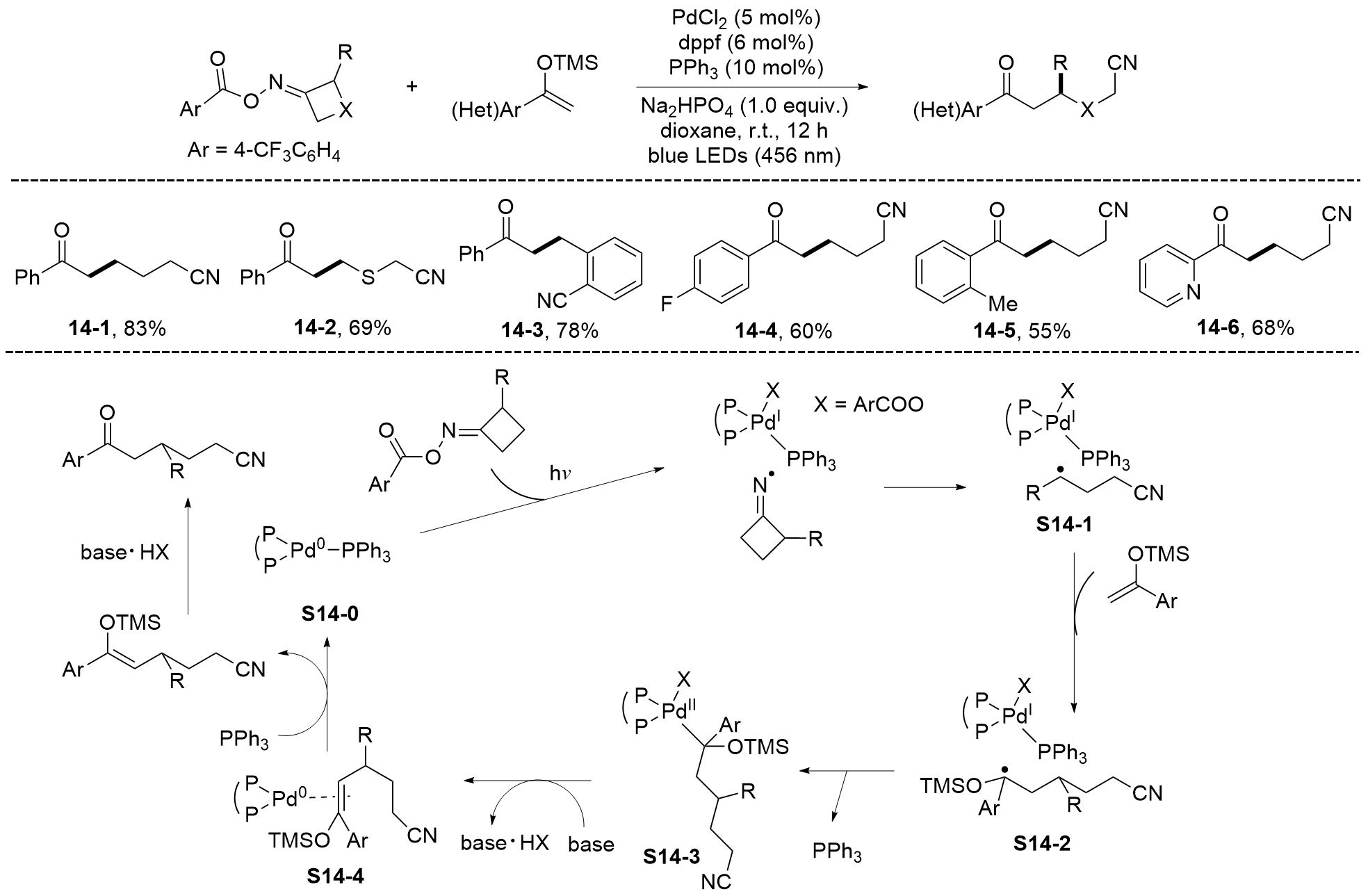
由于烯醇硅醚具有独特的反应活性, 其在有机合成中得到了广泛的应用. 烯醇硅醚能参与Mukaiyama aldol反应和Mukaiyama-Michael加成反应等经典有机合成反应, 从而构建新的C—C键. 但是由于离子型反应的局限性, 很多复杂分子的合成需要借助更多新型高效的反应, 而烯醇硅醚参与的自由基反应能够在多种反应体系中展现出良好的性能. 总结了近十年来烯醇硅醚作为多功能和高效的反应前体合成α-取代羰基化合物和其他功能有机分子的反应, 并讨论了各种反应体系(光促进、金属催化、无金属参与和电催化)下研究人员对反应的设计、机理的研究以及该研究课题未来的展望.
张朝阳, 罗维纬, 周俊. 烯醇硅醚参与的自由基反应研究进展[J]. 有机化学, 2024, 44(9): 2658-2681.
Zhaoyang Zhang, Weiwei Luo, Jun Zhou. Research Progress of Radical Reactions Involving Silyl Enol Ethers[J]. Chinese Journal of Organic Chemistry, 2024, 44(9): 2658-2681.

| [1] |
House, H. O.; Kramar, V. J. Org. Chem. 1963, 28, 3362.
|
| [2] |
Stork, G.; Hudrlik, P, F. J. Am. Chem. Soc. 1968, 90, 4462.
|
| [3] |
(a) Mukaiyama, T.; Banno, K.; Narasaka, K. J. Am. Chem. Soc. 1974, 96, 7503.
pmid: 15957949 |
|
(b) Adhikari, S.; Caille, S.; Hanbauer, M.; Ngo, V. X.; Overman, L. E. Org. Lett. 2005, 7, 2795.
pmid: 15957949 |
|
|
(c) Webb, M. R.; Addie, M. S.; Crawforth, C. M.; Dale, J. W.; Franci, X.; Pizzonero, M.; Donald, C.; Taylor, R. J. K. Tetrahedron 2008, 64, 4778.
pmid: 15957949 |
|
|
(d) Gao, S. H.; Wang, Q. L.; Chen, C. J. Am. Chem. Soc. 2009, 131, 1410.
pmid: 15957949 |
|
| [4] |
(a) Mukaiyama, T. Angew. Chem., Int. Ed. 2004, 43, 5590.
|
|
(b) Frías, M.; Cieślik, W.; Fraile, A.; Rosado-Abón, A.; Garrido-Castro, A. F.; Yuste. F.; Alemán. J. Chem.-Eur. J. 2018, 24, 10906.
|
|
|
(c) Wang, X.; Adachi, S.; Iwai, H.; Takatsuki, H.; Fujita, K.; Kubo, M.; Oku, A.; Harada, T. J. Org. Chem. 2003, 68, 10046.
|
|
| [5] |
Seo, Y. H.; Carroll, K. S. PNAS 2009, 106, 16163.
|
| [6] |
Wright, W. C.; Chenge, J.; Wang, J. H.; Girvan, H. M.; Yang, L.; Chai, S. C.; Huber, A. D.; Wu, J.; Oladimeji, P. O.; Munro, A. W.; Chen, T. S. J. Med. Chem. 2020, 63, 1415.
|
| [7] |
Tsuyoshi, M.; Hidezumi, K.; Hidezumi, K.; Hidezumi, K.; Ya-sumoto, A. CN 1242771, 2000. (in Chinese).
|
|
(松本刚, 河合英村, 冈野清, 森胜之, 足立泰基, CN 1242771, 2000.)
|
|
| [8] |
Allan, G. M.; Vicker, N.; Lawrence, H. R.; Tutill, H. J.; Day, J. M.; Huchet, M.; Ferrandis, E.; Reed, M. J.; Purohit, A.; Potter, B. V. L. Bioorg. Med. Chem. 2008, 16, 4438.
|
| [9] |
Guo, M. M.; Yu, Z. L.; Chen, Y. L.; Ge, D. H.; Ma, M. T.; Shen, Z. L.; Chu, X. Q. Chin. J. Org. Chem. 2022, 42, 3562 (in Chinese).
|
|
(郭檬檬, 于子伦, 陈玉兰, 葛丹华, 马猛涛, 沈志良, 褚雪强, 有机化学, 2022, 42, 3562.)
doi: 10.6023/cjoc202204060 |
|
| [10] |
Levin, V. V.; Dilman, A. D. Chem. Rec. 2023, 23, e202300038.
|
| [11] |
Huang, M. W.; Li, L.; Zhao, Z. G.; Chen, Q. Y.; Guo, Y. Synthesis 2015, 47, 3891.
|
| [12] |
Chernov, G. N.; Levin, V. V.; Kokorekin, V. A.; Struchkova, M. I.; Dilman, A. D. Adv. Synth. Catal. 2017, 359, 3063.
|
| [13] |
Scherbinina, S. I.; Fedorov, O. V.; Levin, V. V.; Kokorekin, V. A.; Struchkova, M. I.; Dilman, A. D. J. Org. Chem. 2017, 82, 12967.
doi: 10.1021/acs.joc.7b02467 pmid: 29172505 |
| [14] |
Yu, W.; Ouyang, Y.; Xu, X.-H.; Qing, F.-L. Chin. J. Chem. 2018, 36, 1024.
|
| [15] |
Esumi, N.; Suzuki, K.; Nishimoto, Y.; Yasuda, M. Org. Lett. 2016, 18, 5704.
|
| [16] |
Han, Y. Y.; Jiao, Y. Y.; Ren, D.; Hu, Z. T.; Shen, S.; Yu, S. Y. Asian J. Org. Chem. 2017, 6, 414.
|
| [17] |
Zhao, B.; Shang, R.; Wang, G, Z.; Wang, S. H.; Chen, H.; Fu, Y. ACS Catal. 2020, 10, 2, 1334.
|
| [18] |
Supranovich, V. I.; Levin, V. V.; Dilman, A. D. Beilstein J. Org. Chem. 2020, 16, 1550.
doi: 10.3762/bjoc.16.126 pmid: 32704320 |
| [19] |
Cao, H. Y.; Ma, S. S.; Feng, Y. H.; Guo, Y. W.; Jiao, P. Chem. Commun. 2022, 58, 1780.
|
| [20] |
Ma, R. S.; Deng, Z. B.; Wang, K. H.; Wang, J. J.; Huang, D. F.; Su, Y. P.; Hu, Y. L.; Lv, X. B. ACS. Omega 2022, 7, 14357.
|
| [21] |
Briand, M.; Thai, L.; Bourdreux, F.; Vanthuyne, N.; Moreau, X.; Magnier, E.; Anselmi, E.; Dagousset, G. Org. Lett. 2022, 24, 9375.
|
| [22] |
Cai, S. H.; Xie, J. H.; Song, S. J.; Ye, L.; Feng, C.; Loh, T. P. ACS Catal. 2016, 6, 5571.
|
| [23] |
(a) Kong, W. G.; Yu, C. J.; An, H. J.; Song, Q. L. Org. Lett. 2018, 20, 349.
|
|
(b) Maslak, P.; Narvaez, J. N. Angew. Chem., Int. Ed. Engl. 1990, 29, 283.
|
|
| [24] |
Zemtsov, A. A.; Ashirbaev, S. S.; Levin, V. V.; Kokorekin, V. A.; Korlyukov, A. A.; Dilman, A. D. J. Org. Chem. 2019, 84, 15745.
doi: 10.1021/acs.joc.9b02478 pmid: 31693367 |
| [25] |
Xing, W. L.; Shang, R.; Wang, G. Z.; Fu, Y. Chem. Commun. 2019, 95, 14291.
|
| [26] |
Luo, Q. Y.; Mao, R. Y.; Zhu, Y.; Wang, Y. H. J. Org. Chem. 2019, 84, 13897.
|
| [27] |
Spinnato, D.; Schweitzer-Chaput, B.; Goti, G.; Ošeka, M.; Melchiorre, P. Angew. Chem., Int. Ed. 2020, 59, 9485.
doi: 10.1002/anie.201915814 pmid: 32053279 |
| [28] |
Selmi-Higashi, E.; Zhang, J. L.; Cambeiro, X. C.; Arseniyadis, S. ; Org. Lett. 2021, 23, 4239.
|
| [29] |
He, F. S.; Bao, P.; Tang, Z. M.; Yu, F. Y.; Deng, W. P.; Wu, J. Org. Lett. 2022, 24, 2955.
|
| [30] |
Cui, W. W.; Guo, G. J.; Wang, Y. F.; Song, X. Y.; Lv, J.; Yang, D. S. Chem. Commun. 2023, 59, 6367.
|
| [31] |
Gong, X, X.; Ding, Y. C.; Fan, X. N.; Wu, J. Adv. Synth. Catal. 2017, 359, 2999.
|
| [32] |
Ye, S. Q.; Zhou, K. D.; Rojsitthisak, P.; Wu, J. Org. Chem. Front. 2020, 7, 14.
|
| [33] |
Huang, Q. P.; Li, W. P.; Li, R.; Zhao, L.; Wang, H. Y.; Li, X. F.; Wang, P.; He, C. Y. Tetrahedron Lett. 2022, 97, 153782.
|
| [34] |
Mao, R.Y.; Yuan, Z.; Li, Y. W.; Wu, J. Chem. Eur. J. 2017, 23, 8176.
|
| [35] |
Wang, J. X.; Ge, W.; Xing, W. L.; Fu, M. C. J. Org. Chem. 2021, 86, 18224.
|
| [36] |
Terlizzi, L. D.; Cola, I.; Raviola, C.; Fagnoni, M.; Protti, S. ACS Org. Inorg Au 2021, 1, 68.
doi: 10.1021/acsorginorgau.1c00020 pmid: 36855752 |
| [37] |
Liu, C.; Shen, N.; Shang, R. Org. Chem. Front. 2021, 8, 4166.
|
| [38] |
Dewanji, A.; van Dalsen, L.; Rossi-Ashton, J. A., Gasson, E.; Crisenza, G. E. M.; Procter, D. J. Nat. Chem. 2023, 15, 43.
|
| [39] |
Li, Y. L.; Liu, J.; Zhao, S.; Du, X. Z.; Guo, M. J.; Zhao, W. T.; Tang, X. Y.; Wang, G. W. Org. Lett. 2018, 20, 917.
|
| [40] |
Li, D. K. Tetrahedron. Lett. 2021, 87, 153551.
|
| [41] |
Li, D. K. J. Org. Chem. 2021, 86, 609.
|
| [42] |
Li, L.; Chen, Q. Y.; Guo, Y. J. Org. Chem. 2014, 79, 5145.
|
| [43] |
Jacquet, J.; Blanchard, S.; Derat, E.; Murr, M. D. E.; Fensterbank, L. Chem. Sci. 2016, 7, 2030.
doi: 10.1039/c5sc03636d pmid: 29899928 |
| [44] |
Amaya, T.; Maegawa, Y.; Masuda, T.; Osafune, Y.; Hirao, T. J. Am. Chem. Soc. 2015, 137, 10072.
doi: 10.1021/jacs.5b05058 pmid: 26244707 |
| [45] |
Amaya, T.; Osafune, Y.; Maegawa, Y.; Hirao, T. Chem. Asian J. 2017, 12, 1301.
|
| [46] |
Osafune, Y.; Jin, Y. Q.; Hirao, T.; Tobisu, M.; Amaya, T. Chem. Commun. 2020, 56, 11697.
|
| [47] |
Yang, H. B.; Selander, N. Chem.-Eur. J. 2017, 23, 1779.
|
| [48] |
Zhang, X. X.; Huang, H. M. Org. Lett. 2018, 20, 4998.
|
| [49] |
Xu, L.; Liu, X. Y.; Alvey, G. R.; Shatskiy, A.; Liu, J. Q.; Kärkäs, M. D.; Wang, X. S. Org. Lett. 2022, 24, 4513.
|
| [50] |
Zhang, T. Y.; Wu, Y.; Liu, S.; Tao, J. Q.; Yang, X.; Wang, X. Q.; Duan, X. H.; Guo, L. N. Org. Lett. 2023, 25, 4329.
|
| [51] |
Ge, H. C.; Du, K. Y.; Sheng, W. J. Chin. J. Org. Chem. 2020, 40, 1625 (in Chinese).
|
|
(葛浩程, 杜科莹, 盛卫坚, 有机化学, 2020, 40, 1625.)
doi: 10.6023/cjoc201911023 |
|
| [52] |
Liu, T. S.; Zheng, D. Q.; Ding, Y. C.; Fan, X. N.; Wu, J. Chem. Asian J. 2017, 12, 465.
|
| [53] |
Parida, K. N.; Pathe, G. K.; Maksymenko, S.; Szpilman, A. M. Beilstein J. Org. Chem. 2018, 14, 992.
|
| [54] |
Felipe-Blanco, D.; Gonzalez-Gomez, J. C. Adv. Synth. Catal. 2018, 360, 2773.
|
| [55] |
Tang, Y. C.; Qu, H.; Zhang, W. X.; Wang, F. F.; Wang, G. Chem. J. Chin. Univ. 2020, 41, 118 (in Chinese).
|
|
(唐裕才, 屈煌, 张文熙, 王菲菲, 王钢, 高等学校化学学报, 2020, 41, 118.)
doi: 10.7503/cjcu20190424 |
|
| [56] |
Strehl, J.; Hilt, G. Org. Lett. 2019, 21, 13, 5259.
|
| [57] |
Jud, W.; Sommer, F.; Kappe, C. O.; Cantillo, D. J. Org. Chem., 2021, 86, 16026.
|
| [58] |
Pastor, M.; Vayer, M.; Weinstabl, H.; Maulide, N. J. Org. Chem. 2022, 87, 606.
|
| [1] | 蒋镓西, 刘全忠. 乙烯基重氮化合物非金属卡宾机制参与的反应[J]. 有机化学, 2024, 44(9): 2640-2657. |
| [2] | 黄真茹, 金国顺, 陈天煜, 冯斌, 史鑫康, 陈敏方, 华路生, 徐清. 氢氧化铯催化温和有氧环化反应高效构建喹喔啉杂环衍生物[J]. 有机化学, 2024, 44(9): 2933-2942. |
| [3] | 陈倩, 韩召斌, 丁奎岭. 过渡金属催化芳香碳环的选择性不对称氢化[J]. 有机化学, 2024, 44(7): 2063-2076. |
| [4] | 陆玲依, 邱晓东. 自由基形式烯烃双烷基化反应研究进展[J]. 有机化学, 2024, 44(6): 1701-1718. |
| [5] | 田永盛, 魏斓枫, 黄嘉为, 韦玉, 徐亮, 刘帅. 四丁基三溴化铵促进的有机硼酸在无过渡金属条件下的脱硼硒化、溴化和羟基化反应[J]. 有机化学, 2024, 44(6): 1987-1997. |
| [6] | 徐光利, 韩鸿萍, 曹露微, 洪思敏, 海林悦, 崔香. 过渡金属催化1,3-共轭二烯基硼化合物合成研究进展[J]. 有机化学, 2024, 44(5): 1480-1493. |
| [7] | 李晨龙, 余志祥. 一氧化碳参与的过渡金属催化的插羰环加成反应研究进展[J]. 有机化学, 2024, 44(4): 1045-1068. |
| [8] | 郭凯杰, 符昕姝, 李靖, 陈艳, 胡美丽, 堵锡华, 谢屿阳, 何燕. 过渡金属催化C—S键活化与转化研究进展[J]. 有机化学, 2024, 44(4): 1124-1150. |
| [9] | 鞠国栋, 周冠宇, 赵应声. 三异丙基硅烷(TIPS)保护苯酚的无过渡金属催化区域选择性硫氰化反应[J]. 有机化学, 2024, 44(4): 1327-1336. |
| [10] | 彭天凤, 赵玉祥, 浦绍健, 罗娟, 刘腾, 缪应纯, 沈先福. 过渡金属催化的关键反应在异戊烯基吲哚生物碱全合成中的研究进展[J]. 有机化学, 2024, 44(4): 1160-1180. |
| [11] | 万云辉, 杨福美, 陈明瀚, 孙德立, 叶丹锋. 无过渡金属催化的N-苄基-N-叔丁氧羰基酰胺与不饱和醇的酯化反应[J]. 有机化学, 2024, 44(4): 1293-1300. |
| [12] | 高淳, 刘欣, 王明慧, 刘淑贤, 朱婷婷, 张怡康, 郝二军, 杨启亮. 电化学不对称合成反应的研究进展[J]. 有机化学, 2024, 44(3): 673-727. |
| [13] | 刘杰, 韩峰, 李双艳, 陈天煜, 陈建辉, 徐清. 无过渡金属参与甲基杂环化合物与醇的选择性有氧烯基化反应[J]. 有机化学, 2024, 44(2): 573-583. |
| [14] | 赵红琼, 于淼, 宋冬雪, 贾琦, 刘颖杰, 季宇彬, 许颖. 羧酸脱羧羟基化反应研究进展[J]. 有机化学, 2024, 44(1): 70-84. |
| [15] | 董江湖, 宣良明, 王池, 赵晨熙, 王海峰, 严琼姣, 汪伟, 陈芬儿. 无过渡金属或无光催化剂条件下可见光促进喹喔啉酮C(3)—H官能团化研究进展[J]. 有机化学, 2024, 44(1): 111-136. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||