有机化学 ›› 2022, Vol. 42 ›› Issue (4): 1033-1060.DOI: 10.6023/cjoc202110026 上一篇 下一篇
综述与进展
梁陆祺a,b, 张立志b,*( ), 彭永利a,*(
), 彭永利a,*( ), 刘会a,b,*(
), 刘会a,b,*( )
)
收稿日期:2021-10-19
修回日期:2021-12-03
发布日期:2021-12-22
通讯作者:
张立志, 彭永利, 刘会
基金资助:
Luqi Lianga,b, Lizhi Zhangb( ), Yongli Penga(
), Yongli Penga( ), Hui Liua,b(
), Hui Liua,b( )
)
Received:2021-10-19
Revised:2021-12-03
Published:2021-12-22
Contact:
Lizhi Zhang, Yongli Peng, Hui Liu
Supported by:文章分享
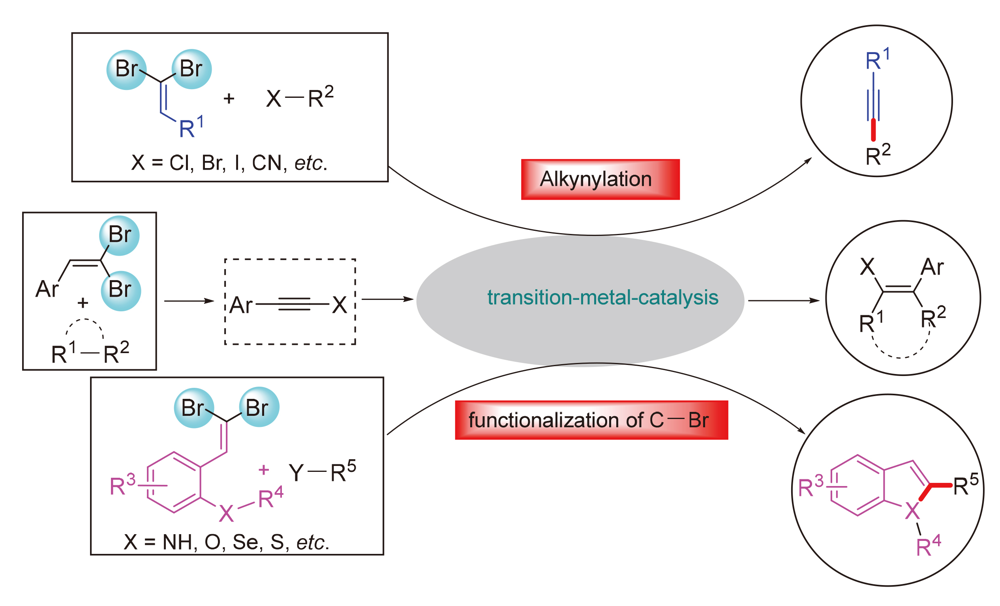
偕二溴烯烃衍生物是有机化学中非常重要的合成工具, 已被广泛应用于功能化分子的构建. 在过去几十年中, 金属催化(如铂、铜、银、金、镍)与偕二溴烯烃衍生物的转化已发展成为合成炔烃、色烯、吲哚、苯并吲哚及苯并噻吩等具有重要生理活性的苯并稠合杂环的有力工具. 总结了自2013年以来过渡金属催化的偕二溴烯烃衍生物转化的研究进展.
梁陆祺, 张立志, 彭永利, 刘会. 过渡金属催化偕二溴烯烃衍生物的偶联反应[J]. 有机化学, 2022, 42(4): 1033-1060.
Luqi Liang, Lizhi Zhang, Yongli Peng, Hui Liu. Transition-Metal Catalyzed Coupling Reactions of gem-Dibromovinyl Derivatives[J]. Chinese Journal of Organic Chemistry, 2022, 42(4): 1033-1060.
| [1] |
Chelucci, G. Chem. Rev. 2012, 112, 1344
doi: 10.1021/cr200165q pmid: 22085400 |
| [2] |
(a) Legrand, F.; Jouvin, K.; Evano, G. Isr. J. Chem. 2010, 50, 588.
doi: 10.1002/ijch.201000037 |
|
(b) Negishi, E. I. Handbook of Organopalladium Chemistry for Organic Synthesis, Wiley, New York, 2002, 650.
|
|
|
(c) Wang, J. R.; Manabe, K. Synthesis 2009, 1405.
|
|
|
(d) Xu, B.; Ma, S. Chin. J. Org. Chem. 2001, 21, 252. (in Chinese)
|
|
|
( 许斌, 麻生明, 有机化学, 2001, 21, 252.)
|
|
| [3] |
(a) Desal, N. B.; Mckelvie, N.; Ramiraz, F. J. Am. Chem. Soc. 1962, 84, 1745.
doi: 10.1021/ja00868a057 |
|
(b) Corey, E. J.; Fuchs, P. L. Tetrahedron Lett. 1972, 36, 3769.
doi: 10.1016/0040-4039(95)90349-6 |
|
| [4] |
Kiruthika, S. E.; Nandakumar, A.; Perumal, P. T. Org. Lett. 2014, 16, 4424.
doi: 10.1021/ol5019085 |
| [5] |
Xu, W.; Zhang, W.; Zhang, F. Heterocycl. Commun. 2016, 22, 165.
|
| [6] |
Rao, M. L. N.; Dasgupta, P. RSC Adv. 2015, 5, 65462.
doi: 10.1039/C5RA13213D |
| [7] |
Huang, Z.; Shang, R.; Zhang, Z.-R.; Tan, X.-D.; Xiao, X.; Fu, Y. J. Org. Chem. 2013, 78, 4551.
doi: 10.1021/jo400616r |
| [8] |
Meng, T.; Zhang, H.-J.; Xi, Z. Tetrahedron Lett. 2012, 53, 4555.
doi: 10.1016/j.tetlet.2012.06.060 |
| [9] |
Aziz, J.; Baladi, T.; Piguel, S. J. Org. Chem. 2016, 81, 4122.
doi: 10.1021/acs.joc.6b00406 |
| [10] |
Ji, Y.; Zhong, N.; Kang, Z.; Yan, G.; Zhao, M. Synlett 2018, 29, 209.
doi: 10.1055/s-0036-1590907 |
| [11] |
Salehi, P.; Shiri, M. Adv. Synth. Catal. 2019, 361, 118.
doi: 10.1002/adsc.201800963 |
| [12] |
He, H.-F.; Ye, Y.; Jiang, Y.; Bao, W. J. Chem. Res. 2014, 38, 399.
doi: 10.3184/174751914X14019525018744 |
| [13] |
Shen, C.; Yang, Y.; Liu, Z.; Zhang, Y. Synth. Commun. 2014, 44, 1970.
doi: 10.1080/00397911.2014.882004 |
| [14] |
Kiruthika, S. E.; Perumal, P. T. Org. Lett. 2014, 16, 484.
doi: 10.1021/ol403365t |
| [15] |
Zeidan, N.; Bognar, S.; Lee, S.; Lautens, M. Org. Lett. 2017, 19, 5058.
doi: 10.1021/acs.orglett.7b02244 |
| [16] |
Li, B.; Guo, S.; Zhang, J.; Zhang, X.; Fan, X. J. Org. Chem. 2015, 80, 5444.
doi: 10.1021/acs.joc.5b00239 |
| [17] |
Gupta, S.; Koley, D.; Ravikumar, K.; Kundu, B. J. Org. Chem. 2013, 78, 8624.
doi: 10.1021/jo4013332 |
| [18] |
Song, J.; Chi, X.; Meng, L.; Zhao, P.; Sun, F.; Zhang, D.; Jiao, L.; Liu, Q.; Dong, Y.; Liu, H. Adv. Synth. Catal. 2019, 361, 3599.
doi: 10.1002/adsc.201900230 |
| [19] |
Fang, Y.-Q.; Lautens, M. Org. Lett. 2005, 7, 3549.
doi: 10.1021/ol051286l |
| [20] |
Zhang, M.; Weng, Z. Org. Lett. 2019, 21, 5838.
doi: 10.1021/acs.orglett.9b01922 |
| [21] |
Bilheri, F. N.; Pistoia, R. P.; Back, D. F.; Zeni, G. Adv. Synth. Catal. 2017, 359, 4208.
doi: 10.1002/adsc.201701095 |
| [22] |
He, H.-F.; Dong, S.; Chen, Y.; Yang, Y.; Le, Y.; Bao, W. Tetrahedron 2012, 68, 3112.
doi: 10.1016/j.tet.2012.01.087 |
| [23] |
Sayyad, M.; Wani, I. A.; Tiwari, D. P.; Ghorai, M. K. Eur. J. Org. Chem. 2017, 2369.
|
| [24] |
Zhang, C.; Ban, M.-T.; Zhang, L.-Y.; Zhu, K.; Luo, Z.-Y.; Guo, S.-N.; Cui, D.-M.; Zhang, Y. Org. Lett. 2017, 19, 3947.
doi: 10.1021/acs.orglett.7b01608 pmid: 28708406 |
| [25] |
Huang, R. Y.; Franke, P. T.; Nicolaus, N.; Lautens, M. Tetrahedron 2013, 69, 4395.
doi: 10.1016/j.tet.2013.01.001 |
| [26] |
Song, X.; Gao, C.; Zhang, X.; Fan, X. J. Org. Chem. 2018, 83, 15256.
doi: 10.1021/acs.joc.8b02456 pmid: 30465428 |
| [27] |
Shi, Y.; Li, M.-S.; Zhang, F.; Chen, B. RSC Adv. 2018, 8, 28668.
doi: 10.1039/C8RA03278E |
| [28] |
Liu, L.; Lv, Y.; Wu, Y.; Gao, X.; Zeng, Z.; Gao, Y.; Tang, G.; Zhao, Y. RSC Adv. 2014, 4, 2322.
doi: 10.1039/C3RA45212C |
| [29] |
Liu, X.; Chen, G.; Zhou, Y.; Liu, P. Tetrahedron Lett. 2018, 59, 3151.
doi: 10.1016/j.tetlet.2018.07.017 |
| [1] | 陈雯雯, 张琴, 张松月, 黄芳芳, 张馨尹, 贾建峰. 无光催化剂条件下可见光诱导炔基碘和亚磺酸钠偶联反应[J]. 有机化学, 2024, 44(2): 584-592. |
| [2] | 赵红琼, 于淼, 宋冬雪, 贾琦, 刘颖杰, 季宇彬, 许颖. 羧酸脱羧羟基化反应研究进展[J]. 有机化学, 2024, 44(1): 70-84. |
| [3] | 高晓阳, 翟锐锐, 陈训, 王烁今. 碳酸亚乙烯酯参与C—H键活化反应的研究进展[J]. 有机化学, 2023, 43(9): 3119-3134. |
| [4] | 陈祖佳, 宇世伟, 周永军, 李焕清, 邱琪雯, 李妙欣, 汪朝阳. BF3•OEt2作为催化剂与合成子在有机合成中的应用进展[J]. 有机化学, 2023, 43(9): 3107-3118. |
| [5] | 陈新强, 张敬. 伯醇的脱羟甲基反应的研究进展[J]. 有机化学, 2023, 43(8): 2711-2719. |
| [6] | 徐光利, 许静, 徐海东, 崔香, 舒兴中. 过渡金属催化烯烃和炔烃合成1,3-共轭二烯化合物研究进展[J]. 有机化学, 2023, 43(6): 1899-1933. |
| [7] | 户晓兢, 郭斐翔, 朱润青, 周柄棋, 张涛, 房立真. 对烷氧基酚的合成及其去芳构化后的合成应用[J]. 有机化学, 2023, 43(6): 2239-2244. |
| [8] | 庞明杨, 常宏宏, 冯璋, 张娟. 过渡金属催化吲哚的串联去芳构化反应研究进展[J]. 有机化学, 2023, 43(4): 1271-1291. |
| [9] | 贾海瑞, 邱早早. 过渡金属催化硼-氢键活化合成含硼-杂原子键邻碳硼烷衍生物的研究进展[J]. 有机化学, 2023, 43(3): 1045-1068. |
| [10] | 吴孔川, 卢铠洪, 林建斌, 张慧君. 莱啉酰亚胺类化合物的邻位C—H键功能化研究进展[J]. 有机化学, 2023, 43(3): 1000-1011. |
| [11] | 蒙玲, 汪君. 硫代黄烷酮类衍生物的合成研究进展[J]. 有机化学, 2023, 43(3): 873-891. |
| [12] | 段康慧, 唐俊龙, 伍婉卿. 稠杂环化合物的合成及其抗肿瘤活性研究进展[J]. 有机化学, 2023, 43(3): 826-854. |
| [13] | 刘宁, 爨晓丹, 李慧, 段希焱. 烯胺酮α-官能团化反应的研究进展[J]. 有机化学, 2023, 43(2): 602-621. |
| [14] | 马彪, 章淼淼, 李占宇, 彭进松, 陈春霞. 无过渡金属催化的Suzuki-Type交叉偶联反应研究进展[J]. 有机化学, 2023, 43(2): 455-470. |
| [15] | 刘婷婷, 胡宇才, 沈安. 亚胺配体协同氮杂环卡宾钯配合物催化碳碳偶联反应的作用机制[J]. 有机化学, 2023, 43(2): 622-628. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||