有机化学 ›› 2025, Vol. 45 ›› Issue (1): 168-188.DOI: 10.6023/cjoc202404040 上一篇 下一篇
综述与进展
张腾飞a, 常喆a,b, 陈春霞a,b,*( ), 彭进松a,b,*(
), 彭进松a,b,*( )
)
收稿日期:2004-04-04
修回日期:2024-07-17
发布日期:2024-07-25
基金资助:
Tengfei Zhanga, Zhe Changa,b, Chunxia Chena,b( ), Jinsong Penga,b(
), Jinsong Penga,b( )
)
Received:2004-04-04
Revised:2024-07-17
Published:2024-07-25
Contact:
*E-mail: Supported by:文章分享

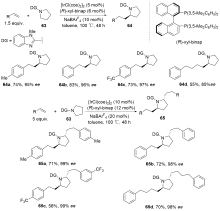
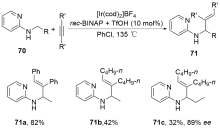
在有机合成化学中, C—H键的官能团化是一个十分重要的研究领域. 在众多处于不同化学环境的C—H键中, N-α位的Csp3—H键因氮原子的诱导效应使其相较于其他的Csp3—H键具有更高的反应活性, 并且在导向基团作用下可以更好地实现N-α位Csp3—H键的区域选择性官能团化反应, 因此氮原子α位Csp3—H键官能团化是一种非常实用的合成策略, 这为含有氮原子的有机化合物(如尼可刹米、奎宁等)的结构修饰及药物开发提供了更多可能. 综述了近二十年来过渡金属催化氮原子α位Csp3—H键官能团化的发展现状, 并展望了此方法在有机合成化学中的潜力.
张腾飞, 常喆, 陈春霞, 彭进松. 过渡金属催化氮原子α位Csp3—H键官能团化反应研究进展[J]. 有机化学, 2025, 45(1): 168-188.
Tengfei Zhang, Zhe Chang, Chunxia Chen, Jinsong Peng. Progress in Functionalization of N-α-Csp3—H Bond Catalyzed by Transition Metals[J]. Chinese Journal of Organic Chemistry, 2025, 45(1): 168-188.




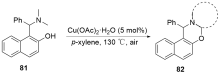





| [1] |
Gonnard, L.; Guérinot, A.; Cossy, J. Tetrahedron 2019, 75, 145.
|
| [2] |
O'Hagan, D. Nat. Prod. Rep. 2000, 17, 435.
|
| [3] |
Lorente, A.; Lamariano-Merketegi, J.; Albericio, F.; Álvarez, M. Chem. Rev. 2013, 113, 4567.
|
| [4] |
Vitaku, E.; Smith, D. T.; Njardarson, J. T. J. Med. Chem. 2014, 57, 10257.
|
| [5] |
Taylor, R. D.; MacCoss, M.; Lawson, A. D. G. J. Med. Chem. 2014, 57, 5845.
|
| [6] |
Edwards, P. M.; Schafer, L. L. Chem. Commun. 2018, 54, 12543.
|
| [7] |
Paul, A.; Seidel, D. J. Am. Chem. Soc. 2019, 141, 8778.
|
| [8] |
Antermite, D.; Bull, J. A. Synthesis 2019, 51, 3171.
|
| [9] |
Ye, Z.; Gettys, K. E.; Dai, M. Beilstein J. Org. Chem. 2016, 12, 702.
|
| [10] |
Inoue, M.; Tsurugi, H.; Mashima, K. Coord. Chem. Rev. 2022, 473, 214810.
|
| [11] |
Campos, K. R. Chem. Soc. Rev. 2007, 36, 1069.
|
| [12] |
Chen, W.; Ma, L.; Paul, A.; Seidel, D. Nat. Chem. 2018, 10, 165.
|
| [13] |
Cai, X. H.; Yang, M. Z.; Xie, B. Lett. Org. Chem. 2019, 16, 779.
|
| [14] |
Antermite, D.; Degennaro, L.; Luisi, R. Org. Biomol. 2017, 15, 34.
|
| [15] |
Ping, L.; Chung, D. S.; Bouffard, J.; Lee, S. G. Chem. Soc. Rev. 2017, 16, 4299.
|
| [16] |
Hernández, J. G. Chem. Eur. J. 2017, 23, 17157.
|
| [17] |
Zhang, Y. H.; Shi, G. F.; Yu, J. Q. Comprehensive Organic Synthesis II 2014, 3, 1101.
|
| [18] |
Xie, J.; Zhu, C. Springer Briefs in Molecular Science 2016, 25.
|
| [19] |
Beak, P.; Lee, W. K. Tetrahedron Lett. 1989, 3, 1197.
|
| [20] |
Jun, C. H.; Hwang, D. C.; Na, S. J. Chem. Commun. 1998, 13, 1405.
|
| [21] |
Chatani, N.; Asaumi, T. Yorimitsu, S.; Ikeda, T.; Kakiuchi, F.; Murai, S. J. Am. Chem. Soc. 2001, 123, 10935.
|
| [22] |
Yi, C. S.; Yun, S. Y.; Guzei, I. A. Organometallics 2004, 23, 5392.
|
| [23] |
Schmitt, D. C.; Lee, J.; Dechert-Schmitt.; A, M. R.; Yamaguchi, E.; Krische, M. J. Chem. Commun. 2013, 49, 6096.
|
| [24] |
Pastine, S. J.; Gribkov, D. V.; Sames, D. J. Am. Chem. Soc. 2006, 128, 14220.
|
| [25] |
Prokopcová, H.; Bergman, S. D.; Aelvoet, K.; Smout, V.; Herrebout, W.; Veken, V. B.; Meerpoel, L.; Maes, B. U. W. Chem.-Eur. J 2010, 16, 13063.
|
| [26] |
Peschiulli, A.; Smout, V. Storr, T. E.; Mitchell, E. A.; Eliáš, Z.; Herrebout, W.; Berthelot, D.; Meerpoel, L.; Maes, B. U. W. Chem.- Eur. J. 2013, 19, 10378.
|
| [27] |
Cao, L.; Zhao, H.; Tan, Z.; Guan, R.; Jiang, H.; Zhang, M. Org. Lett. 2020, 22, 4781.
|
| [28] |
Ishii, Y.; Chatani, N.; Kakiuchi, F.; Murai, S. Organometallics 1997, 16, 3615.
|
| [29] |
Chatani, N.; Asaumi, T.; Ikeda, T.; Yorimitsu, S.; Ishii, Y.; Kakiuchi, F.; Murai, S. J. Am. Chem. Soc. 2000, 122, 12882.
|
| [30] |
Davies, H. M. L.; Hansen, T.; Hopper, D. W.; Panaro, S. A. J. Am. Chem. Soc. 1999, 121, 6509.
|
| [31] |
Li, Q.; Yu, Z. X. J. Am. Chem. Soc. 2010, 132, 4542.
|
| [32] |
Li, Q.; Yu, Z. X. Organometallics 2012, 31, 5185.
|
| [33] |
Anschuber, M.; Pollice, R.; Schnürch, M. Monatsh. Chem. 2019, 150, 127.
|
| [34] |
Greβies, S.; Klauck, F. J.; Kim, J. H.; Daniliuc, C. G.; Glorius, F. Angew. Chem., Int. Ed. 2018, 57, 9950.
|
| [35] |
Singh, P.; Min, J.; Min, S.; Moon, K.; Kim, H. S.; Kim, I. S. Org. Lett. 2023, 26, 57.
|
| [36] |
Spangler, J. E.; Kobayashi, Y.; Verma, P.; Wang, D. H., Yu, J. Q. J. Am. Chem. Soc. 2015, 137, 11876.
|
| [37] |
Jain, P.; Verma, P.; Xia, G.; Yu, J. Q. Nat. Chem. 2017, 9, 140.
|
| [38] |
Jiang, H. J.; Zhong, X. M.; Yu, J.; Zhang, Y.; Zhang, X.; Wu, Y. D.; Gong, L. Z. Angew. Chem., nt. Ed. 2019, 58, 1803.
|
| [39] |
Cheng, S. J.; Wang, G.; Liu, K.; Ye, Z. S. Org. Lett. 2022, 24, 864.
|
| [40] |
Liu, Y. C.; Shi, H. ChemCatChem 2023, 15, 392.
|
| [41] |
Wang, D. H.; Hao, X. S.; Wu, D. F.; Yu, J. Q. Org. Lett. 2006, 8, 3387.
|
| [42] |
Pan, S.; Endo, K.; Shibata, T. Org. Lett. 2011, 13, 4692.
|
| [43] |
Lahm, G.; Opatz, T. Org. Lett. 2014, 16, 4201.
|
| [44] |
Tran, A. T.; Yu, J. Q. Angew. Chem. 2017, 129, 10666.
|
| [45] |
Yamauchi, D.; Nishimura, T.; Yorimitsu, H. Angew. Chem., Int. Ed. 2017, 56, 7200.
|
| [46] |
Verma, P.; Richter, J. M.; Chekshin, N.; Qiao, J. X.; Yu, J. Q. J. Am. Chem. Soc. 2020, 142, 5117.
|
| [47] |
Yamauchi, D.; Yamakawa, K.; Nishimura, T. Org. Lett. 2022, 24, 6828.
|
| [48] |
DeBoef, B.; Pastine, S. J.; Sames, D. J. Am. Chem. Soc. 2004, 126, 6556.
|
| [49] |
Tsuchikama, K.; Kasagawa, M.; Endo, K.; Shibata, T. Org. Lett. 2009, 11, 1821.
|
| [50] |
Pan, S.; Matsuo, Y.; Endo, K.; Shibata, T. Tetrahedron 2012, 68, 9009.
|
| [51] |
Baslé, O.; Li, C. J. Green Chem. 2007, 9, 1047.
|
| [52] |
Nishino, M.; Hirano, K.; Satoh, T.; Miura, M. J. Org. Chem. 2011, 76, 6447.
|
| [53] |
Huang, L.; Niu, T.; Wu, J.; Zhang, Y. J. Org. Chem. 2011, 76, 1759.
|
| [54] |
Li, Z.; Li, C. J. J. Am. Chem. Soc. 2004, 126, 11810.
|
| [55] |
Deb, M. L.; Dey, S. S.; Bento, I.; Barros, M. T.; Maycock, C. D. Angew. Chem. 2013, 125, 9973.
|
| [56] |
Chang, Z.; Huang, J.; Wang, S.; Chen, G.; Zhao, H.; Wang, R.; Zhao, D. Nat. Commun. 2021, 12, 4342.
|
| [57] |
Li, Z.; Bohle, D. S.; Li, C. J. Proc. Natl. Acad. Sci. 2006, 103, 8928.
|
| [58] |
Yatabe, T.; Yamaguchi, K. Nat. Commun. 2022, 13, 6505.
|
| [59] |
Ma, L.; Shi, X.; Li, X.; Shi, D. Org. Chem. Front. 2018, 5, 3515.
|
| [60] |
Zhang, Z.; Hamel, J. D.; Schafer, L. L. Chem.-Eur. J. 2013, 19, 8751.
|
| [61] |
Yan, X. B.; Li, L.; Wu, W. Q.; Xu, L.; Li, K.; Liu, Y. C.; Shi, H. Nat. Commun. 2021, 12, 5881.
|
| [62] |
Zhang, T.; Jiang, S.; Qian, M. Y.; Zhou, Q. L.; Xiao, L. J. J. Am. Chem. Soc. 2024, 5, 30.
|
| [63] |
Yao, W. W.; Li, R.; Chen, H.; Chen, M. K.; Luan, Y. X.; Wang, Y.; Yu, Z. X.; Ye, M. Nat. Commun. 2021, 12, 3800.
|
| [64] |
Li, L.; Liu, Y. C.; Shi, H. J. Am. Chem. Soc. 2021, 143, 4154.
|
| [65] |
Feng, K.; Quevedo, R. E.; Kohrt, J. T.; Oderinde, M. S.; Reilly, U.; White, M. C. Nature 2020, 580, 621.
|
| [1] | 沈佳斌, 沈超, 章鹏飞. 可见光介导的羰基α位C—H官能团化反应合成萘咪酮类衍生物[J]. 有机化学, 2025, 45(2): 677-685. |
| [2] | 袁晨晖, 焦雷. 手性配体在钯催化配位辅助对映选择性C(sp3)—H键官能团化反应中的应用[J]. 有机化学, 2025, 45(2): 602-619. |
| [3] | 田勋, 邓国刚, 羊晓东. 钴催化C(sp2)—H活化构建苯并含氮杂环骨架的研究进展[J]. 有机化学, 2025, 45(2): 655-667. |
| [4] | 王曼曼, 习文慧, 吴昊, 白大昌. 过渡金属催化碳氢键活化合成烷基氟烷基化合物的研究进展[J]. 有机化学, 2025, 45(2): 516-530. |
| [5] | 王淼, 黄雅豪, 胡鹏. 氢原子转移介导的烷烃C(sp3)—H选择性官能团化研究进展[J]. 有机化学, 2025, 45(2): 477-497. |
| [6] | 王君伟, 薛皓, 曲英瑜, 姜若楠, 闫法超, 刘会. 过渡金属催化联烯胺类化合物的碳氢化反应研究进展[J]. 有机化学, 2025, 45(1): 151-167. |
| [7] | 宣良明, 赵伟, 范润东, 严琼姣, 汪伟, 陈芬儿. 基于甘氨酸衍生物α-C(sp3)—H官能团化的催化体系研究进展[J]. 有机化学, 2024, 44(9): 2700-2721. |
| [8] | 陆玲依, 邱晓东. 自由基形式烯烃双烷基化反应研究进展[J]. 有机化学, 2024, 44(6): 1701-1718. |
| [9] | 于蕾, 盛康, 李亭, 唐从辉. 多相铁催化环状醚C(sp3)—H键活化的芳基烯烃氧烷基化[J]. 有机化学, 2024, 44(6): 1978-1986. |
| [10] | 吉崇磊, 高得伟. 不对称催化合成手性1,2-双硼酸酯研究进展[J]. 有机化学, 2024, 44(5): 1385-1402. |
| [11] | 李晨龙, 余志祥. 一氧化碳参与的过渡金属催化的插羰环加成反应研究进展[J]. 有机化学, 2024, 44(4): 1045-1068. |
| [12] | 郭凯杰, 符昕姝, 李靖, 陈艳, 胡美丽, 堵锡华, 谢屿阳, 何燕. 过渡金属催化C—S键活化与转化研究进展[J]. 有机化学, 2024, 44(4): 1124-1150. |
| [13] | 鞠国栋, 周冠宇, 赵应声. 三异丙基硅烷(TIPS)保护苯酚的无过渡金属催化区域选择性硫氰化反应[J]. 有机化学, 2024, 44(4): 1327-1336. |
| [14] | 彭天凤, 赵玉祥, 浦绍健, 罗娟, 刘腾, 缪应纯, 沈先福. 过渡金属催化的关键反应在异戊烯基吲哚生物碱全合成中的研究进展[J]. 有机化学, 2024, 44(4): 1160-1180. |
| [15] | 万云辉, 杨福美, 陈明瀚, 孙德立, 叶丹锋. 无过渡金属催化的N-苄基-N-叔丁氧羰基酰胺与不饱和醇的酯化反应[J]. 有机化学, 2024, 44(4): 1293-1300. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||