有机化学 ›› 2026, Vol. 46 ›› Issue (3): 1000-1007.DOI: 10.6023/cjoc202509013 上一篇 下一篇
研究论文
梁新宇a,†, 米春春a,†, 郭福军a, 谢文斌a,*( ), 史钦钦a,*(
), 史钦钦a,*( ), 黄辉a,b,*(
), 黄辉a,b,*( )
)
收稿日期:2025-09-09
修回日期:2025-11-06
发布日期:2025-12-09
作者简介:†共同第一作者
基金资助:
Xinyu Lianga, Chunchun Mia, Fujun Guoa, Wenbin Xiea,*( ), Qinqin Shia,*(
), Qinqin Shia,*( ), Hui Huanga,b,*(
), Hui Huanga,b,*( )
)
Received:2025-09-09
Revised:2025-11-06
Published:2025-12-09
Contact:
*E-mail: About author:†These authors contributed equally to this work
Supported by:文章分享
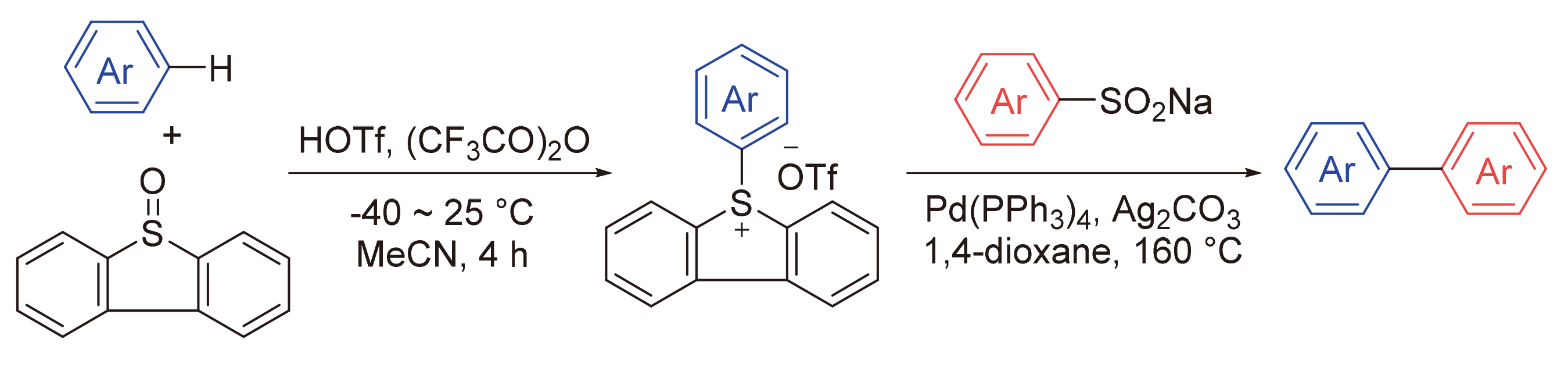
过渡金属催化的交叉偶联反应是有机合成中构建碳-碳键的核心策略. 本研究开发了钯催化下芳基亚磺酸钠与芳基硫鎓盐的交叉偶联反应, 该反应通过间断Pummerer活化C—H键实现. 通过筛选多种芳基亚磺酸钠和芳基硫鎓盐, 验证了该方法的稳定性. 需要特别说明的是, 两个药物后期功能化的案例充分展示了其在药物开发中的应用潜力.
梁新宇, 米春春, 郭福军, 谢文斌, 史钦钦, 黄辉. 芳基亚磺酸钠与芳基硫鎓盐的脱硫交叉偶联反应[J]. 有机化学, 2026, 46(3): 1000-1007.
Xinyu Liang, Chunchun Mi, Fujun Guo, Wenbin Xie, Qinqin Shi, Hui Huang. Desulfinative Cross-Coupling of Aryl Sodium Sulfinate with Aryl Sulfonium Salts[J]. Chinese Journal of Organic Chemistry, 2026, 46(3): 1000-1007.

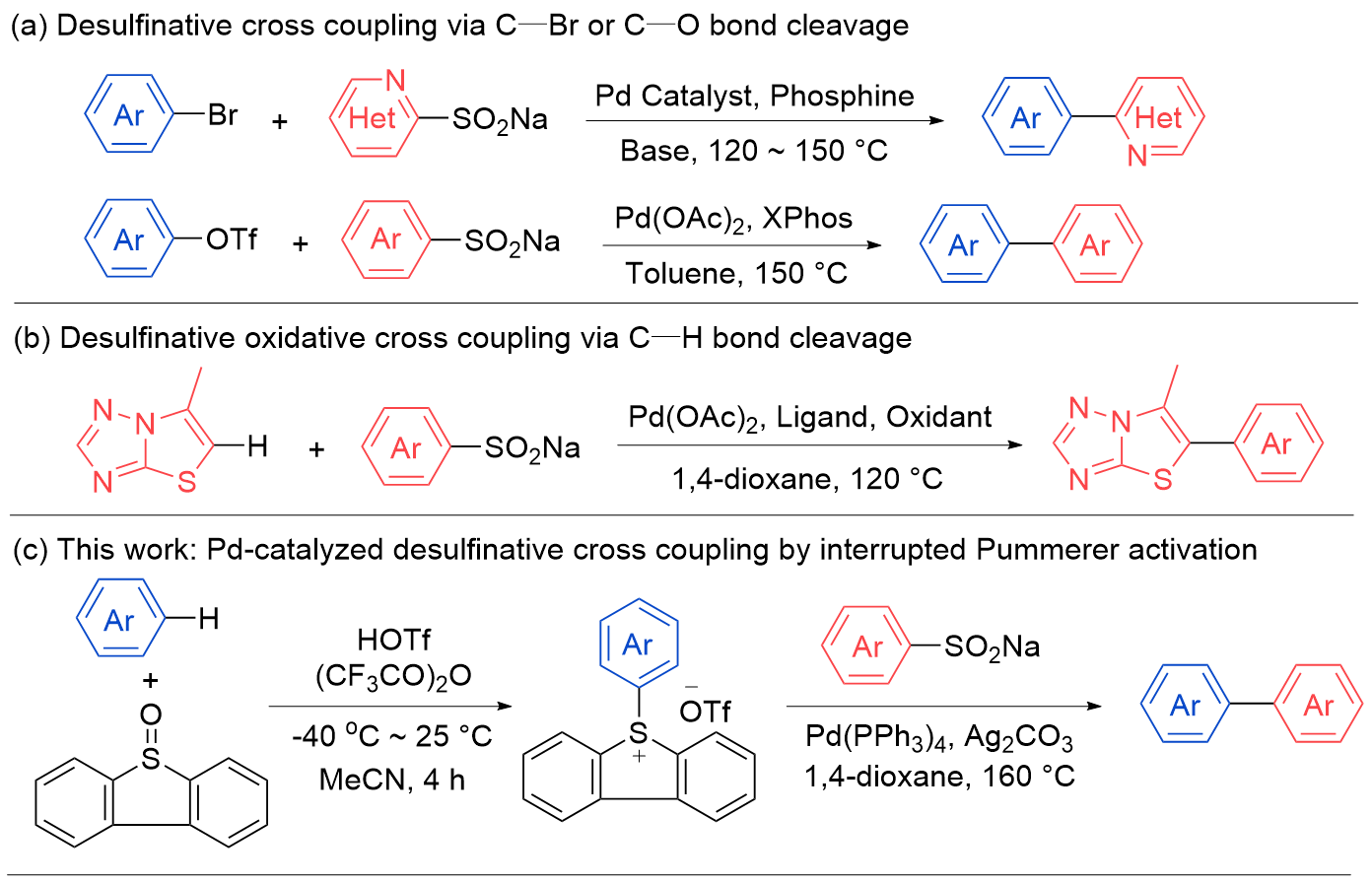
| Entry | [Pd] (10 mol%) | Ligand (20 mol%) | Additive (2.0 equiv.) | Solvent | Temperature/℃ | Yieldb/% |
|---|---|---|---|---|---|---|
| 1 | Pd(OAc)2 | PCy3 | K2CO3 | 1,4-dioxane | 160 | 67 |
| 2 | Pd(OAc)2 | P(t-Bu)3H+BF4- | K2CO3 | 1,4-dioxane | 160 | 42 |
| 3 | Pd(PPh3)4 | — | K2CO3 | 1,4-dioxane | 160 | 72 |
| 4 | Pd(OAc)2 | dtbpf | K2CO3 | 1,4-dioxane | 160 | 63 |
| 5 | Pd(OAc)2 | dppf | K2CO3 | 1,4-dioxane | 160 | 61 |
| 6 | Pd(PPh3)4 | — | KOt-Bu | 1,4-dioxane | 160 | 16 |
| 7 | Pd(PPh3)4 | — | KF | 1,4-dioxane | 160 | 71 |
| 8 | Pd(PPh3)4 | — | Cs2CO3 | 1,4-dioxane | 160 | 16 |
| 9 | Pd(PPh3)4 | — | AgOAc | 1,4-dioxane | 160 | 68 |
| 10 | Pd(PPh3)4 | — | Ag2CO3 | 1,4-dioxane | 160 | 78 (72)c |
| 11 | Pd(PPh3)4 | — | Ag2CO3 | 1,4-dioxane | 110 | 31 |
| 12 | Pd(PPh3)4 | — | Ag2CO3 | DMSO | 160 | 72 |
| Entry | [Pd] (10 mol%) | Ligand (20 mol%) | Additive (2.0 equiv.) | Solvent | Temperature/℃ | Yieldb/% |
|---|---|---|---|---|---|---|
| 1 | Pd(OAc)2 | PCy3 | K2CO3 | 1,4-dioxane | 160 | 67 |
| 2 | Pd(OAc)2 | P(t-Bu)3H+BF4- | K2CO3 | 1,4-dioxane | 160 | 42 |
| 3 | Pd(PPh3)4 | — | K2CO3 | 1,4-dioxane | 160 | 72 |
| 4 | Pd(OAc)2 | dtbpf | K2CO3 | 1,4-dioxane | 160 | 63 |
| 5 | Pd(OAc)2 | dppf | K2CO3 | 1,4-dioxane | 160 | 61 |
| 6 | Pd(PPh3)4 | — | KOt-Bu | 1,4-dioxane | 160 | 16 |
| 7 | Pd(PPh3)4 | — | KF | 1,4-dioxane | 160 | 71 |
| 8 | Pd(PPh3)4 | — | Cs2CO3 | 1,4-dioxane | 160 | 16 |
| 9 | Pd(PPh3)4 | — | AgOAc | 1,4-dioxane | 160 | 68 |
| 10 | Pd(PPh3)4 | — | Ag2CO3 | 1,4-dioxane | 160 | 78 (72)c |
| 11 | Pd(PPh3)4 | — | Ag2CO3 | 1,4-dioxane | 110 | 31 |
| 12 | Pd(PPh3)4 | — | Ag2CO3 | DMSO | 160 | 72 |
| [1] |
(a)
doi: 10.1021/jacs.5c07642 |
|
(b)
doi: 10.1038/s41467-025-62092-3 |
|
|
(c)
doi: 10.1002/anie.v60.39 |
|
| [2] |
(a)
doi: 10.1021/acscatal.5b00448 pmid: 21618370 |
|
(b)
doi: 10.1002/anie.201107017 pmid: 21618370 |
|
|
(c)
doi: 10.1021/cs300082f pmid: 21618370 |
|
|
(d)
doi: 10.1002/anie.201101379 pmid: 21618370 |
|
| [3] |
doi: 10.1021/acs.orglett.7b02424 |
| [4] |
doi: 10.1021/acs.jmedchem.0c01786 |
| [5] |
(a)
doi: 10.1021/ja303401s pmid: 22679903 |
|
(b)
doi: 10.1021/ja400881n pmid: 22679903 |
|
| [6] |
(a)
doi: 10.1021/jacs.6b03283 |
|
(b)
doi: 10.1021/jacs.7b07444 |
|
| [7] |
doi: 10.1007/s00244-004-0105-1 |
| [8] |
doi: 10.1021/acs.chemrev.5b00393 pmid: 26555044 |
| [9] |
(a)
doi: 10.1039/C1CS15127D |
|
(b)
doi: 10.1002/chem.v24.31 |
|
| [10] |
doi: 10.1039/c1cs15093f |
| [11] |
doi: 10.1002/ejoc.v2016.3 |
| [12] |
(a)
doi: 10.1021/jacs.8b09595 pmid: 30412397 |
|
(b)
doi: 10.1002/anie.v60.41 pmid: 30412397 |
|
|
(c)
doi: 10.1021/jo302005s pmid: 30412397 |
|
| [13] |
doi: 10.1055/s-00000083 |
| [14] |
doi: 10.1021/cr500431s |
| [15] |
(a)
doi: 10.1038/s41586-019-0982-0 |
|
(b)
doi: 10.1021/acs.orglett.1c01322 |
|
|
(c)
|
|
|
(d)
doi: 10.1021/acscatal.3c03096 |
|
|
(e)
doi: 10.1021/acscatal.5c00082 |
|
|
(f)
|
|
|
(g)
doi: 10.1039/D2SC01241C |
|
| [16] |
(a)
doi: 10.1039/c7sc00675f pmid: 28936330 |
|
(b)
doi: 10.1021/jacs.9b13260 pmid: 28936330 |
|
| [17] |
(a)
doi: 10.1021/ja00155a007 |
|
(b)
doi: 10.1038/s41467-018-03718-7 |
|
| [18] |
(a)
doi: 10.1021/acs.chemrev.2c00478 pmid: 37134187 |
|
(b)
doi: 10.1021/acs.chemrev.2c00881 pmid: 37134187 |
|
| [19] |
doi: 10.1021/jacs.1c09884 pmid: 34871503 |
| [20] |
doi: 10.1021/ja902046m |
| [21] |
doi: 10.1002/chem.v17.22 |
| [22] |
doi: 10.1021/acs.orglett.9b04474 |
| [23] |
doi: 10.1021/acs.orglett.9b00942 pmid: 30908055 |
| [24] |
|
| [25] |
doi: 10.1039/C7GC02804K |
| [26] |
doi: 10.1002/anie.v54.40 |
| [27] |
|
| [28] |
doi: 10.1021/jo301384r |
| [29] |
doi: 10.1021/jo101709n |
| [30] |
doi: 10.1002/anie.201605584 pmid: 27456275 |
| [31] |
doi: 10.1002/chem.v25.9 |
| [32] |
doi: 10.1007/s11426-019-9652-x |
| [33] |
doi: 10.1039/D1RA04947J |
| [34] |
doi: 10.1021/acscatal.1c04533 |
| [1] | 韦翠, 刘金秋, 邓灿, 邹宁, 周文俊. 螺芴基化合物的合成研究进展[J]. 有机化学, 2026, 46(3): 817-839. |
| [2] | 张晋瑜, 卢志刚, 刘喆, 王聪. 过渡金属催化亚甲基环丙烷的硅氢化和硼化反应[J]. 有机化学, 2026, 46(3): 806-816. |
| [3] | 刘颖杰, 闵来生, 杨锐蓉, 宋冬雪, 彭瑞, 梁德强. CuI催化C—C键偶联反应构建2-羰基-1,4-二酮[J]. 有机化学, 2026, 46(2): 603-611. |
| [4] | 任揽星, 徐阿娜, 肖锡林, 游恒志, 宋利娟. 溶剂效应对Ir催化的不对称氢化反应对映选择性影响的理论研究[J]. 有机化学, 2025, 45(8): 2904-2912. |
| [5] | 陈明, 张敬. 芳基羧酸无痕导向官能化反应的研究进展[J]. 有机化学, 2025, 45(8): 2660-2676. |
| [6] | 杜一鸣, 贾均松, 李玉龙, 舒伟. 手性α-芳基酮的催化合成研究进展[J]. 有机化学, 2025, 45(6): 1838-1870. |
| [7] | 苏雷, 杨熙, 闫捷, 蒋元力, 陈丽娟, 郑庆舒, 刘家旺. 不对称羰基化偶联反应研究进展[J]. 有机化学, 2025, 45(6): 2007-2047. |
| [8] | 王霜, 毛羊杰, 娄绍杰, 许丹倩. 基于氧化型导向基团的不对称C—H键官能团化反应研究进展[J]. 有机化学, 2025, 45(6): 1961-1994. |
| [9] | 田勋, 邓国刚, 羊晓东. 钴催化C(sp2)—H活化构建苯并含氮杂环骨架的研究进展[J]. 有机化学, 2025, 45(2): 655-667. |
| [10] | 王曼曼, 习文慧, 吴昊, 白大昌. 过渡金属催化碳氢键活化合成烷基氟烷基化合物的研究进展[J]. 有机化学, 2025, 45(2): 516-530. |
| [11] | 王轩, 柳茂陈, 钟瑶, 宋仁杰. 共价有机框架的设计及其在催化C—H活化领域的应用进展[J]. 有机化学, 2025, 45(2): 448-465. |
| [12] | 张腾飞, 常喆, 陈春霞, 彭进松. 过渡金属催化氮原子α位Csp3—H键官能团化反应研究进展[J]. 有机化学, 2025, 45(1): 168-188. |
| [13] | 陆玲依, 邱晓东. 自由基形式烯烃双烷基化反应研究进展[J]. 有机化学, 2024, 44(6): 1701-1718. |
| [14] | 鞠国栋, 周冠宇, 赵应声. 三异丙基硅烷(TIPS)保护苯酚的无过渡金属催化区域选择性硫氰化反应[J]. 有机化学, 2024, 44(4): 1327-1336. |
| [15] | 彭天凤, 赵玉祥, 浦绍健, 罗娟, 刘腾, 缪应纯, 沈先福. 过渡金属催化的关键反应在异戊烯基吲哚生物碱全合成中的研究进展[J]. 有机化学, 2024, 44(4): 1160-1180. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||