有机化学 ›› 2023, Vol. 43 ›› Issue (3): 914-923.DOI: 10.6023/cjoc202211041 上一篇 下一篇
所属专题: 中国女科学家专辑
综述与进展
收稿日期:2022-11-30
修回日期:2023-02-01
发布日期:2023-02-14
通讯作者:
王丽佳
基金资助:
Xing Yanga, Xu Liua, Lijia Wanga,b( )
)
Received:2022-11-30
Revised:2023-02-01
Published:2023-02-14
Contact:
Lijia Wang
Supported by:文章分享
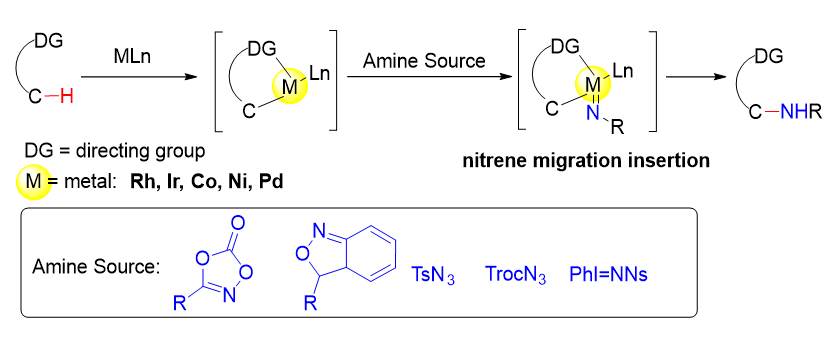
过渡金属催化C(sp3)—H键活化形成碳-氮键的反应一直是具有挑战性且热门的研究领域. 过渡金属催化的C(sp3)—H胺化策略为形成C—N键提供了更为直接高效的方式. 随着碳-氢键活化领域的蓬勃发展, 人们发展出了丰富多样的导向基和过渡金属催化体系, 为通过内轨机制实现C(sp3)—H胺化提供了有效工具. 近年来, 导向基辅助的C(sp3)—H键胺化反应取得了重要进展, 许多基于不同过渡金属的催化体系和廉价高效的胺化试剂得以开发. 综述了近十年来在导向基团辅助下, 过渡金属催化C(sp3)—H氮宾插入反应的研究进展.
杨幸, 刘旭, 王丽佳. 导向基辅助的过渡金属催化C(sp3)—H键氮宾插入反应研究进展[J]. 有机化学, 2023, 43(3): 914-923.
Xing Yang, Xu Liu, Lijia Wang. Recent Progress in Transition Metal Catalyzed C(sp3)—H Nitrene Insertion Reactions Assisted by Directing Groups[J]. Chinese Journal of Organic Chemistry, 2023, 43(3): 914-923.
| [1] |
Ricci, A. Amino Group Chemistry: From Synthesis to the Life Sciences, Wiley-VCH, Weinheim, 2008.
|
| [2] |
(a) Zhao, J.; Zhang, Q. Acta Chim. Sinica 2015, 73, 1235. (in Chinese)
doi: 10.6023/A15010063 |
|
(赵金钵, 张前, 化学学报, 2015, 73, 1235.)
doi: 10.6023/A15010063 |
|
|
(b) Li, J.; Zhang, Y. Nat. Rev. Chem. 2022, 6, 303.
doi: 10.1038/s41570-022-00379-5 |
|
|
(c) Ma, J.-L.; Zhou, X.-M.; Guo, P.-H.; Cheng, H.-C.; Ji, H.-B. Chin. J. Chem. 2022, 40, 1204.
doi: 10.1002/cjoc.v40.10 |
|
|
(d) Saranya, P. V.; Neetha, M.; Philip, R. M. Tetrahedron 2022, 104, 132582.
doi: 10.1016/j.tet.2021.132582 |
|
|
(e) Hwang, H.; Kim, J.; Jeong, J.; Chang, S. J. Am. Chem. Soc. 2014, 136, 10770.
doi: 10.1021/ja5053768 |
|
| [3] |
(a) Davies, H. M. L.; Manning, J. R. Nature 2008, 451, 417.
doi: 10.1038/nature06485 pmid: 32995499 |
|
(b) Davies, H. M. L.; Liao, K.-B. Nat. Rev. Chem. 2019, 3, 347.
doi: 10.1038/s41570-019-0099-x pmid: 32995499 |
|
|
(c) Du, B.; Chan, C.-M.; Au, C.-M.; Yu, W.-Y. Acc. Chem. Res. 2022, 55, 2123.
doi: 10.1021/acs.accounts.2c00283 pmid: 32995499 |
|
|
(d) Liang, H.; Wang, J. Chem.-Eur. J. 2022, 28, e202202461.
pmid: 32995499 |
|
| [4] |
For review: (a) Godula, K.; Sames, D., Science 2006, 312, 67.
pmid: 21500412 |
|
(b) Dick, A. R.; Sanford, M. S. Tetrahedron 2006, 62, 2439.
doi: 10.1016/j.tet.2005.11.027 pmid: 21500412 |
|
|
(c) Zalatan, D. N.; Du Bois, J. Top. Curr. Chem. 2010, 292, 347.
pmid: 21500412 |
|
|
(d) Driver, T. G. Org. Biomol. Chem. 2010, 8, 3831.
doi: 10.1039/c005219c pmid: 21500412 |
|
|
For leading references:
pmid: 21500412 |
|
|
(e) Zhang, S.-Y.; He, G.; Nack, W. A.; Zhao, Y.; Li, Q.; Chen, G. J. Am. Chem. Soc. 2013, 135, 2124.
doi: 10.1021/ja312277g pmid: 21500412 |
|
|
(f) He, J.; Wasa, M.; Chan, K. S. L.; Yu, J.-Q. J. Am. Chem. Soc. 2013, 135, 3387.
doi: 10.1021/ja400648w pmid: 21500412 |
|
|
(g) Zhang, S.-Y.; Li, Q.; He, G.; Nack, W. A.; Chen, G. J. Am. Chem. Soc. 2013, 135, 12135.
doi: 10.1021/ja406484v pmid: 21500412 |
|
|
(h) Shan, G.; Yang, X.; Zong, Y.; Rao, Y. Angew. Chem., Int. Ed. 2013, 52, 13606.
doi: 10.1002/anie.201307090 pmid: 21500412 |
|
|
(i) Chen, K.; Hu, F.; Zhang, S.-Q.; Shi, B.-F. Chem. Sci. 2013, 4, 3906.
doi: 10.1039/c3sc51747k pmid: 21500412 |
|
|
(j) Rodríguez, N.; Romero-Revilla, J. A.; Fernández-Ibáñez, M. Á.; Carretero, J. C. Chem. Sci. 2013, 4, 175.
doi: 10.1039/C2SC21162A pmid: 21500412 |
|
|
(k) Aihara, Y.; Chatani, N. J. Am. Chem. Soc. 2014, 136, 898.
doi: 10.1021/ja411715v pmid: 21500412 |
|
|
(l) Wu, X.; Zhao, Y.; Ge, H. J. Am. Chem. Soc. 2014, 136, 1789
doi: 10.1021/ja413131m pmid: 21500412 |
|
| [5] |
Wang, H.; Tang, G.; Li, X. Angew. Chem., Int. Ed. 2015, 54, 13049.
doi: 10.1002/anie.201506323 pmid: 26480337 |
| [6] |
Dong, Y.; Chen, J.; Xu, H. Chem. Commun. 2018, 54, 11096.
doi: 10.1039/C8CC05637D |
| [7] |
Antien, K.; Geraci, A.; Parmentier, M.; Baudoin, O. Angew. Chem., Int. Ed. 2021, 60, 22948.
doi: 10.1002/anie.v60.42 |
| [8] |
Barsu, N.; Rahman, M. A.; Sen, M.; Sundararaju, B. Chem.-Eur. J. 2016, 22, 9135.
doi: 10.1002/chem.201601597 |
| [9] |
Fukagawa, S.; Kojima, M.; Yoshino, T.; Matsunaga, S. Angew. Chem., Int. Ed. 2019, 58, 18154.
doi: 10.1002/anie.201911268 pmid: 31593365 |
| [10] |
Kato, Y.; Lin, L.; Kojima, M.; Yoshino, T.; Matsunaga, S. ACS Catal. 2021, 11, 4271.
doi: 10.1021/acscatal.1c00765 |
| [11] |
Tan, P. W.; Mak, A. M.; Sullivan, M. B.; Dixon, D. J.; Seayad, J. Angew. Chem., Int. Ed. 2017, 56, 16550.
doi: 10.1002/anie.201709273 |
| [12] |
Fukagawa, S.; Kato, Y.; Tanaka, R.; Kojima, M.; Yoshino, T.; Matsunaga, S. Angew. Chem., Int. Ed. 2019, 58, 1153.
doi: 10.1002/anie.201812215 pmid: 30478868 |
| [13] |
Sekine, D.; Ikeda, K.; Fukagawa, S.; Kojima, M.; Yoshino, T.; Matsunaga, S. Organometallics 2019, 38, 3921.
doi: 10.1021/acs.organomet.9b00407 |
| [14] |
Shi, H.; Dixon, D. J. Chem. Sci. 2019, 10, 3733.
doi: 10.1039/C8SC05225E |
| [15] |
Mahato, S. K.; Ohara, N.; Khake, S. M.; Chatani, N. I. ACS Catal. 2021, 11, 7126.
doi: 10.1021/acscatal.1c01901 |
| [16] |
Du, B.; Ouyang, Y.; Chen, Q.; Yu, W.-Y. J. Am. Chem. Soc. 2021, 143, 14962
doi: 10.1021/jacs.1c05834 |
| [17] |
Kang, T.; Kim, Y.; Lee, D.; Wang, Z.; Chang, S. J. Am. Chem. Soc. 2014, 136, 4141.
doi: 10.1021/ja501014b |
| [18] |
Zhang, T.; Hu, X.; Dong, X.; Li, G.; Lu, H. Org. Lett. 2018, 20, 6260.
doi: 10.1021/acs.orglett.8b02738 pmid: 30232895 |
| [19] |
Han, J.-L.; Qin, Y.; Zhao, D. ACS Catal. 2019, 9, 6020.
doi: 10.1021/acscatal.9b00771 |
| [20] |
Kim, Y. B.; Won, J.; Lee, J.; Kim, J.; Zhou, B.; Park, J.-W.; Baik, M.-H.; Chang, S. ACS Catal. 2021, 11, 3067.
doi: 10.1021/acscatal.1c00070 |
| [21] |
Xiao, X.; Hou, C.; Zhang, Z.; Ke, Z.; Lan, J.; Jiang, H.; Zeng, W. Angew. Chem., Int. Ed. 2016, 55, 11897.
doi: 10.1002/anie.v55.39 |
| [22] |
Huang, X.; Wang, Y.; Lan, J.; You, J. Angew. Chem., nt. Ed. 2015, 54, 9404.
|
| [23] |
Liu, B.; Xie, P.; Zhao, J.; Wang, J.; Wang, M.; Jiang, Y.; Chang, J.; Li, X. Angew. Chem., Int. Ed. 2021, 60, 8396.
doi: 10.1002/anie.v60.15 |
| [24] |
Wang, Y.; Liu, H.; Li, B.; Wang, B. Adv. Synth. Catal. 2019, 361, 1564.
doi: 10.1002/adsc.v361.7 |
| [25] |
Thu, H.-Y.; Yu, W.-Y.; Che, C.-M. J. Am. Chem. Soc. 2006, 128, 9048.
doi: 10.1021/ja062856v |
| [26] |
Yu, S.; Tang, G.; Li, Y.; Zhou, X.; Lan, Y.; Li, X. Angew. Chem., Int. Ed. 2016, 55, 8696.
doi: 10.1002/anie.201602224 |
| [27] |
Tang, C.; Zou, M.; Liu, J.; Wen, X.; Sun, X.; Zhang, Y.; Jiao, N. Chem.-Eur. J. 2016, 22, 11165.
doi: 10.1002/chem.201602556 |
| [28] |
Liu, R.-H.; Shan, Q.-C.; Hu, X.-H.; Loh, T.-P. Chem. Commun. 2019, 55, 5519.
doi: 10.1039/C9CC01715A |
| [1] | 付雅彤, 孙超凡, 张丹, 金成国, 陆居有. 巢式-碳硼烷硼氢键官能化反应研究进展[J]. 有机化学, 2024, 44(2): 438-447. |
| [2] | 刘杰, 韩峰, 李双艳, 陈天煜, 陈建辉, 徐清. 无过渡金属参与甲基杂环化合物与醇的选择性有氧烯基化反应[J]. 有机化学, 2024, 44(2): 573-583. |
| [3] | 赵红琼, 于淼, 宋冬雪, 贾琦, 刘颖杰, 季宇彬, 许颖. 羧酸脱羧羟基化反应研究进展[J]. 有机化学, 2024, 44(1): 70-84. |
| [4] | 董江湖, 宣良明, 王池, 赵晨熙, 王海峰, 严琼姣, 汪伟, 陈芬儿. 无过渡金属或无光催化剂条件下可见光促进喹喔啉酮C(3)—H官能团化研究进展[J]. 有机化学, 2024, 44(1): 111-136. |
| [5] | 王文芳. 过渡金属催化不对称C—H硼化反应研究进展[J]. 有机化学, 2023, 43(9): 3146-3166. |
| [6] | 高晓阳, 翟锐锐, 陈训, 王烁今. 碳酸亚乙烯酯参与C—H键活化反应的研究进展[J]. 有机化学, 2023, 43(9): 3119-3134. |
| [7] | 王灵娜, 刘晓庆, 林钢, 金泓颖, 焦民均, 刘雪粉, 罗书平. 光促进双(4-二苯甲酮)苯醚催化C(sp3)—H键活化构建C—S键[J]. 有机化学, 2023, 43(8): 2848-2854. |
| [8] | 陈新强, 张敬. 伯醇的脱羟甲基反应的研究进展[J]. 有机化学, 2023, 43(8): 2711-2719. |
| [9] | 董思凡, 李昊龙, 秦源, 范士明, 刘守信. 氨基酸作为瞬态导向基在碳氢键活化反应中的研究进展[J]. 有机化学, 2023, 43(7): 2351-2367. |
| [10] | 石义军, 孙馨悦, 曹晗, 别福升, 马杰, 刘哲, 丛兴顺. 室温下酯与伯硫醇的硫酯化反应[J]. 有机化学, 2023, 43(7): 2499-2505. |
| [11] | 徐忠荣, 万结平, 刘云云. 基于热、光以及电化学过程的无过渡金属碳-氢键硫氰化和硒氰化反应[J]. 有机化学, 2023, 43(7): 2425-2446. |
| [12] | 户晓兢, 郭斐翔, 朱润青, 周柄棋, 张涛, 房立真. 对烷氧基酚的合成及其去芳构化后的合成应用[J]. 有机化学, 2023, 43(6): 2239-2244. |
| [13] | 秦娇, 陈杰, 苏艳. 无过渡金属催化的α-溴代茚酮自由基裂解反应合成(2-氰基苯基)乙酸-2,2,6,6-四甲基哌啶酯[J]. 有机化学, 2023, 43(6): 2171-2177. |
| [14] | 徐光利, 许静, 徐海东, 崔香, 舒兴中. 过渡金属催化烯烃和炔烃合成1,3-共轭二烯化合物研究进展[J]. 有机化学, 2023, 43(6): 1899-1933. |
| [15] | 褚杨杨, 韩召斌, 丁奎岭. 动力学拆分在过渡金属催化的不对称(转移)氢化中的应用研究[J]. 有机化学, 2023, 43(6): 1934-1951. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||