有机化学 ›› 2013, Vol. 33 ›› Issue (01): 18-35.DOI: 10.6023/cjoc201208016 上一篇 下一篇
综述与进展
徐清, 李强
收稿日期:2012-08-17
修回日期:2012-09-22
发布日期:2012-10-08
通讯作者:
徐清
E-mail:qing-xu@wzu.edu.cn
基金资助:温州大学引进人才科研启动经费、国家自然科学基金(No. 20902070);教育部第40批留学回国人员科研启动金、浙江省自然科学基金(No. Y4100579)和钱江人才计划D类(No. QJD0902004)资助项目.
Xu Qing, Li Qiang
Received:2012-08-17
Revised:2012-09-22
Published:2012-10-08
Supported by:Project supported by the Startup Funding of Wenzhou University, the National Natural Science Foundation of China (No. 20902070), the Scientific Research Foundation for the Returned Overseas Chinese Scholars of State Education Ministry, the Natural Science Foundation of Zhejiang Province (No. Y4100579) and the Qianjiang Talents Program of Zhejiang Province (No. QJD0902004).
文章分享
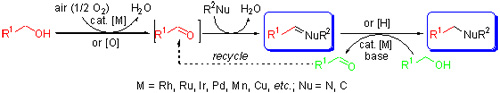
与其他胺和酰胺衍生物的合成方法相比, 过渡金属催化醇与各类胺和酰胺的脱水N-烷基化反应是一种相对绿色、原子经济性较高的方法, 一般被称为“借氢”或“氢自动转移”反应及其方法学. 近年来, 在空气氛围下过渡金属催化醇与胺和酰胺的有氧脱水N-烷基化反应, 可使用更稳定的金属催化剂、可在无配体、空气等更温和简单的条件下进行, 也引起了人们的极大关注. 主要介绍近年来过渡金属催化下醇与胺和酰胺在空气或者氧化剂作用下构建C—N, C=N键合成胺和酰胺衍生物以及亚胺类化合物的有氧脱水反应进展情况, 同时也对相关有氧脱水C-烷基化反应进行简单介绍. 相关反应的机理研究也将作适当讨论.
徐清, 李强. 过渡金属催化醇与胺有氧脱水反应及相关研究进展[J]. 有机化学, 2013, 33(01): 18-35.
Xu Qing, Li Qiang. Recent Advances of Transition Metal-Catalyzed Aerobic Dehydrative Reactions of Alcohols and Amines and Related Researches[J]. Chin. J. Org. Chem., 2013, 33(01): 18-35.
| [1] (a) Brooks, G. T.; Roberts, T. R. Pesticide Chemistry and Bioscience, Royal Society of Chemistry, Cambridge, U.K., 1999. (b) McGuire, J. L. Pharmaceuticals: Classes, Therapeutic Agents, Areas of Application, Vols. 1~4, Wiley-VCH, Weinheim, Germany, 2000. (c) Hili, R.; Yudin, A. K. Nat. Chem. Biol. 2006, 2, 284. (d) Cox, E. D.; Cook, J. M. Chem. Re v. 1995, 95, 1797. (e) Humphrey, J. M.; Chamberlin, A. R. Chem. Rev. 1997, 97, 2243. (f) Hansch, C.; Sammes, P. G.; Taylor, J. B. Comprehensive Medicinal Chemistry, Vol. 2, Pergamon Press, Oxford, 1990, Chapter 7.1. (g) Connor, E. E. Prim. Care Update Ob/Gyns 1998, 5, 32. (h) Kleemann, A.; Engel, J.; Kutscher, B.; Reichert, D. Pharmaceutical Substances, Synthesis, Patents, Applications, Thieme, Stuggart, 1999. (i) Park, S.-Y.; Fung, P.; Nishimura, N.; Jensen, D. R.; Fujii, H.; Zhao, Y.; Lumba, S.; Santiago, J.; Rodrigues, A.; Chow, T. F.; Alfred, S. E.; Bonetta, D.; Finkelstein, R.; Provart, N. J.; Desveaux, D.; Rodriguez, P. L.; McCourt, P.; Zhu, J.-K.; Schroeder, J. I.; Volkman, B. F.; Cutler, S. R. Science 2009, 324, 1068. [2] (a) Bloch, R. Chem. Re v. 1998, 98, 1407. (b) Yet, L. Angew. Chem., Int. Ed. 2001, 40, 875. (c) Ellman, J. A.; Owens, T. D.; Tang, T. P. Acc. Chem. Res. 2002, 35, 984. (d) Taggi, A. E.; Hafez, A. M.; Lectka, T. Acc. Chem. Res. 2003, 36, 10. (e) Córdova, A. Acc. Chem. Res. 2004, 37, 102. (f) Ma, J.-A. Chem. Soc. Rev. 2006, 35, 630. (g) Dömling, A. Chem. Rev. 2006, 106, 17. (h) Erkkilä, A.; Majander, I.; Pihko, P. M. Chem. Rev. 2007, 107, 5416. (i) Gawronski, J.; Wascinska, N.; Gajewy, J. Chem. Rev. 2008, 108, 5227. (j) Yamada, K.-I.; Tomioka, K. Chem. Re v. 2008, 108, 2874. (k) Merino, P.; Marqués-López, E.; Herrera, R. P. Adv. Synth. Catal. 2008, 350, 1195. (l) Ordóñez, M.; Rojas-Cabrera, H.; Cativiela, C. Tetrahedron 2009, 65, 17. (m) Martin, S. F. Pure Appl. Chem. 2009, 81, 195. (n) de Armas, P.; Tejedor, D.; Garía-Tellado, F. Angew. Chem., Int. Ed. 2010, 49, 1013. (o) Li, C.-J. Acc. Chem. Res. 2010, 43, 581. (p) Akhmetova, V. R.; Khabibullina, G. R.; Rakhimova, E. B.; Vagapov, R. A.; Khairullina, R. R.; Niatshina, Z. T.; Murzakova, N. N. Mol. Diversity 2010, 14, 463. (q) Yin, B.; Zhang, Y.; Xu, L.-W. Synthesis 2010, 3583. (r) Kobayashi, S.; Mori, Y.; Fossey, J. S.; Salter, M. M. Chem. Rev. 2011, 111, 2626. (s) Xie, J.-H.; Zhu, S.-F.; Zhou, Q.-L. Chem. Rev. 2011, 111, 1713. (t) Adrio, J.; Carretero, J. C. Chem. Commun. 2011, 47, 6784. (u) Marques, C. S.; Burke, A. J. ChemCatChem 2011, 3, 635. (v) Ramadhar, T. R.; Batey, R. A. Synthesis 2011, 1321. (w) Nielsen, M.; Worgull, D.; Zweifel, T.; Gschwend, B.; Bertelsen, S.; Jøgensen, K. A. Chem. Commun. 2011, 47, 632. [3] (a) Hartwig, J. F. Acc. Chem. Res. 2008, 41, 1534. (b) Surry, D. S.; Buchwald, S. L. Angew. Chem., Int. Ed. 2008, 47, 6338. (c) Evano, G.; Blanchard, N.; Toumi, M. Chem. Rev. 2008, 108, 3054. [4] (a) Tripathi, R. P.; Verma, S. S.; Pandey, J.; Tiwari, V. K. Curr. Org. Chem. 2008, 12, 1093. (b) Burkhardt, E. R.; Karl Matos, K. Chem. Rev. 2006, 106, 2617. (c) Baxter, E. W.; Reitz, A. B. In Organic Reactions, Vol. 59, Ed.: Overman, L. E., Wiley, Singapore, 2002. [5] (a) Müller, T. E.; Hultzsch, K. C.; Yus, M.; Foubelo, F.; Tada, M. Chem. Rev. 2008, 108, 3795. (b) Severin, R.; Doye, S. Chem. Soc. Rev. 2007, 36, 1407. (c) Müller, T. E.; Beller, M. Chem. Rev. 1998, 98, 675. [6] (a) Veige, A. S. Polyhedron 2008, 27, 3177. (b) Beccalli, E. M.; Broggini, G.; Martinelli, M.; Sottocornola, S. Chem. Rev. 2007, 107, 5318. (c) Evano, G.; Coste, A.; Jouvin, K. Angew. Chem., Int. Ed. 2010, 49, 2840. (d) DeKorver, K. A.; Li, H.; Lohse, A. G.; Hayashi, R.; Lu, Z.; Zhang, Y.; Hsung, R. P. Chem. Rev. 2010, 110, 5064. [7] (a) Salvatore, R. N.; Yoon, C. H.; Jung, K. W. Tetrahedron 2001, 57, 7785. (b) Chiappe, C.; Pieraccini, D. Green Chem. 2003, 5, 193. [8] Nef, J. U. Liebigs Ann. Chem. 1901, 318, 137. [9] Guillena, G.; Ramón, D. J.; Yus, M. Chem. Re v. 2010, 110, 1611. [10] (a) Grigg, R.; Mitchell, T. R. B.; Sutthivaiyakit, S.; Tongpenyai, N. J. Chem. Soc., Chem. Commun. 1981, 611. (b) Watanabe, Y.; Tsuji, Y.; Ohsugi, Y. Tetrahedron Lett. 1981, 22, 2667. (c) Maruhashi, S.-I.; Kondo, K.; Hakata, T. Tetrahedron Lett. 1982, 23, 229. [11] (a) Watson, A. J. A.; Williams, J. M. J. Science 2010, 329, 635. (b) Nixon, T. D.; Whittlesey, M. K.; Williams, J. M. J. Dalton Trans. 2009, 753. (c) Hamid, M. H. S. A.; Slatford, P. A.; Williams, J. M. J. Ad v. Synth. Catal. 2007, 349, 1555. (d) Suzuki, T. Chem. Rev. 2011, 111, 1825. (e) Bähn, S.; Imm, S.; Neubert, L.; Zhang, M.; Neumann, H.; Beller, M. ChemCatChem 2011, 3, 1853. (f) Crabtree, R. H. Organometallics 2011, 30, 17. (g) Dobereiner, G. E.; Crabtree, R. H. Chem. Re v. 2010, 110, 681. (h) Guillena, G.; Ramón, D. J.; Yus, M. Angew. Chem., Int. Ed. 2007, 46, 2358. (i) Fujita, K.-I.; Yamaguchi, R. Synlett 2005, 560. [12] (a) Emer, E.; Sinisi, R.; Capdevila, M. G.; Petruzziello, D.; De Vincentiis, F.; Cozzi, P. G. Eur. J. Org. Chem. 2011, 647 and references cited therein. (b) Guérinot, A.; Reymond, S.; Cossy, J. Eur. J. Org. Chem. 2011, 647. (c) Qin, H.; Yamagiwa, N.; Matsunaga, S.; Shibasaki, M. Angew. Chem., Int. Ed. 2007, 46, 409. (d) Zhan, Z.-P.; Yang, W.-Z.; Yang, R.-F.; Yu, J.-L.; Li, J.-P.; Liu, H.-J. Chem. Commun. 2006, 3352. (e) Terrasson, V.; Marque, S.; Georgy, M.; Campagne, J.-M.; Prim, D. Adv. Synth. Catal. 2006, 348, 2063. (f) Zhan, Z.-P.; Yu, J.-L.; Liu, H.-J.; Cui, Y.-Y.; Yang, R.-F.; Yang, W.-Z.; Li, J.-P. J. Org. Chem. 2006, 71, 8298. (g) Zhao, Y.; Foo, S. W.; Saito, S. Angew. Chem., Int. Ed. 2011, 50, 3006. (h) Tsai, C.-Y.; Sung, R.; Zhuang, B.-R.; Sung, K. Tetrahedron 2010, 66, 6869. (i) Sreedhar, B.; Reddy, P. S.; Reddy, M. M.; Neelima B.; Arundhathi, R. Tetrahedron Lett. 2007, 48, 8174. (j) Das, B.; Reddy, P. R.; Sudhakar, C.; Lingaiah, M. Tetrahedron Lett. 2011, 52, 3521. (k) Ozawa, F.; Okamoto, H.; Kawagishi, S.; Yamamoto, S.; Minami, T.; Yoshifuji, M. J. Am. Chem. Soc. 2002, 124, 10968. (l) Ohshima, T.; Miyamoto, Y.; Ipposhi, J.; Nakahara, Y.; Utsunomiya, M.; Mashima, K. J. Am. Chem. Soc. 2009, 131, 14317. (m) Utsunomiya, M.; Miyamoto, Y.; Ipposhi, J.; Ohshima, T.; Mashima, K. Org. Lett. 2007, 9, 3371. (n) Tao, Y.; Wang, B.; Wang, B.; Qu, L.; Qu, J. Org. Lett. 2010, 12, 2726. (o) Roggen, M.; Carreira, E. M. J. Am. Chem. Soc. 2010, 132, 11917. [13] Blackburn, L.; Taylor, R. J. K. Org. Lett. 2001, 3, 1637. [14] Kanno, H.; Taylor, R. J. K. Tetrahedron Lett. 2002, 43, 7337. [15] Guerin, C.; Bellosta, V.; Guillamot, G.; Cossy, J. Org. Lett. 2011, 13, 3534. [16] Guerin, C.; Bellosta, V.; Guillamot, G.; Cossy, J. Eur. J. Org. Chem. 2012, 15, 2990. [17] Likhar, P. R.; Arundhathi, R.; Kantam, M. L. Eur. J. Org. Chem. 2009, 5383. [18] Shi, F.; Tse, M. K.; Cui, X.; Goerdes, D.; Michalik, D.; Thurow, K.; Deng, Y.; Beller, M. Angew. Chem., Int. Ed. 2009, 48, 5912. [19] (a) Martínez-Asencio, A.; Ramón, D. J.; Yus, M. Tetrahedron Lett. 2010, 51, 325. (b) Martínez-Asencio, A.; Ramón, D. J.; Yus, M. Tetrahedron 2011, 67, 3140. [20] Cui, X.; Shi, F.; Tse, M. K.; Goerdes, D.; Thurow, K.; Beller, M.; Deng, Y. Adv. Synth. Catal. 2009, 351, 2949. [21] Feng, S. L.; Liu, C. Z.; Li, Q.; Yu, X. C.; Xu, Q. Chin. Chem. Lett. 2011, 22, 1021. [22] Liu, C.; Liao, S.; Li, Q.; Feng, S.; Sun, Q.; Yu, X.; Xu, Q. J. Org. Chem. 2011, 76, 5759 and references cited therein. [23] (a) Sheldon, R. A.; Arends, I. W. C. E.; Brink, G.-J. T.; Dijksman, A. Acc. Chem. Res. 2002, 35, 774. (b) Gligorich, K. M.; Sigman, M. S. Chem. Commun. 2009, 3854. (c) Stahl, S. S. Angew. Chem., Int. Ed. 2004, 43, 3400. (d) Naota, T.; Takaya, H.; Murahashi, S.-I. Chem. Rev. 1998, 98, 2599. (e) Muzart, J. Tetrahedron 2003, 59, 5789. (f) Arita, S.; Koike, T.; Kayaki, Y.; Ikariya, T. Angew. Chem., Int. Ed. 2008, 47, 2447. (g) Zhang, J.; Li, S.; Fu, X.; Wayland, B. B. Dalton Trans. 2009, 3661. (h) Izumi, A.; Obora, Y.; Sakaguchi, S.; Ishii, Y. Tetrahedron Lett. 2006, 47, 9199. [24] (a) Chohan, Z. H.; Shad, H. A.; Nasim, F.-H. Appl. Organomet. Chem. 2009, 23, 319 and references therein. (b) Cejudo-Marín, R.; Alzuet, G.; Ferrer, S.; Borrás, J. Inorg. Chem. 2004, 43, 6805. (c) Zhang, T.; Wang, W.; Gu, X.; Shi, M. Organometallics 2008, 27, 753. (d) Liang, J.; Lipscomb, W. N. Biochemistry 1989, 28, 9724. (e) Evelhoch, J. L. E.; Bocian, D. F.; Sudmeier, J. L. Biochemistry 1981, 20, 4951. (f) Dimroth, J.; Keilitz, J.; Schedler, U.; Schomäcker, R.; Haag, R. Adv. Synth. Catal. 2010, 352, 2497. [25] (a) Watanabe, Y.; Morisaki, Y.; Kondo, T.; Mitsudo, T. J. Org. Chem. 1996, 61, 4214. (b) Watanabe, Y.; Tsuji, Y.; Ige, H.; Ohsugi, Y.; Ohta, T. J. Org. Chem. 1984, 49, 3359. (c) Fujita, K.-I.; Enkoi, Y.; Yamaguchi, R. Tetrahedron 2008, 64, 1943. [26] Yu, X.; Jiang, L.; Li, Q.; Xie, Y. ; Xu, Q. Chin. J. Chem. 2012, 30, 2322. [27] (a) Layer, R. W. Chem. Rev. 1963, 63, 489. (b) Sprung, M. M. Chem. Rev. 1940, 26, 297. (c) Patai, S. The Chemistry of the Carbon—Nitrogen Double Bond (Chemistry of Functional Goups), Wiley-Interscience, New York, 1970. (d) Adams, J. P. J. Chem. Soc., Perkin Trans. 1 2000, 125. [28] (a) Gladiali, S.; Alberico, E. Chem. Soc. Rev. 2006, 35, 226. (b) Samec, J. S. M.; B?ckvall, J.-E.; Andersson, P. G.; Brandt, P. Chem. Soc. Rev. 2006, 35, 237. (c) Saluzzo, C.; Lemaire, M. Ad v . Synth. Catal. 2002, 344, 915. (d) Noyori, R.; Hashiguchi, S. Acc. Chem. Res. 1997, 30, 97. (e) Krische, M. J.; Sun, Y. Special issue on hydrogenation and transfer hydrogenation. Acc. Chem. Res. 2007, 40, issue 12. [29] (a) Kwon, M. S.; Kim, S.; Park, S.; Bosco, W.; Chidrala, R. K.; Park, J. J. Org. Chem. 2009, 74, 2877. (b) Corma, A.; Ródenas, R.; Sabater, M. J. Chem. Eur. J. 2010, 16, 254. (c) Zhang, Y.; Qi, X.; Cui, X.; Shi, F.; Deng, Y. Tetrahedron Lett. 2011, 52, 1334. [30] Martínez-Asencio, A.; Yus, M.; Ramón, D. J. Synthesis 2011, 3730. [31] Kawahara, R.; Fujita, K.-I.; Yamaguchi, R. Adv. Synth. Catal. 2011, 353, 1161. [32] Ohta, H.; Yuyama, Y.; Uozumi, Y.; Yamada, Y. M. A. Org. Lett. 2011, 13, 3892. [33] Yu, X.; Liu, C.; Jiang, L.; Xu, Q. Org. Lett. 2011, 13, 6184. [34] (a) Gonzalez-Arellano, C.; Yoshida, K.; Luque, L.; Gai, P. L. Green Chem. 2010 12, 1281. (b) Martínez, M.; Ramón, D. J.; Yus, M. Org. Biomol. Chem. 2009, 7, 2176. (c) Valotl, F.; Fachel, F.; Jacquot, R.; Spagnol, M.; Lemairel, M. Tetrahedron Lett. 1999, 40, 3689. [35] (a) Shi, F.; Tse, M. K.; Zhou, S.; Pohl, M. M.; Radnik, J.; Hübner, S.; J?hnisch, K.; Brückner, A.; Beller, M. J. Am. Chem. Soc. 2009, 131, 1775. (b) Cano, R.; Ramón, D. J.; Yus, M. J. Org. Chem. 2011, 76, 5547. (c) Yamaguchi, K.; He, J.; Oishi, T.; Mizuno, N. Chem. Eur. J. 2010, 16, 7199. (d) He, J.; Kim, J. W.; Yamaguchi, K.; Mizuno, N. Angew. Chem., Int. Ed. 2009, 48, 9888. (e) Cui, X.; Zhang, Y.; Shi, F.; Deng, Y. Chem. Eur. J. 2011, 17, 1021. (f) He, L.; Lou, X.-B.; Ni, J.; Liu, Y.-M.; Cao, Y.; He, H.-Y.; Fan, K.-N. Chem. Eur. J. 2010, 16, 13965. [36] (a) Li, C.-J.; Li, Z. Pure Appl. Chem. 2006, 78, 935. (b) Li, C.-J. Acc. Chem. Res. 2009, 42, 335. (c) Scheuermann, C. J. Chem. Asian J. 2010, 5, 436. (d) Li, Z.; Bohle, S.; Li, C.-J. Proc. Natl. Acad. Sci. U. S. A. 2006, 103, 8928. [37] (a) Semmelhack, M. F.; Schmid, C. R.; Cortes, D. A.; Chou, C. S. J. Am. Chem. Soc. 1984, 106, 3374. (b) Markó, I. E.; Giles, P. R.; Tsukazaki, M.; Brown, S. M.; Urch, C. J. Science 1996, 274, 2044. (c) Markó, I. E.; Gautier, A.; Dumeunier, R.; Doda, K.; Philippart, F.; Brown, S. M.; Urch, C. J. Angew. Chem., Int. Ed. 2004, 43, 1588. (d) Gamez, P.; Arends, I. W. C. E.; Reedijk, J.; Sheldon, R. A. Chem. Commun. 2003, 2414. (d) Hoover, J. M.; Stahl, S. S. J. Am. Chem. Soc. 2011, 133, 16901. [38] (a) Wendlandt, A. E.; Suess, A. M.; Stahl, S. S. Angew. Chem., Int. Ed. 2011, 50, 11062. (b) Liu, C.; Zhang, H.; Shi, W.; Lei, A. Chem. Rev. 2011, 111, 1780. (c) Klussmann, M.; Sureshkumar, D. Synthesis 2011, 353. (d) Zhao, Z.; Peng, F. Angew. Chem., Int. Ed. 2010, 49, 9566. (e) Stefani, H. A.; Guarezemini, A. S.; Cella, R. Tetrahedron 2010, 66, 7871. [39] Li, Q.; Fan, S.; Sun, Q.; Tian, H.; Yu, X.; Xu, Q. Org. Biomol. Chem. 2012, 10, 2966 and references cited therein. [40] (a) Deutsch, C.; Krause, N.; Lipshutz, B. H. Chem. Re v. 2008, 108, 2916. (b) Rendler, S.; Oestreich, M. Angew. Chem., Int. Ed. 2007, 46, 498. (c) Lipshutz, B. H. Synlett 2009, 509. [41] Jiang, L.; Jin, L.; Tian, H.; Yuan, X.; Yu, X.; Xu, Q. Chem. Commun. 2011, 47, 10833. [42] Tian, H.; Yu, X.; Li, Q.; Wang, J.; Xu, Q. Adv. Synth. Catal. 2012, 354, 2671. [43] Yamada, Y. M. A.; Uozumi, Y. Org. Lett. 2006, 8, 1375. [44] Yamada, Y. M. A.; Uozumi, Y. Tetrahedron 2007, 63, 8492. [45] Allen, L. J.; Crabtree, R. H. Green Chem. 2010, 12, 1362. [46] (a) Thomé, I.; Nijs, A.; Bolm, C. Chem. Soc. Rev. 2012, 41, 979. (b) Leadbeater, N. E. Nat. Chem. 2010, 2, 913. (c) Buchwald, S. L.; Bolm, C. Angew. Chem., Int. Ed. 2009, 48, 5586. [47] Tang, G.; Cheng, C.-H. Adv. Synth. Catal. 2011, 353, 1918. [48] Liao, S.; Yu, K.; Li, Q.; Tian, H.; Zhang, Z.; Yu, X.; Xu, Q. Org. Biomol. Chem. 2012, 10, 2973 and references cited therein. [49] (a) Palacios, F.; Alonso, C.; Aparicio, D.; Rubiales, G.; de los Santos, J. M. Tetrahedron 2007, 63, 523. (b) Fresneda, P. M.; Molina, P. Synlett 2004, 1. [50] (a) Largeron, M.; Fleury, M.-B. Angew. Chem., Int. Ed. 2012, 51, 5409. (b) Lang, X.; Ji, H.; Chen, C.; Ma, W.; Zhao, J. Angew. Chem., Int. Ed. 2011, 50, 3934. (c) Jiang, G.; Chen, J.; Huang, J.-S.; Che, C.-M. Org. Lett. 2009, 11, 4568. (d) Samec, J. S. M.; Éll, A. H.; Bäckvall, J.-E. Chem. Eur. J. 2005, 11, 2327. [51] Schiff, H. Annals 1864, 131, 118. [52] Medvedeva, A. S.; Mareev, A. V.; Borisova, A. I.; Afonin, A. V. ARKIVOC 2003, 13, 157. [53] Yusubov, M. S.; Chi, K.-W.; Park, J. Y.; Karimovc, R.; Zhdankinc, V. V. Tetrahedron Lett. 2006, 47, 6305. [54] (a) Gnanaprakasam, B.; Zhang, J.; Milstein, D. Angew. Chem., Int. Ed. 2010, 49, 1468. (b) Maggi, A.; Madsen, R. Organometallics 2012, 31, 451. (c) Esteruelas, M. A.; Honczek, N.; Oliván, M.; Onate, E.; Valencia, M. Organometallics 2011, 30, 2468. (d) Cano, R.; Ramón, D. J.; Yus, M. J. Org. Chem. 2011, 76, 5547. (e) Shiraishi, Y.; Ikeda, M.; Tsukamoto, D.; Tanaka, S.; Hiraia, T. Chem. Commun. 2011, 47, 4811. [55] Sun, H.; Su, F.-Z.; Ni, J.; Cao, Y.; He, H.-Y.; Fan, K.-N. Angew. Chem., Int. Ed. 2009, 48, 4390. [56] Kim, J. W.; He, J.; Yamaguchi, K.; Mizuno, N. Chem. Lett. 2009, 38, 920. [57] Kegnaes, S.; Mielby, J.; Mentzel, U. V.; Christensen, C. H.; Riisager, A. Green Chem. 2010, 12, 1437. [58] He, W.; Wang, L.; Sun, C.; Wu, K.; He, S.; Chen, J.; Wu, P.; Yu, Z. Chem. Eur. J. 2011, 17, 13308. [59] Kang, Q.; Zhang, Y. Green Chem. 2012, 14, 1016. [60] Sithambaram, S.; Kumar R.; Son, Y.-C.; Suib, S. L. J. Catal. 2008, 253, 269. [61] Kwon, M. S.; Kim, N.; Seo, S. H.; Park, I. S.; Cheedrala, R. K.; Park, J. Angew. Chem., Int. Ed. 2005, 44, 6913. [62] Kim, S.; Bae, S. W.; Lee, J. S.; Park, J. Tetrahedron 2009, 65, 1461. [63] Xu, Q.; Tian, H.; Jin, L. CN 102775288, 2012 [Chem. Abstr. 2012, 158, 11329]. |
| [1] | 刘杰, 韩峰, 李双艳, 陈天煜, 陈建辉, 徐清. 无过渡金属参与甲基杂环化合物与醇的选择性有氧烯基化反应[J]. 有机化学, 2024, 44(2): 573-583. |
| [2] | 张勇, 田志高, 黄琳, 侯秋飞, 范红红, 汪万强. α-氰醇甲磺酸酯在合成α-氨基腈类化合物中的应用[J]. 有机化学, 2024, 44(2): 561-572. |
| [3] | 王化坤, 任晓龙, 宣宜宁. 卤盐催化的α,β-环氧羧酸酯与异氰酸酯[3+2]环加成反应研究[J]. 有机化学, 2024, 44(1): 251-258. |
| [4] | 赵红琼, 于淼, 宋冬雪, 贾琦, 刘颖杰, 季宇彬, 许颖. 羧酸脱羧羟基化反应研究进展[J]. 有机化学, 2024, 44(1): 70-84. |
| [5] | 童红恩, 郭宏宇, 周荣. 可见光促进惰性碳-氢键对羰基的加成反应进展[J]. 有机化学, 2024, 44(1): 54-69. |
| [6] | 蒋宜欣, 唐伯孝, 毛海波, 陈雪霞, 俞洋杰, 全翠英, 徐昭阳, 石金慧, 刘益林. 水-聚乙二醇(PEG-200)中烯烃与碘代芳烃绿色可循环无负载偶联反应的研究[J]. 有机化学, 2023, 43(9): 3210-3215. |
| [7] | 鄢伯钰, 吴阶良, 邓金飞, 陈丹, 叶秀深, 姚秋丽. 光诱导醇的直接脱羟基衍生化研究进展[J]. 有机化学, 2023, 43(9): 3055-3066. |
| [8] | 高晓阳, 翟锐锐, 陈训, 王烁今. 碳酸亚乙烯酯参与C—H键活化反应的研究进展[J]. 有机化学, 2023, 43(9): 3119-3134. |
| [9] | 张晓雨, 李欣燕, 崔冰, 邵志晖, 赵铭钦. 四氢-β-咔啉衍生物的设计、合成及抗氧化性能研究[J]. 有机化学, 2023, 43(8): 2885-2894. |
| [10] | 陈新强, 张敬. 伯醇的脱羟甲基反应的研究进展[J]. 有机化学, 2023, 43(8): 2711-2719. |
| [11] | 高艳华, 张银潘, 张妍, 宋涛, 杨勇. 可见光驱动表面富含氧空位Nb2O5催化醇氧化反应[J]. 有机化学, 2023, 43(7): 2572-2579. |
| [12] | 石义军, 孙馨悦, 曹晗, 别福升, 马杰, 刘哲, 丛兴顺. 室温下酯与伯硫醇的硫酯化反应[J]. 有机化学, 2023, 43(7): 2499-2505. |
| [13] | 徐光利, 许静, 徐海东, 崔香, 舒兴中. 过渡金属催化烯烃和炔烃合成1,3-共轭二烯化合物研究进展[J]. 有机化学, 2023, 43(6): 1899-1933. |
| [14] | 刘甜甜, 张鸿鹏, 焦晓梦, 白银娟. 多信号同时检测生物硫醇荧光探针的研究进展[J]. 有机化学, 2023, 43(6): 2081-2095. |
| [15] | 户晓兢, 郭斐翔, 朱润青, 周柄棋, 张涛, 房立真. 对烷氧基酚的合成及其去芳构化后的合成应用[J]. 有机化学, 2023, 43(6): 2239-2244. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||