有机化学 ›› 2023, Vol. 43 ›› Issue (10): 3414-3453.DOI: 10.6023/cjoc202307025 上一篇 下一篇
所属专题: 有机硅化学专辑-2023
综述与进展
南宁a,b, 吴双a,b, 秦景灏a,b,*( ), 李金恒a,b,c,d,*(
), 李金恒a,b,c,d,*( )
)
收稿日期:2023-07-27
修回日期:2023-09-09
发布日期:2023-09-15
基金资助:
Ning Nana,b, Shuang Wua,b, Jinghao Qina,b( ), Jinheng Lia,b,c,d(
), Jinheng Lia,b,c,d( )
)
Received:2023-07-27
Revised:2023-09-09
Published:2023-09-15
Contact:
*E-mail: Supported by:文章分享

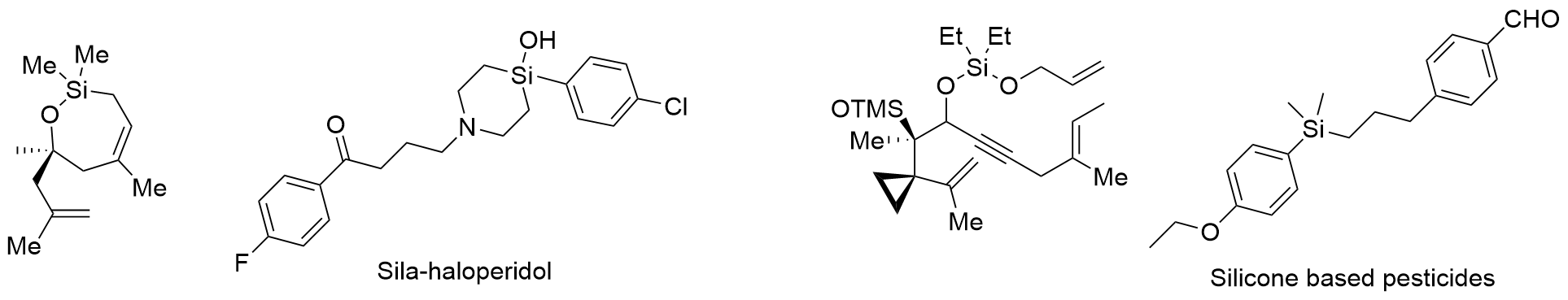
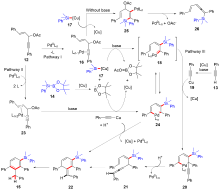
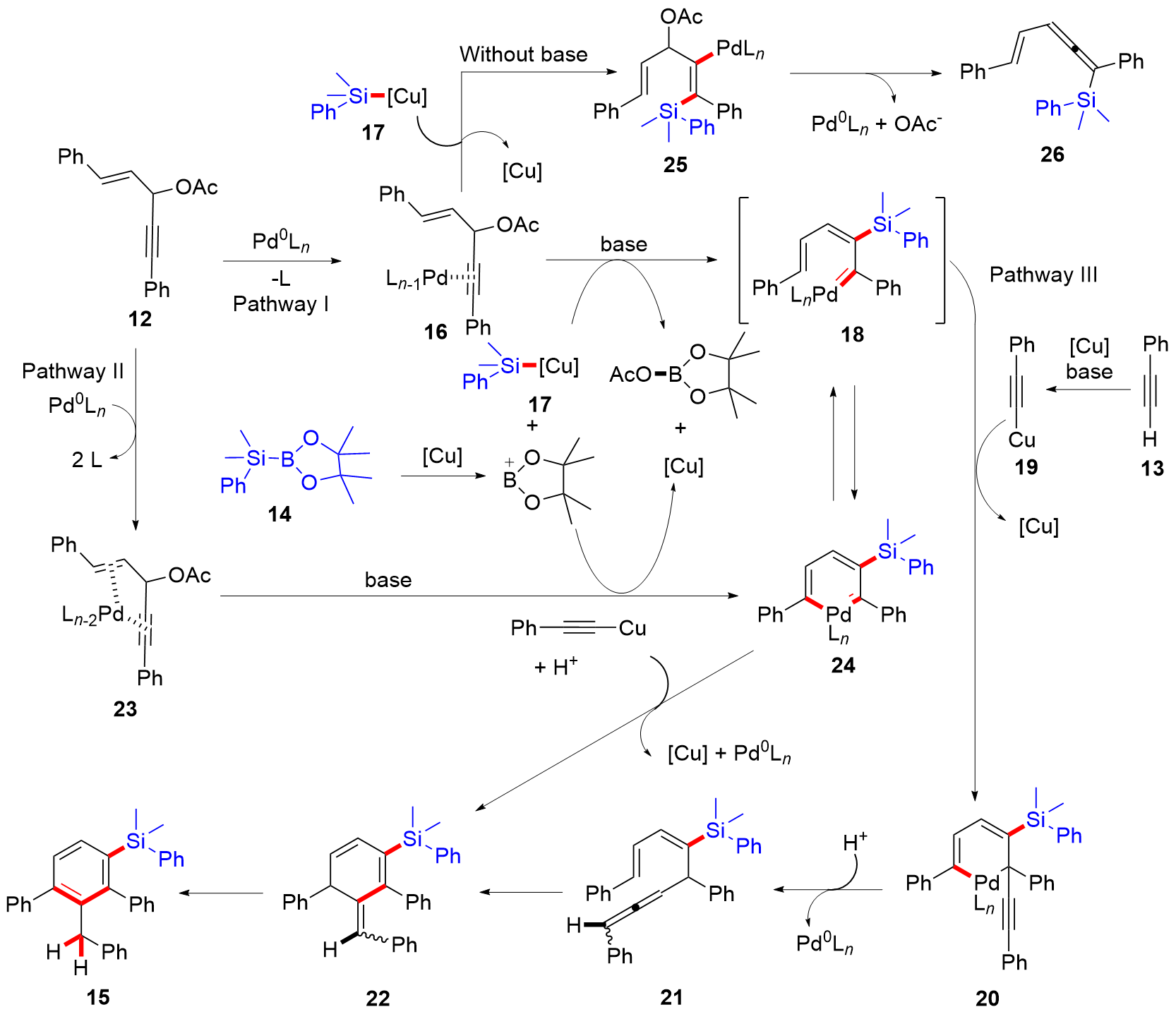
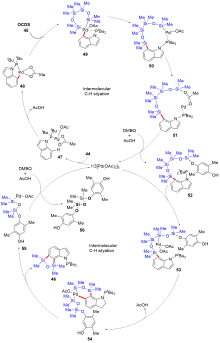
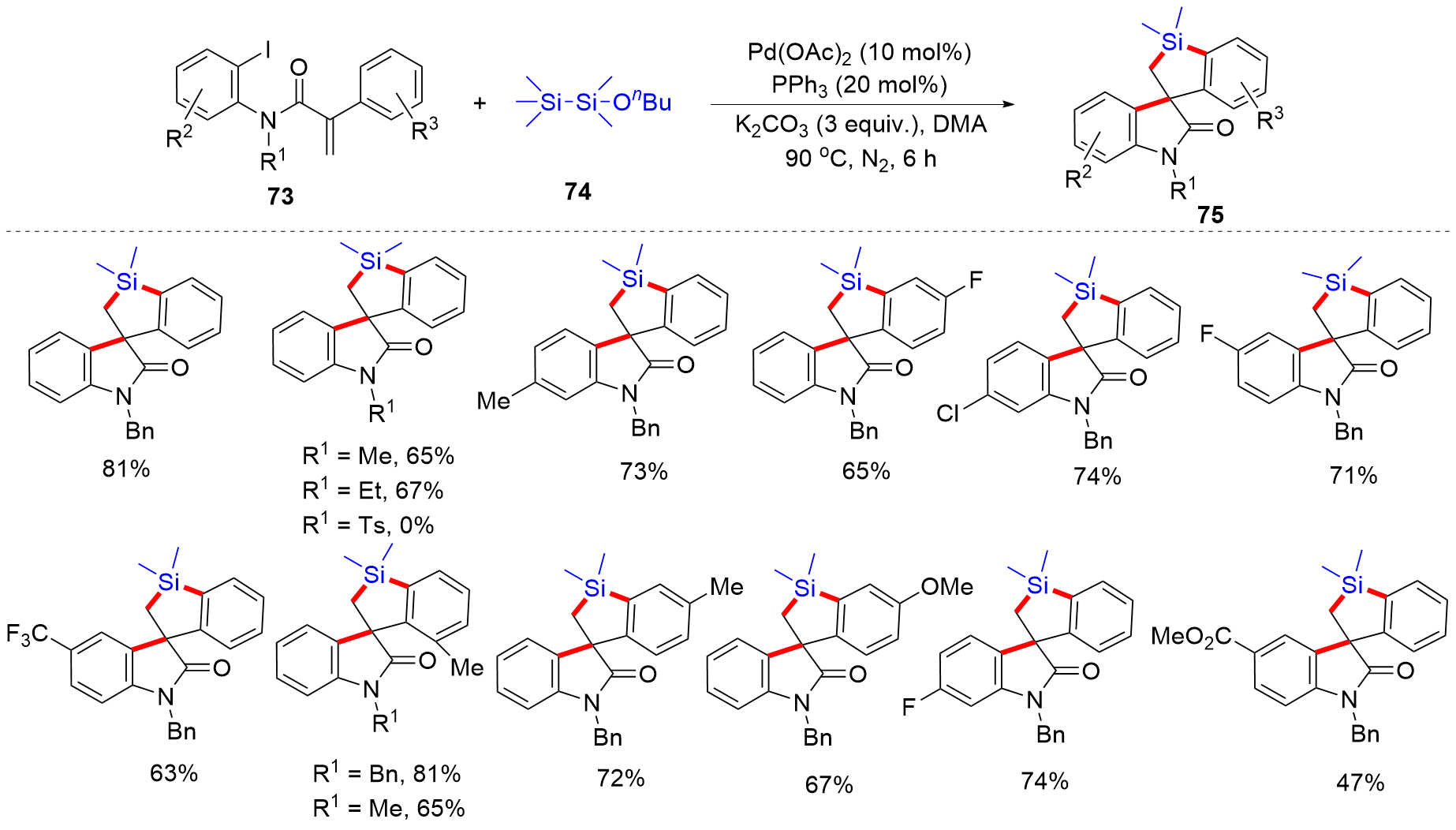
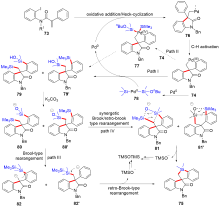
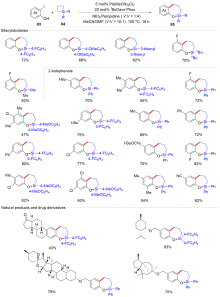
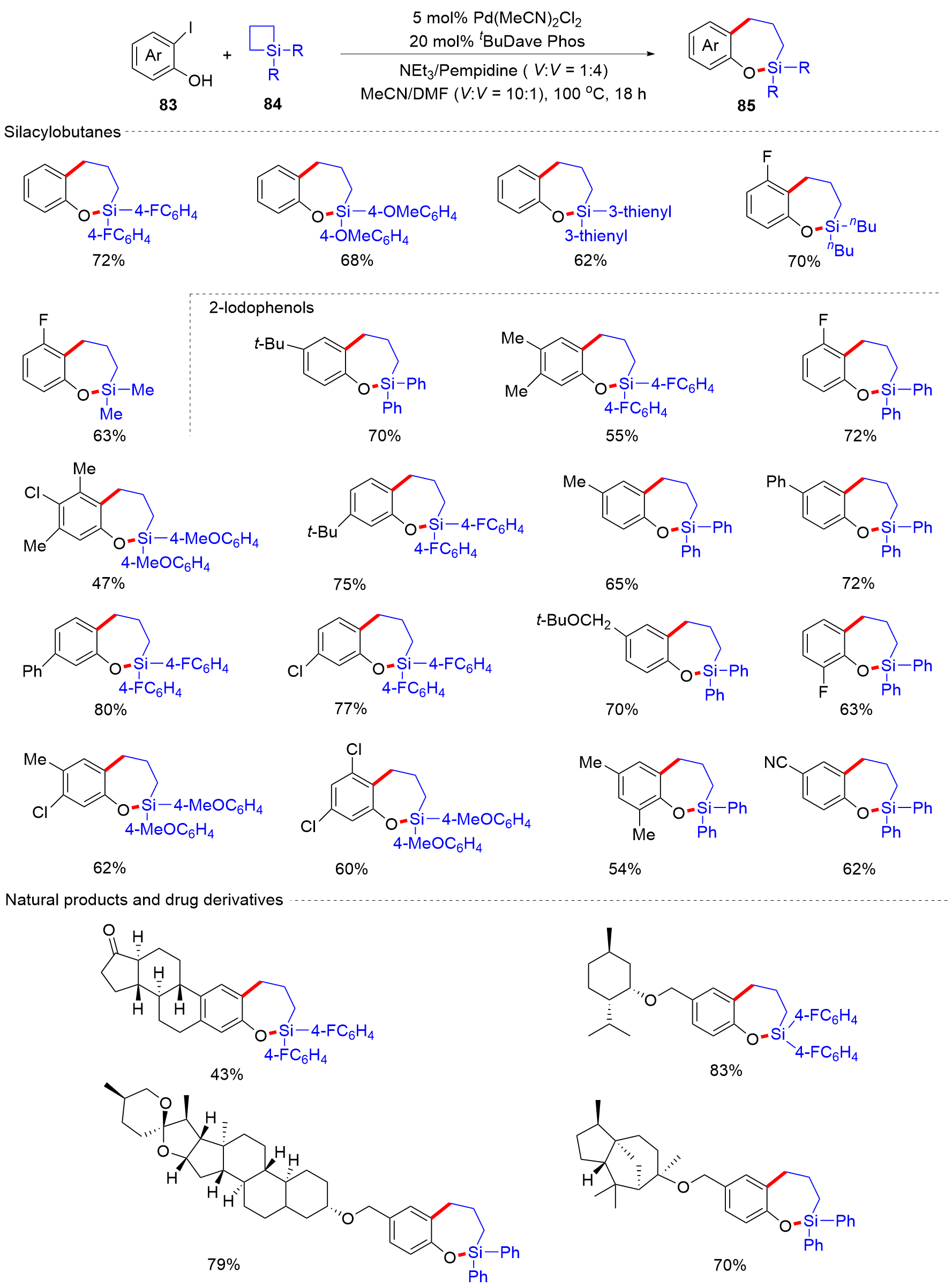
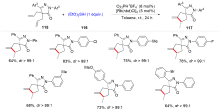
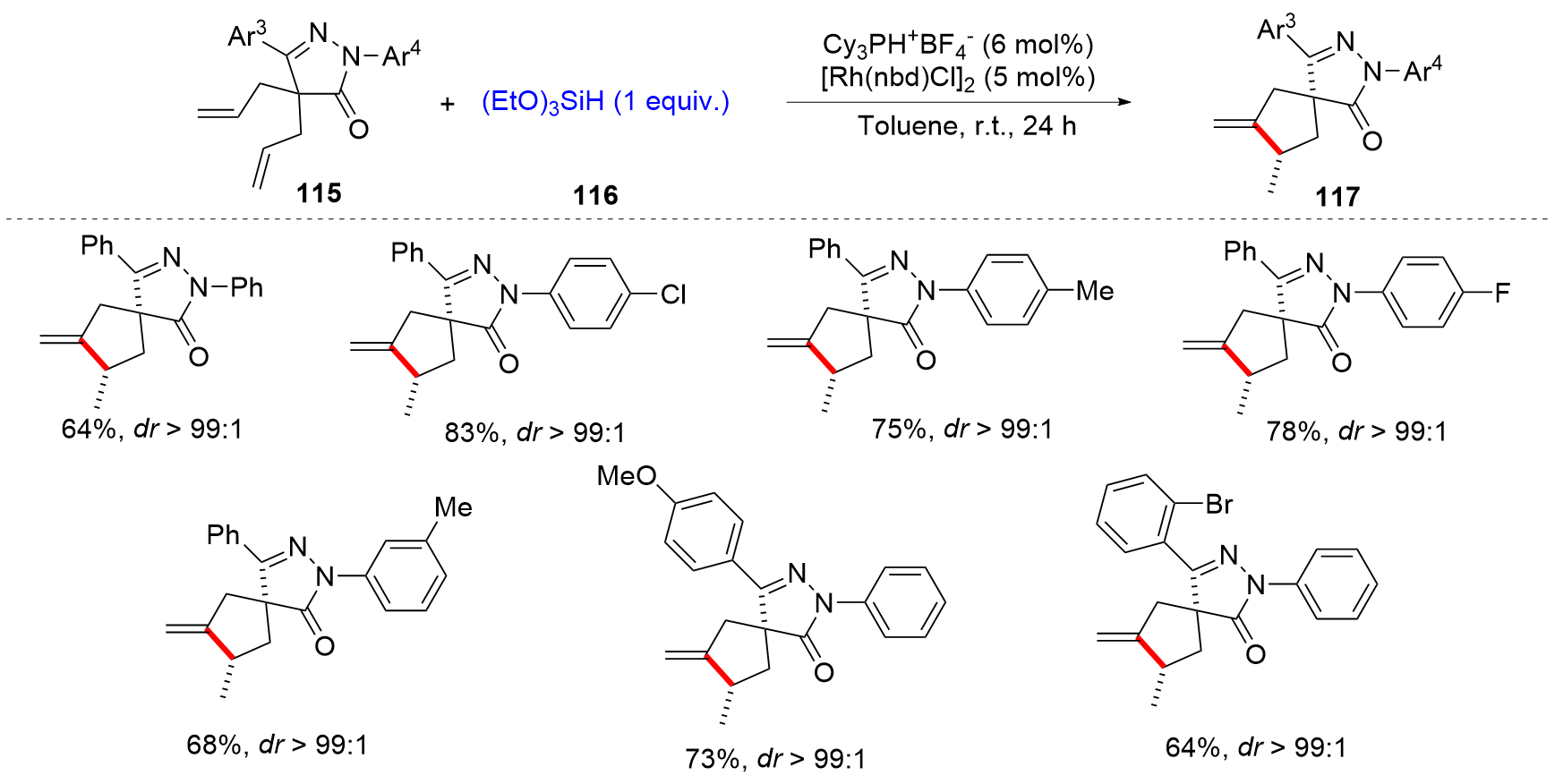
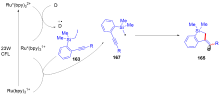
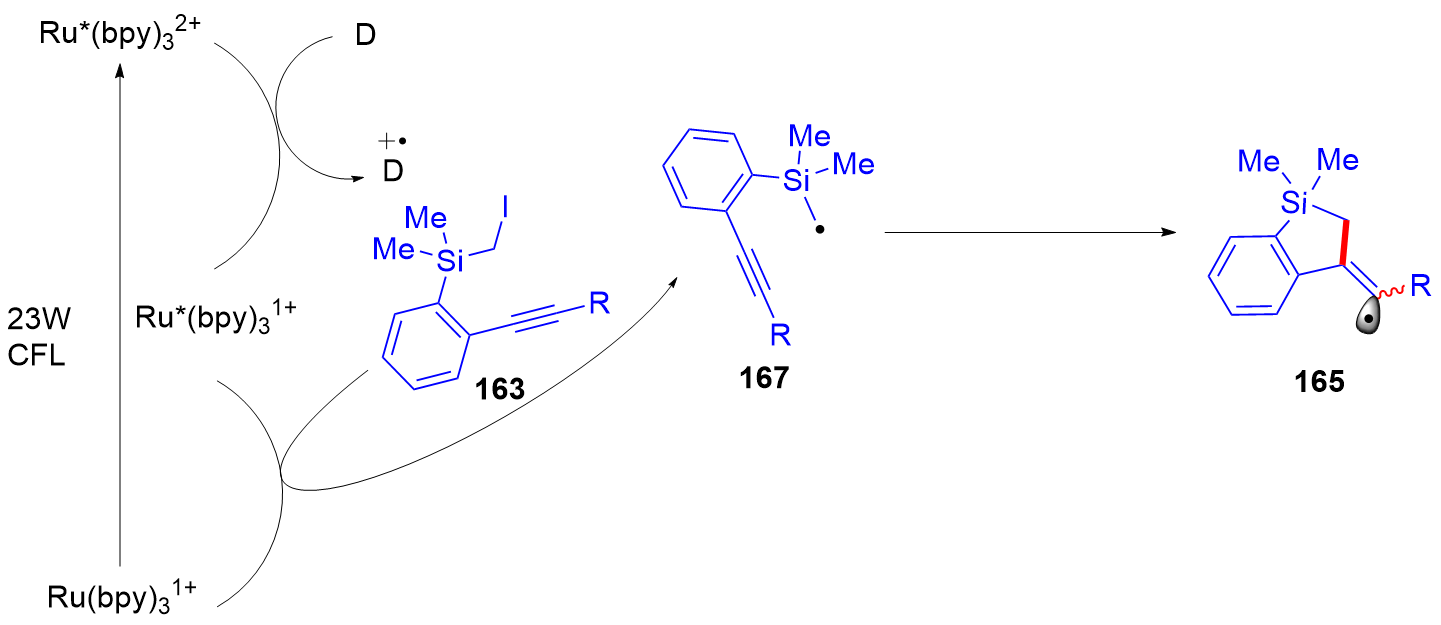
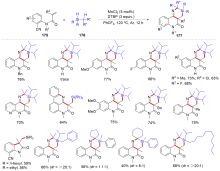
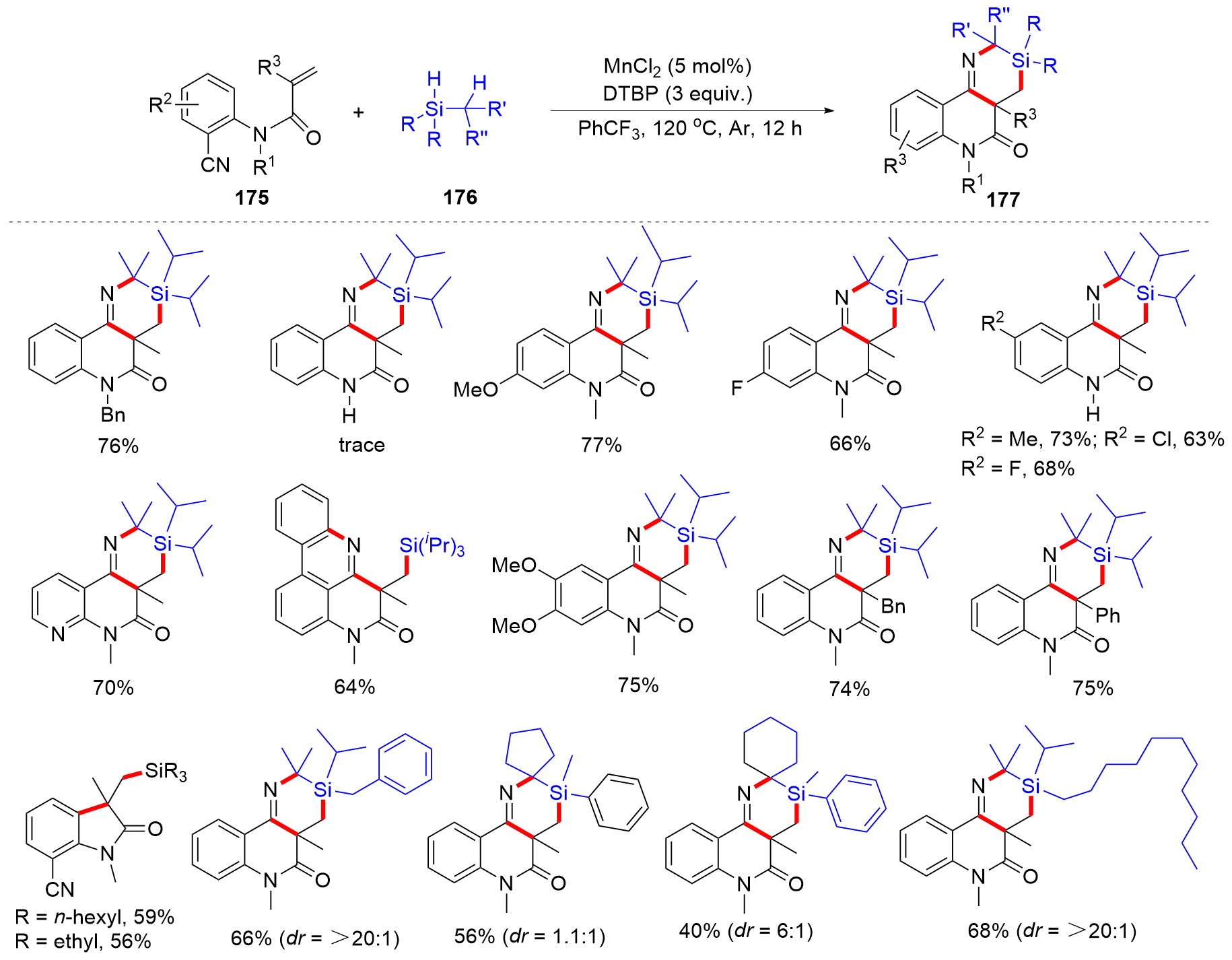
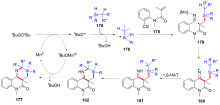
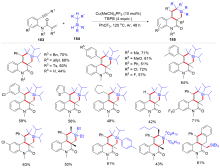
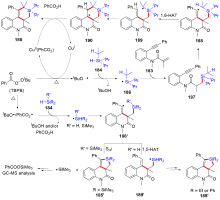
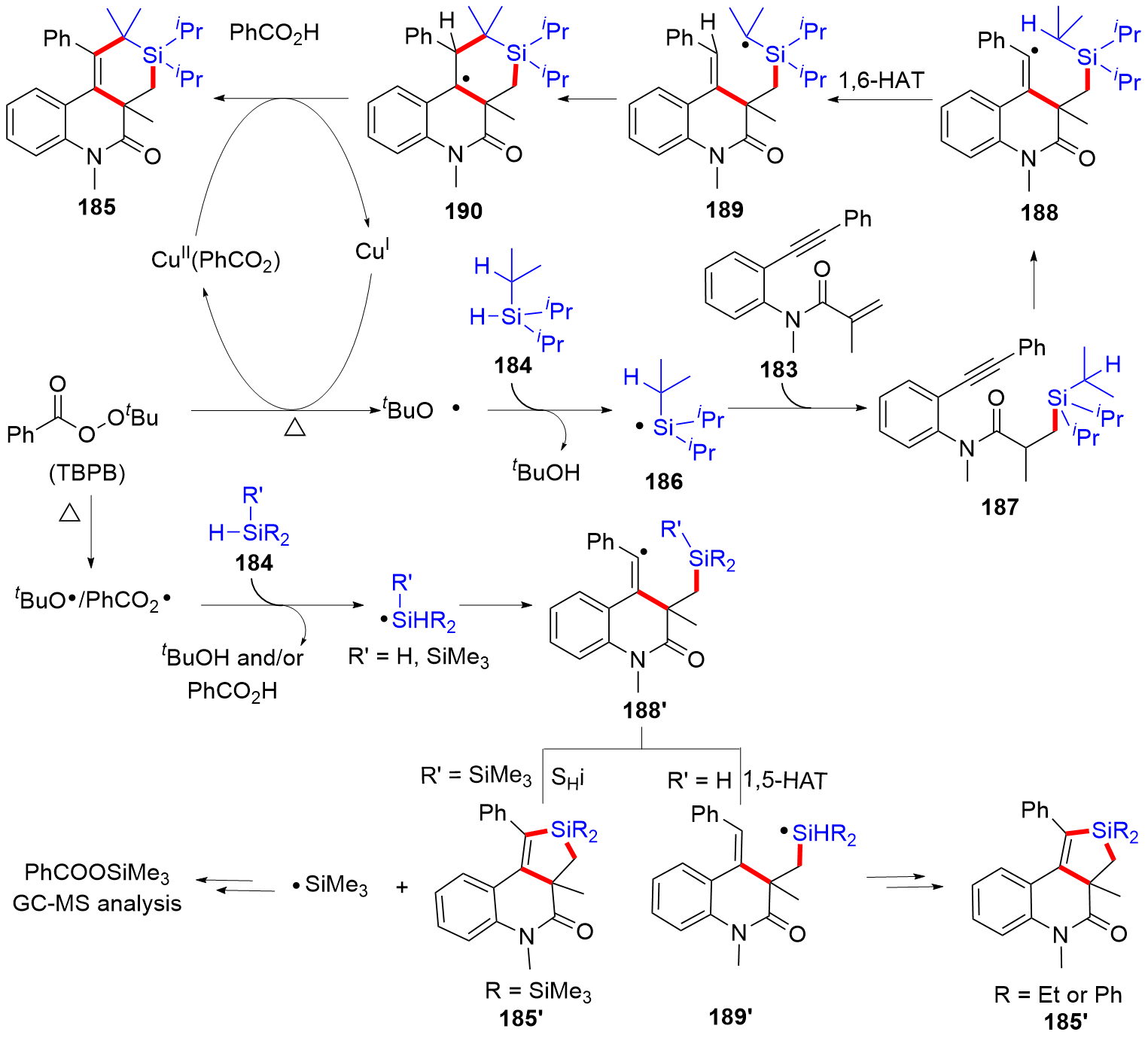
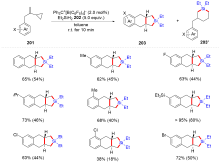
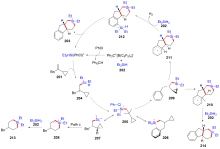
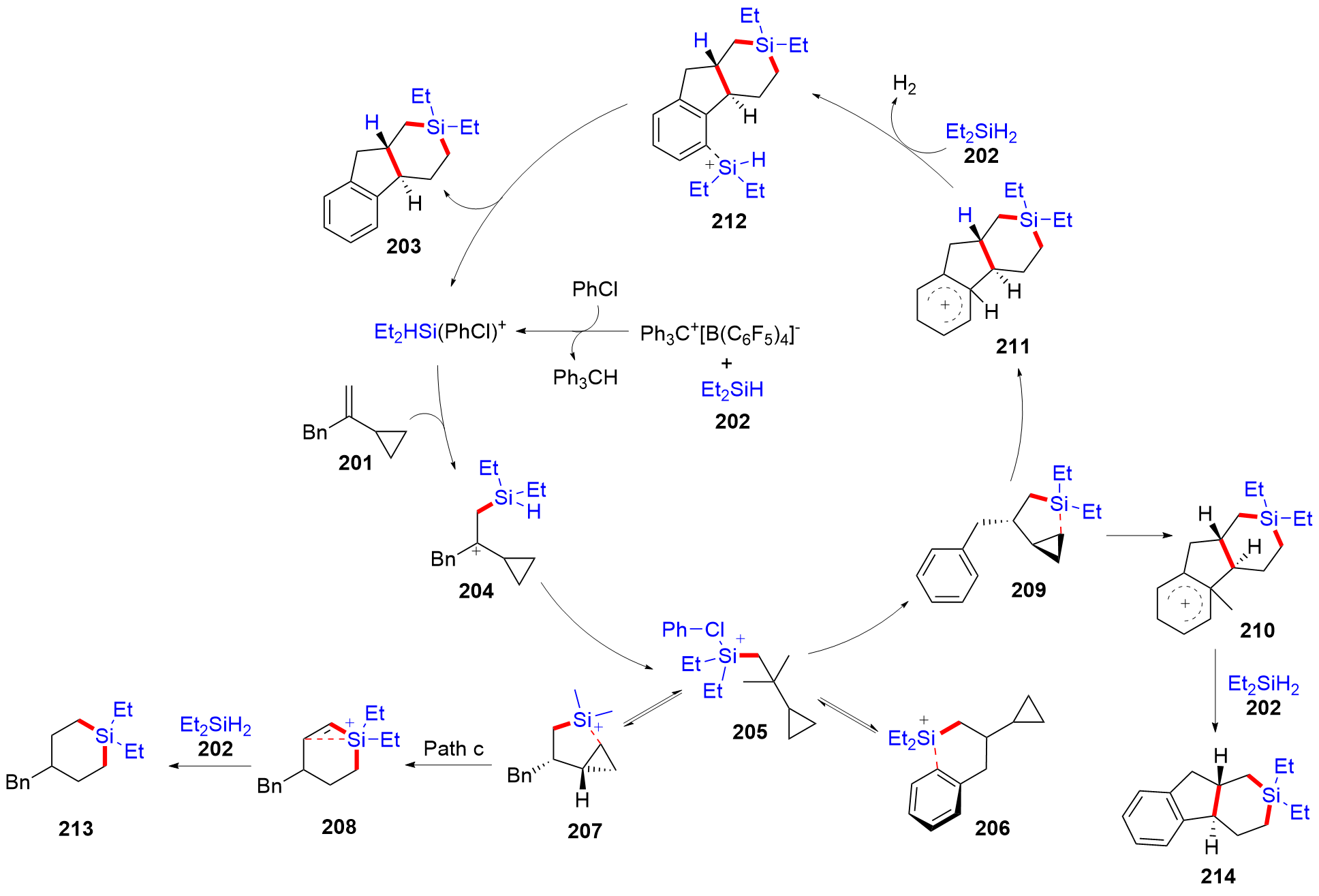
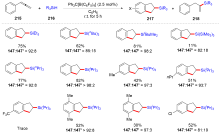
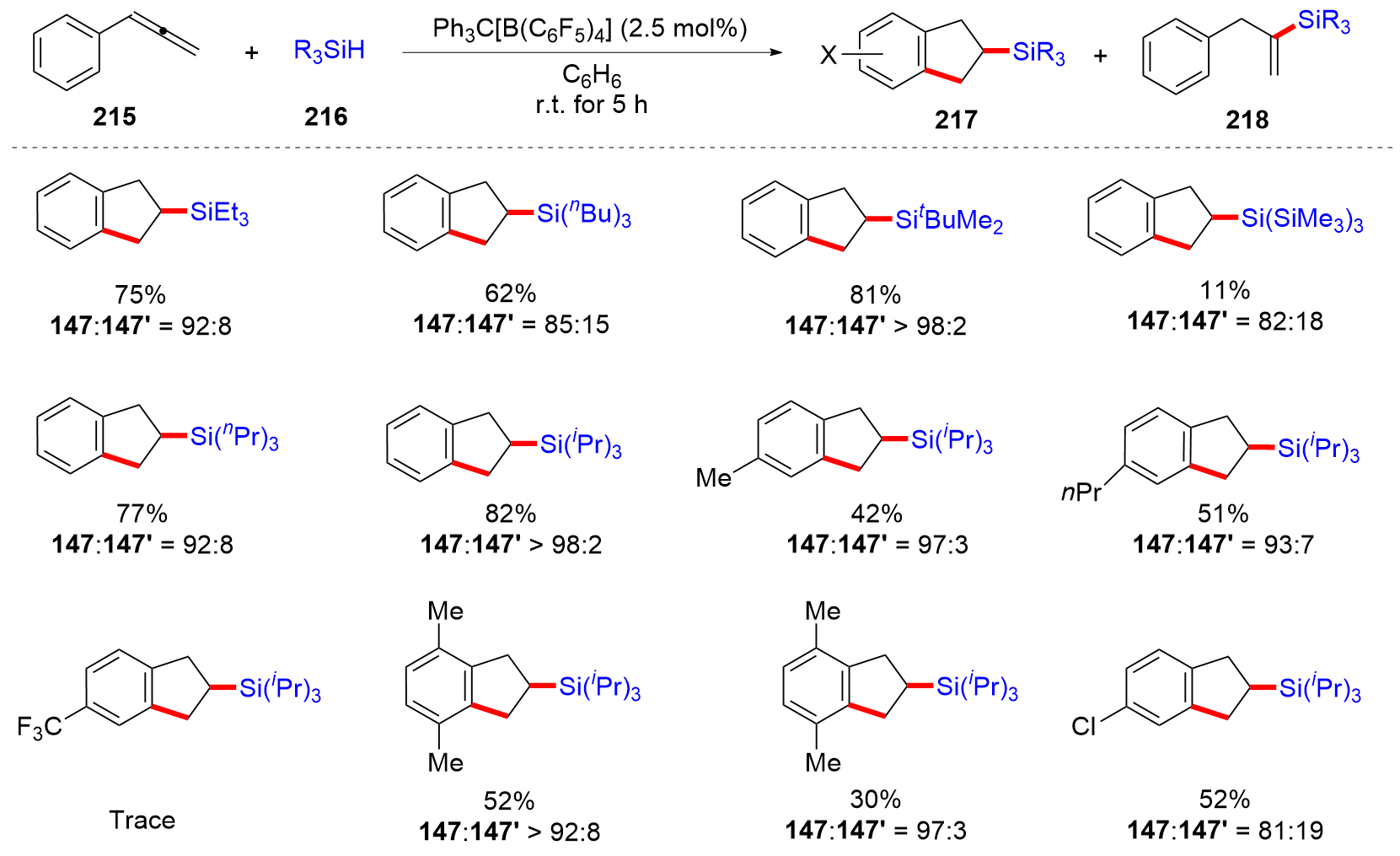
有机硅化合物是许多材料的重要基元和有用的有机分子, 是化学合成中用途广泛的合成中间体. 因此, 化学家们一直致力于开发构建含硅化学键的新方法, 特别是C—Si键. 自从Sakurai和Imai在1975年报道了第一个钯催化的硅环丁烷与炔的环加成反应以来, 过渡金属催化硅基环化反应得到了迅速的发展. 随着自由基反应的迅猛发展, 研究者将其拓展到有机硅分子间环化反应, 硅的环化反应迎来了新的发展. 主要从过渡金属催化的硅环化反应、自由基引发的硅环化反应、C+离子引发的硅环化反应展开讨论, 最后对当前的研究进展进行了总结.
南宁, 吴双, 秦景灏, 李金恒. 基于硅烷化启动的环化反应研究进展[J]. 有机化学, 2023, 43(10): 3414-3453.
Ning Nan, Shuang Wu, Jinghao Qin, Jinheng Li. State-of-Art Advances on Silylation-Initiated Annulation Reactions[J]. Chinese Journal of Organic Chemistry, 2023, 43(10): 3414-3453.
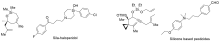







| [1] |
(a) Feldman D. J. Polym. Sci., Part C: Polym. Lett. 1990, 28, 207.
doi: 10.1002/pol.12.v28:116 |
|
(b) Steinmetz M. G. Chem. Rev. 1995, 95, 1527.
doi: 10.1021/cr00037a017 |
|
|
(c) Thomas M. J. K. Polym. Int. 2001, 50, 256.
|
|
|
(d) Marciniec B. Coord. Chem. Rev. 2005, 249, 2374.
doi: 10.1016/j.ccr.2005.02.025 |
|
|
(e) Molle A.; Grazianetti C.; Tao L.; Taneja D.; Alam M. H.; Akinwande D. Chem. Soc. Rev. 2018, 47, 6370.
doi: 10.1039/C8CS00338F |
|
|
(f) Kyushin S.; Kurosaki Y.; Otsuka K.; Imai H.; Ishida S.; Kyomen T.; Hanaya M.; Matsumoto H. Nat. Commun. 2020, 11, 4009.
doi: 10.1038/s41467-020-17815-z |
|
|
(g) Li L.; Wei Y.-L.; Xu L.-W. Synlett 2020, 31, 21.
doi: 10.1055/s-0039-1691496 |
|
| [2] |
(a) Yamamoto Y. Chem. Rev. 2012, 112, 4736.
doi: 10.1021/cr300050n |
|
(b) Wang Y.; Attam A.; Fan H.; Zheng W.; Liu W. Small 2023, doi:10.1002/smll.202303804.
|
|
| [3] |
(a) Huang T.; Li T.; Wang J.; Qin G.; Xiao T. Chin. J. Org. Chem. 2019, 39, 1511 (in Chinese).
|
|
(黄鸿泰, 李涛, 王家状, 秦贵平, 肖铁波, 有机化学, 2019, 39, 1511.)
doi: 10.6023/cjoc201903078 |
|
|
(b) Zhang J.; Ten Y.; Li X.; Wang S. Chin. J. Org. Chem. 2007, 228, 1358 (in Chinese).
|
|
|
(张金东, 滕雅娣, 李旭日, 王思林, 有机化学, 2007, 228, 1358.)
|
|
|
(c) Li J.; Peng J.; Li X.; Ma L.; Bai Y.; Zhang G.; Lai G. Chin. J. Org. Chem. 2010, 30, 1468 (in Chinese).
|
|
|
(厉嘉云, 彭家建, 李小年, 马磊, 白赢, 张国栋, 来国桥, 有机化学, 2010, 30, 1468.)
|
|
| [4] |
(a) Kim U. B.; Jung D. J.; Jeon H. J.; Rathwell K.; Lee S.-G. Chem. Rev. 2020, 120, 13382.
doi: 10.1021/acs.chemrev.0c00245 |
|
(b) Zhang Y.; Feng B. Chin. J. Org. Chem. 2014, 34, 2406 (in Chinese).
doi: 10.6023/cjoc201408030 |
|
|
(张艳; 冯柏年, 有机化学, 2014, 34, 2406.)
doi: 10.6023/cjoc201408030 |
|
|
(c) Shi X.; Han X.; Ma W.; Wei J. Chin. J. Org. Chem. 2011, 31, 297 (in Chinese).
|
|
|
(石先莹; 韩晓燕; 马文娟; 魏俊发, 有机化学, 2011, 31, 297.)
|
|
|
(d) Marciniec B.; Pietraszuk C.; Pawluć P.; Maciejewski H. Chem. Rev. 2022, 122, 3996.
doi: 10.1021/acs.chemrev.1c00417 |
|
| [5] |
Wu L.-J.; Yang L.-F.; Li J.-H.; Wang Q.-A. Chem. Commun. 2020, 56, 1669.
doi: 10.1039/C9CC09077K |
| [6] |
Wu L.-J.; Teng F.; Lv G.-F.; Li J.-H. Org. Lett. 2020, 22, 8544.
doi: 10.1021/acs.orglett.0c03144 pmid: 33075230 |
| [7] |
Qin Y.; Han J.-L.; Ju C.-W.; Zhao D. Angew. Chem., Int. Ed. 2020, 59, 8481.
doi: 10.1002/anie.v59.22 |
| [8] |
Wang X.-B.; Zheng Z.-J.; Xie J.-L.; Gu X.-W.; Mu Q.-C.; Yin G.-W.; Ye F.; Xu Z.; Xu L.-W. Angew. Chem., Int. Ed. 2020, 59, 790.
doi: 10.1002/anie.v59.2 |
| [9] |
Wang D.; Li M.; Chen X.; Wang M.; Liang Y.; Zhao Y.; Houk K. N.; Shi Z. Angew. Chem., Int. Ed. 2021, 60, 7066.
doi: 10.1002/anie.v60.13 |
| [10] |
Zhu M.-H.; Zhang X.-W.; Usman M.; Cong H.; Liu W.-B. ACS Catal. 2021, 11, 5703.
doi: 10.1021/acscatal.1c00975 |
| [11] |
Li H.; Huang W.-S.; Yang K.-F.; Ye F.; Yin G.-W.; Xu Z.; Xu L.-W. Asian J. Org. Chem. 2021, 10, 2883.
doi: 10.1002/ajoc.v10.11 |
| [12] |
Xu Y.; Xu W.; Chen X.; Luo X.; Lu H.; Zhang M.; Yang X.; Deng G.; Liang Y.; Yang Y. Chem. Sci. 2021, 12, 11756.
doi: 10.1039/D1SC03487A |
| [13] |
Qin Y.; Li L.; Liang J.-Y.; Li K.; Zhao D. Chem. Sci. 2021, 12, 14224.
doi: 10.1039/D1SC04180K |
| [14] |
Xu H.; Fang X.-J.; Huang W.-S.; Xu Z.; Li L.; Ye F.; Cao J.; Xu L.-W. Org. Chem. Front. 2022, 9, 5272.
doi: 10.1039/D2QO00943A |
| [15] |
Xu Y.; Sun M.; Xu W.; Deng G.; Liang Y.; Yang Y. J. Am. Chem. Soc. 2023, 145, 15303.
doi: 10.1021/jacs.3c02875 |
| [16] |
Zhao W.-T.; Lu Z.-Q.; Zheng H.; Xue X.-S.; Zhao D. ACS Catal. 2018, 8, 7997.
doi: 10.1021/acscatal.8b01992 |
| [17] |
Chen H.; Chen Y.; Tang X.; Liu S.; Wang R.; Hu T.; Gao L.; Song Z. Angew. Chem., Int. Ed. 2019, 58, 4695.
doi: 10.1002/anie.v58.14 |
| [18] |
Tang R.-H.; Xu Z.; Nie Y.-X.; Xiao X.-Q.; Yang K.-F.; Xie J.-L.; Guo B.; Yin G.-W.; Yang X.-M.; Xu L.-W. iScience 2020, 23, 101268.
doi: 10.1016/j.isci.2020.101268 |
| [19] |
Li H.-L.; Huang W.-S.; Ling F.-Y.; Li L.; Yan J.-H.; Xu H.; Xu L.-W. Chem.-Aslan J. 2021, 16, 1730.
|
| [20] |
Wang X.; Huang S.-S.; Zhang F.-J.; Xie J.-L.; Li Z.; Xu Z.; Ye F.; Xu L.-W. Org. Chem. Front. 2021, 8, 6577.
doi: 10.1039/D1QO01386F |
| [21] |
Zeng Y.; Fang X.-J.; Tang R.-H.; Xie J.-Y.; Zhang F.-J.; Xu Z.; Nie Y.-X.; Xu L.-W. Angew. Chem. Int. Ed. 2022, 61, e202214147.
|
| [22] |
Chen H.; Zhang H.; Du H.; Kuang Y.; Pang Q.; Gao L.; Wang W.; Yang C.; Song Z. Org. Lett. 2023, 25, 1558.
doi: 10.1021/acs.orglett.3c00346 |
| [23] |
Long P.-W.; Bai X.-F.; Ye F.; Li L.; Xu Z.; Yang K.-F.; Cui Y.-M.; Zheng Z.-J.; Xu L.-W. Adv. Synth. Catal. 2018, 360, 2825.
doi: 10.1002/adsc.v360.15 |
| [24] |
You Y. E.; Ge S. Angew. Chem., Int. Ed. 2021, 60, 12046.
doi: 10.1002/anie.v60.21 |
| [25] |
Zhao M.; Wang Y.; Wang Z.-L.; Xu J.-L.; Dai K.-Y.; Xu Y.-H. Org. Lett. 2021, 23, 3859.
doi: 10.1021/acs.orglett.1c00968 |
| [26] |
(a) Liu Y.; Luo P.; Fu Y.; Hao T.; Liu X.; Ding Q.; Peng Y. Beilstein J. Org. Chem. 2021, 17, 2462.
doi: 10.3762/bjoc.17.163 pmid: 34630726 |
|
(b) Jiang S.; Nan N.; He J.; Guo J.; Qin J.; Xie Y.; Ouyang X.-H.; Song R. Chin J. Org. Chem. 2022, 42, 3959 (in Chinese).
doi: 10.6023/cjoc202210013 pmid: 34630726 |
|
|
(姜松, 南宁, 何景昊, 郭嘉程, 秦景灏, 谢叶香, 欧阳旋慧, 宋仁杰, 有机化学, 2022, 42, 3959.)
doi: 10.6023/cjoc202210013 pmid: 34630726 |
|
|
(c) Zhao Q.; Chen J. Chin. J. Org. Chem. 2021, 41, 871 (in Chinese).
doi: 10.6023/cjoc202100016 pmid: 34630726 |
|
|
(赵全庆, 陈加荣, 有机化学, 2021, 41, 871.)
doi: 10.6023/cjoc202100016 pmid: 34630726 |
|
| [27] |
Lin X.; Gan Z.; Lu J.; Su Z.; Hu C.; Zhang Y.; Wu Y.; Gao L.; Song Z. Chem. Commun. 2016, 52, 6189.
doi: 10.1039/C6CC00635C |
| [28] |
Wu L.-J.; Tan F.-L.; Li M.; Song R.-J.; Li J.-H. Org. Chem. Front. 2017, 4, 350.
doi: 10.1039/C6QO00691D |
| [29] |
Wu L.-J.; Yang Y.; Song R.-J.; Yu J.-X.; Li J.-H.; He D.-L. Chem. Commun. 2018, 54, 1367.
doi: 10.1039/C7CC08996A |
| [30] |
Yang Y.; Song R.-J.; Li Y.; Ouyang X.-H.; Li J.-H.; He D.-L. Chem. Commun. 2018, 54, 1441.
doi: 10.1039/C7CC08964C |
| [31] |
Hou H.; Xu Y.; Yang H.; Chen X.; Yan C.; Shi Y.; Zhu S. Org. Lett. 2020, 22, 1748.
doi: 10.1021/acs.orglett.0c00024 |
| [32] |
Ye T.; Zhao J.; Zheng W.-X.; Zhang J.; Wang Z.; Zhang F.-L. Org. Chem. Front. 2023, 10, 2165.
doi: 10.1039/D3QO00153A |
| [33] |
(a) Jiang X.; Wang S.; Guo G.; Lu B. Chin. J. Org. Chem. 2017, 37, 841 (in Chinese).
doi: 10.6023/cjoc201610010 |
|
(江欣, 王斯顿, 郭贵敏, 卢贝丽, 有机化学, 2017, 37, 841.)
doi: 10.6023/cjoc201610010 |
|
|
(b) Yao S.; Xiong Y.; Driess M. Organometallics 2011, 30, 1748.
doi: 10.1021/om200017h |
|
|
(c) Tyagi A.; Yadav N.; Khan J.; Singh S.; Hazra C. K. Asian J. Org. Chem. 2021, 10, 334.
doi: 10.1002/ajoc.v10.2 |
|
| [34] |
He T.; Wang G.; Long P.-W.; Kemper S.; Irran E.; Klare H. F. T.; Oestreich M. Chem. Sci. 2021, 12, 569.
doi: 10.1039/D0SC05553K |
| [35] |
Rej S.; Klare H. F. T.; Oestreich M. Org. Lett. 2022, 24, 1346.
doi: 10.1021/acs.orglett.2c00011 |
| [36] |
Rej S.; Klare H. F. T.; Oestreich M. Org. Lett. 2023, 25, 426.
doi: 10.1021/acs.orglett.2c04166 |
| [1] | 董江湖, 宣良明, 王池, 赵晨熙, 王海峰, 严琼姣, 汪伟, 陈芬儿. 无过渡金属或无光催化剂条件下可见光促进喹喔啉酮C(3)—H官能团化研究进展[J]. 有机化学, 2024, 44(1): 111-136. |
| [2] | 张素珍, 张文文, 杨慧, 顾庆, 游书力. 铑催化2-烯基苯酚与炔烃的对映体选择性螺环化反应[J]. 有机化学, 2023, 43(8): 2926-2933. |
| [3] | 许晓萍, 张翼飞, 莫小渝, 江俊. 铑催化3-重氮吲哚-2-亚胺与吡唑啉酮的C—H官能团化反应制备3-吡唑基吲哚[J]. 有机化学, 2023, 43(7): 2519-2527. |
| [4] | 陈玉琢, 孙红梅, 王亮, 胡方芝, 李帅帅. 基于α-氢迁移策略构建杂环骨架的研究进展[J]. 有机化学, 2023, 43(7): 2323-2337. |
| [5] | 孙李星, 孙婷婷, 王海清, 吴淑芳, 王小烨, 刘天雅, 张宇辰. Lewis酸催化下3-烷基-2-吲哚烯与α,β-不饱和N-磺酰基亚胺的[2+4]环化反应[J]. 有机化学, 2023, 43(6): 2178-2188. |
| [6] | 任志军, 罗维纬, 周俊. 银介导的N-芳基丙烯酰胺串联环化反应研究进展[J]. 有机化学, 2023, 43(6): 2026-2039. |
| [7] | 李靖鹏, 黄顺桃, 杨棋, 李伟强, 刘腾, 黄超. 利用连续流动技术合成(Z)-N-乙烯基取代N,O-缩醛[J]. 有机化学, 2023, 43(4): 1550-1558. |
| [8] | 南江, 黄冠杰, 胡岩, 王波. 钌催化喹唑啉酮与碳酸亚乙烯酯的C—H [4+2]环化反应[J]. 有机化学, 2023, 43(4): 1537-1549. |
| [9] | 王海清, 杨爽, 张宇辰, 石枫. 邻羟基苄醇参与的催化不对称反应研究进展[J]. 有机化学, 2023, 43(3): 974-999. |
| [10] | 桑田, 贾帆, 何静, 李春天, 刘岩, 刘平. I2催化β-酮腈与1H-吡唑-5-胺的环化反应[J]. 有机化学, 2023, 43(1): 195-201. |
| [11] | 刘东汉, 鲁席杭, 柴张梦洁, 杨浩琦, 孙瑜琳, 余富朝. 构建2H-吡咯-2-酮骨架的研究进展[J]. 有机化学, 2023, 43(1): 57-73. |
| [12] | 王川川, 马志伟, 侯学会, 杨龙华, 陈亚静. N-Ts氰胺在有机合成中的研究与应用[J]. 有机化学, 2023, 43(1): 74-93. |
| [13] | 覃小婷, 邹宁, 农彩梅, 莫冬亮. 九元氮杂环化合物合成最新研究进展[J]. 有机化学, 2023, 43(1): 130-155. |
| [14] | 刘浩阳, 孙爽爽, 马献力, 陈艳艳, 徐燕丽. 可见光促进异腈插入反应合成硒代螺环[吲哚-3,3'-喹啉]衍生物[J]. 有机化学, 2022, 42(9): 2867-2876. |
| [15] | 王苛莉, 黄静, 刘伟, 伍智林, 于贤勇, 蒋俊, 何卫民. 由N-(2-丙炔基)苯胺和磺酰氯直接合成3-砜基喹啉[J]. 有机化学, 2022, 42(8): 2527-2534. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||