有机化学 ›› 2021, Vol. 41 ›› Issue (12): 4758-4765.DOI: 10.6023/cjoc202109011 上一篇 下一篇
研究论文
收稿日期:2021-09-06
修回日期:2021-10-19
发布日期:2021-11-03
通讯作者:
金伟伟, 刘晨江
基金资助:
Ailing Tang, Weiwei Jin( ), Chenjiang Liu(
), Chenjiang Liu( )
)
Received:2021-09-06
Revised:2021-10-19
Published:2021-11-03
Contact:
Weiwei Jin, Chenjiang Liu
Supported by:文章分享

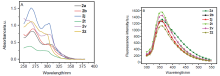
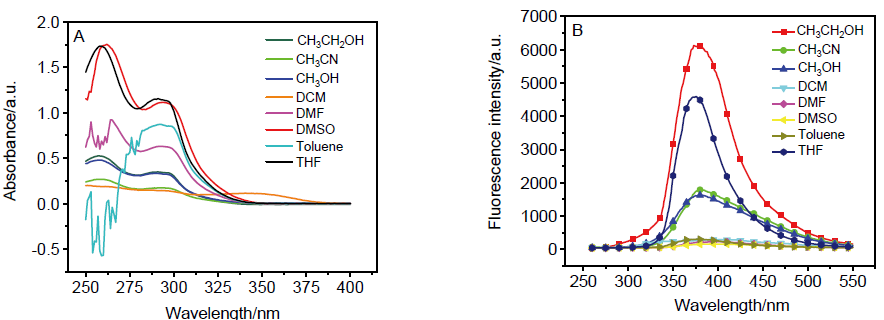
报道了一种三甲基溴硅烷促进的通过碳-碳键交叉偶联反应合成N-甲基吲哚二聚体的方法. 在温和条件下以最高95%的收率方便地合成了一系列2,3′-吲哚基二氢吲哚类化合物. 克级反应证明了该方法的实用性. 初步研究了目标产物的紫外-可见吸收和荧光光谱性质.
唐爱玲, 金伟伟, 刘晨江. 三甲基溴硅烷诱导的N-保护吲哚的区域选择性二聚合成2,3′-吲哚基二氢吲哚[J]. 有机化学, 2021, 41(12): 4758-4765.
Ailing Tang, Weiwei Jin, Chenjiang Liu. Trimethylsilyl Bromide-Induced Regioselective Dimerization of N-Protected Indoles to 2,3'-Linked Indolylindolines[J]. Chinese Journal of Organic Chemistry, 2021, 41(12): 4758-4765.
| Entry | Base | Solvent | Additive | Yield of 2ab/% |
|---|---|---|---|---|
| 1 | K2CO3 | DCM | TMSCl | 61 |
| 2 | KOH | DCM | TMSCl | 24 |
| 3 | K3PO4•3H2O | DCM | TMSCl | 63 |
| 4 | K3PO4•3H2O | CHCl3 | TMSCl | 59 |
| 5 | K3PO4•3H2O | DCM/CHCl3 | TMSCl | 68 |
| 6 | K3PO4•3H2O | DCM/CHCl3 | TfOH | 50 |
| 7 | K3PO4•3H2O | DCM/CHCl3 | TMSOTf | 55 |
| 8 | K3PO4•3H2O | DCM/CHCl3 | TMSI | 29 |
| 9 | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 79 |
| 10c | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 35 |
| 11d | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 78 |
| 12 | — | DCM/CHCl3 | TMSBr | n.r. |
| 13 | K3PO4•3H2O | DCM/CHCl3 | — | n.r. |
| Entry | Base | Solvent | Additive | Yield of 2ab/% |
|---|---|---|---|---|
| 1 | K2CO3 | DCM | TMSCl | 61 |
| 2 | KOH | DCM | TMSCl | 24 |
| 3 | K3PO4•3H2O | DCM | TMSCl | 63 |
| 4 | K3PO4•3H2O | CHCl3 | TMSCl | 59 |
| 5 | K3PO4•3H2O | DCM/CHCl3 | TMSCl | 68 |
| 6 | K3PO4•3H2O | DCM/CHCl3 | TfOH | 50 |
| 7 | K3PO4•3H2O | DCM/CHCl3 | TMSOTf | 55 |
| 8 | K3PO4•3H2O | DCM/CHCl3 | TMSI | 29 |
| 9 | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 79 |
| 10c | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 35 |
| 11d | K3PO4•3H2O | DCM/CHCl3 | TMSBr | 78 |
| 12 | — | DCM/CHCl3 | TMSBr | n.r. |
| 13 | K3PO4•3H2O | DCM/CHCl3 | — | n.r. |


| [1] |
Yu, H.; Yu, Z. Angew. Chem., nt. Ed. 2009, 48, 2929.
|
| [2] |
(a) Ishikura, M.; Yamada, K. Nat. Prod. Rep. 2009, 26, 803.
doi: 10.1039/b820693g pmid: 19471686 |
|
(b) Lee, G. W.; Kim, N.-K.; Jeong, K.-S. Org. Lett. 2010, 12, 2634.
doi: 10.1021/ol100830b pmid: 19471686 |
|
| [3] |
(c) Deng, Y.; Haimowitz, T.; LaPorte, M. G.; Rippin, S. R.; Alexander, M. D.; Kumar, P. T.; Hendi, M. S.; Lee, Y.-H.; Condon, S. M. ACS Med. Chem. Lett. 2016, 7, 318.
doi: 10.1021/acsmedchemlett.5b00461 |
|
(d) Lee, C.-H.; Yoon, H.; Jang, W.-D. Chem.-Eur. J. 2009, 15, 9972.
doi: 10.1002/chem.v15:39 |
|
| [4] |
(a) Hinman, R. L.; Shull, E. R. J. Org. Chem. 1961, 26, 2339.
doi: 10.1021/jo01351a046 |
|
(b) Chisholm, J. D.; Van Vranken, D. L. J. Org. Chem. 1995, 60, 6672.
doi: 10.1021/jo00126a011 |
|
| [5] |
(a) Pal, B.; Giri, V. S.; Jaisankar, P. Catal. Commun. 2005, 6, 711.
doi: 10.1016/j.catcom.2005.07.003 |
|
(b) Shelke, G. M.; Kumar, A. Synthesis 2017, 49, 4321.
doi: 10.1055/s-0036-1588181 |
|
|
(c) Fujino, K.; Yanase, E.; Nakatsuka, S. Heterocycl. Commun. 2004, 10, 265.
|
|
| [6] |
Nemoto, K.; Tanaka, S.; Konno, M.; Onozawa, S.; Chiba, M.; Tanaka, Y.; Sasaki, Y.; Okubo, R.; Hattori, T. Tetrahedron 2016, 72, 734.
doi: 10.1016/j.tet.2015.12.028 |
| [7] |
Higuchi, K.; Tago, T.; Kokubo, Y.; Ito, M.; Tayu, M.; Sugiyama, S.; Kawasaki, T. Org. Chem. Front. 2018, 5, 3219.
doi: 10.1039/C8QO00798E |
| [8] |
(a) Wu, Y.; Chen, J.-Y.; Ning, J.; Jiang, X.; Deng, J.; Deng, Y.; Xu, R.; He, W.-M. Green Chem. 2021, 23, 3950.
doi: 10.1039/D1GC00562F |
|
(b) Wang, X.; Li, G.; Sun, K.; Zhang, B. Chin. J. Org. Chem. 2020, 40, 913. (in Chinese)
doi: 10.6023/cjoc202002040 |
|
|
( 王薪, 李国锋, 孙凯, 张冰, 有机化学, 2020, 40, 913.)
doi: 10.6023/cjoc202002040 |
|
|
(c) Yi, R.; He, W.-M. Chin. J. Org. Chem. 2021, 41, 1267. (in Chinese)
doi: 10.6023/cjoc202100022 |
|
|
( 易荣楠, 何卫民, 有机化学, 2021, 41, 1267.)
doi: 10.6023/cjoc202100022 |
|
|
(d) Han, Y.; Cui, X. Chin. J. Org. Chem. 2021, 41, 2929. (in Chinese)
doi: 10.6023/cjoc202100056 |
|
|
( 韩宇轩, 崔秀灵, 有机化学, 2021, 41, 2929.)
doi: 10.6023/cjoc202100056 |
|
| [9] |
(a) Liu, S.; Zhao, F.; Chen, X.; Deng, G.-J.; Huang, H. Adv. Synth. Catal. 2020, 362, 3795.
doi: 10.1002/adsc.v362.18 |
|
(b) Cacchi, S.; Fabrizi, G. Chem. Rev. 2005, 105, 2873.
doi: 10.1021/cr040639b |
|
|
(c) Cerveri, A.; Bandini, M. Chin. J. Chem. 2020, 38, 287.
doi: 10.1002/cjoc.v38.3 |
|
|
(d) Yu, Y.; Zhong, J-S.; Xu, K.; Yuan, Y.; Ye, K.-Y. Adv. Synth. Catal. 2020, 362, 2102.
doi: 10.1002/adsc.v362.11 |
|
| [10] |
(a) Luo, J.; Xu, X.; Zheng, J. Chin. J. Org. Chem. 2018, 38, 363. (in Chinese)
doi: 10.6023/cjoc201707031 |
|
( 骆钧飞, 徐星, 郑俊良, 有机化学, 2018, 38, 363.)
doi: 10.6023/cjoc201707031 |
|
|
(b) Wang, D.; Salazar, C. A.; Stahl, S. S. Organometallics 2021, 40, 2198
doi: 10.1021/acs.organomet.1c00139 |
|
|
(c) Liang, R.-X.; Zhong, C.; Liu, Z.-H.; Yang, M.; Tang, H.-W.; Chen, J.-F.; Yang, Y.-F.; Jia, Y.-X. ACS Catal. 2021, 11, 1827.
doi: 10.1021/acscatal.0c05020 |
|
| [11] |
(a) Andorfer, M. C.; Park, H. J.; Vergara-Coll, J.; Lewis, J. C. Chem. Sci. 2016, 7, 3720.
pmid: 27347367 |
|
(b) Sun, L.; Zhang, X.; Li, Z.; Ma, J.; Zeng, Z.; Jiang, H. Eur. J. Org. Chem. 2018, 4949.
pmid: 27347367 |
|
| [12] |
(a) Hu, K.; Zhang, Y.; Zhou, Z.; Yang, Y.; Zha, Z.; Wang, Z. Org. Lett. 2020, 22, 5773.
doi: 10.1021/acs.orglett.0c01821 pmid: 32441518 |
|
(b) Zhang, Z.; Zhang, B.-S.; Li, K.-L.; An, Y.; Liu, C.; Gou, X.-Y.; Liang, Y.-M. J. Org. Chem. 2020, 85, 7817.
doi: 10.1021/acs.joc.0c00475 pmid: 32441518 |
|
| [13] |
(a) Kona, C. N.; Nishii, Y.; Miura, M. Org. Lett. 2021, 23, 6252.
doi: 10.1021/acs.orglett.1c01990 pmid: 32065752 |
|
(b) Wang, Z.-T.; Zheng, Z.-A.; Li, P.-J.; Zhou, C.-N.; Cai, S.-J.; Xiao, B.; Wang, L. Chin. J. Chem. 2021, 39, 2823.
doi: 10.1002/cjoc.v39.10 pmid: 32065752 |
|
|
(c) Pradhan, S.; Mishra, M.; De, P. B.; Banerjee, S.; Punniyamurthy, T. Org. Lett. 2020, 22, 1720.
doi: 10.1021/acs.orglett.9b04612 pmid: 32065752 |
|
| [14] |
(a) Fang, S.; Jiang, G.; Li, M.; Liu, Z.; Jiang, H.; Wu, W. Chem. Commun. 2019, 55, 13769.
doi: 10.1039/C9CC07263B |
|
(b) Wu, W.; Fang, S.; Jiang, G.; Li, M.; Jiang, H. Org. Chem. Front. 2019, 6, 2200.
doi: 10.1039/C8QO01261J |
|
| [15] |
Li, Y.; Wang, W.-H.; Yang, S.-D.; Li, B.-J.; Feng, C.; Shi, Z.-J. Chem. Commun. 2010, 46, 4553.
doi: 10.1039/c0cc00486c |
| [16] |
Liang, Z.; Zhao, J.; Zhang, Y. J. Org. Chem. 2010, 75, 170.
doi: 10.1021/jo902265s |
| [17] |
Li, Y.-X.; Ji, K.-G.; Wang, H.-X.; Ali, S.; Liang, Y.-M. J. Org. Chem. 2011, 76, 744.
doi: 10.1021/jo1023014 |
| [18] |
(a) Sun, Y.; Wang, R.; Liu, T.; Jin, W.; Wang, B.; Zhang, Y.; Xia, Y.; Liu, C. Eur. J. Org. Chem. 2021, 3743.
|
|
(b) Liu, Y.; Ma, X.; Wu, G.; Liu, Z.; Yang, X.; Wang, B.; Liu, C.; Zhang, Y.; Huang, Y. New J. Chem. 2019, 43, 9255.
doi: 10.1039/C9NJ01728C |
|
|
(c) Cao, D.; Zhang, Y.; Liu, C.; Wang, B.; Sun, Y.; Abdukader, A.; Hu, H.; Liu, Q. Org. Lett. 2016, 18, 2000.
doi: 10.1021/acs.orglett.6b00605 |
|
| [19] |
Sun, Q.; Liu, W.; Ying, S.; Wang, L.; Xue, S.; Yang, W. RSC Adv. 2015, 5, 73046.
doi: 10.1039/C5RA12969A |
| [20] |
Shelke, G. M.; Kumar, A. Synthesis 2017, 49, 4321.
doi: 10.1055/s-0036-1588181 |
| [21] |
Ji, Y.-Z.; Li, H.-J.; Wang, Y.-R.; Zhang, Z.-Y.; Wu, Y.-C. Adv. Synth. Catal. 2020, 362, 1039.
doi: 10.1002/adsc.v362.5 |
| [1] | 梅青刚, 李清寒. 可见光促进C(3)(杂)芳硫基吲哚化合物的合成研究进展[J]. 有机化学, 2024, 44(2): 398-408. |
| [2] | 童红恩, 郭宏宇, 周荣. 可见光促进惰性碳-氢键对羰基的加成反应进展[J]. 有机化学, 2024, 44(1): 54-69. |
| [3] | 贝文峰, 潘健, 冉冬梅, 刘伊琳, 杨震, 冯若昆. 基于钴催化吲哚酰胺与二炔和单炔的[4+2]环化反应合成γ-咔啉酮[J]. 有机化学, 2023, 43(9): 3226-3238. |
| [4] | 蒋宜欣, 唐伯孝, 毛海波, 陈雪霞, 俞洋杰, 全翠英, 徐昭阳, 石金慧, 刘益林. 水-聚乙二醇(PEG-200)中烯烃与碘代芳烃绿色可循环无负载偶联反应的研究[J]. 有机化学, 2023, 43(9): 3210-3215. |
| [5] | 岁丹丹, 岑南楠, 龚若蕖, 陈阳, 陈文博. 无支持电解质条件下连续流电化学合成三氟甲基化氧化吲哚[J]. 有机化学, 2023, 43(9): 3239-3245. |
| [6] | 王熠, 张键, 刘飏子, 罗晓燕, 邓卫平. 钯催化不对称[3+4]环加成构建吲哚并环庚烷[J]. 有机化学, 2023, 43(8): 2864-2877. |
| [7] | 吴秀蓉, 肖朝江, 沈怡, 汤红霞, 朱俊逸, 姜北. 植物来源抗疟倍半萜类天然产物研究(1972~2022)[J]. 有机化学, 2023, 43(8): 2764-2789. |
| [8] | 冯莹珂, 王贺, 崔梦行, 孙然, 王欣, 陈阳, 李蕾. 可见光诱导的新型官能化芳基异腈化合物的二氟烷基化环化反应[J]. 有机化学, 2023, 43(8): 2913-2925. |
| [9] | 张彦波, 孙萌. 铑催化碳酸亚乙烯酯与吲哚啉C(7)位C—H甲酰甲基化反应[J]. 有机化学, 2023, 43(8): 2905-2912. |
| [10] | 孙李星, 孙婷婷, 王海清, 吴淑芳, 王小烨, 刘天雅, 张宇辰. Lewis酸催化下3-烷基-2-吲哚烯与α,β-不饱和N-磺酰基亚胺的[2+4]环化反应[J]. 有机化学, 2023, 43(6): 2178-2188. |
| [11] | 任志军, 罗维纬, 周俊. 银介导的N-芳基丙烯酰胺串联环化反应研究进展[J]. 有机化学, 2023, 43(6): 2026-2039. |
| [12] | 孙泽人, 翟冰新, 何光超, 沈慧, 陈琳雅, 张杉, 邹毅, 朱启华, 徐云根. 新型1,2,3-三氮唑类衍生物的合成及抗炎活性研究[J]. 有机化学, 2023, 43(6): 2143-2155. |
| [13] | 童宇星, 王子维, 刘奔, 徐耀威, 高颂, 唐向兵, 张兴华. 吲哚-3-硫醚类化合物的合成研究进展[J]. 有机化学, 2023, 43(4): 1310-1324. |
| [14] | 庞明杨, 常宏宏, 冯璋, 张娟. 过渡金属催化吲哚的串联去芳构化反应研究进展[J]. 有机化学, 2023, 43(4): 1271-1291. |
| [15] | 黄华, 李鑫, 苏建科, 宋秋玲. 二氟卡宾参与下从邻乙烯基苯胺出发构建3-取代吲哚酮类化合物[J]. 有机化学, 2023, 43(3): 1146-1156. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||